Аденозин влияние на сосуды
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 15 августа 2020; проверки требует 1 правка.
Аденози́н — нуклеозид, состоящий из аденина, соединенного с рибозой (рибофуранозой) β-N9-гликозидной связью[1]. Входит в состав некоторых ферментов, АТФ и нуклеиновых кислот.
Аденозин играет важную роль в биохимических процессах, таких как передача энергии (АТФ и АДФ) и сигналов (цАМФ). Аденозин также является нейротрансмиттером ингибиторного типа.
Полагают, что он играет роль в стимуляции сна и подавлении бодрости, поскольку его концентрация увеличивается во время продолжительного бодрствования организма и уменьшается во время последующего сна[2][3].
Фармакологические эффекты[править | править код]
Аденозин — эндогенный пуриновый нуклеозид, модулирующий многие физиологические процессы. Передача клеточных сигналов происходит через 4 известных подтипа аденозиновых рецепторов (A1, A2A, A2B, и A3)[4], в которые входит 7 трансмембранных рецепторов, связанных с G-белком. Более подробная классификация внутри этих четырёх подтипов основана на их способности стимулировать или ингибировать аденилатциклазную активность. Рецепторы A2A и A2B сопряжены с Gάs и опосредуют активацию аденилатциклазы. Аденозиновые рецепторы типов A1 и A3 сопряжены с Gάi, который подавляет аденилатциклазную активность. Кроме того, рецепторы типа A1 сопряжены с белком Gάo, который, по имеющимся данным, опосредует ингибирование аденозином кальциевой проводимости. В то же время, рецепторы типов A2B и A3 сопряжены с Gάq и стимулируют фосфолипазную активность. Внеклеточная концентрация аденозина вблизи нормальных клеток составляет примерно 300 нМ. Однако, в ответ на повреждение клетки (например, в воспаленных или ишемичных тканях) концентрация аденозина быстро возрастает до 600—1200 нМ. Таким образом, в ответ на стресс или ранение аденозин проявляет в основном цитопротекторное действие, защищая ткани от повреждения в случаях гипоксии, ишемии или судорог. Активация рецепторов типа A2A вызывает широкий спектр ответов, которые можно в общем классифицировать как противовоспалительные.
Воздействие на мозг[править | править код]
В синаптической щели экто-АТФазы расщепляют некоторую долю АТФ, образуя аденозин. Он через рецепторы А1 активирует К-каналы, гиперполяризируя мембрану нейрона. Также АТФ через белок P2X7 опосредует выработку ФНО, ИЛ-1 и АТФ (новая доля). ФНО активирует в нейронах фактор NFkB (ядерный фактор каппа В), вследствие повышается восприимчивость нейронов к аденозину (чувствительность рецепторов А1).
Интенсивная работа мозга ведет к накоплению аденозина, который вызывает гиперполяризацию нейронов, что ослабляет передачу информации. Важно отметить, что дальнейшее действие аденозина происходит не из-за накопления его в нейронах, а из-за повышения чувствительности к нему по вышеописанному механизму.
Противовоспалительные свойства[править | править код]
Аденозин является сильным противовоспалительным агентом, действующим на 4 рецептора, связанных с G-белком. Показано, что местное применение аденозина для лечения ран конечностей у лабораторных животных, страдающих сахарным диабетом, существенно ускоряет заживление тканей. Местное применение аденозина при замедленном заживлении ран и сахарном диабете у человека в настоящее время проходит клинические испытания.
Воздействие на сердце[править | править код]
При внутривенном введении аденозин вызывает временную блокаду сердца в атриовентрикулярном узле. Это воздействие передается через рецептор А1, ингибирующий аденилатциклазу и снижающий концентрацию цАМФ, вызывая таким образом гиперполяризацию клеток через усиление потока ионов K+ извне. Это также вызывает эндотелиально-зависимую релаксацию гладкой мускулатуры, находящейся внутри стенок артерий. Следствием этого становится расширение «нормальных» сегментов артерий, в которых эндотелий не отделен от tunica media атеросклеротическими бляшками. Это свойство аденозина позволяет использовать его при диагностике блокады коронарных артерий, поскольку он увеличивает разницу между нормальными и аномальными сегментами артерий.
Аденозин используется для идентификации ритма у людей, предположительно страдающих суправентрикулярной тахикардией (СВТ). Некоторые виды СВТ могут быть успешно купированы аденозином. В них входят любые возвратные аритмии (например, AVRT и AVNRT). В некоторых случаях аденозином может быть купирована предсердная тахикардия.
Аденозин имеет непрямой эффект на предсердную ткань, вызывая укорочение рефракторного периода. Показано, что при введении через центральный катетер аденозин вызывает фибрилляцию предсердий. У людей с дополнительными проводящими каналами наступление фибрилляции предсердий может привести к фибрилляции желудочков.
Быстрые сердечные ритмы, локализованные в предсердиях или желудочках, не затрагивающие AV-узел, обычно не прекращаются после введения аденозина, однако он может вызвать временное снижение скорости ответа желудочков.
Из-за эффекта, который аденозин оказывает на AV-зависимые суправентрикулярные тахикардии, он считается противоаритмическим препаратом класса V. При использовании аденозина в качестве средства для купирования аритмии нормальным эффектом считается желудочковая асистолия в течение нескольких секунд. Такой эффект может дезориентировать пациента, находящегося в сознании, и связан с неприятными ощущениями в груди.
Фармакологический эффект может притупляться у людей, принимающих большие количества метилксантинов, например кофеина или теофиллина.
Стимулирующий эффект кофеина возникает в основном из-за ингибирования действия аденозина при связывании с теми же рецепторами. По природе своей пуриновой структуры кофеин связывается с частью аденозиновых рецепторов в ЦНС, эффективно блокируя их. Снижение активности аденозина приводит к увеличенной активности нейротрансмиттеров допамина и глутамата.
Дозировка[править | править код]
Для диагностики и лечения СВТ начальная доза составляет 6 мг при быстром внутривенном или внутрикостном введении. Из-за очень короткого периода полураспада внутривенная инъекция делается наиболее проксимально к сердцу, например в локтевую ямку. За внутривенным введением аденозина часто следует немедленное введение 5-10 мл изотонического раствора. При отсутствии эффекта дополнительная доза (12 мг) может быть введена через 1—2 минуты. Ещё 12 мг может быть введено через 1—2 минуты при отсутствии эффекта. Некоторые врачи предпочитают вводить большую дозу (обычно 18 мг), чем повторять введение того же самого количества препарата. Для расширения артерий обычно используется дозировка 0,14 мг/кг/мин в течение 4—6 минут.
Рекомендованная доза может быть увеличена в случае пациентов, принимающих теофиллин. Доза должна быть снижена в случае пациентов, принимающих дипиридамол или валиум, поскольку аденозин потенцирует действие этих препаратов. Доза снижается вдвое для пациентов с сердечной недостаточностью, инфарктом миокарда, шоком, гипоксией, печеночной или почечной недостаточностью, а также для пожилых пациентов.
Примечания[править | править код]
Ссылки[править | править код]
- Дубынин В. Глицин и аденозин. ИД «ПостНаука» (11 ноября 2016). — лекция. Дата обращения: 21 ноября 2016.
Источник
Содержание
- Структурная формула
- Латинское название вещества Аденозин
- Фармакологическая группа вещества Аденозин
- Нозологическая классификация (МКБ-10)
- Характеристика вещества Аденозин
- Фармакология
- Применение вещества Аденозин
- Противопоказания
- Ограничения к применению
- Применение при беременности и кормлении грудью
- Побочные действия вещества Аденозин
- Взаимодействие
- Передозировка
- Пути введения
- Способ применения и дозы
- Меры предосторожности вещества Аденозин
- Взаимодействия с другими действующими веществами
- Торговые названия
Структурная формула
Русское название
Аденозин
Латинское название вещества Аденозин
Adenosinum (род. Adenosini)
Химическое название
6-Амино-9-бета-D-рибофуранозил-9H-пурин
Брутто-формула
C10H13N5O4
Фармакологическая группа вещества Аденозин
- Антиаритмические средства
Нозологическая классификация (МКБ-10)
Код CAS
58-61-7
Характеристика вещества Аденозин
Аденозин — эндогенный нуклеозид, присутствующий во всех клетках организма.
Белый кристаллический порошок. Растворим в воде и практически нерастворим в этаноле. Растворимость повышается при нагревании и снижении pH раствора. Молекулярная масса 267,24.
Фармакология
Фармакологическое действие – антиаритмическое, диагностическое.
Оказывает антиаритмическое действие (главным образом при наджелудочковых тахиаритмиях). Замедляет образование импульсов в синусно-предсердном узле, уменьшает время проведения через предсердно-желудочковый узел, может прерывать пути повторного проведения возбуждения через предсердно-желудочковый узел. Способствует восстановлению нормального синусового ритма у больных с пароксизмальной наджелудочковой тахикардией. Начало действия — немедленное.
Аденозин является также сильным вазодилататором в большинстве сосудистых регионов, за исключением почечных афферентных артериол и печеночных вен, где он вызывает вазоконстрикцию. Оказывает коронарорасширяющее действие. Может вызвать артериальную гипотензию (главным образом при медленной в/в инфузии в дозах свыше 12 мг).
Возникновение многих фармакологических эффектов аденозина, возможно, обусловлено активацией пуриновых рецепторов — клеточно-поверхностных аденозиновых рецепторов A1 (ингибируют аденилатциклазу) и A2 (активируют аденилатциклазу).
Механизм расширяющего действия на коронарные артерии связан с повышением проводимости для К+ и подавлением вызванного цАМФ входа Ca2+ в клетку. Результатом этого является гиперполяризация и подавление кальцийзависимых потенциалов действия, релаксация гладкой мускулатуры стенок сосудов.
После в/в введения очень быстро биотрансформируется с участием циркулирующих ферментов в эритроцитах и клетках эндотелия сосудов, прежде всего путем дезаминирования, до неактивного инозина, а также посредством фосфорилирования с помощью аденозинкиназы до АМФ. T1/2 из крови — менее 10 с. Выводится почками в виде метаболитов (преобладающий конечный метаболит — мочевая кислота).
Канцерогенность, мутагенность, влияние на фертильность
Исследований на животных с целью оценки потенциальной канцерогенности аденозина не проводили.
Аденозин не проявлял генотоксичности в тесте Эймса (с использованием штаммов Salmonella) или в тесте с микросомами млекопитающих. Аденозин, как и другие нуклеозиды, в миллимолярных концентрациях вызывал изменения хромосом в культуре клеток.
При исследовании фертильности у крыс и мышей при внутрибрюшинном введении аденозина в дозах 50, 100 и 150 мг/кг/сут в течение 5 дней зафиксировано снижение сперматогенеза и увеличение числа дефектных сперматозоидов.
Применение вещества Аденозин
Для болюсного в/в введения: пароксизмальная наджелудочковая тахикардия (в т.ч. при WPW-синдроме). Для в/в инфузии: дифференциальная диагностика наджелудочковых тахиаритмий (тахикардия с уширенными комплексами QRS), диагностические электрофизиологические исследования (определение локализации AV блока).
Противопоказания
Гиперчувствительность, AV-блокада II и III степени или синдром слабости синусного узла (за исключением больных с искусственным водителем ритма), бронхиальная астма (риск бронхоспазма).
Ограничения к применению
Синусовая брадикардия, нестабильная стенокардия, пороки сердца, перикардит, гиповолемия.
Применение при беременности и кормлении грудью
При беременности допустимо в случае крайней необходимости (адекватных и строго контролируемых исследований у человека не проведено). Поскольку аденозин является эндогенным интермедиантом организма, осложнений не предполагается и в немногочисленных сообщениях о применении аденозина у беременных женщин сведения об осложнениях у плода или матери отсутствуют.
Категория действия на плод по FDA — C.
Считают, что в связи с быстрым исчезновением из кровотока аденозин не проникает в грудное молоко.
Побочные действия вещества Аденозин
При быстром в/в болюсном введении
При проведении контролируемых клинических испытаний в США после в/в введения аденозина наблюдались следующие неблагоприятные эффекты (в группе плацебо все эти реакции были отмечены менее чем в 1% случаев):
Со стороны нервной системы и органов чувств: легкое головокружение (2%), головная боль (2%), покалывание в руках, ощущение онемения (1%), нервозность, нарушение зрения, боль в шее и спине (менее 1%).
Со стороны сердечно-сосудистой системы и крови (кроветворение, гемостаз): прилив крови к лицу (18%), сердцебиение, боль в грудной клетке, снижение АД (менее 1%).
Со стороны респираторной системы: одышка (12%), давление в груди (7%), гипервентиляция.
Со стороны органов ЖКТ: тошнота (3%), металлический привкус во рту, ощущение сдавливания в горле.
Прочие: усиленное потоотделение (менее 1%).
В постмаркетинговых наблюдениях отмечались случаи возникновения новых аритмий — экстрасистолия желудочковая и предсердная, синусовая брадикардия, синусовая тахикардия, выпадение пульса (вновь возникшие аритмии обычно продолжаются несколько секунд), транзиторное повышение давления, бронхоспазм.
При в/в инфузии
При проведении контролируемых и неконтролируемых клинических испытаний в США после в/в введения аденозина (n=1421) наблюдались следующие неблагоприятные эффекты, которые были отмечены по крайней мере в 1% случаев.
Несмотря на короткий T1/2 аденозина в 10,6% случаев побочные эффекты регистрировались не в момент инфузии, а спустя несколько часов после ее окончания. В 8,4% случаев проявление побочных эффектов совпало с началом инфузии и завершилось через 24 ч после ее окончания. Во многих случаях нет возможности определить, являются ли более поздние побочные эффекты результатом инфузии аденозина.
Приливы крови к лицу (44%), ощущение дискомфорта в груди (40%), диспноэ (28%), головная боль (18%), ощущение дискомфорта в горле, челюстях, или шее (15%), расстройство ЖКТ (13%), головокружение (12%), ощущение дискомфорта в руках (4%), снижение сегмента ST (3%), AV-блокада I степени (3%), AV-блокада II степени (3%), парестезия (2%), артериальная гипотензия (2%), нервозность (2%), аритмия (1%).
Побочные эффекты разной степени выраженности, отмеченные менее чем у 1% пациентов, включали:
Организм в целом: ощущение дискомфорта в спине и/или в нижних конечностях, слабость.
Со стороны сердечно-сосудистой системы и крови (кроветворение, гемостаз): инфаркт миокарда без смертельного исхода, угрожающая жизни вентрикулярная аритмия, AV-блокада III степени, брадикардия, сердцебиение, потливость, изменения зубца Т, артериальная гипертензия (сАД >200 мм рт. рт.).
Со стороны нервной системы и органов чувств: сонливость, эмоциональная лабильность, тремор, нарушение зрения.
Со стороны респираторной системы: кашель.
Прочие: сухость во рту, дискомфорт в ушах, металлический привкус во рту, заложенность носа, скотома, дискомфорт в языке.
Взаимодействие
Дипиридамол усиливает действие аденозина путем торможения захвата его клетками (рекомендуется снижение дозы). Вазоактивные эффекты аденозина ослабляют антагонисты рецепторов аденозина, например метилксантины, в т.ч. кофеин и теофиллин (могут понадобиться более высокие дозы аденозина или изменение лечения). Карбамазепин может усиливать блокаду сердца, вызванную аденозином. Следует соблюдать осторожность при в/в введении аденозина с другими кардиотропными ЛС (такими как бета-адреноблокаторы, сердечные гликозиды, БКК), поскольку их эффективность в таких случаях систематично не оценивалась; хотя неблагоприятного взаимодействия не отмечено, потенциально возможно аддитивное или синергическое угнетающее действие в отношении синоатриальной и AV-проводимости.
Передозировка
Вследствие короткого T1/2 нежелательные явления (в случае их возникновения) быстро исчезают. Конкурентные антагонисты аденозина — кофеин, теофиллин и другие метилксантины.
Пути введения
В/в (болюсно или инфузионно).
Способ применения и дозы
В качестве антиаритмического средства: взрослым — в/в болюсно (в течение 1–3 с) в центральную или крупную периферическую вену вводят 6 мг под контролем ЭКГ и АД, при необходимости через 1–2 мин — 12 мг, если нет эффекта — через 1–2 мин повторно 12 мг. На любом из этапов введение прекращают после устранения аритмии или развитии AV блокады высокой степени. Максимальная разовая доза для взрослых — 12 мг. У получающих дипиридамол начальная доза 0,5–1 мг. Детям — 50 мкг/кг. Дозу можно увеличивать на 50 мкг/кг каждые 2 мин до максимальной дозы 250 мкг/кг. В качестве вспомогательного диагностического средства: в/в (инфузия) в дозе 140 мкг/кг/мин в течение 6 мин (общая доза — 840 мкг/кг). У больных с высоким риском побочных эффектов инфузию начинают с более низких доз (от 50 мкг/кг/мин).
Меры предосторожности вещества Аденозин
При применении рекомендуется измерение АД, ЧСС, мониторирование ЭКГ.
Введение через центральные вены снижает риск развития побочных эффектов.
В/в введение допустимо только в условиях стационара, где есть возможность мониторинга деятельности сердца. Для пациентов, у которых применение одной дозы аденозина осложнилось AV блокадой, дополнительные дозы вводить не следует.
Взаимодействия с другими действующими веществами
Перейти
Торговые названия
Источник
Вазодилататорная и гипоксическая теория регуляции кровотока в органах и тканяха) Вазодилататорная теория краткосрочной регуляции местного кровотока — возможная роль аденозина. В соответствии с этой теорией усиление метаболизма или дефицит кислорода (или питательных веществ) в тканях приводит к усиленному образованию сосудорасширяющих веществ клетками тканей. Полагают, что сосудорасширяющие вещества диффундируют к прекапиллярным сфинктерам, метартериолам и артериолам и вызывают их расширение. Такими сосудорасширяющими веществами предположительно являются аденозин, углекислый газ, аденозинфосфаты, гистамин, ионы калия и ионы водорода. Авторы большинства вазодилататорных теорий считают, что сосудорасширяющие вещества выделяются клетками тканей в ответ на недостаток кислорода. Так, эксперименты показали, что недостаток кислорода приводит к высвобождению в межклеточные пространства как аденозина, так и молочной кислоты (содержащей ионы водорода). Эти вещества вызывают расширение сосудов и, таким образом, являются частично или полностью ответственными за регуляцию местного кровотока. Многие физиологи полагают, что аденозин как сосудорасширяющий фактор оказывает первостепенное влияние на местный кровоток. Так, например, при резком снижении коронарного кровотока из кардиомиоцитов выделяется небольшое количество аденозина — и этого оказывается достаточно, чтобы кровоток в сердечной мышце вернулся к нормальному уровню за счет расширения коронарных сосудов. Кроме того, во всех случаях, когда сердечная деятельность усиливается и уровень метаболизма в сердце увеличивается, это приводит к повышенной утилизации кислорода, что сопровождается (1) уменьшением концентрации кислорода в кардиомиоцитах с (2) последующим расщеплением аденозинтрифосфата, что приводит к (3) образованию аденозина. Полагают, что большая часть аденозина выделяется из кардиомиоцитов, вызывая расширение коронарных сосудов и увеличение коронарного кровотока, — для удовлетворения возросших потребностей активно работающего сердца. Многие физиологи полагают, что тот же механизм с участием аденозина является главным в регуляции кровотока не только в сердечной мышце, но и в скелетных мышцах и многих других тканях. Проблема, с которой сталкиваются физиологи, заключается в следующем: невозможно привести доказательства того, что какое-либо одно сосудорасширяющее вещество, образующееся в тканях, вызывает увеличение кровотока. Однако комбинация различных вазодилататоров, несомненно, является причиной такого увеличения. б) Гипоксическая теория регуляции местного кровотока. Несмотря на то, что вазодилататорная теория является общепризнанной, ряд физиологов, опираясь на имеющиеся факты, придерживается так называемой гипоксической теории (а точнее, нутриент-дефицитной теории, т.к. наряду с недостатком кислорода ткани испытывают недостаток и питательных веществ). Кислород (и питательные вещества) необходимы гладкомышечным клеткам сосудистой стенки для сокращения. Следовательно, недостаток этих веществ приводит к тому, что гладкие мышцы расслабляются, а сосуды расширяются. Кроме того, увеличение потребления кислорода тканями при активации их метаболизма теоретически может привести к снижению концентрации кислорода в гладкомышечных клетках сосудов, а также вызвать местное расширение сосудов.
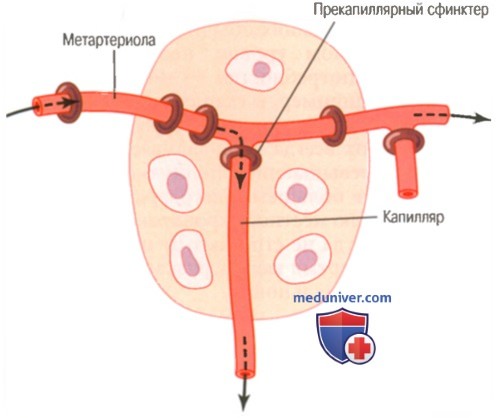
На рисунке показан участок ткани, получающий кровоснабжение из метартериолы по одному отходящему от нее боковому капилляру. В начальной части капилляра показан прекапиллярный сфинктеру а также гладкомышечные волокна, расположенные в отдельных участках метартериолы. Наблюдая подобную структуру в микроскоп (например, в крыле летучей мыши), можно видеть, что прекапиллярный сфинктер в норме то полностью открыт, то полностью закрыт. Число прекапиллярных сфинктеров, открытых в данный момент, пропорционально метаболическим потребностям ткани. Прекапиллярный сфинктер и метартериола открываются и закрываются периодически, несколько раз в минуту. Продолжительность пребывания их в открытом состоянии также пропорциональна уровню метаболизма. Периодическое открывание и закрывание мелких сосудов получило название вазомоции (или вазомоторики). Попробуем объяснить, каким образом концентрация кислорода в тканях может регулировать уровень местного кровотока. Гладкой мышце для сокращения требуется кислород, поэтому можно предположить, что сила сокращения сфинктера будет увеличиваться при увеличении концентрации кислорода. Если концентрация кислорода в тканях окажется выше определенного уровня, сфинктеры метартериол, по-видимому, останутся закрытыми до тех пор, пока клетки не используют избыток кислорода. Когда же концентрация кислорода понизится, сфинктеры откроются, и весь цикл начнется сначала. Таким образом, опираясь на имеющиеся данные, и вазодилататорная, и гипоксическая теории способны объяснить краткосрочную регуляцию местного кровотока в ответ на изменение метаболических потребностей тканей. В основе регуляции, по-видимому, лежит сочетание этих двух механизмов. – Также рекомендуем “Реактивная гиперемия. Активная гиперемия” Оглавление темы “Регуляция кровоснабжения”: |
Источник
