Адреналин вызывает сужение сосудов кожи расширение сосудов сердца
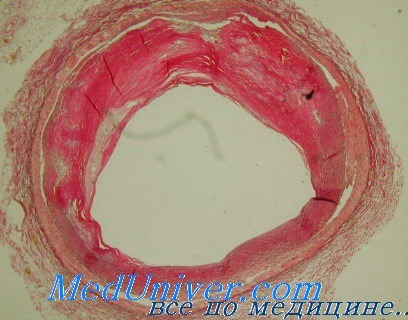
Влияние адреналина на сосуды. Применение тиреоидных гормонов в лечении атеросклерозаКатехоламины, в частности адреналин, оказывают воздействие на коронарное кровообращение, а также вызывают органические изменения в венечных сосудах. Введение адреналина может вызывать некроз средней оболочки коронарных артерий и утолщение интимы, что в свою очередь способствует развитию атеросклероза. Wilkens и Sapeika (1964) нашли, что при введении адреналина почти в 1/2 (48%) случаев у кроликов развивается атеросклероз. Помимо изменений обмена липидов, адреналин, по данным ряда авторов, вызывает у кроликов фиброз и отек интимы и накопление в ней липидов и мукополисахаридов. Подобные изменения в интиме сосудов были установлены Jagannathan с соавт. (19G4) в сосудах у обезьян под влиянием введения адреналина. По мнению этих авторов, найденные ими изменения очень напоминают ранние стадии атеросклероза, однако в отличие от него прогрессирования процесса при этом не наблюдается, по-видимому, потому что экзогенный адреналин быстро ииактивируется, тогда как длительное повышенное образование эндогенного адреналина может привести к нарастанию изменений в сосудах. Такая же противоречивость данных существует и в отношении функционального состояния щитовидной железы у больных атеросклерозом. Наряду с данными о снижении функции щитовидной железы у больных с коронарным атеросклерозом (К. Н. Простяков с соавт., 1957; Я. С. Вайнбаум, 1961; А. Н. Митропольский и А. Ф. Мурчакова, 1959), имеются указания на нормальную функцию щитовидной железы при коронарном атеросклерозе. Пользуясь более точными методами определения PBJ, поглощения J131 и основного обмена, И. К. Комарова (1962) нашла у больных с умеренно выраженными проявлениями атеросклероза нормальные показатели функции щитовидной железы, и только при тяжелом и распространенном атеросклерозе наблюдалась тенденция к снижению функции щитовидной железы. Однако, несмотря на имеющиеся в литературе противоречия, многие авторы, учитывая отчетливое влияние тиреоидных гормонов на обмен липидов, рекомендуют их применение при атеросклерозе. По наблюдениям Starr (1960), Cohen и Loewe (1962), дача тироксина больным с высокой гиперхолестеринемией вызвала у них отчетливое снижение уровня холестерина (на 32,3% по Cohen), которое не сопровождалось повышением основного обмена. Такие же данные были получены и в эксперименте (Owen с соавт., 1962). С помощью меченого С14 холестерина Rabinowitch с соавт. (1962) установил, что снижение холестерина достигается путем повышения его экскреции. Больные, лечившиеся тироксином, почти в 2-3 раза быстрее освобождались от радиоактивного холестерина, чем контрольные лица. Введение тироксина и трийодтиронина экспериментальным животным приводит к снижению уровня холестерина в крови. Это послужило поводом к очень интенсивному изучению механизма действия тиреоидных гормонов на процессы всасывания, распределения и катаболизма экзогенного холестерина, а также на биосинтез его в организме (Chin, 1961).
Введение тиреоидных гормонов крысам не вызывает понижения всасывания холестерина, а его снижение связано, по-видимому, с повышенным выведением из организма и угнетением биосинтеза. Erickson (1957) указывает, что понижение уровня холестерина в крови при введении животным тиреоидных гормонов связано с ускорением процесса перехода холестерина в печени в желчные кислоты и выведением его из организма. К такому же заключению приходят Von Itallic и Hashim (1965). Изучая действие тиреоидина на инфильтрацию сосудистой стенки холестерином при алиментарном атеросклерозе, Л. Л. Мясников и В. Н. Зайцев (1962) применили меченый холестерин и нашли, что в этих условиях холестерин откладывается преимущественно в печени и надпочечниках, а не в стенках сосудов. Таким образом, можно думать, что тиреоидин влияет не только на уровень холестерина в крови, но также препятствует его отложению в сосудистой стенке. Все эти наблюдения послужили поводом к попытке применения препаратов щитовидной железы с лечебной целью при коронарном атеросклерозе. Применение этих препаратов предусматривает преимущественное действие их на уровень холестерина в крови. Нежелательным, побочным эффектом этих препаратов является их влияние на повышение основного обмена, что усиливает потребление кислорода миокардом. Strisower с соавт. (1957) пробовал применять тиреоидин и наблюдал значительное снижение бета-липопротеидов у больных коронарным атеросклерозом. За последние годы было получено несколько изомеров тироксина; некоторые из них вызывают только снижение холестерина и бета-липопротеидов, не влияя на основной обмен. Клиническое испытание этих изомеров было впервые проведено Starr в 1958 г., а затем многими другими (Green, 1961; Bernstein с соавт., 1962; Winters и Saloff, 1962; Davis с соавт., и ряд др.). Было установлено, что декстро-изомер d-тироксин оказывает гораздо более выраженное влияние на снижение уровня холестерина, чем L-тироксин, и при этом гораздо меньше влияет на обменные процессы. Davis с соавторами (1962), применяя этот препарат у 239 больных атеросклерозом, наблюдал значительное и стойкое снижение холестерина. Аналогичные результаты были получены Best и Duncan (1961), Jones и Cohen (1961), Oliver и Boyd (1960) и рядом других. – Также рекомендуем “Декстро-трийодтиронин при атеросклерозе. Влияние половых гормонов на обмен холестерина” Оглавление темы “Участие гормонов в развитии атеросклероза”:
|
Источник
 Адреналин – один из катехоламинов, он является гормоном мозгового слоя надпочечников и вненадпочечников хромаффинной ткани. Под влиянием адреналина происходит повышение содержания глюкозы в крови и усиление тканевого обмена. Адреналин усиливает глюконеогенез (синтез глюкозы), тормозит синтез гликогена в печени и скелетных мышцах, усиливает захват и утилизацию глюкозы тканями, повышая активность гликолетических ферментов. Также адреналин усиливает липолиз (распад жиров) и тормозит синтез жиров. В высоких концентрациях адреналин усиливает катаболизм белков.
Адреналин – один из катехоламинов, он является гормоном мозгового слоя надпочечников и вненадпочечников хромаффинной ткани. Под влиянием адреналина происходит повышение содержания глюкозы в крови и усиление тканевого обмена. Адреналин усиливает глюконеогенез (синтез глюкозы), тормозит синтез гликогена в печени и скелетных мышцах, усиливает захват и утилизацию глюкозы тканями, повышая активность гликолетических ферментов. Также адреналин усиливает липолиз (распад жиров) и тормозит синтез жиров. В высоких концентрациях адреналин усиливает катаболизм белков.
Адреналин обладает способностью повышать артериальное давление за счет сужения сосудов кожи и других мелких периферических сосудов, ускорять ритм дыхания. Содержание адреналина в крови повышается, в том числе, и при усиленной мышечной работе либо понижении уровня сахара. Количество выделяемого в первом случае адреналина прямо пропорционально интенсивность тренировочной сессии. Адреналин вызывает расслабление гладкой мускулатуры бронхов и кишечника, расширение зрачков (вследствие сокращения радиальных мышц радужной оболочки, имеющих адренергическую иннервацию). Именно свойство резко повышать уровень сахара в крови сделало адреналин незаменимым средством при выведении пациентов из состояния глубокой гипогликемии, вызванной передозировкой инсулина.
Адреналин – это мощный стимулятор и α, и β-адренорецепторов, и поэтому его эффекты многообразны и cложны. Большая часть тех эффектов, которые приведены в табл. 6.1, возникают в ответ на введение экзогенного адреналина. В то же время многие реакции (например, потоотделение, пилоэрекция, расширение зрачков) зависят от физиологического состояния организма в целом. Особенно сильное действие адреналин оказывает на сердце, а также на сосуды и другие гладкомышечные органы.
Артериальное давление. Адреналин – это одно из самых мощных прессорных веществ. При в/в введении в фармакологических дозах он вызывает быстрое повышение АД, степень которого прямо зависит от дозы. Систолическое АД при этом растет больше, чем диастолическое,то есть пульсовое АД увеличивается. По мере того как реакция на адреналин спадает, среднее АД может на какое-то время стать ниже исходного и только потом возвратиться к прежнему значению.{_st-d-1}
Прессорное действие адреналина обусловлено тремя механизмами: 1) прямым стимулирующим действием на рабочий миокард (положительным инотропным эффектом), 2) повышением ЧСС (положительным хронотропным эффектом), 3) сужением резистивных прекапиллярных сосудов многих бассейнов (особенно кожи, слизистых и почек) и выраженным сужением вен. На высоте подъема АД ЧСС может снизиться из-за рефлекторного повышения парасимпатического тонуса. В малых дозах (0,1 мкг/кг) адреналин может вызвать снижение АД. Этот эффект, так же как и двухфазное действие больших доз адреналина, объясняется более высокой чувствительностью к этому веществу β2-адренорецепторов (вызывающих расширение сосудов) по сравнению с α-адренорецепторами.
При п/к или медленном в/в введении адреналина картина несколько иная. При п/к введении адреналин из-за местного сужения сосудов всасывается медленно: эффект такого введения 0,5-1,5 мг адреналина такой же, как при в/в инфузии со скоростью 10-30 мкг/мин. Наблюдается умеренный рост систолического АД и сердечного выброса вследствие положительного инотропного эффекта. ОПСС снижается из-за того, что преобладает активация β2-адренорецепторов сосудов скелетных мышц (мышечный кровоток при этом растет); в результате диастолическое АД уменьшается. Поскольку среднее АД, как правило, увеличивается незначительно, компенсаторные барорефлекторные влияния на сердце выражены слабо. ЧСС, сердечный выброс, ударный объем и ударная работа левого желудочка повышаются – в результате как прямого стимулирующего влияния на сердце, таки возросшего венозного возврата (показателем последнего служит повышение давления в правом предсердии). При несколько более высокой скорости инфузии ОПСС и диастолическое АД могут не изменяться или слегка увеличиваться – в зависимости от дозы, а следовательно, и соотношения между активацией а- и β-адренорецепторов в разных сосудистых бассейнах. Кроме того, могут развиваться компенсаторные рефлекторные реакцииАдреналин действует главным образом на артериолы и прекапиллярные сфинктеры, хотя на него реагируют также вены и крупные артерии. Сосуды разных органов отвечают на адреналин по-разному, что приводит к существенному перераспределению кровотока.
Экзогенный адреналин вызывает резкое снижение кожного кровотока за счет сужения прекапиллярных сосудов и венул. Именно поэтому падает кровоток в кистях и ступнях. В слизистых при местном нанесении адреналина после первоначальной вазоконстрикции развивается гиперемия. Она обусловлена, видимо, не активацией β-адренорецепторов, а реакцией сосудов на гипоксию.
У человека терапевтические дозы адреналина вызывают повышение мышечного кровотока. Оно частично связано с резкой активацией β2-адренорецепторов, лишь в небольшой степени компенсируемой активацией α-адренорецепторов. На фоне α-адреноблокаторов расширение мышечных сосудов становится еще более выраженным, ОПСС и среднее АД снижаются (парадоксальная реакция на адреналин). На фоне же неизбирательных β-адреноблокаторов, напротив, сосуды сужаются и АД резко повышается.
Влияние адреналина на мозговой кровоток опосредовано изменениями АД. В терапевтических дозах адреналин вызывает лишь слабое сужение мозговых сосудов. При повышении симпатического тонуса в условиях стресса мозговые сосуды также не сужаются, что физиологически вполне оправдано – возможное увеличение мозгового кровотока в ответ на повышение АД ограничивается механизмами ауторегуляции.
В дозах, мало влияющих на среднее АД, адреналин повышает сопротивление почечных сосудов, снижая почечный кровоток примерно на 40%. В этой реакции участвуют все почечные сосуды. Поскольку СКФ меняется лишь незначительно, фильтрационная фракция резко возрастает. Экскреция Na+, К+ и СГ снижается; диурез же может увеличиваться, уменьшаться или не изменяться. Максимальные скорости канальцевой реабсорбции и секреции не изменяются. В результате прямого действия адреналина на бета-адренорецепторы юкстагломерулярных клеток повышается секреция ренина.
Под действием адреналина повышается давление в легочных артериях и венах. Причиной служит не только прямое сосудосуживающее действие адреналина на легкие, но и, безусловно, перераспределение крови в пользу малого круга из-за сокращения мощных гладких мышц системных вен. В очень высоких концентрациях адреналин вызывает отек легких вследствие повышения фильтрационного давления в легочных капиллярах и, возможно, увеличения их проницаемости.
В физиологических условиях адреналин и возбуждение симпатических сердечных нервов вызывают повышение коронарного кровотока. Это наблюдается даже при введении таких доз адреналина, которые не повышают давление в аорте (то есть перфузионное давление коронарных сосудов). В основе данного эффекта лежат два механизма. Во-первых, при повышении ЧСС растет относительная продолжительность диастолы (см. ниже); впрочем, этому частично противодействует снижение коронарного кровотока во время систолы из-за более мощного сокращения сердца и сдавления коронарных сосудов. Если же вдобавок повышается давление в аорте, то коронарный кровоток в диастолу еще больше возрастает. Во-вторых, повышение силы сокращений и потребления сердцем кислорода приводят к выбросу сосудорасширяющих метаболитов (прежде всего аденозина); действие этих метаболитов преодолевает прямое сужающее влияние адреналина на коронарные сосуды.{_st-d-2}
Сердце. Адреналин оказывает мощный стимулирующий эффект на сердце. Он действует преимущественно на β1-адренорецепторы клеток рабочего миокарда и проводящей системы, так как эти рецепторы в сердце преобладают (имеются также α- и β2-адренорецепторы, хотя их содержание в сердце сильно зависит от вида животного).
В последнее время большой интерес вызывает роль β1- и β2-адренорецепторов в регуляции сердца у человека, и особенно – в развитии сердечной недостаточности. Под влиянием адреналина ЧСС повышается, и часто возникают аритмии. Систола укорачивается, сила сокращений и сердечный выброс повышаются, работа сердца и потребление им кислорода резко возрастают. Коэффициент полезного действия сердца, показателем которого служит отношение работы к потреблению кислорода, снижается. К первичным эффектам адреналина относятся повышение силы сокращений, скорости нарастания давления в фазу изоволюмического напряжения и спада давления в фазу изоволюмического расслабления, уменьшение времени достижения максимального внутрижелудочкового давления, повышение возбудимости, рост ЧСС и автоматизма клеток проводящей системы.
Повышая ЧСС, адреналин одновременно укорачивает систолу, так что длительность диастолы обычно не уменьшается. Это достигается, в частности, за счет того, что активация β-адренорецепторов сопровождается увеличением скорости диастолического расслабления. Повышение ЧСС обусловлено ускорением спонтанной диастолической деполяризации (фазы 4) клеток синусового узла; при этом мембранный потенциал быстрее достигает критического уровня, при котором возникает потенциал действия (гл. 35). Увеличиваются также амплитуда и крутизна потенциала действия. Часто наблюдается миграция водителя ритма в пределах синусового узла (из-за активации латентных водителей ритма). Адреналин повышает скорость спонтанной диастолической деполяризации и в волокнах Пуркинье, что также может привести к активации латентных водителей ритма. В рабочих кардиомиоцитах эти изменения не наблюдаются, так как в фазу 4 у них регистрируется не спонтанная диастолическая деполяризация, а стабильный потенциал покоя. В высоких дозах адреналин может вызвать желудочковые экстрасистолы – предвестники более грозных нарушений ритма. При использовании терапевтических доз у человека это наблюдается редко, однако в условиях повышенной чувствительности сердца к адреналину (например, под действием некоторых средств для обшей анестезии) или при инфаркте миокарда выброс эндогенного адреналина может вызвать желудочковые экстрасистолы, желудочковую тахикардию и даже фибрилляцию желудочков. Механизмы этого явления изучены плохо.
Некоторые эффекты адреналина на сердце обусловлены повышением ЧСС и в условиях навязанного ритма не наблюдаются либо непостоянны. К ним относятся, например, изменения реполяризации рабочих кардиомиоцитов предсердий и желудочков и волокон Пуркинье. Повышение ЧСС само по себе вызывает укорочение потенциала действия, а следовательно, и рефрактерного периода.
Проведение в системе волокон Пуркинье зависит от их мембранного потенциала в момент прихода волны возбуждения. Выраженная деполяризация приводит к нарушениям проведения – от замедления до блокады. В этих условиях адреналин часто восстанавливает нормальный мембранный потенциал, а тем самым – и проводимость.
Адреналин укорачивает рефрактерный период АВ-узла (хотя в тех дозах, при которых ЧСС из-за рефлекторного повышения парасимпатического тонуса снижается, адреналин может вызвать и непрямое удлинение этого периода). Кроме того, адреналин уменьшает степень АВ-блокады, обусловленной заболеваниями сердца, приемом некоторых препаратов или повышенным парасимпатическим тонусом. На фоне повышенного парасимпатического тонуса адреналин может вызвать наджелудочковые аритмии. В вызванных адреналином желудочковых аритмиях определенную роль также, видимо, играют парасимпатические влияния, приводящие к замедлению частоты разрядов синусового узла и скорости АВ-проведения. Эго подтверждается тем, что риск подобных аритмий снижается на фоне препаратов, уменьшающих парасимпатические влияния на сердце. Повышение автоматизма сердца под влиянием aдреналина и его аритмогенное действие эффективно подавляются β-адреноблокаторами, например пропранололом. В большинстве структур сердца имеются и α1-адренорецепторы; их активация приводит к удлинению рефрактерного периода и повышению силы сокращений.
Описаны нарушения ритма сердца у человека после случайного в/в введения адреналина в дозах, предназначенных для в/в введения. Возникали желудочковые экстрасистолы, за которыми следовала политопная желудочковая тахикардия или фибрилляция желудочков. Известен и адреналиновый отек легких. Под действием адреналина у здоровых лиц снижается амплитуда зубца Т. У животных при введении сравнительно высоких доз наблюдаются и другие изменения зубца Т и сегмента ST: зубецТ после снижения становится двухфазным, а сегмент ST отклоняется в ту или другую сторону от изолинии. Такие же изменения сегмента ST наблюдаются у больных ИБС со спонтанным или вызванным адреналином приступом стенокардии,а поэтому эти изменения приписывают ишемии миокарда. Кроме того, адреналин и другие катехоламины могут вызвать гибель кардиомиоцитов, особенно при в/в введении. Острые токсические эффекты адреналина проявляются контрактурным повреждением миофибрилл и другими патоморфологическими изменениями. В последнее время активно исследуется вопрос о том может ли длительная симпатическая стимуляция сердца (например, при сердечной недостаточности) вызвать апоптоз кардиомиоцитов.
ЖКТ, матка и мочевые пути. Влияние адреналина на разные гладкомышечные органы зависит от того, какие адренорецепторы в них преобладают (табл. 6.1). Действие его на сосуды имеет важнейшее физиологическое значение; влияния же на ЖКТ далеко не так существенна. Как правило, адреналин вызывает расслабление гладких мышц ЖКТ вследствие активации как α-, так и β-адренорецепторов. Тонус кишечника и частота его спонтанных сокращений снижаются. Желудок обычно расслабляется, а сфинктер привратника и ил и о цекальный сфинктер – сокращаются, однако эти эффекты зависят от исходного тонуса. Если этот тонус высокий, то адреналин вызывает расслабление, а если низкий – сокращение.
Дыхательная система. Влияние адреналина на дыхательную систему сводится главным образом к расслаблению гладких мышц бронхов. Мощное бронходилатируюшее действие адреналина еще больше усиливается в условиях бронхоспазма – возникающего, например, при приступе бронхиальной астмы или вследствие приема некоторых лекарственных средств. В таких случаях адреналин играет роль антагониста бронхоконстрикторных веществ, и его эффект может быть чрезвычайно сильным.
Эффективность адреналина при бронхиальной астме может быть связана также с подавлением вызванного антигенами высвобождения медиаторов воспаления из тучных клеток и, в меньшей степени, со снижением секреции трахеобронхиальных желез и с уменьшением отека слизистой. Подавление дегрануляиии тучных клеток обусловлено активацией β2-адренорепепторов, а влияния на слизистую бронхов – активацией а-адренореиепторов. Впрочем, при бронхиальной астме противовоспалительные эффекты таких веществ, как глюкокортикоиды и антагонисты лейкотриенов, гораздо сильнее.
ЦНС. Молекула адреналина достаточно полярная, поэтому он плохо проникает через гематоэнцефалический барьер и в терапевтических дозах психостимулирующего влияния не оказывает. Беспокойство, тревожность, головная боль и тремор, нередко возникающие при введении адреналина, объясняются скорее его влияниями на сердечно-сосудистую систему, скелетные мышцы и метаболизм; иными словами, они могут возникать вследствие психической реакции на характерные для стресса соматические и вегетативные проявления. Некоторые другие адренергические средства способны проникать через гематоэнцефалический барьер.
Метаболизм. Адреналин влияет на многие обменные процессы. Он повышает концентрации глюкозы и молочной кислоты в крови. Активация а2-адреноре-цепторов приводит к торможению выработки инсулина, а β2-адренорецепторов – наоборот; при действии адреналина преобладает тормозный компонент. Действуя на P-адренорецепторы α-клеток островков поджелудочной железы, адреналин стимулирует секрецию глюкагона. Он подавляет также захват глюкозы тканями, по меньшей мере частично – за счет торможения выработки инсулина, но также, возможно, за счет прямого действия на скелетные мышцы.
Источник
