Анализы при атеросклерозе сосудов головного мозга

Атеросклероз сосудов головного мозга – процесс образования атеросклеротических бляшек внутри церебральных сосудов, влекущий за собой расстройства мозгового кровоснабжения. Может иметь субклиническое течение или проявляться дисциркуляторной энцефалопатией, ТИА, инсультом. В диагностике используется РЭГ, УЗДГ, дуплексное сканирование или МРТ церебральных сосудов, а также электроэнцефалография, КТ и МРТ головного мозга. Терапия комбинированная с назначением гиполипидемических, антиагрегантных, ноотропных, нейрометаболических, сосудистых фармпрепаратов. При наличии показаний производится хирургическое лечение.
Общие сведения
Атеросклероз сосудов головного мозга составляет примерно пятую часть всей неврологической патологии и около половины сердечно-сосудистых заболеваний. Атеросклеротические процессы в церебральных сосудах могут стартовать уже в 20-30-летнем возрасте, однако, благодаря длительному субклиническому течению, манифестация заболевания обычно происходит после 50-ти лет. Клинические проявления церебрального атеросклероза связаны с постепенно развивающейся в результате поражения сосудов недостаточностью мозгового кровообращения и ишемией тканей мозга. Хроническая ишемия головного мозга, наряду с ишемической болезнью сердца, является наиболее тяжелым следствием атеросклероза. Она может выступать причиной таких осложнений как инсульт и деменция. Ввиду большой распространенности и высокой частоты осложнений атеросклероз сосудов головного мозга относится к самым приоритетным проблемам современной неврологии.
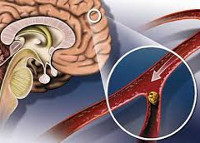
Атеросклероз сосудов головного мозга
Причины
Известен целый ряд факторов, способствующих развитию церебрального атеросклероза. К ним относят, прежде всего, возраст. С возрастом атеросклероз сосудов в той или иной степени наблюдается у всех. Более раннее развитие атеросклеротических изменений и более быстрое прогрессирование церебрального атеросклероза отмечается при несбалансированном питании (чрезмерное употребление жиров и углеводов, недостаточное количество растительной пищи, переедание, наличие в рационе жаренных и острых блюд и т. п.), нарушении обмена веществ (ожирение, сахарный диабет, гормональные сбои), гиподинамии, курении, частом приеме больших доз алкоголя.
Благоприятные условия для возникновения и прогрессирования атеросклероза формируются на фоне артериальной гипертензии. Зачастую атеросклероз и гипертоническая болезнь развиваются совместно, взаимно усугубляя друг друга. Хронические инфекции и интоксикации, оказывающие неблагоприятное воздействие на сосудистую стенку, также являются факторами, способствующими возникновению атеросклероза церебральных сосудов. Немаловажное значение имеет психоэмоциональное состояние, обуславливающее восприятие человеком различных жизненных событий. Отсутствие спокойного доброжелательного отношения приводит к тому, что многие ситуации становятся для человека стрессовыми. Стресс негативно воздействует на тонус стенок церебральных сосудов и вызывает перепад давления. Многочисленный повтор таких сосудистых изменений является благоприятной основой для развития церебрального атеросклероза.
Не все вопросы этиологии атеросклероза окончательно ясны. Существование большого количества предрасполагающих факторов наводит на мысль о полиэтиологичности этого процесса. Однако остается открытым вопрос, почему у одних пациентов наблюдается поражение преимущественно сердечных сосудов, а у других – церебральных. Необходимо также учитывать определенную роль наследственных механизмов, поскольку широко известны семейные случаи возникновения такого осложнения церебрального атеросклероза, как инсульт.
Патогенез
Основным фактором в механизме развития атеросклероза считается дисметаболизм липидов. В результате сбоя в обмене веществ происходит отложение холестерина липопротеидов низкой плотности (ЛПНП) на внутренней поверхности стенок церебральных сосудов. В процесс вовлекаются преимущественно артерии крупного и среднего калибра. Формирование т. н. атеросклеротической бляшки происходит стадийно – от жирового пятна до атерокальциноза. Образовавшаяся атеросклеротическая бляшка, увеличиваясь в размерах, постепенно все больше перекрывает просвет пораженного сосуда и может служить источником тромбоэмболов.
В первом случае из-за прогрессирующего уменьшения просвета сосуда происходит снижение кровоснабжения определенного участка головного мозга. В церебральных тканях этой зоны возникает гипоксия и нехватка питательных веществ – развивается хроническая ишемия, которая со временем приводит к дегенерации и гибели отдельных нейронов. Клинически этот процесс проявляется симптомами дисциркуляторной энцефалопатии (ДЭП). Выраженность последних зависит от распространенности атеросклероза, калибра пораженного сосуда, размеров атеросклеротической бляшки, степени развития альтернативного (коллатерального) кровоснабжения ишемизированной зоны мозга.
Во втором случае часть атеросклеротической бляшки отрывается от нее и в виде эмбола с током крови переносится в более мелкий артериальный сосуд, вызывая его внезапную и полную окклюзию (тромбоз). В зависимости от размеров зоны кровоснабжения окклюзированной артерии и степени развития сосудистых коллатералей возникает транзиторная ишемическая атака (ТИА) или ишемический инсульт. Более редко атеросклероз сосудов головного мозга выступает причиной геморрагического инсульта. Разрыв сосудистой стенки происходит из-за нарушения ее эластичности в месте образования атеросклеротических отложений и зачастую обусловлен высокой артериальной гипертензией.
Симптомы
Клинически атеросклероз сосудов головного мозга начинает проявляться, когда находящиеся внутри сосудов атеросклеротические бляшки перекрывают церебральный кровоток настолько, что возникает ишемия и развивается дисциркуляторная энцефалопатия. В соответствии с выраженностью расстройств церебрального кровообращения различают 3 стадии церебрального атеросклероза.
- Начальная стадия. Симптомы имеют преходящий характер, зачастую возникают при психоэмоциональных и физических перегрузках и исчезают в условиях отдыха. Имеет место астенический синдром: слабость, необычная утомляемость, повышенная раздражительность, вялость, сложности с концентрацией внимания. Возможны периодические нарушения сна в виде инсомнии и/или дневной сонливости, иногда возникающие головокружения. Отмечается некоторое снижение темпа мышления, способности запоминать и удерживать в памяти новую информацию. У многих пациентов в этот период на первый план выходит жалоба на головную боль, сочетающуюся с шумом в голове, ушах или одном ухе.
- Прогрессирующий церебральный атеросклероз. Усугубляются мнестические расстройства и психоэмоциональные изменения в характере. Снижается общий фон настроения, может развиться депрессия. Пациент становится мнительным и тревожным. Нарушения памяти становятся четко выраженными – пациент и его родственники говорят о том, что он не может запомнить события текущего дня, путает их. Шум в голове приобретает постоянный характер. Отмечается вестибулярная атаксия, нечеткость речи. Возможен тремор пальцев или головы, зачастую наблюдается снижение зрения и некоторая тугоухость. Постепенно теряется способность к продуктивной профессиональной деятельности.
- Деменция. Прогрессирует интеллектуальное снижение, наблюдаются провалы в памяти, нарушение речи, апатия, неряшливость, полное исчезновение интересов. Пациент утрачивает способность ориентироваться в обстановке и во времени, теряет навыки самообслуживания, требует присмотра.
Диагностика
В неврологическом статусе пациентов с церебральным атеросклерозом в зависимости от стадии заболевания может выявляться парез взора кверху, горизонтальный нистагм, некоторая анизорефлексия, симметричное повышение или вялость рефлексов, неустойчивость в позе Ромберга, тремор вытянутых пальцев рук, нарушение координаторных проб. После перенесенного инсульта возможно наличие парезов и другого неврологического дефицита. Офтальмоскопия, проведенная офтальмологом, может выявить атеросклеротические изменения сосудов сетчатки. При понижении слуха показана консультация отоларинголога с аудиометрией.

КТ головного мозга. На уровне турецкого седла выраженное атеросклеротическое обызвествление стенок интракраниальных сонных артерий с обеих сторон
Более точно диагностировать атеросклероз сосудов головного мозга позволяют сосудистые исследования. Наиболее доступным из них является РЭГ. Более информативны УЗДГ сосудов головы, дуплексное сканирование и МРТ сосудов головного мозга. Важное значение имеет проведение сосудистых исследований в динамике, оценка степени окклюзии сонных артерий и магистральных интракраниальных артерий. Для анализа функционального состояния мозга используется ЭЭГ, с целью визуализации церебральных тканей (особенно в ходе диагностики инсультов) – КТ и МРТ головного мозга.

КТ головного мозга. Обызвествление стенки интракраниальной части левой позвоночной артерии
Лечение
Вылечить церебральный атеросклероз невозможно, но путем своевременной, регулярной и комплексной терапии можно замедлить его прогрессирование. В первую очередь следует устранить факторы, усугубляющие развитие атеросклеротического процесса. Необходимо соблюдать растительную диету с исключением нутриентов с высоким содержанием холестерина (мясо, яйца, маргарин, рыбные консервы, колбаса, фастфуд), ввести ежедневные пешие прогулки, снизить психоэмоциональную нагрузку, исключить курение и прием спиртного, оптимизировать массу тела. Гипертоники нуждаются в тщательном подборе гипотензивного лечения. Важное значение имеет коррекция липидного спектра крови, которая назначается по результатам исследования содержания холестерина и липидов в крови. Назначаются гиполипидемические фармпрепараты: симвастатин, атромидин, флувастатин, гемфиброзил и др.
Патогенетическое лечение церебрального атеросклероза имеет целью улучшить метаболизм и кровоснабжение нейронов, повысить их устойчивость к условиям ишемии, предупредить тромбообразование, улучшить мнестические функции. В качестве антиагрегантной терапии назначается длительный прием тиклида или небольших доз ацетилсалициловой кислоты. Сосудистая терапия проводится препаратами пентоксифиллина и винпоцетина, нифедипином. Нейрометаболическое лечение включает назначение витаминов группы В, глицина, препаратов гингко билобы. Улучшению когнитивных способностей способствует прием ноотропов: пирацетама, пикамилона, ницерголина и пр.
Повторные ТИА, перенесенный малый инсульт, окклюзия сонных артерий с уменьшением ее просвета более чем на 70% являются показаниями к хирургическому лечению церебрального атеросклероза. Различают 2 вида операций: эндартерэктомия (удаление атеросклеротической бляшки вместе с участком интимы сосуда) и создание сосудистого шунта, идущего в обход обтурированного атеросклеротической бляшкой участка артерии. По показаниям нейрохирурги производят каротидную эндартерэктомию, формирование экстра-интракраниального анастомоза, протезирование брахиоцефального ствола и другие операции.
Прогноз
Прогноз церебрального атеросклероза весьма вариабелен. Многое зависит от возраста пациента, своевременности начатых лечебных мероприятий, возможности полностью устранить имеющиеся факторы риска. Наиболее тяжелыми осложнениями атеросклероза церебральных сосудов выступают инсульт и деменция, в результате которых происходит грубая инвалидизация пациента и возможен летальный исход.
Профилактика атеросклероза
Лучшей профилактикой атеросклероза любой локализации является здоровый образ жизни, подразумевающий разумные физические нагрузки, рациональное питание, пребывание на свежем воздухе, спокойный ритм жизни с адекватным чередованием труда и отдыха. Предупреждением развития атеросклеротического процесса является исключение из своей жизни всех факторов, способствующих его прогрессированию, в т. ч. недоброжелательных реакций (гнева, злости, обиды, раздражения и т. п.), которые провоцируют тонические изменения церебральных сосудов. Своевременное приведение в порядок своего образа жизни, адекватное лечение, при необходимости улучшение мозгового кровотока хирургическим путем – все эти мероприятия можно отнести к мерам вторичной профилактики церебрального атеросклероза, позволяющим избежать таких его осложнений, как инсульт и деменция.
Источник
Комплексное исследование для определения риска атеросклероза.
Синонимы русские
Лабораторные и генетические маркеры атеросклероза; анализы крови для оценки риска ИБС.
Синонимы английские
Laboratory and genetic risk factors for atherosclerosis; CAD risk assessment; Atherosclerosis Lab Panel.
Какой биоматериал можно использовать для исследования?
Буккальный (щечный) эпителий, венозную кровь.
Как правильно подготовиться к исследованию?
- Не принимать пищу в течение 12 часов до исследования, можно пить чистую негазированную воду.
- Исключить физическое и эмоциональное перенапряжение в течение 30 минут до исследования.
- Не курить в течение 30 минут до исследования.
Общая информация об исследовании
Для оценки риска атеросклероза и его клинических проявлений (инфаркта миокарда и других форм ишемической болезни сердца, инсульта, заболеваний периферических сосудов) используют несколько факторов. К так называемым традиционным факторам риска относятся возраст, отягощенный по ранней ИБС семейный анамнез, артериальная гипертензия, курение, сахарный диабет, ожирение, недостаточная физическая активность, стресс и повышение уровня холестерина крови (дислипидемия). В настоящий момент именно традиционные факторы включены в большинство калькуляторов для расчета риска ИБС. С другой стороны, появляются данные о том, что новые факторы могут иметь большее прогностическое значение. К таким новым, нетрадиционным, факторам относятся С-реактивный белок (СРБ), аполипопротеины А1 (апоА1) и B-100 (апоВ) и определенные полиморфизмы генов эндотелиальной синтазы и факторов свертывания крови V и II. Комплексное определение традиционных и новых факторов риска позволяет получить наиболее точную информацию об индивидуальной предрасположенности пациента к заболеваниям сердечно-сосудистой системы.
Развернутая лабораторная диагностика атеросклероза включает в себя:
1. Развернутая липидограмма.
Холестерол общий. Это холестерол всех липопротеинов крови, в том числе липопротеинов низкой, высокой, промежуточной и очень низкой плотности, а также холестерол, входящий в состав липопротеина (а). Это интегральный показатель обмена холестерола липопротеинами крови. Высокий уровень общего холестерола (более 240 мг/дл) – один из самых значимых факторов риска сердечно-сосудистых заболеваний. Концентрация общего холестерола не должна превышать 200 мг/дл.
Холестерол – липопротеины низкой плотности (ЛПНП). Это основные переносчики холестерола в крови. Из всего многообразия атерогенных липидных частиц именно ХС-ЛПНП имеет наибольшее значение в формировании коронарного риска. Оптимальная концентрация ХС-ЛПНП зависит от нескольких факторов, в том числе наличия ИБС, атеросклероза сосудов головного мозга и сахарного диабета, и различается в каждой конкретной ситуации. В общем случае желаемой считается концентрация ХС-ЛПНП менее 100 мг/дл.
Аполипопротеин B (апо B) – это основной белковый компонент атерогенных липопротеинов ЛПНП, ЛППП и ЛПОНП. Апо В необходим для связывания ЛПНП с его рецептором и, таким образом, обеспечивает транспорт холестерола в периферические ткани. Так как каждая их этих липопротеиновых частиц содержит только по одной молекуле апо В, то общая концентрация апо В в плазме крови отражает общее число атерогенных липопротеиновых частиц. Показано, что концентрация апо В может иметь большее прогностическое значение в отношении сердечно-сосудистых заболеваний, чем ХС-ЛПНП. Измерение апо В особенно важно при наличии гипертриглицеридемии (например, при метаболическом синдроме, сахарном диабете, заболеваниях печени и почек). Это связано с тем, что показатель ХС-ЛПНП получается не при прямом исследовании, а при расчете на основании концентрации триглицеридов, ХС-ЛПВП и общего холестерола и поэтому зависит от этих показателей. У пациентов с гипертриглицеридемией расчетный уровень ХС-ЛПНП не соответствует реальным значениям, что затрудняет его применение в качестве прогностического фактора. В отличие от ХС-ЛПНП, уровень апо В не зависит от концентрации триглицеридов.
Холестерол – липопротеины высокой плотности (ЛПВП). Обладают многими функциями, препятствующими развитию атеросклероза, в том числе обеспечивают обратный транспорт холестерола из периферических тканей в печень, препятствуют воспалению, окислению ЛПНП и образованию тромбов в сосудах. Считается, что высокий уровень холестерола ЛПВП снижает риск сердечно-сосудистых заболеваний. Показано, что повышение уровня холестерина ЛПВП на каждые 10 мг/л снижает риск сердечно-сосудистых заболеваний на 2-3 %.
Аполипопротеин А1 (апо А1) – это основной белковый компонент ЛПВП. Он необходим для осуществления обратного транспорта холестерина из периферических тканей. Концентрация апо А1 хорошо соотносится с концентрацией ХС-ЛПВП. Показано, что низкий уровень апоА1 может иметь большее прогностическое значение в отношении сердечно-сосудистых заболеваний, чем низкий уровень ХС-ЛПВП.
Триглицериды – эфиры органического спирта глицерола и жирных кислот, в форме которых энергия пищи запасается в жировой ткани и печени и транспортируется в клетки по мере необходимости. Основными переносчиками триглицеридов в крови являются хиломикроны и ЛПОНП. Повышение концентрации триглицеридов также является фактором риска сердечно-сосудистых заболеваний, однако не таким значительным, как повышение уровня холестерола. Оптимальным считается уровень триглицеридов менее 150 мг/дл.
2. С-реактивный белок.
С-реактивный белок (СРБ) – один из белков острой фазы воспаления, синтезируемый в печени. Концентрация СРБ отражает степень системного воспаления. Так, при острой инфекции или другом остром воспалении уровень СРБ обычно превышает 10 мг/л. Атеросклероз – это тоже воспалительный процесс, интенсивность которого, однако, гораздо меньше. Хроническое, вялотекущее воспаление в сосудистой стенке также приводит к повышению СРБ, но это повышение менее значительное (менее 3 мг/л). С помощью новых, более точных, методик удается определить такую низкую концентрацию СРБ. В недавних исследованиях показано, что повышенный уровень СРБ является фактором риска сердечно-сосудистых заболеваний. Учет этого клинико-лабораторного маркера особенно полезен у пациентов с промежуточным риском, рассчитанным на основании традиционных факторов риска. Показано, что при учете уровня СРБ 11 % мужчин из группы промежуточного риска могут быть переквалифицированы в группу высокого риска, а 12 % – в группу низкого риска.
3. Определение полиморфизма гена эндотелиальной синтазы
Синтаза оксида азота (NO-синтаза) – это фермент, катализирующий образование оксида азота NO из L-аргинина. В сосудистой стенке находится одна из изоформ фермента, называемая эндотелиальной синтазой (eNOS, NOS3). Оксид азота, образующийся благодаря NOS3, оказывает разностороннее воздействие на сосудистую стенку, в том числе обеспечивает расширение сосудов. Снижение нормальной функции NOS3 приводит к нарушению механизма вазодилатации и, возможно, таким образом участвует в патогенезе атеросклероза и сердечно-сосудистых заболеваний.
Снижение нормальной функции NOS3 может быть обусловлено внешними факторами (например, курение сигарет) или иметь генетическую основу. Показано, что определенные полиморфизмы гена NOS3 ассоциированы с повышенным риском сердечно-сосудистых заболеваний. Наибольшее клиническое значение имеют следующие полиморфизмы:
- NOS3G894T. Замена азотистого основания гуанина на тимин в позиции 894 кодирующей области гена приводит к замене остатка глутаминовой кислоты на аспарагиновую в положении 298 белковой последовательности эндотелиальной синтазы. Это сопровождается снижением активности фермента и в итоге снижением уровня оксида азота. Показано, что носительство аллеля T (гомозиготы T/T и гетерозиготы G/T) ассоциировано с повышенным риском артериальной гипертензии, ишемического инсульта, раннего инфаркта миокарда и других форм ИБС.
- NOS3T(-786)C. Замена азотистого основания тимина на цитозин в позиции -786 регуляторной области гена не влияет на белковую последовательность фермента, но значительно снижает уровень экспрессии гена и, как следствие, концентрацию фермента и оксида азота. Носительство аллеля C (гомозиготы С/С и гетерозиготы С/С) ассоциировано с вазоспазмом и повышенным риском ИБС.
Полиморфизмы NOS3 связаны с умеренным повышением риска сердечно-сосудистых заболеваний, которое не превосходит по силе традиционные факторы риска. Например, у гомозигот по аллелю T полиморфизма NOS3 G894T риск повышен в 1,3 раза (для сравнения высокий уровень ХС-ЛПНП ассоциирован с 3-кратным увеличением риска). Поэтому в настоящий момент генетически полиморфизмы рассматриваются в качестве дополнительных факторов риска.
4. Определение полиморфизма генов факторов свертывания крови V и II
Механизм свертывания крови представляет собой сложную систему взаимодействия факторов, обладающих про- и антикоагулянтными свойствами. Врождённые или приобретенные нарушения механизма коагуляции могут приводить к повышенному тромбообразованию.
Среди генетически обусловленных тромбофилий самой частой причиной является мутация в гене фактора VF5, так называемая Лейденовская мутация. Около 5 % населения являются носителями мутантного аллеля гена F5. Лейденовская мутация возникает в результате замены азотистого основания гуанин на аденин в позиции 1691 гена F5, что приводит к замене аргинина на глутамин в белковой последовательности фактора V. Измененный белок оказывается более устойчивым к расщеплению активированным белком C, что нарушает нормальную работу противосвертывающей системы крови и в итоге приводит к гиперкоагуляции. Риск тромбообразования повышен в 2-5 раз у гетерозигот по Лейденовской мутации и в 20-50 раз – у гомозигот.
Вторая по частоте встречаемости причина наследственной тромбофилии – мутация гена фактора 2 (протромбина) F2, представленная заменой азотистого основания гуанин на аденин в положении 20210 регуляторной области гена. Около 3 % населения являются носителями мутантного аллеля гена F2. У гетерозигот по аллелю A уровень протромбина повышен, что приводит к увеличению риска тромбоза в 3 раза. Нередко один и тот же пациент является носителем как Лейденовской мутации, так и мутации в гене протромбина.
Указанные полиморфизмы гена F5 и гена протомбина ассоциированы с повышенным риском венозных, но не артериальных тромбозов. Существуют и другие факторы, связанные с повышенным риском тромбообразования, в том числе повышенный уровень гомоцистеина, наличие антифосфолипидных антител, волчаночного антикоагулянта, дефицит протеина C, S и антитромбина III.
С помощью указанных лабораторных и генетических маркеров можно оценить индивидуальный риск развития сердечно-сосудистых заболеваний. Для оценки эффективности воздействия лечебных мероприятий на модифицируемые факторы риска может быть рекомендован повторный анализ.
Для чего используется исследование?
- Для оценки индивидуального риска сердечно-сосудистых заболеваний;
- для оценки эффективности лечебных мероприятий.
Когда назначается исследование?
- При профилактическом осмотре пациента;
- при обследовании пациента с факторами риска сердечно-сосудистых заболеваний (сахарный диабет, курение табака, гипертоническая болезнь, наличие родственника с преждевременной ишемической болезнью сердца, возраст > 45 лет у мужчин и > 55 лет у женщин);
- при лечении пациента с повышенным риском сердечно-сосудистых заболеваний.
Что означают результаты?
Референсные значения
Для каждого показателя, входящего в состав комплекса:
- [06-008] Аполипопротеин B
- [06-009] Аполипопротеин A 1
- [06-028] Холестерол – Липопротеины высокой плотности (ЛПВП)
- [06-029] Холестерол – Липопротеины низкой плотности (ЛПНП)
- [06-041] Триглицериды
- [06-048] Холестерол общий
- [06-050] С-реактивный белок, количественно (высокочувствительный метод)
- [18-030] Фактор свертываемости крови 5 (F5). Выявление мутации G1691A (Arg506Gln)
- [18-031] Фактор свертываемости крови 2, протромбин (F2). Выявление мутации G20210A (регуляторная область гена)
- [18-032] Эндотелиальная синтаза оксида азота (NOS3). Выявление мутации G894T (Glu298Asp)
- [18-033] Эндотелиальная синтаза оксида азота (NOS3). Выявление мутации T(-786)C (регуляторная область гена)
Важные замечания
- Результат анализа оценивается с учетом анамнестических, дополнительных лабораторных и инструментальных данных.
Также рекомендуется
[03-011] Фибриноген
[06-016] Гомоцистеин
[13-047] Антитела к кардиолипину, IgG и IgM
[03-004] Волчаночный антикоагулянт
Кто назначает исследование?
Кардиолог, терапевт, врач общей практики.
Источник
