Аномальные сосуды головного мозга
- Авторы
- Резюме
- Файлы
- Ключевые слова
- Литература
Суханова О.П. 1 Блинов И.М. 1 Семенютина А.С. 1 Атанов Н.Д. 1
1 ФГБОУ ВО «Ростовский государственный медицинский университет» Минздрава России
На основания изучения данных современной литературы уточнены основные этапы развития сосудов головного мозга в антенатальном периоде развития. Систематизированы имеющиеся сведения об аномалиях развития сосудов мозга (аномалия Киммерле, персистирующая тригеминальная артерия, фенестрация, аплазия и гипоплазия мозговых артерий, артериовенозные мальформации), совмещены с собственными данными СКТ ангиографии сосудов мозга. Мультиспиральная компьютерно-томографическая ангиография является необходимой для исследования сосудов большого мозга. Сравнение результатов исследования с нормальной анатомией сосудов головного мозга увеличит диагностическую и лечебную эффективность, позволит отличить варианты, мимикрирующие патологию, и те аномалии, которые нуждаются в оперативном хирургическом вмешательстве. А знание развития сосудов головного мозга способствует пониманию многих анатомических фактов и решению тяжелых клинических случаев.
эмбриональное развитие
аномалии сосудов мозга
мультиспиральная компьютерно-томографическая ангиография
1. Горбунов А.В. Классификация вариантов артерий и вариантов артериального круга большого мозга человека / А.В.Горбунов // Вестник Тамбовского университета. Серия: Естественные и технические науки.- 2013.- Т. 18, В. 1.- С.277-279.
2. Каплунова О.А., Фишман А.Ю., Пивоварова В.В. Морфогенез синусов твердой оболочки головного мозга. Журнал фундаментальной медицины и биологии, 2016, №2.-С.16-22.
3. Каплунова О.А., Чаплыгина Е.В., Домбровский В.И., Суханова О.П., Блинов И.М. Развитие внутримозговых сосудов и артериовенозные мальформации. Журнал анатомии и гистопатологии. 2015. Т.4, № 4 (16).-С.18-25.
4. Николенко В.Н. Морфобиомеханические закономерности строения средней мозговой артерии взрослых людей / В.Н. Николенко, О.А. Фомкина, Ю.А. Неклюдов, Ю.Д. Алексеев // Саратовский научно-медицинский журнал. – 2012.- Т 8, № 1. – С.9-14.
5. Фомкина О.А. Морфобиомеханические особенности задней соединительной артерии взрослых людей / О.А. Фомкина, В.Н. Николенко, Ю.А.Гладилин // Морфология.- 2010. -Т. 136, № 4. – С.202.
6. Труфанов Г.Е. Лучевая диагностика сосудистых мальформаций и артериальных аневризм головного мозга / Г.Е. Труфанов, Т.Е. Рамешвили, В.А. Фокин, Д.В. Свистов. СПб.: «ЭЛБИ СПб». 2005. 224 с.
7. Чаплыгина Е.В. Развитие, аномалии развития и варианты артерий головного мозга / Е.В.Чаплыгина, О.А.Каплунова, В.И. Домбровский, О.П. Суханова, И.М.Блинов, Л.И.Чистолинова // Журнал анатомии и гистопатологии, 2015.-Т.4, №2 (14).-С 52-59.
8. Чаплыгина Е.В., Каплунова О.А., Домбровский В.И., Суханова О.П., Блинов И.М. Персистирующая тригеминальная артерия. Фундаментальные исследования № 1 (часть 8) 2015, стр. 1730-1734.
9. Чаплыгина Е.В., Каплунова О.А., Домбровский В.И., Суханова О.П., Блинов И.М., Фишман А.Ю., Муканян С.С. Морфофункциональная характеристика аномалии Киммерле. Морфология, 2015, Т.147, №3, С.27-31.
10. Conway E.M. Molecular mechanisms of blood vessel growth / E.M. Conway, D. Collen, P.Carmeliet // Cardiovascular Res.- 2001.- V. 49. -P. 507-521.
11. Eichmann A. Vascular development: from precursor cells to branched arterial and venous networks / A. Eichmann, L. Yuan, D. Moyon F. Lenoble, L. Pardanaud, C. Breant // Int. J. Dev. Biol. 2005. V. 49. P. 259-267.
12. Elliot R. The Prevalence of Ponticus (Arcus Foramen) and its Importance in the Goel-Harms Procedure: -Analysis and Review of the Literature / R.Elliot, O.Tanweer // World Neurosurgery.-2014.-Vol. 82, 1/2.-P.335-343.
13. Kathuria S., Chen J., Gregg L., Parmar Y.A., Gandhi D. Congenital arterial and venous anomalies of the brain and skull Base. Neuroimag / S.Kathuria, J.Chen, L.Gregg, Y.A.Parmar, D. Gandhi // Clin. N. Am. -2011.- V. 21. -P. 545-562.
14. Niederberger E. Anatomic variants of the anterior part of the cerebral arterial circle at multidetector computed tomography angiography / E.Niederberger, J.-Y.Gauvrit, X.Morandi, B.Carsin-Nicol, T.Gauthier, J.-C. Ferre // J. of Neuroradiology. -2010. -V.37. -P. 139-147.
15. Padget D.N. The development of the cranial arteries in the human embryo / D.N. Padget // Contrib. Embryol. -1948. -V. 32. -P. 205-261.
16. Raybaud C. Normal and abnormal embryology and development of the intracranial vascular system / C. Raybaud // Neusurg. Clin. N. Am. -2010. -V. 21, N. 3. P. -399-426.
Врожденные сосудистые аномалии мозга: аплазия или гипоплазия нормальных сосудов, сосуды с ненормальной морфологией – результат раннего нарушения развития сосудов мозга. Некоторые из них компенсированы и клинически бессимптомны. Другие являются причиной заболеваний и смерти в результате кровоизлияний или ишемии [13]. Несмотря на большое количество работ, посвященных возрастной, половой, билатеральной изменчивости мозговых артерий [1, 4, 5], работы, касающиеся развития [10, 11, 15, 16] и аномалий развития сосудов головного мозга, – единичные [2, 3, 7, 8, 14].
Аномалия Киммерле – наиболее часто встречающаяся аномалия развития краниовертебральной зоны – костная перемычка над бороздой позвоночной артерии атланта, встречается у 12-16% людей [9, 12], является одним из факторов риска нарушения мозгового кровообращения, особенно при сочетании с другими аномалиями черепа, головного мозга или мозговых сосудов.
Цель исследования – на основания изучения данных литературы уточнить основные этапы развития сосудов головного мозга, возможные механизмы образования их аномалий и проиллюстрировать СКТ-ангиограммами из архива кафедры лучевой диагностики ФПК и ППС РостГМУ. СКТ-ангиография была выполнена на мультисрезовом спиральном рентгеновском компьютерном томографе «Brilliance 64 Slice» («Philips Medical Systems», Нидерданды) у 650 пациентов в возрасте от 14 до 70 лет.
Материалы и методы исследования. Проанализированы спиральные компьютерные ангиотомограммы, выполненные на мультисрезовом спиральном рентгеновском компьютерном томографе «Brilliance 64 Slice» («Philips Medical Systems», Нидерданды) у 650 пациентов в возрасте от 14 до 70 лет.
Результаты исследования и их обсуждение. При анализе СКТ-ангиограмм у 91 обследованного была выявлена аномалия Киммерле (14% случаев) с одной или с двух сторон, при этом костный канал для позвоночной артерии может быть частично или полностью замкнутым (рис.1).
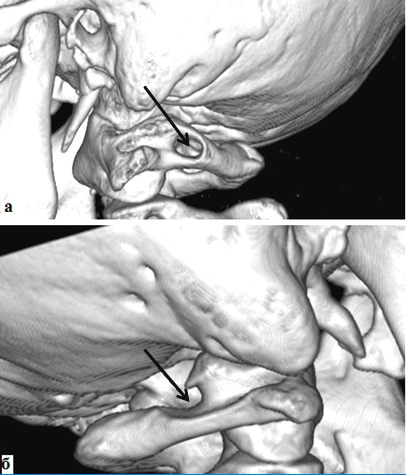
Рис. 1. Спиральная компьютерная томограмма шейного отдела позвоночного столба, а – вид слева, б – вид справа (SSD изображение оттененных поверхностей). Аномалия Киммерле. Костный канал для позвоночной артерии полностью замкнутый – (а) и частично замкнутый (б).
Известны основные принципы развития сосудов головного мозга [15, 16]. У эмбриона 4-5 мм длиной на 28-й день эмбриогенеза сонные артерии снабжают передний и средний мозг. Ромбовидный мозг снабжается через транзитные каротидно-базилярные анастомозы: тригеминальную, ушную, подъязычную и проатлантовую артерии. Эти артерии существуют короткое время [13]. Редко они могут персистировать и функционировать как анатомические варианты или мальформации в клинических случаях.
При проведении спиральной компьютерной ангиографии нами была обнаружена персистирующая тригеминальная артерия (рис.2) у 4 пациентов (0,6 % случаев).
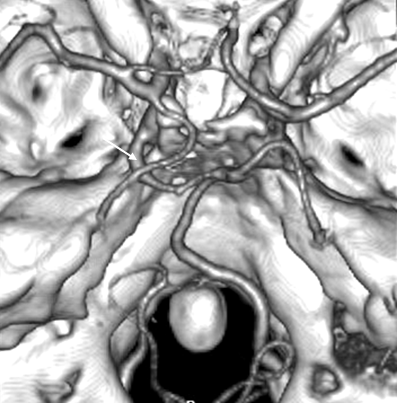
Рис. 2. СКТ ангиограмма сосудов основания мозга, вид сверху (ISSD – изображение оттененных поверхностей). Примитивная тригеминальная артерия слева (показана стрелкой). Задняя трифуркация левой внутренней сонной артерии. Гипоплазия левой позвоночной артерии.
Ангиогенез артерий мозга начинается из поверхностной лептоменингеальной сети. Многие артерии мозга образуются в результате слияния элементов сосудистой сети. Нарушение этого процесса может быть причиной фенестрации, которая характеризуется частичными просветами между 2 отчетливыми, параллельными артериями, покрытыми эндотелием. Аномалия бессимптомна, но подобно артериальным бифуркациям, склонна к образованию аневризм [13].
При выполнении СКТ ангиографии фенестрация мозговых артерий нами была выявлена в 0,03% случаев.
В процессе развития артерий головного мозга из переднего сосудистого сплетения появляются три передние мозговые артерии. Третья артерия следует курсом двух передних мозговых артерий и известна как срединная артерия мозолистого тела. Срединная артерия мозолистого тела и переднее сосудистое сплетение далее регрессируют [15]. Такая аномалия развития как добавочная передняя мозговая артерия является персистирующей срединной артерией мозолистого тела.
На 29-й день эмбриогенеза каудальная часть внутренней сонной артерии соединяется с билатеральной продольной мозговой артерией, образуя заднюю соединительную артерию. Продольные мозговые артерии начинают в краниокаудальном направлении сливаться, формируя примитивную базилярную артерию, а на 32 день позвоночные артерии начинают формировать продольный анастомоз между шейными межсегментарными артериями [15].
«Классическое» строение Виллизиева круга встречается часто, но существует большое количество вариантов его строения [1, 4, 5, 7]. Основные аномалии мозговых артерий: аплазия, гипоплазия. Наиболее часто встречаются варианты нетипичного ответвления артерий, с асимметрией диаметров и разомкнутый круг. Возможны и разнообразные сочетания вариантов и аномалий развития артерий большого мозга.
По данным Горбунова А.В. [1], большинство часто встречающихся аномалий базилярной артерии следующие: девиация (4,5% случаев), изгиб (0,6% случаев), извитость (1,9% случаев), удвоение при неслиянии (1,9% случаев), возможны и их сочетании. Нарушение соединения базилярных артерий может проявляться фенестрациями [7].
Наиболее часто встречающиеся аномалии внутричерепного отдела позвоночной артерии по данным Горбунова А.В. [1]: гипоплазия (10,9% случаев), избыточная извитость (0,6% случаев), S-образная позвоночная артерия (0,6% случаев), возможны и их сочетания.
Ангиогенез вен мозга, также как и артерий, начинается из поверхностной лептоменингеальной сети. Развитие сосуда в артерию, вену или в капилляр зависит от направления кровотока. Экспериментально доказана большая роль сигнальных молекул в артериовенозной дифференцировке и развитии архитектоники внутримозговых сосудов [11].
Артериовенозные мальформации головного мозга – наиболее часто встречающиеся сосудистые аномалии. Образование АВМ объясняют недостаточностью развития капиллярного участка кровеносной системы [6].
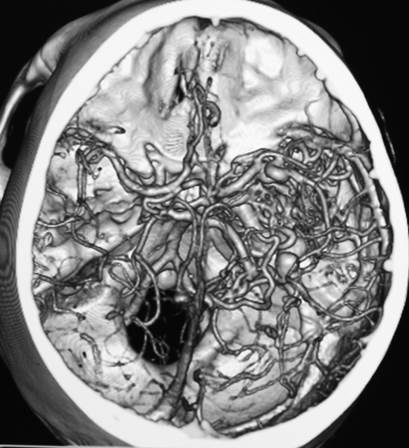
Типичные артериовенозные мальформации представлены тремя основными компонентами: приносящими артериями, клубком измененных сосудов мальформации и дренирующими венами [3, 6]. Артериовенозные мальформации представляют собой неправильное соединение артериальных и венозных сосудов, формирующих клубок, минуя капиллярную сеть (рис.3).

Рис. 3. СКТ ангиограмма сосудов мозга, вид сверху (SSD – изображение оттененных поверхностей). Артериовенозная мальформация в правой височной доле мозга. Питание АВМ осуществляется из бассейна правой средней мозговой мозговой артерии, оболочечных артерий и правой задней мозговой артерии; сброс крови – через множественные расширенные оболочечные вены.
На основания анализа данных литературы и собственных данных спиральной компьютерной ангиографии сосудов мозга установлено, что чаще встречаются артериовенозные мальформации глубинно расположенные в полушариях большого мозга, преимущественно в лобных, теменных, реже – в височных долях. Артериовенозные мальформации имеют форму пирамид, с основанием, расположенным параллельно поверхности коры, и вершиной, направленной к желудочку.
Заключение
Мультиспиральная компьютерно-томографическая ангиография является необходимой для исследования сосудов большого мозга. Сравнение результатов исследования с нормальной анатомией сосудов головного мозга увеличит диагностическую эффективность, позволит отличить варианты, мимикрирующие патологию, и те аномалии, которые нуждаются в хирургическом вмешательстве. А знание развития сосудов мозга способствует пониманию многих анатомических фактов.
Библиографическая ссылка
Суханова О.П., Блинов И.М., Семенютина А.С., Атанов Н.Д. АНОМАЛИИ РАЗВИТИЯ СОСУДОВ ГОЛОВНОГО МОЗГА // Международный студенческий научный вестник. – 2017. – № 1.;
URL: https://eduherald.ru/ru/article/view?id=16848 (дата обращения: 02.06.2021).
Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)
Источник
Артериовенозная мальформация (АВМ) головного мозга – это локальный дефект архитектоники внутричерепных сосудов, при котором формируется беспорядочное соединение между артериями и венами с образованием извитого сосудистого клубка. Патология возникает вследствие ошибки морфогенеза, а потому в основном является врожденной. Может быть одиночной или распространенной.
При мозговой АВМ кровоток осуществляется аномально: кровь из артериального бассейна прямиком, обходя капиллярную сеть, перебрасывается в венозную магистраль. В зоне мальформации отсутствует нормальная промежуточная капиллярная сеть, а связующий узел представлен фистулами или шунтами в количестве 1 и более единиц. Стенки артерий дегенерированы и не имеют надлежащего мышечного слоя. Вены, как правило, расширены и истончены по причине нарушенной ауторегуляции мозгового кровотока.
АВМ головного мозга, как и аневризмы, опасны внезапным внутримозговым кровоизлиянием, которое возникает вследствие разрыва стенки патологического сосуда. Разорвавшаяся мальформация чревата ишемией мозга, отеком, гематомой, прогрессией неврологического дефицита, что не всегда для больного заканчивается благополучно.
Статистика заболеваемости и последствий патологии
Артериовенозная мальформация в структуре всех патологий с объемными образованиями в тканях головного мозга в среднем составляет 2,7%. В общей статистике острых нетравматических геморрагий в субарахноидальное пространство, 8,5%-9% случаев кровоизлияний происходят по причине мальформаций. Инсультов головного мозга – 1%.
Встречаемость заболевания происходит со следующей средней частотой в год: 4 случая на 100 тыс. населения. Некоторые зарубежные авторы указывают другую цифру – 15-18 случаев. Несмотря на врожденную природу развития, клинически проявляется только у 20%-30% детей. Причем возрастной пик обнаружения АВМ ГМ у детей приходится на младенчество (≈13,5%) и возраст 8-9 лет (столько же %). Считается, что у ребенка с таким диагностированным сосудистым нарушением риски разрыва гораздо выше.
Видео ангиографии:
По статистике, мальформации проявляют себя по большей мере в возрасте 30-40 лет, поэтому диагностируются чаще у людей именно этой возрастной группы. Заболевание обычно протекает скрыто в течение десятков лет, чем и объясняется такая тенденция его определения далеко не в детские годы. Половой закономерности в развитии церебральных АВМ у мужского и женского пола пациентов не обнаружено.
При наличии мальформации ГМ вероятность разрыва составляет от 2% до 5% в год, с каждым последующим годом риски увеличиваются. Если кровоизлияние уже состоялось, риск его повторного рецидива существенно возрастает, вплоть до 18%.
Летальные исходы из-за внутричерепного кровоизлияния, которое часто является первым проявлением болезни (в 55%-75% случаев), случаются у 10%-25% пациентов. Смертность вследствие разрыва, согласно исследованиям, больший процент имеет у детей (23%-25%), чем у взрослых людей (10%-15%). Инвалидизация от последствий заболевания отмечается у 30%-50% больных. Примерно к 10%-20% пациентов возвращается полноценное или приближенное к норме качество жизни. Причина такой грозной тенденции заключается в поздней диагностике, несвоевременном получении квалифицированной медицинской помощи.
В какой части головы локализируются АВМ головного мозга?
Распространенная локализация артериовенозной аномалии – это супратенториальное пространство (верхние отделы мозга), проходящее над палаткой мозжечка. Чтобы было понятнее, изъяснимся проще: сосудистый дефект примерно в 85% случаев обнаруживается в больших полушариях. Преобладают поражения сосудистых звеньев теменной, лобной, затылочной, височной долей больших полушарий.
В целом, АВМ могут располагаться в любом полюсе головного мозга, причем как в поверхностных частях, так и глубинных слоях (таламусе и др.). Достоверно определить точную локализацию очага возможно только после прохождения аппаратного исследования с возможностями визуализации мягких тканей. К базовым принципам диагностики относят МРТ и метод ангиографии. Эти методы позволяют качественно оценить порядок ветвления артерий и построение вен, их соединение между собой, калибр ядра АВМ, афференты артерий, дренирующие вены.
Причины развития артериовенозного порока и симптомы
Заболевание является врожденным, поэтому анормальная закладка сосудов в определенных зонах мозга происходит в ходе внутриутробного периода. Достоверные причины развития патологии до текущего момента так и не установлены. Но, по словам специалистов, на аномальное строение сосудистой системы ГМ у плода предположительно могут способствовать негативные факторы в течение беременности:
- получение организмом матери высоких доз радиации;
- внутриутробные инфекции, передающиеся в дородовом периоде от матери к ребенку;
- хронические или острые интоксикации;
- курение и прием алкогольных напитков;
- наркотические средства, в том числе из ряда медикаментов;
- лекарственные препараты, обладающие тератогенным действием;
- хронические болезни у беременной в анамнезе (клубочковый нефрит, диабет, бронхиальная астма, пр.).
Специалисты также полагают, что в формировании порока может играть роль и генетический фактор. Наследственность до недавнего времени не воспринималась как причина патологии серьезно. Сегодня же все больше поступает сообщений о причастности и данного фактора. Так, в ряде случаев у кровных родственников больного определяются аналогичного типа сосудистые пороки. Предположительно их вызывает передающаяся по наследству генная мутация, затрагивающая хромосому 5q, локус СМС1 и RASA1.
МРТ.
Как было сказано ранее, для заболевания характерно продолжительное «немое» течение, которое может продолжаться десятилетиями. О диагнозе либо узнают случайно в момент диагностического обследования структур головного мозга, либо уже после случившегося разрыва мальформации. В немногочисленных вариантах болезнь может давать о себе знать до того как лопнет сосуд. Тогда клиника патологии чаще проявляется такими симптомами, как:
- шум в ушах (звон, гул, шипение и т.п.);
- частые головные боли;
- судорожный синдром, который схож с эпилептическими приступами;
- неврологические симптомы (парестезии, ощущения онемения, покалывания, вялость и апатия, пр.).
Клиническая картина при разрыве АВМ подобна всем типам внутричерепных кровоизлияний:
- резкое появление сильной головной боли, быстро прогрессирующей;
- головокружение, спутанность сознания;
- обмороки, вплоть до развития комы;
- тошнота, рвота;
- выпадение чувствительности половины тела;
- нарушение зрения, слуха;
- экспрессивная афазия, дизартрия (нарушения произношения);
- быстро нарастающий неврологический дефицит.
У детей заболевание зачастую проявляется отставанием в психическом развитии, задержкой речевых функций, эпиприступами, симптомами сердечной недостаточности, когнитивными нарушениями.
Виды церебральных мальформаций венозно-артериального русла
Патологические образования принято различать по топографо-анатомическому признаку, гемодинамической активности, размерам. Первый параметр характеризует место расположения мальформации в головном мозге, отсюда происходят их названия:
- поверхностные АВМ – сосредоточены в коре больших полушарий мозга (на поверхности мозга) и прилежащих структурах белого вещества;
- глубинные АВМ – локализуются в глубине мозговых извилин, базальных ганглиях, внутри желудочков, в структурах ствола ГМ.
По гемодинамической активности выделяют мальформации:
- активные – к ним причисляют смешанного вида АВМ ГМ (самая частая разновидность, при которой обнаруживается частичная деструкция капилляров) и фистулезного типа (артерия прямо переходит в вену, капиллярная сеть полностью разрушена);
- неактивные – капиллярные (телеангиоэктазии), венозные, артериовенозные кавернозные.
Поражение также оценивается по размерам, учитывается диаметр только клубка мальформации. При диагностике размеров используют следующие наименования АВМ:
- микромальформации – менее 10 мм;
- малые – от 10 мм до 20 мм;
- средние – 20-40 мм
- большие – 40-60 мм
- гигантские – более 6 см в диаметре.
Для предупреждения тяжелой геморрагии и связанных с ней необратимых осложнений крайне важно выявить и устранить очаг в ближайшее время, до разрыва. Почему? Объяснение куда более убедительное – при разрывах слишком большой процент людей погибает (до 75% пациентов) от обширного кровоизлияния, несопоставимого с жизнью.
Необходимо понимать, что сосуды АВМ слишком подвержены прорывам, так как они серьезно истощены на почве ненормального строения и нарушенного тока крови. Одновременно с этим, крупные порочные образования сдавливают и повреждают окружающие мозговые ткани, что несет дополнительную угрозу состоятельности функций ЦНС. Поэтому, если диагноз подтвержден клинически, оттягивать с лечением ни в коем случае нельзя.
Методы лечения мальформаций сосудов головного мозга
Терапия заключается в полной резекции или полноценной облитерации сосудистого дефекта хирургическим путем. Существует 3 вида высокотехнологичных операций, которые применяются в этих целях: эндоваскулярное лечение, стереотаксическая радиохирургия, микрохирургическое вмешательство.
- Эндоваскулярная операция. Метод подходит для лечения глубоко расположенных и крупных образований. Вмешательство выполняется под рентгенологическим контролем, анестезиологическое обеспечение – наркоз общего типа. Эта малоинвазивная тактика нередко является начальным этапом лечения перед предстоящей открытой операцией.
- К патологической части головного мозга через бедренную артерию по сосудам подводят тонкую трубочку катетера.
- Через установленный проводник в область мальформации подается специальный клеевый биоматериал, похожий на монтажную пену.
- Нейрохирург пенным составом перекрывает участки поражения, то есть тромбирует аномально развитые сосуды при сохранении здоровых.
- Эмболизация позволяет «выключить» патологическое сплетение из общей системы мозгового кровообращения.
- После выполненной операции под стационарным наблюдением пациент обычно находится 1-5 суток.
- Стереотаксическая радиохирургия. Лечебная тактика хоть и относится к ангионейрохирургии, но не является травматичной. Это означает, что никаких разрезов, введения внутрисосудистых зондов вообще не будет. Подходит для лечения сосудистого порока небольших размеров (до 3,5 см) или в том случае, когда очаг расположен в неоперабельной секции мозга.
- Радиохирургия предполагает разрушение ангиом системами вида Кибер-нож или Гамма-нож.
- Аппараты работают по принципу прицеленного воздействия на аномалию радиоактивным облучением.
- Лучи испускаются с разных сторон и сходятся в одной точке только дефектной зоны, здоровые структуры не затрагиваются. В результате сосуды АВМ срастаются, очаг подавляется.
- На Кибер- или Гамма-ноже процедуры абсолютно безболезненные, во время лечения пациент находится в сознании. Аппараты, на кушетке которых нужно будет просто неподвижно лежать (от 30 минут до 1,5 часов), напоминают традиционные томографы.
- При лечении Гамма-ножом на голову надевается специальный шлем и жестко фиксируется. Чтобы пациент, которому ставят шлем, не испытывал чувства дискомфорта, делают поверхностное местное обезболивание отдельных участков головы. Операция на Кибер-ноже не требует анестезии и помещения головы в жесткую конструкцию.
- В госпитализации нет необходимости. Но возможно понадобится пройти не один сеанс радиохирургии, чтобы окончательно ликвидировать остаточные явления АВМ ГМ. Иногда процесс облитерации длится 2-4 года.
- Прямое микрохирургическое удаление. Микрохирургия при данном диагнозе – единственный метод, который дает максимально высокие шансы на радикальное излечение патологии, сведение до минимума рисков рецидива. Является «золотым стандартом» в лечении данного заболевания с поверхностной локализацией и компактными формами узла.
- Микрохирургическая операция не обходится без типичной краниотомии, обязательно выполняется экономное вскрытие черепа для проведения основных хирургических манипуляций на мозге.
- Вмешательство проходит под общей эндотрахеальной анестезией, под контролем сверхмощного интраоперационного микроскопа и ультразвукового оборудования.
- Для предотвращения кровяного сброса по питающему артериальному сосуду и вене применяется метод биполярной коагуляции, то есть осуществляется прижигание.
- Далее единым блоком через трепанационное окно производится одномоментное иссечение всего тела мальформации с минимальными кровопотерями.
- В конце операционного сеанса отверстие в черепе закрывается костным лоскутом, на кожные покровы накладывается шов.
- Выписка возможна ориентировочно через 14 суток после операции. Далее нужно продолжить послеоперационное восстановление в специализированном центре реабилитации. Продолжительность реабилитации устанавливается индивидуально.
Видео открытой операции можно посмотреть по ссылке: https://www.youtube.com/watch?v=WA2FTX1NK1Y
В определенных ситуациях невозможно сразу приступить к прямой микрохирургии ввиду высоких интраоперационных рисков, особенно при АВМ больших размеров. Или же другой вариант: ангиома после стереотаксии или катетерной эмболизации лишь частично компенсирована, что крайне плохо. Поэтому иногда целесообразно обращаться к поэтапному лечению, используя последовательную комбинацию нескольких ангионейрохирургических методов.
Где лучше оперироваться и цены операции
Грамотно спланированный алгоритм лечебных действий поможет полностью удалить сосудистый конгломерат не в ущерб жизненно важным тканям. Адекватность терапии с учетом принципа индивидуальности убережет от прогрессии неврологических отклонений, возможного раннего рецидива со всеми вытекающими последствиями.
Оперировать высший орган ЦНС, который отвечает за множество функций в организме (двигательные способности, память, мышление, речь, обоняние, зрение, слух и пр.), следует доверять мирового уровня нейрохирургам. Кроме того, медучреждение должно быть снаряжено широкой базой высокотехнологичного интраоперационного оборудования передового образца.
В зарубежных странах с высокоразвитой нейрохирургией услуги стоят дорого, зато там, что называется, возвращают пациентов к жизни. Среди популярных направлений, одинаково продвинутых в хирургии головного мозга, выделяют Чехию, Израиль и Германию. В чешских клиниках цены на медицинскую помощь по поводу артериовенозных мальформаций самые низкие. Невысокая стоимость, совершенная квалификация чешских врачей-нейрохирургов сделали Чехию самым востребованным направлением. В это государство стремятся попасть не только пациенты из России и Украины, но и Германии, Израиля, других стран. И коротко о ценах.
Центральный военный госпиталь г.Прага.
| Метод хирургии | Россия (руб.) | Чехия (евро) | Германия, Израиль (евро) |
| Операция на CyberKnife или GammaKnife | от 200000 | 8000-12000 | от 20000 |
| Эндоваскулярное вмешательство | от 75000 | до 8000 | от 15000 и более |
| Микрохирургическая резекция | 150000-250000 | 7000-10000 | 13000-18000 |
Источник
