Чему равно давление газа в первом сосуде
Давление является одним из трех основных термодинамических макроскопических параметров любой газовой системы. В данной статье рассмотрим формулы давления газа в приближении идеального газа и в рамках молекулярно-кинетической теории.
Идеальные газы
Каждый школьник знает, что газ является одним из четырех (включая плазму) агрегатных состояний материи, в котором частицы не имеют определенных положений и движутся хаотичным образом во всех направлениях с одинаковой вероятностью. Исходя из такого строения, газы не сохраняют ни объем, ни форму при малейшем внешнем силовом воздействии на них.
В любом газе средняя кинетическая энергия его частиц (атомов, молекул) больше, чем энергия межмолекулярного взаимодействия между ними. Кроме того, расстояния между частицами намного превышают их собственные размеры. Если молекулярными взаимодействиями и размерами частиц можно пренебречь, тогда такой газ называется идеальным.
В идеальном газе существует лишь единственный вид взаимодействия – упругие столкновения. Поскольку размер частиц пренебрежимо мал в сравнении с расстояниями между ними, то вероятность столкновений частица-частица будет низкой. Поэтому в идеальной газовой системе существуют только столкновения частиц со стенками сосуда.
Все реальные газы с хорошей точностью можно считать идеальными, если температура в них выше комнатной, и давление не сильно превышает атмосферное.
Причина возникновения давления в газах
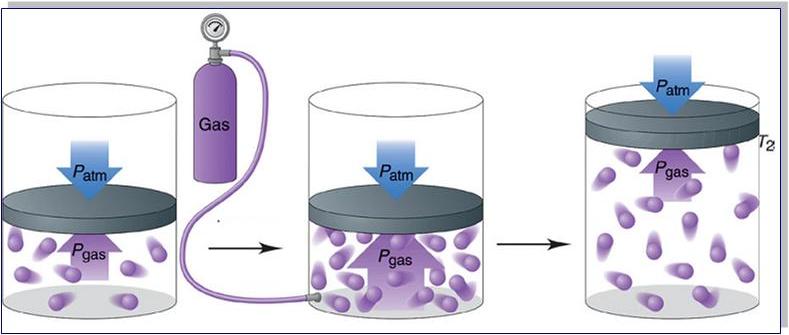
Прежде чем записать формулы расчета давления газа, необходимо разобраться, почему оно возникает в изучаемой системе.
Согласно физическому определению, давление – это величина, равная отношению силы, которая перпендикулярно воздействует на некоторую площадку, к площади этой площадки, то есть:
P = F/S
Выше мы отмечали, что существует только один единственный тип взаимодействия в идеальной газовой системе – это абсолютно упругие столкновения. В результате них частицы передают количество движения Δp стенкам сосуда в течение времени соударения Δt. Для этого случая применим второй закон Ньютона:
F*Δt = Δp
Именно сила F приводит к появлению давления на стенки сосуда. Сама величина F от столкновения одной частицы является незначительной, однако количество частиц огромно (≈ 1023), поэтому они в совокупности создают существенный эффект, который проявляется в виде наличия давления в сосуде.
Формула давления газа идеального из молекулярно-кинетической теории
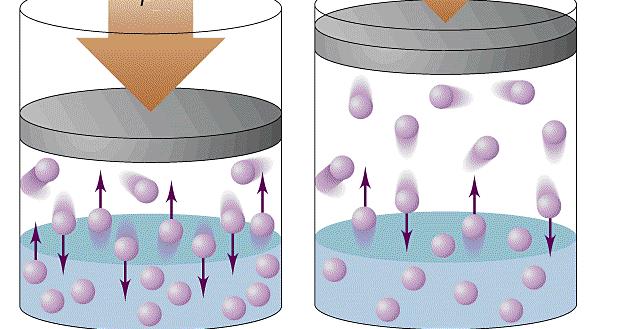
При объяснении концепции идеального газа выше были озвучены основные положения молекулярно-кинетической теории (МКТ). Эта теория основывается на статистической механике. Развита она была во второй половине XIX века такими учеными, как Джеймс Максвелл и Людвиг Больцман, хотя ее основы заложил еще Бернулли в первой половине XVIII века.
Согласно статистике Максвелла-Больцмана, все частицы системы движутся с различными скоростями. При этом существует малая доля частиц, скорость которых практически равна нулю, и такая же доля частиц, имеющих огромные скорости. Если вычислить среднюю квадратичную скорость, то она примет некоторую величину, которая в течение времени остается постоянной. Средняя квадратичная скорость частиц однозначно определяет температуру газа.
Применяя приближения МКТ (невзаимодействующие безразмерные и хаотично перемещающиеся частицы), можно получить следующую формулу давления газа в сосуде:
P = N*m*v2/(3*V)
Здесь N – количество частиц в системе, V – объем, v – средняя квадратичная скорость, m – масса одной частицы. Если все указанные величины определены, то, подставив их в единицах СИ в данное равенство, можно рассчитать давление газа в сосуде.
Формула давления из уравнения состояния

В середине 30-х годов XIX века французский инженер Эмиль Клапейрон, обобщая накопленный до него экспериментальный опыт по изучению поведения газов во время разных изопроцессов, получил уравнение, которое в настоящее время называется универсальным уравнением состояния идеального газа. Соответствующая формула имеет вид:
P*V = n*R*T
Здесь n – количество вещества в молях, T – температура по абсолютной шкале (в кельвинах). Величина R называется универсальной газовой постоянной, которая была введена в это уравнение русским химиком Д. И. Менделеевым, поэтому записанное выражение также называют законом Клапейрона-Менделеева.
Из уравнения выше легко получить формулу давления газа:
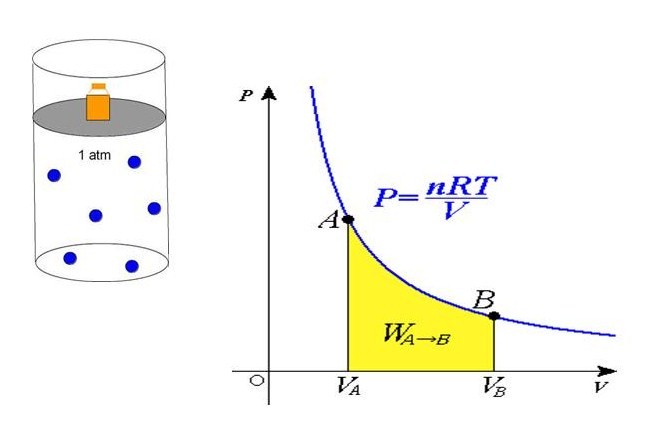
P = n*R*T/V
Равенство говорит о том, что давление линейно возрастает с температурой при постоянном объеме и увеличивается по гиперболе с уменьшением объема при постоянной температуре. Эти зависимости отражены в законах Гей-Люссака и Бойля-Мариотта.

Если сравнить это выражение с записанной выше формулой, которая следует из положений МКТ, то можно установить связь между кинетической энергией одной частицы или всей системы и абсолютной температурой.
Давление в газовой смеси
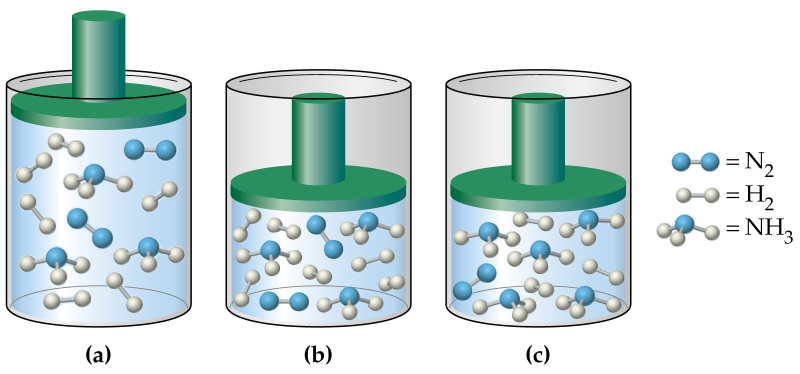
Отвечая на вопрос о том, как найти давление газа и формулы, мы ничего не говорили о том, является ли газ чистым, или речь идет о газовой смеси. В случае формулы для P, которая следует из уравнения Клапейрона, нет никакой связи с химическим составом газа, в случае же выражения для P из МКТ эта связь присутствует (параметр m). Поэтому при использовании последней формулы для смеси газов становится непонятным, какую массу частиц выбирать.
Когда необходимо рассчитать давление смеси идеальных газов, следует поступать одним из двух способов:
- Рассчитывать среднюю массу частиц m или, что предпочтительнее, среднее значение молярной массы M, исходя из атомных процентов каждого газа в смеси;
- Воспользоваться законом Дальтона. Он гласит, что давление в системе равно сумме парциальных давлений всех ее компонентов.
Пример задачи
Известно, что средняя скорость молекул кислорода составляет 500 м/с. Необходимо определить давление в сосуде объемом 10 литров, в котором находится 2 моль молекул.
Ответ на задачу можно получить, если воспользоваться формулой для P из МКТ:
P = N*m*v2/(3*V)
Здесь содержатся два неудобных для выполнения расчетов параметра – это m и N. Преобразуем формулу следующим образом:
m = M/NA;
n = N/NA;
m*N = M*n;
P = M*n*v2/(3*V)
Объем сосуда в кубических метрах равен 0,01 м3. Молярная масса молекулы кислорода M равна 0,032 кг/моль. Подставляя в формулу эти значения, а также величины скорости v и количества вещества n из условия задачи, приходим к ответу: P = 533333 Па, что соответствует давлению в 5,3 атмосферы.
Источник
Опубликовано 1 год назад по предмету
Физика
от kakadu44
Не тот ответ, который вам нужен?
Найди нужный
Самые новые вопросы
Математика – 9 месяцев назад
Сколько здесь прямоугольников
История – 1 год назад
Какое управление было в древнейшем риме? как звали первого и последнего из царей рима?
Литература – 1 год назад
Уроки французского ответе на вопрос : расскажите о герое по следующему примерному плану: 1.почему мальчик оказался в райцентре ? 2.как он чувствовал себя на новом месте? 3.почему он не убежал в деревню? 4.какие отношения сложились у него с товарищами? 5.почему он ввязался в игру за деньги? 6.как характеризуют его отношения с учительницей ? ответе на эти вопросы пожалуйста ! сочините сочинение пожалуйста
Русский язык – 1 год назад
Помогите решить тест по русскому языку тест по русскому языку «местоимение. разряды местоимений» для 6 класса
1. укажите личное местоимение:
1) некто
2) вас
3) ни с кем
4) собой
2. укажите относительное местоимение:
1) кто-либо
2) некоторый
3) кто
4) нам
3. укажите вопросительное местоимение:
1) кем-нибудь
2) кем
3) себе
4) никакой
4. укажите определительное местоимение:
1) наш
2) который
3) некий
4) каждый
5. укажите возвратное местоимение:
1) свой
2) чей
3) сам
4) себя
6. найдите указательное местоимение:
1) твой
2) какой
3) тот
4) их
7. найдите притяжательное местоимение:
1) самый
2) моего
3) иной
4) ничей
8. укажите неопределённое местоимение:
1) весь
2) какой-нибудь
3) любой
4) этот
9. укажите вопросительное местоимение:
1) сколько
2) кое-что
3) она
4) нами
10. в каком варианте ответа выделенное слово является притяжательным местоимением?
1) увидел их
2) её нет дома
3) её тетрадь
4) их не спросили
Русский язык – 1 год назад
Переделай союзное предложение в предложение с бессоюзной связью.
1. океан с гулом ходил за стеной чёрными горами, и вьюга крепко свистала в отяжелевших снастях, а пароход весь дрожал.
2. множество темноватых тучек, с неясно обрисованными краями, расползались по бледно-голубому небу, а довольно крепкий ветер мчался сухой непрерывной струёй, не разгоняя зноя
3. поезд ушёл быстро, и его огни скоро исчезли, а через минуту уже не было слышно шума
Русский язык – 1 год назад
помогите прошу!перепиши предложения, расставляя недостающие знаки препинания. объясни, что соединяет союз и. если в предложении один союз и, то во втором выпадающем списке отметь «прочерк».пример:«я шёл пешком и,/поражённый прелестью природы/, часто останавливался».союз и соединяет однородные члены.ночь уже ложилась на горы (1) и туман сырой (2) и холодный начал бродить по ущельям.союз и соединяет:1) части сложного предложенияоднородные члены,2) однородные членычасти сложного предложения—.поэт — трубач зовущий войско в битву (1) и прежде всех идущий в битву сам (ю. янонис).союз и соединяет:1) части сложного предложенияоднородные члены,2)
Физика – 1 год назад
Вокруг прямого проводника с током (смотри рисунок) существует магнитное поле. определи направление линий этого магнитного поля в точках a и b.обрати внимание, что точки a и b находятся с разных сторон от проводника (точка a — снизу, а точка b — сверху). рисунок ниже выбери и отметь правильный ответ среди предложенных.1. в точке a — «от нас», в точке b — «к нам» 2. в точке a — «к нам», в точке b — «от нас» 3. в обеих точках «от нас»4. в обеих точках «к нам»контрольная работа по физике.прошу,не наугад важно
Информация
Посетители, находящиеся в группе Гости, не могут оставлять комментарии к данной публикации.
Источник
Итоговые задания по теме «Основы молекулярно-кинетической теории»
материал по физике (10 класс) по теме
В данном материале подобраны задания для итогового повторения по теме «Основы молекулярно-кинетической теории»
Скачать:
| Вложение | Размер |
|---|---|
| itogovye_zadaniya_po_teme_osnovy_mkt.docx | 17.65 КБ |
Предварительный просмотр:
- Во сколько раз масса молекулы углекислого газа отличается от массы атома алюминия?
- Какое количество вещества (в молях) содержится в 117 г поваренной соли?
- Сколько атомов водорода содержит аммиак, взятый в количестве 0,5 моль?
- Сколько атомов содержится в 14 г кремния?
- Сколько атомов кислорода содержится в 9 л воды?
- Средние кинетические энергии молекул газов в сосудах 1 и 2 одинаковы. Для первого сосуда: V, m= 4г H 2 , n 1 =6х10 24 м -3 ; для второго: 0,5V, m= 2г Не, р 2 = 3х10 5 Па.
А) Чему равна концентрация молекул во втором сосуде?
Б) Чему равно давление газа в первом сосуде?
В) Чему равен объем первого сосуда?
Г) Чему равна средняя кинетическая энергия молекул газов?
Д) Во сколько раз отличаются средние скорости теплового движения молекул в сосудах?
7. Из сосуда, содержащего 4г водорода, через трещину ежесекундно выходит миллиард молекул. Через какое время сосуд опустеет? (1 год = 3Х10 7 с)
8. Сколько атомов содержится в 120 г кальция?
9.Сколько атомов водорода содержит вода, взятая в количестве 5 моль?
10. Какова масса водорода в 1 л воды?
11. Из открытого стакана за время равное 20 суткам испарилась вода массой 200 г. Сколько молекул испарилось за время равное 1секунде?
12.Какова средняя кинетическая энергия поступательного движения и средняя квадратичная скорость молекул водорода при температуре 27 0 С?
13. На изделие, поверхность которого 20 см 2 , нанесли слой серебра толщиной 1 мкм. Сколько атомов серебра содержится в покрытии? Плотность серебра 10,5х10 3 кг/м 3 .
1.Во сколько раз масса молекулы кислорода отличается от массы атома алюминия?
2.Какое количество вещества (в молях) содержится в 105 г поваренной соли?
3.Сколько атомов водорода содержит аммиак, взятый в количестве 1,5 моль?
4.Сколько атомов содержится в 14 г алюминия?
5.Сколько атомов водорода содержится в 9 л воды?
6.Средние кинетические энергии молекул газов в сосудах 1 и 2 одинаковы. Для первого сосуда: V, m= 4г H 2 , n 1 =6х10 24 м -3 ; для второго: 0,5V, m= 2г Не, р 2 = 3х10 5 Па.
А) Чему равна концентрация молекул во втором сосуде?
Б) Чему равно давление газа в первом сосуде?
В) Чему равен объем первого сосуда?
Г) Чему равна средняя кинетическая энергия молекул газов?
Д) Во сколько раз отличаются средние скорости теплового движения молекул в сосудах?
7. Из сосуда, содержащего 5г водорода, через трещину ежесекундно выходит миллиард молекул. Через какое время сосуд опустеет? (1 год = 3Х10 7 с)
8. Сколько атомов содержится в 120 г цинка?
9.Сколько атомов кислорода содержит вода, взятая в количестве 5 моль?
10. Какова масса водорода в 2 л воды?
11. Из открытого стакана за время равное 10 суткам испарилась вода массой 100 г. Сколько молекул испарилось за время равное 2 секунде?
12.Какова средняя кинетическая энергия поступательного движения и средняя квадратичная скорость молекул кислорода при температуре 27 0 С?
13.Сравните число атомов, из которых состоят серебряная и алюминиевая ложки равного объема. Плотность серебра 10.5х10 3 кг/м 3 , а алюминия – 2,7х103 кг/м 3 .
По теме: методические разработки, презентации и конспекты
Урок обучения новому материалу методом индивидуально-группового обучения по учебнику Г.Я.Мякишева. Прилагается конспект урока, лист индивидуального обучения (учащиеся должны его заполнить самос.
Интегрированный урок по физике и химии по теме «Молекулярная физика, Основы молекулярно-кинетической теории». Рассмотрен исторический аспект развития МКТ. Закон Авогадро и следствия из него. Количеств.
Данная разработка может быть использована при изучении темы МКТ идеального газа в 10 классе. Урок расчитан на 2 часа, но можно использовать элементы урока отдельно. В работе использованы с.
Ознакомить учащихся с основными положениями МКТ. Материал представлен в блочно- модульной технологии. блок состоит из трех модулей.
Материалы по теме «Молекулярно-кинетическая теория». Физика 10 кл.1.Тест «Графики изопроцессов». Проектор2. Тест «Подготовка к контрольной работе по теме «Молекулярно-кинетическая теория». Проектор3. .
Материалы по теме «Молекулярно-кинетическая теория». Физика 10 кл.1.Тест «Графики изопроцессов». Проектор2. Тест «Подготовка к контрольной работе по теме «Молекулярно-кинетическая теория». Проектор3. .
План-конспект урока физики «Идеальный газ в молекулярно-кинетической теории. Основное уравнение молекулярно- кинетической теории газа.».
Источник
Какое давление на стенки сосуда производят молекулы газа?
Основное уравнение молекулярно-кинетической теории (МКТ) идеального газа:
Концентрацию молекул газа n находят как отношение числа молекул N к объему газа V:
Произведение массы одной молекулы m0 на количество молекул N по смыслу есть масса газа m, поэтому:
Подставив в эту формулу исходные данные, можно вычислить какое давление на стенки сосуда производят молекулы газа.
1 · Хороший ответ
Сколько молекул находиться в воде массой 72гр?
m воды = 72 г. Ищем количество молекул N
Определяем молярную массу воды:
Мг = 1*2 + 16 = 18.
М = 18 г/моль.
Тогда количество вещества воды: v = m/M = 72/18 = 4 моль.
Число молекул воды: N = vN(A) = 4*6*10^23 = 24*10^23 молекул.
Где N(A) — число Авогадро.
Ответ: в воде массой 72 г содержится 24*10^23 молекул.
5 · Хороший ответ
Почему вода не горит? Она же состоит из водорода и кислорода. Водород горит, а без кислорода горение невозможно?
Вода — это уже водород, сгоревший в кислороде. Это продукт горения.
Впрочем, вода може гореть в атмосфере фтора (то есть, если встретится с окислителем, более сильным, чем кислород). Вот уравнение этой реакции:
2F2 + 2H2O -> 4HF + O2.
4 · Хороший ответ
Какова масса молекулы водорода?
Масса молекулы водорода, состоящей из двух атомов водорода рассчитывается исходя из массы отдельных атомов, путем обычного суммирования двух масс атома водорода.
Масса молекулы водорода, состоящей из двух атомов протия(самого распространенного изотопа водорода), с формулой H2, соответственно, будет равна приблизительно 2,016 а.е.м, где 1 а. е. м. = 1,660 539 066 60(50)⋅10−27 кг. — атомная единица массы, определяемая как 1/12 массы атома углерода-12 в состоянии покоя.
Масса молекулы, состоящей из комбинации двух изотопов водорода, рассчитывается так же с учетом массы отдельных атомов-изотопов, составляющих данную молекулу.
Так же возможна ионизированная форма молекулы водорода, массу которой можно получить тем же способом, затем отнять от неё массу 1 электрона.
Удачи в рассчетах!
1 · Хороший ответ
Какой объём займёт 1 кг воздуха при 17 градусах и давлении 101.3 кпа?
Воздух при данных условиях можно рассматривать как идеальный газ. Поэтому для решения задачи можно использовать уравнение Менделеева-Клапейрона (уравнение состояния идеального газа).
pV=(m/M)RT, где p — давление газа, V — объем газа, R — универсальная газовая постоянная, равная 8,31 Дж/(моль*К), m — масса газа, M — молярная масса газа (в данном случае — воздуха), равная 0,029 кг/мол.
Отсюда V = m*R*T/(M*p)
Переводим величины в основные единицы СИ
17 градусов = 290 К
101,3 кПа = 101300 Па
Таким образом V = 1 * 8.31 * 290/(0.029 * 101300)
6 · Хороший ответ
По Эйнштейну, чем ближе тело или частица к скорости света, тем огромнее становится его масса. И вот,в Большом адронном коллайдере, протоны и ионы, движутся почти со скоростью света, и что это значит?
Релятивистской массы нет в природе и, согласно релятивистской механике Эйнштейна, масса остаётся инвариантной и равной массе покоя всегда, независимо от скорости (недоверчивым сюда).
Темп роста энергии частицы (E) с ростом скорости β = v/c (в единицах скорости света c) получен мною здесь. Если тело обладало скоростью β₁ = 0,9 при энергии Е₁, то для достижения скорости β₂ = 0,9. 999 (n девятoк после запятой), потребуется энергия E₂ = (3,16)ⁿ⁻¹⋅Е₁. Получается, что с каждой новой девяткой в величине скорости (β), энергия должна быть увеличена в 3,16 раз. Таким образом, неограниченный рост числа девяток (n) в численном значении скорости (β), приводит к неограниченному росту энергии.
Mаксимальная скорость зарегистрированного материального объекта (протона), ускоренного до околосветовых скоростей в космическом пространстве, равна β = 0,9. 999 (всего 23 девятки), а соответствующая энергия, E
10¹¹ ГэВ. Области в галактиках и механизмы ускорения до этих скоростей пока неизвестны. Максимальные энергии столкновения протонов, достигнутые на ускорителе БАК (LHC) в ЦЕРН, равны 1,3×10⁴ ГэВ, что в системе отсчёта неподвижной мишени соответствует энергии протона = 9×10⁷ ГэВ или скорости протона β = 0,999 999 999 999 9999 (16 девяток). В обоих случаях масса протона остаётся неизменной и равной массе покоя, 0.938 ГэВ.
Согласно релятивистской механике, со скоростью света (β = 1) могут лететь только безмассовые частицы (фотоны), но и у них есть недостаток − они не могут лететь медленнее.
Источник
Чему равно давление газа в первом сосуде
В сосуде неизменного объема находилась при комнатной температуре смесь двух идеальных газов, по 1 моль каждого. Половину содержимого сосуда выпустили, а затем добавили в сосуд 1 моль первого газа. Как изменились в результате парци-альные давления газов и их суммарное давление, если температура газов в сосуде поддерживалась неизменной? Для каждой величины определите соответствующий характер изменения:
3) не изменилось.
Запишите в таблицу выбранные цифры для каждой физической величины. Цифры в ответе могут повторяться.
| Парциальное давление первого газа | Парциальное давление второго газа | Давление смеси газов Вначале оба идеальных газа в сосуде находились в полностью равных условиях. Полное количество вещества было равно 2 моля. Когда выпустили половину содержимого сосуда, и количество первого газа, и количество второго газа уменьшилось, в сосуде остался 1 моль газов. Затем в сосуд добавили еще 1 моль первого газа. Количество вещества вновь стало равно 2 моля. Следовательно, давление смеси газов в сосуде не изменилось, поскольку оно определяется только полной концентрацией молекул в сосуде. Парциальные давления газов, напротив, изменились. Первого газа стало больше, чем 1 моль, значит, его парциальное давление увеличилось. Второго газа стало меньше, чем 1 моль: парциальное давление второго газа уменьшилось. «давление смеси газов в сосуде не изменилось, поскольку оно определяется только полной концентрацией молекул в сосуде» мы же не знаем пропорции и концентрации газов, как можно тогда считать что давление не изменилось? Отношение между получившимися концентрациями знать и не нужно. Существенно только, что температура остается неизменной. Смотрите. Обозначим объем сосуда через . Изначально обоих газов по 1 моль, то есть число молекул каждого газа равно числу Авагадро . То есть парциальные давления равны: , . Полное давление: После выпускания газов,число молекул первого и второго газов уменьшилось до и соответственно. При этом , поскольку всего в сосуде остался 1 моль. Теперь добавляют 1 моль первого газа, следовательно, число молекул становится и . Теперь . Тогда парциальное давление первого газа после всех операций: . Парциальное давление второго газа: . Новое общее давление: . Источник ➤ Adblock |
Источник

Ответ
Ответ дан
cjddjccd
n2=12 p2=567 E=79 вот если я правельно паняла