Что такое окклюзия коронарных сосудов

Определение
Окклюзия сосудов – это ограничение проходимости сосудов, которое связано с тем, что на одном из участков сосудистый просвет перекрыт. Окклюзия сосуда – опасное состояние, поскольку она ведет к развитию ишемии органов, вызывая сердечные приступы и инсульты. Острая окклюзия несет в себе угрозу, поскольку в считанные часы она приводит к некротическим процессам в тканях.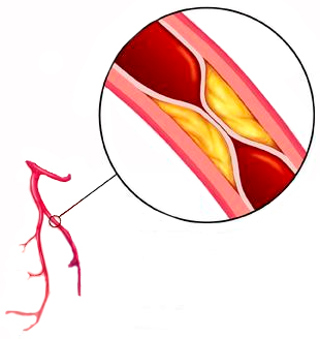
Причины
Окклюзии сосудов связаны с состоянием сосудистой недостаточности. Окклюзионный процесс возникает:
- в результате полученных травм, если артерия пережата.
- из-за того, что просвет закупорен тромбом или эмболом.
Образованию тромбов способствует хроническое заболевание – атеросклероз сосудов. Разрастаясь и увеличиваясь в диаметре, атероматозные бляшки мешают нормальному кровотоку. Атеросклеротическая бляшка приводит к свертыванию крови и образованию тромба. Окклюзию вызывают отделившиеся фрагменты бляшки, которые свободно двигаются по сосудистому руслу. Кроме того, в результате атеросклероза стенки сосудов теряют упругость, становятся тоньше и расслаиваются под давлением крови, что становится причиной образования аневризм. На участке сосуда, где появилось расширение, с большой вероятностью возникают тромбоз или эмболия.
Симптомы
Симптомы окклюзии зависят от того, в каком артериальном бассейне произошла закупорка сосуда.
Окклюзия сосудов сердца
Опасным состоянием считается острая окклюзия коронарных артерий, которые снабжают кровью сердечную мышцу. Это происходит в результате атеросклероза коронарных артерий и ишемической болезни сердца. Если при хроническом течении заболевания человек сталкивается со стенокардией, то острая форма чревата инфарктом и даже смертью пациента. Типичные признаки окклюзии сосудов сердца – боли за грудиной, которые продолжаются более 10 минут и не проходят в состоянии покоя или после приема нитроглицерина. В этом случае используют понятие острый коронарный синдром: больной с такими симптомами должен быть немедленно госпитализирован.
Опасность заключается в том, что симптомы ишемической болезни человек поначалу игнорирует или попросту не ощущает, не предпринимая никаких мер. Для окклюзии сосудов характерна внезапность и неожиданность, поэтому при первых признаках развивающейся ишемической болезни немедленно обратитесь к врачу.
Окклюзия периферических сосудов сосудов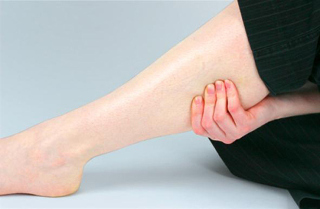
Окклюзии сосудов подвержены крупные артерии конечностей, чаще – нижних. Окклюзии являются неприятным последствием заболеваний сосудов ног. При этом угроза острого окклюзионного процесса в этой области опасна развитием некроза тканей, что ведет к ампутации пораженной конечности. Характерными признаками облитерирующего тромбангиита, атеросклероза сосудов ног и других распространенных патологий являются:
- боли в ногах, которые не проходят в состоянии покоя;
- бледность кожных покровов конечностей;
- холодность в ногах;
- ощущение покалывания, онемения в конечности;
- нарушение двигательных функций конечности.
При появлении данных симптомов рекомендуется немедленно провести обследование и лечение сосудов конечностей: малейшее промедление может обернуться развитием гангрены. На ранних стадиях развития недуга лечение облитерирующего атеросклероза нижних конечностей и прочих патологий склеротического происхождения проводится консервативными методами, тогда как в запущенной форме бороться с болезнью трудно.
Окклюзионные процессы возникают в артериях почек – в результате развивается реноваскулярная гипертензия, дисфункция почек. Поражениям подвергается и аорта, поскольку это самый крупный сосуд. О последствиях атеросклероза аорты читайте, перейдя по ссылке.
 Окклюзия сосудов, снабжающих кровью головной мозг
Окклюзия сосудов, снабжающих кровью головной мозг
Окклюзионные процессы в артериях, питающих головной мозг, таят в себе опасные последствия. Нарушение мозгового кровоснабжения чревато развитием инсульта или ишемического инфаркта мозга, а это часто заканчивается смертью пациента, парализацией или слабоумием. Распространенная причина этого – окклюзия сонных артерий. Она сопровождается потерей сознания, тошнотой и рвотой, нарушениями координации, речи и зрения, слабостью и онемением конечностей. Предвестником инсультов становятся транзиторные (церебральные) ишемические атаки, о которых мы подробно рассказывали ранее.
Лечение
Чаще всего единственный способ устранить окклюзию и возобновить кровоснабжение – оперативное вмешательство. При полной закупорке приходится выполнять шунтирование артерий – открытую операцию по замене пораженного участка сосуда искусственным протезом.
Источник
Острая окклюзия сосудов конечностей – внезапный тромбоз или эмболия периферической артерии, сопровождающиеся острым нарушением кровообращения в конечности дистальнее места обтурации сосуда. Острая окклюзия сосудов характеризуется болью, бледностью кожных покровов, отсутствием пульсации, парестезиями, параличом конечности. В комплекс диагностики острой окклюзии сосудов конечностей входят лабораторные тесты, допплерография, ангиография. При острой окклюзии сосудов конечностей проводится антитромботическая, фибринолитическая, спазмолитическая, инфузионная терапия; при неэффективности выполняется тромбэмболэктомия, эндартерэктомия, обходное шунтирование, ампутация конечности.
Общие сведения
Острая окклюзия сосудов конечностей – внезапная сосудистая непроходимость, обусловленная эмболией, тромбозом или спазмом артерий. Острая окклюзия сосудов конечностей сопровождается резким ухудшением или прекращением артериального кровотока, развитием острого ишемического синдрома, что несет потенциальную угрозу жизнеспособности конечности. В кардиологии и ангиохирургии острая окклюзия сосудов конечностей относится к числу неотложных состояний, поскольку может привести к потере конечности и инвалидности. Обычно острая окклюзия сосудов конечностей развивается у мужчин старше 60 лет. Пациенты с острой окклюзией сосудов конечностей составляют 0,1% всех больных хирургического профиля.

Острая окклюзия сосудов конечностей
Причины острой окклюзии сосудов конечностей
Понятие «острая окклюзия сосудов конечности» является собирательным, поскольку объединяет случаи внезапно возникшей артериальной недостаточности периферического кровотока, вызванные острым тромбозом, эмболией, спазмом или травматическим поражением сосуда.
Тромбоэмболии являются самой частой причиной острой окклюзии сосудов конечностей, составляя до 95% случаев. Материальным субстратом артериальных тромбоэмболий служат жировые, тканевые, воздушные, микробные, опухолевые фрагменты, а также фрагменты первичного тромба, которые с током крови из основного очага мигрируют на периферию.
Большинство случаев острой окклюзии сосудов конечностей возникают на фоне ишемической болезни сердца, инфаркта миокарда, пороков сердца (чаще – митрального стеноза), аритмий, гипертонической болезни, атеросклероза и аневризмы аорты или ее ветвей, аневризмы сердца, эндокардита, дилатационной кардиомиопатии.
Эмбологенными очагами могут служить опухоли легких и сердца, в частности миксома левого предсердия. Возможно возникновение парадоксальной эмболии, при попадании тромба в артерии большого круга через открытое овальное окно, открытый артериальный проток, дефекты межпредсердной или межжелудочковой перегородки. Реже причинами острой окклюзии сосудов конечностей выступают предшествующие операции на артериях, отморожения, электротравмы, заболевания системы крови (лейкозы, полицитемия), экстравазальная компрессия, сосудистые спазмы.
Факторами риска острой окклюзии сосудов конечностей служат заболевания периферических сосудов: облитерирующий атеросклероз, облитерирующий эндартериит, неспецифический аортоартериит (болезнь Такаясу), узелковый периартериит. Фрагментация и мобилизация первичного тромбоэмбола может происходить при изменении ритма сердца и силы сердечных сокращений, перепадах АД, физическом и психическом напряжении, приеме некоторых лекарств и др. В 5-10% случаев не удается выявить источник эмболии ни при клиническом обследовании, ни на аутопсии.
Патогенез
Острые ишемические расстройства, развивающиеся при окклюзии сосудов конечностей, обусловлены не только механическим фактором (внезапной закупоркой артерии эмболом), но и артериальным спазмом. В кратчайшие сроки после окклюзии и спазма артерии в просвете сосуда формируется тромб. Условия для тромбообразования создаются в связи с уменьшением скорости кровотока, гиперкоагуляцией и изменениями сосудистой стенки. Распространяясь в дистальном и проксимальном направлениях, тромб последовательно обтурирует коллатерали, еще более усугубляя картину острой ишемии.
Первичное формирование артериального тромба происходит в сосудах с уже измененной стенкой. Факторами местного тромбообразования выступают повреждение эндотелия, замедление скорости регионарного кровотока, нарушение свертываемости крови.
Ишемические расстройства в пораженной конечности при острой окклюзии сосудов патогенетически связаны с кислородным голоданием тканей, нарушением всех видов обмена и выраженным ацидозом. Вследствие гибели клеточных элементов и повышенной клеточной проницаемости развивается субфасциальный мышечный отек, усиливающий нарушения кровообращения.
Классификация окклюзий сосудов
Среди окклюзирующих поражений артериальных сосудов на первом месте по частоте возникновения стоит острая окклюзия мезентериальных сосудов (40%), на втором – окклюзия артерий головного мозга (35%), на третьем – тромбоэмболия бифуркации аорты и артерий конечностей (25%). В порядке убывания частоты встречаемости острые окклюзии сосудов конечностей располагаются следующим образом: окклюзии бедренных артерий (34-40%), подвздошных артерий и бифуркации аорты (22-28%), подколенных артерий (9-15%), подключичных и плечевых артерий (14-18%), артерий голени.
В практике встречаются одиночные и множественные тромбоэмболии артерий. Последние могут быть многоэтажными (разноуровневые тромбоэмболии в одной артерии), комбинированными (тромбоэмболы в артериях разных конечностей) и сочетанными (при поражении артерий конечностей и церебральной или висцеральной артерии).
Ишемические изменения, обусловленные острой окклюзией сосудов конечностей, проходят несколько стадий: На стадии ишемии напряжения признаки нарушения кровообращения в покое отсутствуют и появляются лишь при нагрузке.
I степень – чувствительность и движения в конечности сохранны:
- IA – похолодание, парестезии, онемение конечности
- IБ – боли в дистальных отделах конечности в покое.
II степень – возникают расстройства движения и чувствительности конечности:
- IIА – парез конечности (снижение мышечной силы и объема активных движений в дистальных отделах)
- IIБ – паралич конечности (отсутствие активных движений)
III степень – развиваются некробиотические явления:
- IIIА – субфасциальный отек
- IIIБ – парциальная мышечная контрактура
- IIIВ – тотальная мышечная контрактура
Степени ишемии конечности учитываются при выборе метода лечения острой окклюзии сосудов.
Симптомы окклюзии сосудов
Острая окклюзия сосудов конечностей проявляется симптомокомплексом, обозначаемым в англоязычной литературе как «комплекс пяти P» (рain – боль, рulselessness – отсутствие пульса, рallor – бледность, рaresthesia – парестезии, рaralysis – паралич). Наличие хотя бы одного из этих признаков заставляет думать о возможной острой окклюзии сосудов конечностей.
Внезапная боль дистальнее места окклюзии возникает в 75-80% случаев и обычно служит первым признаком острой окклюзии сосудов конечностей. При сохранности коллатерального кровообращения боль может быть минимальной или отсутствовать. Чаще боль носит разлитой характер с тенденцией к усилению, не стихает при изменении положения конечности; в редких случаях спонтанного разрешения окклюзии боль самостоятельно исчезает.
Важным диагностическим признаком острой окклюзии сосудов конечностей является отсутствие пульсации артерий дистальнее места окклюзии. При этом конечность вначале бледнеет, затем приобретает цианотический оттенок с мраморным рисунком. Кожная температура резко снижена – конечность холодная на ощупь. Иногда при осмотре выявляются признаки хронической ишемии – морщинистость и сухость кожи, отсутствие волос, ломкость ногтей.
Расстройства чувствительности и двигательной сферы при острой окклюзии сосудов конечностей проявляются онемением, ощущением покалывания и ползания «мурашек», снижением тактильной чувствительности (парестезиями), снижением мышечной силы (парезом) или отсутствием активных движений (параличом) сначала в дистальных, а затем в проксимальных суставах. В дальнейшем может наступить полная обездвиженность пораженной конечности, что указывает на глубокую ишемию и является грозным прогностическим признаком. Конечным результатом острой окклюзии сосудов может стать гангрена конечности.
Диагностика острой окклюзии сосудов конечностей
Диагностический алгоритм при подозрении на острую окклюзию сосудов конечностей предусматривает проведение комплекса физикальных, лабораторных, инструментальных исследований. Пальпация пульса в типичных точках (на тыльной артерии стопы, в подколенной ямке, на заднебольшеберцовой и бедренной артерии и др.) выявляет отсутствие пульсации артерии ниже окклюзии и ее сохранение выше участка поражения. Важную информацию при первичном обследовании дают функциональные пробы: маршевая (проба Дельбе-Пертеса), коленный феномен (проба Панченко), определение зоны реактивной гиперемии (проба Мошковича).
Лабораторные исследования крови (коагулограмма) при острой окклюзии сосудов конечностей обнаруживают повышение ПТИ, уменьшение времени кровотечения, увеличение фибриногена. Окончательная диагностика острой окклюзии сосудов конечностей и выбор лечебной тактики определяются данными УЗДГ (дуплексного сканирования) артерий верхних или нижних конечностей, периферической артериографии, КТ-артериографии, МР-ангиографии.

КТ-ангиография брюшной аорты и ее ветвей. Полная окклюзия просвета левой внутренней подвздошной артерии
Дифференциальная диагностика проводится с расслаивающейся аневризмой брюшной аорты и острым тромбофлебитом глубоких вен.
Лечение острой окклюзии сосудов конечностей
При подозрении на острую окклюзию сосудов конечностей пациент нуждается в неотложной госпитализации и консультации сосудистого хирурга. При ишемии напряжения и ишемии IА степени проводится интенсивная консервативная терапия, включающая введение тромболитиков (гепарин внутривенно), фибринолитических средств (фибринолизина, стрептокиназы, стрептодеказы, тканевого активатора плазминогена), антиагрегантов, спазмолитиков. Показаны физиотерапевтические процедуры (диадинамотерапия, магнитотерапия, баротерапия) и экстракорпоральная гемокоррекция (плазмаферез).
При отсутствии положительной динамики в течение 24 ч от момента возникновения острой окклюзии сосудов конечностей необходимо выполнение органосохраняющей хирургической операции – тромбэмболэктомии из периферической артерии с помощью баллонного катетера Фогарти или эндартерэктомии.
При ишемии IБ-IIБ степеней необходимо экстренное вмешательство, направленное на восстановление кровотока: эмбол- или тромбэктомия, обходное шунтирование. Протезирование сегмента периферической артерии проводится при непротяженных острых окклюзиях сосудов конечностей.
Ишемия IIIА-IIIБ степеней является показанием к экстренной тромб- или эмболэктомии, обходному шунтированию, которые обязательно дополняются фасциотомией. Восстановление кровообращения при ограниченных контрактурах позволяет выполнить отсроченную некрэктомию или последующую ампутацию на более низком уровне.
При ишемияи IIIВ степени операции на сосудах противопоказаны, поскольку восстановление кровотока может привести к развитию постишемического синдрома (аналогичному травматической токсемии при синдроме длительного раздавливания) и гибели больного. На данной стадии выполняется ампутация пораженной конечности. В послеоперационном периоде продолжается антикоагулянтная терапия для предупреждения ретромбоза и повторной эмболии.
Прогноз и профилактика
Важнейшим прогностическим критерием при острой окклюзии сосудов конечностей является фактор времени. Ранняя операция и интенсивная терапия позволяют восстановить кровоток в 90% случаев. При поздно начатом лечении или его отсутствии наступает инвалидизация вследствие утраты конечности или летальный исход. При развитии реперфузионного синдрома гибель может наступить от сепсиса, почечной недостаточности, полиорганной недостаточности.
Профилактика острой окклюзии сосудов конечностей заключается в своевременном устранении потенциальных источников тромбоэмболии, профилактическом приеме антиагрегантов.
Источник

За последнее десятилетие во всем мире выросла доля эндоваскулярных методов лечения ишемической болезни сердца (ИБС). Выбор данной тактики лечения ИБС, в противовес хирургическому лечению, в сочетании с консервативной терапией обусловлен непосредственной эффективностью и безопасностью эндоваскулярной процедуры, позволяющей добиться адекватного восстановления коронарного кровотока в большинстве случаев.
При атеросклеротическом поражении коронарного русла вид эндоваскулярного вмешательства выбирают на основании рентгенморфологических характеристик поражения венечных сосудов. У пациентов с поражением одного коронарного сосуда основным вмешательством является процедура транслюминальной баллонной ангиопластики (ТЛАП) или стентирования пораженного сегмента коронарной артерии. Операция аортокоронарного шунтирования (АКШ) рекомендуется преимущественно пациентам с поражением ствола ЛКА или пациентам с многососудистым поражением венечного русла. Однако в этом случае при наличии серьезных сопутствующих заболеваний, являющихся противопоказанием к проведению операции АКШ, бывает необходимо проведение эндоваскулярных вмешательств. При выявлении многососудистого поражения коронарных артерий возможно выполнение одномоментной эндоваскулярной процедуры реваскуляризации миокарда на нескольких коронарных сосудах или же выполнение поэтапной эндоваскулярной процедуры.
Увеличивающееся из года в год количество эндоваскулярных вмешательств на коронарных сосудах делает проблему лечения выявленных хронических окклюзий весьма актуальной. Хронически окклюзированные коронарные артерии составляют значительную часть коронарных поражений, выявляемых у пациентов при проведении диагностической коронароангиографии (КАГ) и, в определенной клинической ситуации, требуется проведение реваскуляризации миокарда.
Так, окклюзированные коронарные артерии выявляются примерно у 38% пациентов, а коронарная ангиопластика на хронически окклюзированных коронарных артериях составляет 10-20% всех интервенционных процедур [1, 2, 4].
Выявление полной окклюзии коронарной артерии при КАГ у больных с ИБС может серьезно влиять на выбор дальнейшей лечебной тактики. Хронически окклюзированная коронарная артерия часто является фактором, определяющим выбор специалистов в пользу проведения хирургического лечения, а не эндоваскулярной процедуры.
 |
| Рисунок 2. Хроническая окклюзия ПМЖВ в средней трети и гемодинамически значимый стеноз ОВ в проксимальной трети у пациентки Ш. |
В Научно-практическом центре интервенционной кардиоангиологии (НПЦИК) Департамента здравоохранения г. Москвы при проведении плановой КАГ также довольно часто обнаруживаются полные хронические окклюзии одной, двух или более коронарных артерий.
Соотношение между общим количеством больных, которым в период с октября 1997 г. по декабрь 2002 г. выполнялась в НПЦИК диагностическая КАГ, и числом пациентов, у которых были выявлены одна или более хронически окклюзированные коронарные артерии, представлено на рисунке 1.
Большинство исследователей в своих работах показали, что одной из главных причин, определяющих различия в тактике лечения больных с наличием или отсутствием окклюзии коронарной артерии, является преобладание больных с трехсосудистым поражением коронарного русла. Считается, что наличие перенесенного инфаркта миокарда в области, кровоснабжаемой окклюзированной артерией, может препятствовать проведению более агрессивной процедуры реваскуляризации миокарда [3].
По данным большинства авторов, наличие окклюзии коронарной артерии у больных ИБС может изменить терапевтическую тактику по нескольким причинам.
- Катетерная реканализация требует более высокой квалификации врача.
- Доля первичного (непосредственного) успешного результата оказывается ниже, чем при стенотических поражениях венечного русла.
- Реканализация сосуда может быть чреспросветной, субинтимальной, пере- и трансатероматозной.
- Имеется риск развития диссекции или разрыва сосуда в месте воздействия инструмента. (У 42% больных непосредственно после ангиопластики окклюзий выявляются ангиографические признаки диссекции сосудов [3]. Известно, что диссекция значительно реже встречается при дилятации стенозов и относится к факторам, способствующим тромбообразованию.)
- При отсутствии удовлетворительного результата приходится увеличивать число и продолжительность раздуваний баллона, что впоследствии может приводить к развитию рестеноза.
- Кроме того, при наличии окклюзии имеется более высокий риск дилятации другого сосуда.
Как было сказано выше, коронарная ангиопластика хронических окклюзий составляет, по данным разных авторов, 10-20% всех интервенционных процедур [1, 2, 4]. Наряду с этим, эндоваскулярное восстановление просвета коронарной артерии при ее хронической окклюзии часто остается технически сложной задачей.
Реканализация становится более проблематичной при наличии негативных факторов, влияющих на успех процедуры, таких, как старые повреждения, протяженные, ангиографически неблагоприятные окклюзии, наличие мостовых коллатералей.
Проведению эндоваскулярной реваскуляризации при этом типе поражений препятствуют не только технические трудности, связанные с проведением проводников и других устройств, но и повышенный уровень рестеноза в отдаленном периоде [5, 6, 7].
Известно, что частота непосредственного успеха при ангиопластике на хронически окклюзированных артериях ниже, тогда как времени на облучение, использование аппаратуры затрачивается больше и стоимость процедуры выше, чем при ангиопластике у больных со стенотическими поражениями венечного русла [8].
В НПЦИК в период с октября 1997 г. по декабрь 2002 г. проведено 380 попыток механической реканализации хронически окклюзированных коронарных артерий у 375 больных. При этом успех процедуры был достигнут у 253 больных (67,5%), которым было реканализировано 258 сегментов. В 122 случаях (32,5%) процедура реканализации была безуспешной. Проводниковая реканализация и коронарная ангиопластика окклюзированной коронарной артерии выполнялись 107 больным на 107 сегментах; реканализация, ТЛАП и стентирование – 146 больным, которым был реканализирован 151 сегмент.
 |
| Рисунок 3. Хроническая окклюзия ПКА в проксимальной трети у пациентки Ш. |
По результатам исследований, проведенных в НПЦИК, с технической стороны успех процедуры определялся как способность пройти окклюзированный сегмент и проводником, и баллонным катетером и успешно открыть окклюзированную артерию с величиной остаточного стеноза менее 40%.
При этом эффективной процедура считалась, если не было серьезных кардиальных осложнений на госпитальном этапе. Серьезные кардиальные осложнения определялись как случаи смерти, развития острого инфаркта миокарда или необходимость в проведении экстренной процедуры реваскуляризации миокарда.
По нашему мнению, важным в данной клинической ситуации, является проведение обязательного всестороннего контрольного обследования через 6 мес после эндоваскулярного вмешательства, включающего в себя проведение нагрузочных проб и контрольной КАГ для выявления возможного прогрессирования атеросклеротического процесса в коронарных артериях и развития in-stent стеноза.
Мы хотим продемонстрировать целесообразность проведения эндоваскулярных процедур у больной с двумя хронически окклюзированными коронарными артериями и несколькими гемодинамически значимыми стенозами, с высоким риском проведения операции аортокоронарного шунтирования, обусловленным тяжелой сопутствующей патологией.
Больная Ш., 59 лет поступила в мае 2001 г. в НПЦИК для планового обследования с диагнозом ИБС. Стенокардия напряжения III функционального класса (ФК), гипертоническая болезнь II степени, аутоиммунный тиреоидит Хашимото, гипотиреоз на стадии компенсации, ожирение III степени.
При поступлении в стационар пациентка предъявляла жалобы на давящие боли за грудиной при незначительной физической нагрузке и в покое, кратковременный эффект достигался при приеме нитроглицерина.
 |
| Рисунок 4. Механическая реканализация, баллонная ангиопластика и стентирование средней трети ПМЖВ и прямое стентирование проксимальной трети ОВ у пациентки Ш. |
Из анамнеза было известно, что больная длительное время отмечает подъемы артериального давления до максимальных цифр 200/120 мм рт. ст. Около 6 лет беспокоят приступы стенокардии напряжения и покоя. Ухудшение самочувствия с 19.04.2001 г., когда при незначительной физической нагрузке стали возникать интенсивные загрудинные боли, с кратковременным эффектом от приема нитратов. Была госпитализирована в НПЦИК с подозрением на прогрессирующую стенокардию для обследования и лечения.
Состояние при поступлении: средней степени тяжести. Пациентка повышенного питания. В легких дыхание везикулярное, хрипов нет, ЧДД 16/мин. Тоны сердца приглушены, ритмичные, шумов нет. ЧСС 74/ мин. АД 140/90 мм рт. ст. Со стороны желудочно-кишечного тракта без патологии. Неврологический статус без особенностей.
В биохимических анализах крови у пациентки обращала на себя внимание гиперхолестеринемия – 6,7 ммоль/л.
На ЭКГ: ритм синусовый, нарушение кровоснабжения передне-перегородочно-верхушечно-боковой области левого желудочка, Т(-)III, aVF, V1 – V5.
По данным ЭхоКГ: полости сердца не расширены. ЛЖ сократимость: удовлетворительная, ФВ – 66%, КДР – 5,1 см, КСР – 3,2 см, КДО – 123 см3, КСО – 41 см3, толщина межжелудочковой перегородки в диастолу 13,3 мм, толщина задней стенки в диастолу 12,3 мм. Умеренная симметричная гипертрофия ЛЖ. Митральный клапан: движение створок разнонаправленное. Аорта уплотнена, не расширена, склероз створок аортального клапана. При Д-ЭхоКГ патологических потоков не выявлено.
 |
| Рисунок 5. Механическая реканализация, ТЛАП и стентирование проксимальной трети ПКА, ТЛАП дистальной трети ПКА у пациентки Ш. |
При проведении суточного мониторирования ЭКГ было выявлено два эпизода депрессии сегмента S-T по 1 каналу до 2 мм, связанных с болевыми ощущениями.
По данным велоэргометрической пробы, на фоне отмены за 1 сут до исследования антиангинальной и гипотензивной терапии результат расценен как положительный: на нагрузке
75 Вт/мин появились типичные ангинозные боли без изменений на ЭКГ. Толерантность к нагрузке низкая.
Учитывая данные клинического течения основного заболевания, жалобы при поступлении в стационар, а также данные инструментальных методов обследования, пациентке было решено провести диагностическую вентрикулографию и коронароангиографию с целью выявления поражения коронарного русла и выработки дальнейшей тактики лечения основного заболевания. Вентрикулография: КДО – 91,3 мл, КСО – 21,2 мл,
ФВ – 77%. Митральная регургитация отсутствует. Сегментарная сократимость (правая косая проекция) удовлетворительная. Зон асинергии выявлено не было. Тип коронарного кровообращения правый. Ствол ЛКА обычно развит, не изменен. Передняя межжелудочковая ветвь (ПМЖВ) окклюзирована после отхождения первой диагональной ветви (1 ДВ). Коллатеральное заполнение дистального русла через межсистемные коллатерали отсутствует, через внутрисистемные – слабое (рис. 2). Огибающая ветвь (ОВ) стенозирована на двух уровнях: в проксимальном сегменте эксцентрический стеноз до 70% протяженностью до 10 мм с вовлечением устья, эксцентрический стеноз 60% маргинальной ветви (МВ) диаметром 2,5 мм в дистальном сегменте протяженностью до 10 мм. ПКА окклюзирована в проксимальном сегменте (рис. 3). Коллатеральное заполнение дистального русла через межсистемные коллатерали хорошее, через внутрисистемные – отсутствует.
Пациентке были выполнены механическая реканализация, баллонная ангиопластика и стентирование средней трети ПМЖВ (баллонная дилятация U-Pass 2 x 20, 17 атм 120 с – три дилятации давлением 14, 17, 12 атм по 120 с и установка стента Bx Velocity 2,5 х 23 мм, 13 атм, 45 с), прямое стентирование проксимальной трети ОВ (стентом Bx Velocity 3,5 х 8мм, 14 атм, 45 с) (рис. 4), проведена механическая реканализация, ТЛАП и стентирование проксимальной трети ПКА (баллон Raptor 2,5 х 15, 18 атм, 120 с, установка стента Multi Tetra 3,5 х 13, 12 атм, 45 с, с последующей оптимизацией просвета сосуда в проксимальных и дистальных сегментах стента доставочным баллоном под давлением 12 атм по 120 с) и ТЛАП дистальной трети ПКА – баллонная дилятация (баллон Raptor 2,5 х 18, 15 атм, 150 с) (рис. 5).
 |
| Рисунок 6. Выявленный через 6 месяцев после эндоваскулярного лечения in-stent стеноз ПМЖВ и ОВ у пациентки Ш. |
После механической реканализации, ТЛАП и стентирования ПКА и ПМЖВ – определялся кровоток TIMI 3, диффузные изменения без резких стенозов.
Послеоперационный период протекал гладко, ангинозные боли не рецидивировали. Пациентка была выписана под наблюдение кардиолога по месту жительства, рекомендован прием следующих лекарственных средств: атенолол 25 мг 2 раза в день, норваск 2,5 мг 2 раза в день, эналаприл 2,5 мг 2 раза в день, аспирин 125 мг 1 раз в день после еды, моно мак 20 мг 1 табл. х 2 раза в день, L-тироксин – 1 табл. утром.
С целью оценки отдаленного результата процедуры стентирования при выявленных хронических окклюзиях коронарных артерий пациентка Ш. была вновь обследована. При поступлении в стационар – жалобы на редкие приступы болей за грудиной при физической нагрузке.
 |
| Рисунок 7. Удовлетворительный среднеотдаленный результат механической реканализации, ТЛАП и стентирования проксимальной трети ПКА |
После выписки переносимость физических нагрузок значительно улучшилась, однако сохранялись боли при ходьбе быстрым шагом. Постоянно принимает атенолол, моно мак, эналаприл, аспирин.
В биохимических анализах крови выявлены гиперхолестеринемия, гипертриглицеридемия: холестерол 7,4 ммоль/л, триглицериды 2,8 ммоль/л.
При обследовании – на ЭКГ: ритм синусовый, правильный, ЧСС 68/мин, отрицательные зубцы Т в грудных отведениях.
На ЭхоКГ: полости сердца не расширены. Левый желудочек – сократимость удовлетворительная, ФВ – 69%, КДР – 5,0 см, КСР – 3,0 см, КДО -122 см3, КСО – 36 см3, толщина межжелудочковой перегородки в диастолу 13 мм, толщина задней стенки в диастолу 12,3 мм. Умеренная симметричная гипертрофия миокарда ЛЖ. Митральный клапан: движение створок разнонаправленное. Аорта не расширена, уплотнена, склероз створок аортального клапана. При Д-ЭхоКГ патологических потоков не выявлено.
 |
| Рисунок 8. Процедура ангиопластики in-stent стеноза среднего сегмента ПМЖВ на нескольких уровнях (в устье ПМЖВ и после отхождения диагональной ветви), процедура баллонной ангиопластики in-stent стеноза ОВ |
При проведении контрольной диагностической вентрикулографии и КАГ было выявлено: КДО – 120 мл, КСО – 30 мл, ФВ – 75%. Сегментарная сократимость удовлетворительная. Зон асинергии не выявлено. Тип коронарного кровообращения правый. Ствол ЛКА обычно развит, не изменен. ПМЖВ диффузно изменена, отмечается рестеноз после стентирования – 75% (рис. 6). ОВ диффузно изменена, отмечается рестеноз после стентирования в проксимальном конце стента на 75% (рис. 6). ПКА: диффузно изменена, в проксимальной трети состояние после стентирования без рестенозирования, в дистальной трети стенозирована на 75% (протяженностью около 10 мм) с вовлечением бифуркации задней межжелудочковой ветви и пастеро-латеральной ветви (рис. 7). Выполнены процедуры ангиопластики in-stent стеноза среднего сегмента ПМЖВ на нескольких уровнях (в устье ПМЖВ и после отхождения ДВ) и ангиопластики in-stent стеноза ОВ с хорошим эффектом. Гладкий послеоперационный период. Пациентка была выписана из стационара под дальнейшее наблюдение у кардиолога и эндокринолога по месту жительства, рекомендован прием следующих лекарственных средств: кардикет 20 мг 2 раза в день, аспирин 125 мг 1 раз в день, тиклид 250 мг 2 раза в день в течение 2 нед с дальнейшей отменой препарата, атенолол 12,5 мг 2 раза в день. В связи с гиперхолестеринемией и гипертриглицеридемией назначен зокор 10 мг на ночь. С целью контроля уровня гормонов щитовидной железы и коррекции заместительной терапии пациентке было рекомендовано продолжать прием L-тироксина в дозе 100 мкг 1 раз в день.
С целью оценки результатов ТЛАП in-stent стенозов ПМЖВ и ОВ через 6 мес после проведения эндоваскулярного вмешательства пациентке была вновь проведена диагностическая коронароангиография. Эффективность ТЛАП in-stent стенозов была подтверждена (рис. 9).
 |
| Рисунок 9. Отдаленные ангиографические результаты ТЛАП in-stent стенозов ПМЖВ и ОВ у пациентки Ш. |
Таким образом, на данном клиническом примере показано, что эндоваскулярные процедуры при многососудистом поражении венечного русла являются альтернативой аортокоронарного шунтирования у больных с тяжелыми сопутствующими заболеваниями. Кроме этого, применение интервенционных методов лечения ИБС эффективно и безопасно.
Литература
- Бабунашвили А. М., Иванов В. А., Бирюкова С. А. Эндопротезирование (стентирование) венечных артерий сердца. – М.: АСВ, 2001. – 704 с.
- Савченко А. П., Абдуллин Н. И., Матчин Ю. Г. и др. Особенности клинического течения и ангиографической картины при хронической окклюзии коронарной артерии//Вестник рентгенологии и радиологии/ – 2000; 4: 4-10.
- Бакланов Д. В., Огурцова О., Мэзден Р. Рестенозирование после успешной ангиопластики при окклюзиях коронарных артерий // Кардиология. – 1998; 1:10-126.
- Delacretaz E., Meier B. Therapeutic Strategy With Total Coronary Artery Occlusions // Am J Cardiol, 1997, 79: 185 – 187.
- Bauters C., Banos J. L., Van Belle E., Mc Fadden E. P., Lablanche J.M., Bertrand M.E. Six-month angiographic outcome after successful repeat percutaneous intervention for in-stent restenosis // Circulation 1998 Feb 3;97(4):318-21.
- Elchaninoff H., Koning R., Tron C., Gupta V., Cribier A. Balloon angioplasty for the treatment of coronari in-stent restenosis: imte results and 6-month angiographic recurrent restenosis rate // J Am Coll Cardiol 1998 Oct;32(4):980-4
- Rubartelli P., Niccoli L., Verna E. et al. Stent Implantation Versus Balloon Angioplasty in Chronic Coronary Occlusions: Results From the GISSOC Trial. J Am Coil Cardiol 1998; 32: 90-6.Edelman ER., Rogers C. // Hoop Dreams. Stent without restenosis // Circulation, 1996, 94: p. 1199-1202.
Д. Г. Иоселиани, доктор медицинских наук, профессор
А. В. Кононов
М. В
