Что такое резекция сосуда с замещением

Инсульт – вторая по частоте «болезнь – убийца» во всем мире. Даже если человека удалось спасти, острые нарушения кровообращения мозга не проходят бесследно. Как и любую болезнь, инсульт легче и проще не допустить, чем восстанавливаться после недуга. Именно поэтому первичной профилактике врачи уделяют особое внимание. Как убрать бляшки из сосудов до того, пока они не привели к болезни, узнал корреспондент «АиФ-Тюмень».
Снизить на сотни раз
Инсульты бывают двух типов: геморрагический, когда происходит кровоизлияние в головной мозг, и ишемический, когда нарушение мозгового кровообращения возникает из-за закупорки просвета сосуда тромбом. У геморрагического инсульта прогнозы более неблагоприятные, а восстановление проходит намного сложнее. Не допустить развитие ишемического инсульта можно, вовремя убрав причину – холестериновую бляшку, но проблема в том, что, пока «не грянет гром», тромб ничем не беспокоит.
«Удалив холестериновую бляшку до того, как она полностью закроет собой просвет сосуда, или ее оторвавшаяся часть закупорит мозговую артерию, мы фактически предупреждаем развитие инсульта, – говорит заведующий Региональным сосудистым центром ОКБ №2 Дмитрий Некрасов. – Особенно опасна закупорка брахиоцефальных артерий – магистральных сосудов на шее, питающих мозг».
Как правило, бляшки на сонных артериях обнаруживают случайно, при проведении профилактических осмотров, поэтому специалисты рекомендуют не пренебрегать диспансеризацией, а людям группы риска делать УЗИ сосудов шеи, особенно тем, у кого есть лишний вес, повышенный холестерин, наследственная предрасположенность, гипертония, сахарный диабет, мерцательная аритмия, пожилой возраст.
Проведение профилактического осмотра. Фото: АиФ/ Сирень Бабаева
Каротидная эндартерэктомия (операция по удалению бляшки из сонной артерии) позволяет снизить вероятность острого нарушения мозгового кровообращения в десятки раз. Хирурги Регионального сосудистого центра выполняют сотни подобных операций в год, по количеству и качеству каротидной эндартерэктомии тюменские врачи занимают третье место по стране.
В среднем операция длится сорок минут, на время удаления бляшки артерию перекрывают, и кровь поступает в мозг по второй сонной артерии. Иногда только прочистить сосуды не удается, они бывают настолько забиты бляшкой, что этот участок становится словно каменный. Если бляшку не удается «пробить», приходится удалять ее вместе с частью артерии.
«Ничего необычного в этом нет, после удаления артерию немного стягивают и сшивают по кругу», – поясняет Дмитрий Некрасов.
Особенно сложный случай у хирургов был, когда за раз им пришлось делать сразу две операции: на артериях шеи и мозга. Тогда они одномоментно устранили две жизнеугрожающие болезни, которые с высокой долей вероятности могли привести к инсульту. У женщины на одном из сосудов мозга образовалась аневризма – вздутие стенки сосуда, которое могло лопнуть в любой момент. А чуть ниже аневризмы в сонной артерии обнаружили еще и большую холестериновую бляшку. Она почти полностью перекрывала просвет сосуда, и кровь в мозг поступала с трудом. Медлить было нельзя. Как правило, в таких случаях обычно последовательно, с небольшим перерывом на реабилитацию, выполняется две операции: сначала удаляется бляшка, а затем – аневризма. Но в этом случае ожидание могло закончиться смертью пациентки, тогда врачи решили пойти на риск и выполнить обе операции одномоментно.
«Такие операции уникальны даже в мировой практике, не говоря уже о Тюмени. Хирург должен обладать навыками как сосудистого хирурга, так и рентгенэндоваскулярного хирурга, – поясняет доктор Некрасов. – Сначала мы удалили холестериновую бляшку из просвета артерии, а затем ввели в кровеносные сосуды мозга микрокатетеры и уже с их помощью заполнили полость аневризмы микроскопическими спиралями. После этого восстановили мозговое кровоснабжение. Самое сложное было – решиться на такую операцию. Нужно было все сделать аккуратно, подобрать правильные технологии, малейшая ошибка могла стоить очень дорого».
После каротидной эндартерэктомии пациентов из стационара обычно выписывают на четвертый день, о перенесенном им напоминает только небольшой шрам на шее.
Не оставляйте без внимания
При проявлении симптомов инсульта самое главное – вовремя доставить человека в больницу. Если пациент попадает в терапевтическое окно – 4,5-6 часов с момента развития признаков инсульта – можно провести тромболитическую терапию, но при условии, что причиной закупорки сосуда стал сгусток крови, а не холестериновая бляшка.
«Не надо думать, как помочь человеку с признаками инсульта, нужно набирать номер скорой помощи. Если быстро не помочь, то очаг гибели нейронов будет постоянно увеличиваться, и восстановление пациента станет намного сложнее, а порой и вообще невозможно», – напоминает врач.
Работа хирургов. Фото: pixabay.com
Если растворить тромб не получается, то пациенту делают тромбэкстракцию – механическое удаление тромба. Для этого делается пункция артерии, например, бедренной, и в артерии головного мозга заводится специальное устройство, с помощью которого убирают помеху в сосуде. Пока эта процедура находится в стадии внедрения в широкую практику.
Сразу же после госпитализации в стационар начинается и реабилитация пациента. В это время подключаются и социальные работники, которые задействуют так называемую биопсихосоциальную модель реабилитации, когда пациента не просто лечат, но пытаются реабилитировать после болезни, приспособить к изменившимся условиям его жизни. Принимает участие в реабилитации и эрготерапевт, он занимается адаптацией человека в окружающей обстановке, обучает пациента тому, как себя вести на кухне, как обращаться с бытовой техникой и выполнять действия, о которых здоровый человек даже не задумывается.
«Та же чистка зубов нам кажется простым делом, но для человека, перенесшего инсульт, – это очень тяжело. Задача мультидисциплинарной бригады – разбудить «спящие» нейроны, которые расположены рядом с пораженной областью мозга, чтобы они активизировались и взяли на себя функцию утраченных участков головного мозга. Но, несмотря на все усилия врачей, вернуть человека к полноценной прежней жизни удается не всегда, поэтому мы не устаем говорить о профилактике инсульта, о том, что нужно внимательнее относиться к пожилым родственникам. Нередко бывает так, что пожилые люди живут одни в квартире, на даче и, если случится беда, об этом никто не узнает, пока не начнут искать человека. Порой больной с инсультом по нескольку дней находится у себя дома без помощи, пока родственники не забьют тревогу и не начнут искать его».
Чтобы еще четче и слаженнее оказывать первую помощь при сосудистых катастрофах, врачи отрабатывают навыки еще и виртуально. В специальную программу «заводятся» данные условного пациента – каждый раз разного, причем, для исходных параметров берутся реальные случаи. Врач оттачивает на виртуальном пациенте каждое действие. Такая программа позволяет довести до автоматизма навык распределения времени, что очень важно, ведь при инсульте важна каждая секунда.
«Улыбнись – заговори – подними руки»
Симптомы инсульта, как правило, развиваются очень быстро. Сценарий примерно одинаков, может меняться только последовательность их возникновения. Для инсульта характерен односторонний парез, когда мышечная слабость проявляется только на левой или на правой стороне тела. Из-за онемения мышц одной половины тела меняется походка – она становится неустойчивой, человек падает. Парез (онемение) мышц лица приводит к тому, что рот «перекашивается», и черты лица изменяются. Нередко развивается афазия – нарушения речи: человек либо говорит, словно с кашей во рту, либо тараторит быстро и непонятно. Также больному становится трудно формулировать свои мысли и подбирать слова.
Врачи рекомендуют запомнить три основных приема распознавания симптомов инсульта: «Улыбнись – заговори – подними руки» (УЗП).
Важно своевременно распознать симптомы инсульта. Фото: pixabay.com
Попросите человека улыбнуться. При инсульте улыбка получается «кривой», поскольку мышцы одной стороны лица слушаются гораздо хуже.
Заговорите с ним и попросите ответить на простой вопрос, например: «Как тебя зовут?». Обычно в момент мозговой катастрофы человек не может связно выговорить даже свое имя.
Предложите ему поднять обе руки одновременно. Как правило, с этим заданием больному справиться не удается, руки не могут подняться на один уровень, поскольку одна сторона тела слушается хуже.
Источник
Сегодня существует несколько неинвазивных методик, эффективно используемых при сужении сосудов.
К самым популярным в современной эндоваскулярной (сосудистой) хирургии методам относятся ангиопластика и стентирование.
Малоинвазивные операции на сосудах производятся через небольшой прокол или разрез на коже пациента. В сделанное 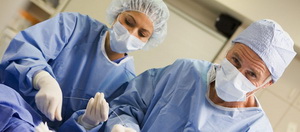 отверстие хирург вводит сначала иглу со специальной сердцевиной – стилетом, а затем катетер – тонкую полую трубочку. Ход процедуры контролируется с помощью рентгеновского монитора. Продвигая катетер вверх по руслу сосуда, его подводят к локализованному заранее посредством ангиографии месту сужения артерии. В зависимости от специфики процедуры, на конце катетера прикреплен стент или баллон.
отверстие хирург вводит сначала иглу со специальной сердцевиной – стилетом, а затем катетер – тонкую полую трубочку. Ход процедуры контролируется с помощью рентгеновского монитора. Продвигая катетер вверх по руслу сосуда, его подводят к локализованному заранее посредством ангиографии месту сужения артерии. В зависимости от специфики процедуры, на конце катетера прикреплен стент или баллон.
Просвет здоровой артерии равномерно широкий, а стенки гладкие. Возраст и атеросклероз провоцируют появление на стенках сосудов отложений, состоящих из фиброзной ткани, кальция и холестерина. Это так называемые атеросклеротические бляшки. Чем больше на стенках артерий таких бляшек, тем сильнее сужается просвет сосуда и ухудшается кровоток. В конечном итоге сужение достигает критической степени, и нормальный кровоток становится невозможен. Развивается ишемия (недостаточное кровоснабжение) и, как следствие, боль и даже некроз (омертвение) тканей.
Ангиопластика (балонная) чаще всего используется для лечения заболеваний периферических сосудов, иногда – для восстановления функциональной проходимости вен. Кроме того, она бывает единственной медицинской альтернативой коронарного шунтирования, в частности, потому что не требует разреза для проведения манипуляций, выполняется под местной анестезией, а период реабилитации после операции достаточно короткий.
Стентирование применяется в случае, если нужно не просто расширить просвет сосуда, но и армировать его постановкой стента – миниатюрного проволочного каркаса.
Показания к операции
Традиционно операция на сосудах показана всем пациентам с умеренным или тяжелым сужением сосудов.
Противопоказанием может служить значительная закупорка сосуда (кончик катетера не проходит через место сужения).
Осложнения, возникающие после стентирования
Нельзя исключать возможность возникновения осложнения после стентирования:
- кровотечение в точке введения катетера;
- образование канала между веной и артерией;
- высокий риск образования тромбов вокруг стента (в первые месяцы после операции);
- возникновение рестеноза;
- закупорка просвета артерии ниже места сужения;
- образование тромба в артерии;
- почечная недостаточность;
- ослабление или разрыв стенки сосуда;
- аллергия на контраст;
- расслоение стенки артерии
Операция по коронарной ангиопластике
Предоперационная подготовка к коронарной ангиопластике (транслюминальной реконструкции) заключается в полном обследовании пациента, в ходе которого обязательно проводятся:
- рентгенографическое исследования грудной клетки;
- электрокардиограмма;
- лабораторные анализы мочи и крови;
- тест на переносимость рентгеноконтраста (в случае, если перед операцией назначено ангиографическое исследование сосудов сердца)
Перед операцией рекомендовано воздерживаться от приема пищи. Касательно приема лекарств (особенно, противодиабетических препаратов) необходимо проконсультироваться у кардиолога.
Специфика процедуры
Через бедренную артерию пациента вводится катетер и проводится к суженному участку артерии для интраоперационной коронарографии, в ходе которой выявляется место и стадия сужения артериального просвета.
На основании полученных данных, кардиохирург выбирает баллон соответствующего размера и подходящий катетер-проводник. Для того чтобы предупредить тромбообразование и дополнительно разжижить кровь, пациенту назначается гепарин.
Катетер-проводник – это тончайшая проволока, имеющая рентгеноконтрастный наконечник, которая вводится в пораженную коронарную артерию пациента. Получив полную картину, кардиохирург направляет проводник в нужное место.
Наконечник выводится за место сужения просвета артерии.
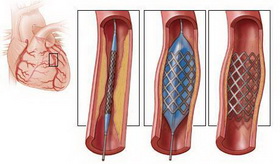
После этого через проводник вводится баллонный катетер, который доставляет баллон на место сужения. После надувания, баллон расширяет просвет артерии, расплющивая бляшку. Если целью операции является постановка стента, то он при раздувании баллона вдавливается в стенку сосуда, армируя пораженный участок и не давая ему сужаться.
Эффект и реабилитация
Как правило, в результате успешно проведенной операции по коронарной ангиопластике значительно улучшается кровоток в коронарных сосудах и значительно сокращается вероятность проведения аортокоронарного шунтирования.
Чтобы минимизировать проявления основного заболевания, следует придерживаться предписанной врачом диеты, воздерживаться от курения и исключить стрессовые моменты.
Уже через шесть часов после успешной операции пациенту разрешают вставать и ходить, но первые два дня он проводит в стационаре кардиоцентра.
Реабилитационный период длится в среднем неделю.
Источник
Из-за многообразия причин сосудистых заболеваний, их клинических проявлений и прогноза для жизни лечение поражений сосудов является достаточно сложной задачей. Потому сосудистые хирурги подходят к ней с большой осторожностью, особенно когда речь заходит о хирургическом вмешательстве и определении вида и объема подобного вмешательства.
Основная цель, которой руководствуются специалисты в этой области при выборе метода лечения – это сохранение максимально возможной жизненной активности больного при минимальном риске для его здоровья и жизни.
Виды операций на сосудах
Операции на сосудах носят реконструктивный характер, т.е. направлены на восстановление утраченной или деформированной функции сосудов.
В сосудистой хирургии реконструктивные операции подразделяются на эндоваскулярные (внутрипросветные) и открытые вмешательства на сосудах.
Открытые реконструктивные операции
Они бывают следующих трех видов:
- Шунтирование – наиболее распространенный вид вмешательства, целью которого является обход закупоренного участка путем соединения собственной трубки (вены) больного или искусственного сосудистого эксплантата с проходимым участком артерии. Эту трубку проводят к незакупоренному участку ниже места закупорки и соединяют с проходимой частью артерии, обеспечивая беспрепятственный проход для крови, а следовательно, и нормальное питание органа или конечности.
- Протезирование – предполагает замещение по прямой закупоренного участка точно такой же трубкой. В отличие от шунтирования, при протезировании беспрепятственный прямой путь для кровотока обеспечивается без сохранения боковых ветвей.
- Эндартерэктомия – предполагает удаление закупоривающей бляшки открытым способом. Этот вид реконструктивной операции проводится на ограниченном участке артерии, чаще всего на глубоких артериях бедра или на сонных артериях. Отверстие в артерии после удаления бляшки ушивается (либо с заплатой, либо без). Преимуществом этого вида хирургического вмешательства является сохранение естественных условий кровотока и отсутствие инородного материала. А недостатками эндартерэктомии являются истончение стенки артерии и большая раневая поверхность в ней.
Эндоваскулярные реконструктивные операции
Этот вид операций осуществляется через просвет сосуда путем проведения через закупоренный участок артерии специального проводника, после установки которого по нему проводят специальный свернутый баллон. Раздуваясь, он разрывает бляшки в просвете сосуда (ангиопластика), в результате чего его проходимость восстанавливается. Затем в обработанную таким образом стенку сосуда внедряется сетчатая металлическая конструкция (стент), чтобы закрепить ее и предотвратить повторную закупорку просвета разорванными бляшками.
Процедура внутрипросветной ангиопластики непродолжительна и проводится под местной анестезией, потому ее можно проводить, в том числе и у ослабленных пациентов.
Отдаленные результаты при открытых реконструктивных операциях значительно лучше, чем при ангиопластике и стентировании. Однако последние являются наиболее предпочтительными в труднодоступных артериях, на которых открытый доступ чреват большой травматичностью.
Однако, несмотря на все потрясающие возможности современной сосудистой хирургии, нужно осознавать, что эти вмешательства лишь позволяют восстановить кровоток из одной точки в другую. Лечение же причины закупорки сосудов – атеросклероза и других заболеваний сосудов – во многом зависит от грамотной медикаментозной терапии и здорового образа жизни.
Источник
Атеросклероз, хирургическое лечение окклюзионных поражений. Хирургия атеросклеротических поражений аорты и артерий получила широкое развитие в 50-60-е годы нашего столетия.
Этому в значительной степени способствовали успехи ангиографических исследований, усовершенствование инструментальной техники, прогресс химии, фармакологии и других наук. В настоящее время реконструктивные оперативные вмешательства при атеросклеротических окклюзиях аорты и артерий выполняются не только на аорте и крупных артериальных стволах, но и на сосудах небольшого диаметра, таких как сосуды сердца, мозга, диаметр которых не превышает 2-3 мм. Широко внедрены в практику реконструктивные операции при атеросклеротических поражениях брюшной аорты и артерий конечностей. Получают распространение оперативные вмешательства при окклюзиях ветвей дуги аорты, чревной, мезентериальных и почечных артерий, а также хирургическое лечение аневризм (см.). Значительным событием являются успехи восстановительной хирургии коронарных артерий при ишемической болезни сердца и вмешательства на сосудах головного мозга.
Условием выполнения реконструктивных операций на аорте и артериях является наличие локализованного, сегментарного атеросклеротического стеноза или окклюзии с сохранением проходимости сосуда выше и ниже участка поражения.
Показанием к операции служит наличие выраженных функциональных, а порой уже и морфологических изменений в органах и тканях, обусловленных недостаточным притоком артериальной крови.
Противопоказанием к оперативным вмешательствам служат генерализация процесса с вовлечением нескольких сосудистых бассейнов и тяжелые сопутствующие заболевания, исключающие значительные по объему хирургические вмешательства.
К первым хирургическим методам лечения относятся, в частности, резекция артерии в сочетании с поясничной симпатэктомией, перевязка одноименной вены (создание редуцированного кровообращения, по В. А. Оппелю).
Первые операции, направленные на улучшение коллатерального кровообращения при атеросклеротических окклюзиях аорты и артерий, были выполнены Леришем (R.Leriche) в 1915 году.
Шейная, грудная, поясничная симпатэктомии до наст, времени сохраняют значение в хирургии атеросклеротических окклюзий брюшной аорты и артерий конечностей. Эти операции оказываются достаточно эффективными только при отсутствии резко выраженной декомпенсации кровообращения с развитием трофических язв и гангрены (см. Симпатэктомия).
Полностью не потеряли значения шейная и грудная симпатэктомии при патологии ветвей дуги аорты и коронарных артерий. Особенно же стволовые симпатэктомии оправданы как дополнение к реконструктивным операциям на сосудах.
Большую роль в развитии реконструктивной хирургии аорты и артерий сыграли работы Карреля (A. Carrel, 1917) и В. Р. Брайцева (1916). В 40-50-х годах 20 века были проведены экспериментальные клинические исследования по выбору пластического материала (гетеро-, гомо-, ауто- и аллопротезы), используемого для восстановления проходимости атеросклеротических окклюзий аорты и др. артерий.
Методом выбора при атеросклеротических окклюзиях аорты и др. артерий являются восстановительные операции.
Из них наиболее распространены следующие: 1) тромбэндартериэктомия; 2) резекция сосуда с протезированием; 3) постоянное обходное шунтирование; 4) боковая пластика сосуда; 5) операция «переключения» артерий; 6) комбинированные операции.
Тромбэндартeриэктомия [предложил дос Сантос (J. С. dos Santos) в 1947 году]. Операция заключается в удалении тромба и измененной внутренней оболочки закупоренного сосуда. Существует несколько способов этой операции.
При «открытой» тромбэндартериэктомии внутреннюю оболочку и тромб удаляют из сосуда после его продольного рассечения на всем протяжении поражения.

Рис. 1. Открытая тромбэндартериэктомия из плече-головного ствола с последующей боковой пластикой заплатой из аллоткани: а – удаление тромба; б – синтетическая заплата вшита.
Для предупреждения сужения просвета артерии и ретромбоза закрытие артерии производят в ряде случаев с помощью аутовенозной или синтетической заплаты, вшиваемой в разрез сосуда (рис. 1). Использование боковой аутовенозной пластики вполне оправдано при тромбартериэктомии из артерий конечностей. Применение же данной методики при реконструкции аорты и ее ветвей нецелесообразно из-за опасности развития аневризмы в области расположения заплаты.
«Полузакрытую» тромбэндартериэктомию производят из нескольких продольных или поперечных разрезов сосуда. Непременным условием в этом случае остается обязательная артериотомия у самой дистальной части поражения. Это дает возможность при необходимости фиксировать внутреннюю оболочку и предупредить ее заворачивание под действием тока крови.
Для удаления измененной внутренней оболочки артерии при «полузакрытой» тромбэндартериэктомии используют различные инструменты: лопаточки, кольца, петли, катетеры и т. д. Удачным в этом отношении следует считать газовую тромбэндартериэктомию. При этом методе внутреннюю оболочку отделяют от средней оболочки сосуда с помощью углекислого газа, который вводят под определенным давлением через иглу и специальный полый зонд со шпателем на конце.
Недостатком «полузакрытой» тромбэндартериэктомии является отсутствие уверенности в полном удалении всей измененной внутренней оболочки, так как без контроля зрения полноценно выполнить эту манипуляцию довольно трудно. Этого недостатка лишена тромбэндартериэктомия методом «выворачивания» [эверсионная эндартериэктомия по Харрисону (J. Н. Harrison), 1967]. Сосуд, пораженный атеросклерозом на небольшом протяжении, выделяют из окружающих тканей и производят поперечный разрез ниже места окклюзии. Тупым инструментом осторожно циркулярно отслаивают измененный внутренний слой артерии вместе с тромбом. Наружныи и средний слои сосуда выворачивают наизнанку до конца окклюзии в проксимальном направлении. Тромб вместе с внутренним слоем удаляют единым слепком. После этого внутреннюю поверхность трансплантата тщательно осматривают, удаляют все обрывки внутренней оболочки, свободно располагающиеся на нем, артерию вворачивают и накладывают анастомоз с периферическим концом сосуда конец в конец.

Рис. 2. Тромбэндартериэктомия методом выворачивания с реимплантацией бифуркации аорты, общих и наружных подвздошных и бедренных артерий: а – тромбоз бифуркации аорты (черным цветом обозначен участок тромбоза); б – иссечение пораженного участка сосуда; в и г – подготовка трансплантата методом выворачивания (черным цветом обозначен тромб); д – проверка трансплантата на герметичность; е – трансплантат вшит.
При поражении атеросклерозом сосуда на значительном протяжении применяют операции эндартериэктомии методом выворачивания с реимплантацией артерии. Сосуд выделяют на всем протяжении и полностью резецируют. Далее артерию извлекают из раны и производят удаление тромба и внутренней оболочки единым слепком по описанной выше методике. Приготовленный таким образом трансплантат проверяют на герметичность и вшивают на прежнее место с наложением анастомозов конец в конец (рис. 2).
Резекция сосуда с протезированием. Это оперативное вмешательство целесообразно выполнять при сравнительно небольших по протяженности поражениях артерий (5-10 см). Дефект артерии замещают либо пластмассовым сосудистым протезом соответствующей длины и диаметра, либо аутовенозным трансплантатом, в качестве которого используют обычно большую подкожную вену бедра. В отдельных случаях при пластике коронарных, сонных и почечных артерий применяют аутоартерию (глубокую артерию бедра или внутреннюю подвздошную артерию).
Преимущества применения аутоартериальных трансплантатов по сравнению с аутовенозными вполне очевидны. Гистологические исследования аутовен в отдаленные сроки после пластики артерий показали, что венозная стенка подвергается резким соединительнотканным изменениям или быстро поражается атеросклерозом, что приводит либо к образованию аневризм, либо к ретромбозу.
Из синтетических протезов наиболее широко применяют лавсановые и дакроновые. В СССР разработаны и внедряются в клинику полубиологические протезы. Полубиологический протез состоит из синтетического каркаса повышенной порозности, пропитанного раствором коллагена и гепарина. Введенный в состав стенки протеза гепарин играет роль местного антикоагулянтного фактора и значительно снижает возможность внутрипротезного тромбообразования. В ряде клиник СССР применяют оригинальные электропроводные протезы с вплетенной в них в виде решетки серебряной нитью. Эти протезы обладают антитромбогенными свойствами, так как их внутренняя стенка несет отрицательный электрический потенциал, аналогичный заряду нормальной внутренней оболочки артерий.
В качестве сосудистых трансплантатов могут использоваться также лиофилизированные гомоартерии и гетероартерии, обработанные различными ферментами.

Рис. 3. Постоянное обходное шунтирование из восходящей аорты в обе подключичные артерии (черным цветом указаны окклюзированные участки артерий).
Постоянное обходное шунтирование. При значительном распространении атеросклеротической окклюзии или при отсутствии возможности выполнения тромбэндартериэктомии (резко выраженный кальциноз артерии) оптимальным методом сосудистой реконструкции является постоянное обходное шунтирование с помощью синтетических протезов или аутовены (рис. 3).
Операция обходного шунтирования имеет некоторые преимущества по сравнению с другими методами реконструкций. При выполнении этой операции полностью сохраняются функционирующие коллатерали, имеющие нередко большое значение для кровоснабжения реваскуляризируемого органа. Кроме того, при тромбозе шунта не столь резко нарушается регионарное кровоснабжение, как это бывает при ретромбозах после резекции артерии с протезированием или после тромбэндартериэктомии.

Рис. 4. Постоянное обходное аутовенозное шунтирование из восходящей аорты в обе коронарные артерии: а – до наложения шунта (черным цветом на коронарных артериях обозначены участки тромбоза, пунктирными кружками на аорте – места вшивания аутовены); б – шунтирование с помощью аутовены завершено.
При окклюзионных поражениях аорты и общих подвздошных артерий используются в основном синтетические протезы. Исключение составляет только аорто-коронарное шунтирование, при котором применяют в основном аутовену (рис. 4). Аутовенозные трансплантаты являются также наилучшими при обходном шунтировании на уровне бедренных, подколенных артерий и сосудов голеней.
При использовании вены в качестве шунта следует учитывать наличие венозных клапанов. Последние должны быть иссечены под контролем зрения. Можно использовать вену для обходного шунтирования и без иссечения клапанов после ее инверсии, если венозные клапаны располагаются по направлению тока крови и не препятствуют кровотоку.
Боковая пластика сосуда производится при сегментарном умеренном стенозе артерии. Операция заключается в расширении просвета сосуда путем вшивания в продольный разрез его стенки заплаты. К этой операции прибегают сравнительно редко, так как непременным условием для ее проведения является наличие сравнительно малоизмененной внутренней оболочки.
Операция «переключения» артерии – весьма редко применяемый вид реконструктивной операции. Она заключается в перераспределении крови из одного сосудистого бассейна в другой. Примером могут служить селезеночно-почечный артериальный анастомоз, переключение наружной сонной артерии в дистальные отделы внутренней. Эти операции проводят в случаях, когда невозможно произвести какую-либо другую хирургическую коррекцию.
Комбинированные операции. В ряде случаев приходится сочетать одновременно несколько вышеуказанных методов восстановления магистрального кровотока. Так, обходное шунтирование нередко сочетают с тромбэндартериэктомией из области дистального анастомоза. При аутоаллопластике синтетические протезы наращивают аутовеной или аутоартерией и т. д. Необходимость и целесообразность подобного сочетания определяются в каждом конкретном случае индивидуально.
Независимо от характера восстановительной операции в техническом отношении неукоснительно должен соблюдаться ряд рекомендаций. Перед пережатием реконструируемого сосуда в дистальный отдел последнего для предупреждения тромбообразования вводят 3000-5000 ЕД гепарина. Концы внутренней оболочки в дистальном участке сосуда, противостоящие току крови, подлежат обязательной фиксации с помощью П-образных швов, завязывающихся снаружи сосуда. Непосредственный успех операции во многом определяет своевременная ликвидация патологического спазма реконструируемых артерий. Это достигается в комплексе с другими мероприятиями механическим расширением артерий специальными пластмассовыми или металлическими бужами.
Эффективность оперативного вмешательства на операционном столе должна оцениваться по определенным объективным тестам. Помимо определения пульсации артерии при пальпации дистальнее места реконструкции, необходимо измерять градиент давления в пораженном сосуде до и после реконструкции. Особенно ценную информацию можно получить путем измерения объемного кровотока по реконструированному сосуду (например, с помощью электромагнитного флюориметра). Исходя из нормальных средних значений объемного кровотока по тому или иному сосуду, можно максимально объективно оценить адекватность хирургической коррекции.
В ближайшем и отдаленном послеоперационном периоде для объективной оценки результатов реконструктивных операций на аорте и артериях используются осциллография, плетизмография, реовазография и аортоартериография. На основании данных, полученных при исследовании, можно судить о величине анастомозов, диаметре сосуда, развитии коллатералей.
В случаях выраженной гиперкоагуляции с резкой активацией свертывающей и угнетением противосвертывающей систем крови проводят, начиная со 2-3-х суток, гепаринотерапию по 2500-5000 ЕД через 4 часа. Введение гепарина продолжают в среднем 3-5 суток, а затем назначают антикоагулянты кумаринового ряда, лечение которыми при особой наклонности к активации свертывающей системы можно рекомендовать на протяжении нескольких недель и даже месяцев.
В ближайшем послеоперационном периоде может развиться острый тромбоз реконструированной сосудистой магистрали. По данным различных авторов, общее количество послеоперационных острых тромбозов колеблется в довольно широких пределах: от 3 до 20%.
Основными причинами развития острых послеоперационных тромбозов являются: дефекты оперативной техники; недостатки анестезиологического пособия (коллапс, неадекватное восполнение кровопотери); послеоперационные осложнения (паравазальные и парапротезные гематомы, нагноение).
При острых послеоперационных тромбозах, протекающих с резким нарушением кровообращения и нарушением функции соответствующего органа, показана экстренная повторная тромбэктомия. В остальных случаях допустимо проведение антикоагулянтного лечения с использованием тромболитических препаратов: фибринолизина, стрептокиназы, урокиназы, тромболитина.
Тяжелым осложнением после реконструктивных операций на сосудах является кровотечение. Следует различать первичные кровотечения, возникающие в первые 3 суток после операции, и вторичные – аррозионные, возникающие в сроки примерно от 5 суток до нескольких месяцев. Причиной первичных кровотечений обычно бывают дефекты оперативной техники и нарушения со стороны свертывающей системы крови, обусловленные неправильным назначением антикоагулянтов на фоне недостаточно хорошего гемостаза.
Вторичные аррозионные кровотечения, как правило, связаны с нагноением раны.
При любых видах кровотечения показана немедленная операция с ревизией раны и остановкой кровотечения. В гнойной ране при аррозионных кровотечениях допустимы только лигатурные способы их остановки. Пластмассовые материалы из раны в этих случаях должны быть удалены. Профилактика послеоперационных кровотечений – совершенная техника сосудистого шва, правильный выбор пластического материала, тщательный гемостаз, назначение антикоагулянтов по строгим показаниям и правильное ведение послеоперационной раны.
Отдаленные результаты реконструктивных операций при атеросклеротических окклюзиях аорты и др. артерий вполне ободряющие. Они будут несравненно лучше, если удастся разработать эффективные методы профилактики прогрессирования атеросклеротического процесса, который в отдаленном периоде является основной причиной ретромбозов.
Библиография: Колесов В. И. Хирургическое лечение коронарной болезни сердца, М., 1966; Петровский Б. В., Князев М. Д. и Скуиня М. А. Операции при хронических окклюзиях аорто-бедренной зоны, Хирургия, № 1, с. 12, 1971, библиогр.; Реконструктивная хирургия, под ред. Б. В. Петровского, в. 2, М., 1971; Хилькин А. М. и др. О конструкции полубиологических сосудистых протезов, в кн.: Трансплантация о
