Давление азота на сосуд

Äàëåå: 1.2.
Çàäà÷è äëÿ ñàìîñòîÿòåëüíîãî
Ââåðõ: 1.
Ìîëåêóëÿðíàÿ ôèçèêà è
Íàçàä: 1.
Ìîëåêóëÿðíàÿ ôèçèêà è
1.1. Ïðèìåðû ðåøåíèÿ
çàäà÷
Ïðèìåð 1.1. Ñæèæåííûå ãàçû õðàíÿò â ñîñóäàõ,
ñîîáùàþùèõñÿ ñ àòìîñôåðîé. Ìîæíî ëè
äîïóñòèòü èñïàðåíèå æèäêîãî àçîòà îáúåìîì ![]() è
è
ïëîòíîñòüþ
![]() â
â
çàêðûòîì ñîñóäå îáúåìîì ![]() ïðè íàãðåâàíèè
ïðè íàãðåâàíèè
åãî äî òåìïåðàòóðû ![]() , åñëè ñòåíêè ñîñóäà
, åñëè ñòåíêè ñîñóäà
âûäåðæèâàþò äàâëåíèå
![]() ?
?
 Ðåøåíèå.
Ðåøåíèå.
Ïðè ïîâûøåíèè òåìïåðàòóðû æèäêèé àçîò ïåðåéäåò â ãàçîîáðàçíîå
ñîñòîÿíèå.
Ïðèìåì åãî ïðè òåìïåðàòóðå ![]() çà èäåàëüíûé ãàç è
çà èäåàëüíûé ãàç è
ïðèìåíèì äëÿ ðåøåíèÿ
óðàâíåíèå Êëàïåéðîíà – Ìåíäåëååâà:
| (1) |
ãäå ![]() ,
, ![]() è
è ![]() – äàâëåíèå, îáúåì è
– äàâëåíèå, îáúåì è
òåìïåðàòóðà ãàçà; ![]() – åãî ìàññà,
– åãî ìàññà, ![]() – ìàññà
– ìàññà
ìîëÿ àçîòà, ðàâíàÿ ![]() ;
; ![]() – óíèâåðñàëüíàÿ
– óíèâåðñàëüíàÿ
ãàçîâàÿ ïîñòîÿííàÿ.
Äëÿ îòâåòà íà âîïðîñ çàäà÷è íóæíî îïðåäåëèòü äàâëåíèå ãàçîîáðàçíîãî
àçîòà è ñðàâíèòü åãî ñ
ìàêñèìàëüíî äîïóñòèìûì.
Âûðàçèì èñêîìîå äàâëåíèå èç óðàâíåíèÿ 1:
| (2) |
çäåñü íåèçâåñòíà ìàññà ãàçà, åå ìîæíî îïðåäåëèòü ÷åðåç îáúåì è
ïëîòíîñòü æèäêîãî àçîòà:
![]() . Âûðàæåíèå äëÿ èñêîìîãî äàâëåíèÿ â îáùåì âèäå:
. Âûðàæåíèå äëÿ èñêîìîãî äàâëåíèÿ â îáùåì âèäå:
| (3) |
Ïðîâåðêà íàèìåíîâàíèÿ åäèíèöû èñêîìîé âåëè÷èíû:
![]()
Ýòî åäèíèöà äàâëåíèÿ â ÑÈ, ñëåäîâàòåëüíî, âûðàæåíèå â îáùåì âèäå
ïîëó÷åíî ïðàâèëüíî.
Âû÷èñëåíèÿ: ïîäñòàâèì ÷èñëà (âñå îíè äîëæíû áûòü âûðàæåíû â
ÑÈ):
![]()
Ïðåæäå ÷åì âû÷èñëÿòü, ïðîâåäåì äåéñòâèÿ ñî ñòåïåíÿìè:
![]()
Èñêîìîå äàâëåíèå ðàâíî ![]() èëè
èëè ![]() è ïðåâûøàåò
è ïðåâûøàåò
äîïóñòèìîå.
Îòâåò: èñïàðåíèå æèäêîãî àçîòà äàííîé ìàññû â çàêðûòîì ñîñóäå
óêàçàííîãî îáúåìà íåëüçÿ
äîïóñòèòü, òàê êàê ïðè ![]() äàâëåíèå ïðåâûñèò
äàâëåíèå ïðåâûñèò
äîïóñòèìîå. Ïîýòîìó ñæèæåííûå ãàçû õðàíÿò
â îòêðûòûõ ñîñóäàõ.
Ïðèìåð 1.2. Öèëèíäðè÷åñêàÿ òðóáêà äëèíîé ![]() íàïîëîâèíó ïîãðóæåíà â ðòóòü. Çàêðûâ åå ñâåðõó,
íàïîëîâèíó ïîãðóæåíà â ðòóòü. Çàêðûâ åå ñâåðõó,
òðóáêó âûíèìàþò, ïðè ýòîì ÷àñòü ðòóòè âûëèâàåòñÿ. Êàêîé äëèíû ñòîëáèê
ðòóòè îñòàíåòñÿ â òðóáêå,
åñëè àòìîñôåðíîå äàâëåíèå ðàâíî ![]() ìì ðò. ñò.?
ìì ðò. ñò.?
 Ðåøåíèå.
Ðåøåíèå.
Ïðèìåì âîçäóõ, íàõîäÿùèéñÿ â òðóáêå íàä ðòóòüþ, çà èäåàëüíûé ãàç.
Ïîñêîëüêó â óñëîâèè çàäà÷è
èçìåíåíèå òåìïåðàòóðû íå îãîâîðåíî, ê ñòîëáèêó âîçäóõà ìîæíî ïðèìåíèòü
çàêîí Áîéëÿ – Ìàðèîòòà:
| (4) |
ãäå ![]() è
è ![]() — äàâëåíèå è îáúåì
— äàâëåíèå è îáúåì
âîçäóõà â ïåðâîì ñîñòîÿíèè; ![]() è
è ![]() — òî æå âî
— òî æå âî
âòîðîì ñîñòîÿíèè.

Äëÿ îòâåòà íà âîïðîñ çàäà÷è íóæíî âûðàçèòü ïàðàìåòðû ãàçà ÷åðåç
èçâåñòíûå â îáùåì âèäå
âåëè÷èíû – ![]() è
è ![]() . Îáîçíà÷èì èñêîìóþ
. Îáîçíà÷èì èñêîìóþ
äëèíó ñòîëáèêà ðòóòè ÷åðåç ![]() .  ïåðâîì
. Â ïåðâîì
ñîñòîÿíèè ñòîëáèê âîçäóõà äëèíîé ![]() , òî åñòü îáúåìîì
, òî åñòü îáúåìîì
![]() (
(![]() – ïëîùàäü
– ïëîùàäü
ñå÷åíèÿ òðóáêè), íàõîäèëñÿ ïîä àòìîñôåðíûì äàâëåíèåì, òàê êàê òðóáêà
áûëà îòêðûòà ñâåðõó.
Âûðàçèì àòìîñôåðíîå äàâëåíèå: ![]() ,
,
ãäå ![]() – ïëîòíîñòü ðòóòè. Òàêèì îáðàçîì,
– ïëîòíîñòü ðòóòè. Òàêèì îáðàçîì,
| (5) |
Âî âòîðîì ñîñòîÿíèè äëèíà ñòîëáèêà âîçäóõà ñòàëà ðàâíîé ![]() , à åãî îáúåì
, à åãî îáúåì ![]() .
.
Äàâëåíèå âîçäóõà â ñóììå ñ äàâëåíèåì îñòàâøåãîñÿ ñòîëáèêà ðòóòè âûñîòîé
![]() óðàâíîâåøèâàåòñÿ
óðàâíîâåøèâàåòñÿ
àòìîñôåðíûì äàâëåíèåì, äåéñòâóþùèì ñîãëàñíî çàêîíó Ïàñêàëÿ íà íèæíèé
îòêðûòûé êîíåö òðóáêè:
![]() , îòêóäà äàâëåíèå
, îòêóäà äàâëåíèå
![]()
| (6) |
Ïîäñòàâèâ âûðàæåíèÿ (5 è 6)
â èñõîäíîå óðàâíåíèå (4) è
ñîêðàòèâ íà ![]() , ïîëó÷èì êâàäðàòíîå óðàâíåíèå
, ïîëó÷èì êâàäðàòíîå óðàâíåíèå
îòíîñèòåëüíî ![]() :
:
| (7) |
Äâà êîðíÿ ýòîãî óðàâíåíèÿ:
![]()
Ìàòåìàòè÷åñêàÿ ÷àñòü çàäà÷è âûïîëíåíà: íàéäåíû êîðíè êâàäðàòíîãî
óðàâíåíèÿ. Îäíàêî
óñëîâèþ ôèçè÷åñêîé çàäà÷è êîðåíü óðàâíåíèÿ ñî çíàêîì “+” íå
óäîâëåòâîðÿåò, òàê êàê äëèíà
ñòîëáèêà ðòóòè â ýòîì ñëó÷àå ïðåâûøàåò äëèíó òðóáêè ![]() . Ïîýòîìó
. Ïîýòîìó
![]() . Âèäíî, ÷òî
. Âèäíî, ÷òî ![]() ïîëó÷èòñÿ â åäèíèöàõ äëèíû.
ïîëó÷èòñÿ â åäèíèöàõ äëèíû.
 ÷èñëîâîì âàðèàíòå ðåøåíèÿ ïîäîáíîé çàäà÷è ![]() è
è ![]() íóæíî ïîäñòàâëÿòü â îäèíàêîâûõ
íóæíî ïîäñòàâëÿòü â îäèíàêîâûõ
åäèíèöàõ äëèíû, íàïðèìåð, â ì.
Îòâåò: èñêîìàÿ äëèíà ñòîëáèêà âûðàæàåòñÿ òàê:
![]()
Ïðèìåð 1.3.  ñòåêëÿííîì ñôåðè÷åñêîì ñîñóäå ñ
âíóòðåííèì äèàìåòðîì ![]() íàõîäèòñÿ àçîò,
íàõîäèòñÿ àçîò,
äàâëåíèå êîòîðîãî ïðè òåìïåðàòóðå ![]()
ðàâíî 1,33 Ïà. Íà ñòåíêàõ âíóòðè ñîñóäà èìååòñÿ
ìîíîìîëåêóëÿðíûé (òîëùèíîé â îäíó ìîëåêóëó) ñëîé àäñîðáèðîâàííîãî, òî
åñòü ïîãëîùåííîãî
ïîâåðõíîñòíûì ñëîåì, àçîòà. Îäíà ìîëåêóëà çàíèìàåò ïëîùàäü
![]() . Íàéòè
. Íàéòè
äàâëåíèå àçîòà â ñîñóäå ïðè òåìïåðàòóðå ![]() ,
,
ïðè êîòîðîé îí ïîëíîñòüþ äåñîðáèðóåòñÿ
ñî ñòåíîê.
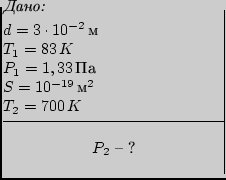 Ðåøåíèå.
Ðåøåíèå.
Àçîò ïðè òàêîì íèçêîì äàâëåíèè ìîæíî ðàññìàòðèâàòü êàê èäåàëüíûé ãàç è
ïðèìåíèòü ñîîòâåòñòâóþùóþ òåîðèþ.
Èñêîìîå äàâëåíèå ![]() áóäåò ñêëàäûâàòüñÿ èç äàâëåíèÿ
áóäåò ñêëàäûâàòüñÿ èç äàâëåíèÿ
ãàçà, ïåðâîíà÷àëüíî íàõîäèâøåãîñÿ
â ñîñóäå ![]() , è äàâëåíèÿ
, è äàâëåíèÿ ![]() , êîòîðîå ñîçäàäóò
, êîòîðîå ñîçäàäóò
ìîëåêóëû, ïåðåøåäøèå ñî ñòåíîê
â cocóä ïðè òåìïåðàòóðå ![]() :
:
| (8) |
Âûðàçèì äàâëåíèå ![]() , ó÷èòûâàÿ, ÷òî ïîâûøåíèå
, ó÷èòûâàÿ, ÷òî ïîâûøåíèå
òåìïåðàòóðû ïðîèñõîäèò ïðè ïîñòîÿííîì
îáúåìå. Ñîãëàñíî çàêîíó Øàðëÿ:
![]()
| (9) |
Âèäíî, ÷òî åäèíèöà èçìåðåíèÿ ![]() ïîëó÷àåòñÿ òàêàÿ æå,
ïîëó÷àåòñÿ òàêàÿ æå,
êàê ![]() – Ïà.
– Ïà.
Äàâëåíèå ![]() âûðàçèì èç îñíîâíîãî óðàâíåíèÿ
âûðàçèì èç îñíîâíîãî óðàâíåíèÿ
êèíåòè÷åñêîé òåîðèè èäåàëüíîãî ãàçà:
| (10) |
ãäå ![]() – îáùåå ÷èñëî äåñîðáèðîâàííûõ ìîëåêóë,
– îáùåå ÷èñëî äåñîðáèðîâàííûõ ìîëåêóë, ![]() – èõ êîíöåíòðàöèÿ,
– èõ êîíöåíòðàöèÿ,
![]() – ïîñòîÿííàÿ Áîëüöìàíà,
– ïîñòîÿííàÿ Áîëüöìàíà, ![]() – îáúåì ñîñóäà:
– îáúåì ñîñóäà:
![]() .
.
Îáùåå ÷èñëî ìîëåêóë, ïåðåøåäøèõ ñî ñòåíîê â ñîñóä, ìîæíî âûðàçèòü êàê
îòíîøåíèå
ïëîùàäè âíóòðåííåé ïîâåðõíîñòè ñôåðè÷åñêîãî ñîñóäà ![]()
ê ïëîùàäè îäíîé ìîëåêóëû: ![]() . Îêîí÷àòåëüíî äëÿ äàâëåíèÿ
. Îêîí÷àòåëüíî äëÿ äàâëåíèÿ ![]() ïîëó÷èì:
ïîëó÷èì:
| (11) |
Ïðîâåðêà åäèíèö èçìåðåíèÿ èñêîìîé âåëè÷èíû:
![]()
Ïîëó÷åíà åäèíèöà äàâëåíèÿ, òî åñòü âûðàæåíèå â îáùåì âèäå ïðàâèëüíî.
Òàêèì îáðàçîì,
| (12) |
Âû÷èñëåíèÿ:
![]()
![]()
Âèäíî, ÷òî ïî ïîðÿäêó âåëè÷èíû äåéñòâèå îáîèõ ôàêòîðîâ: ðîñòà äàâëåíèÿ
ñ ïîâûøåíèåì
òåìïåðàòóðû è óâåëè÷åíèÿ êîíöåíòðàöèè ìîëåêóë â ñîñóäå — ñîãëàñóåòñÿ
ïî ïîðÿäêó âåëè÷èí.
Âòîðîé ôàêòîð â äàííîì ñëó÷àå îêàçûâàåò áîëüøåå äåéñòâèå.
Îòâåò: äàâëåíèå àçîòà â ñîñóäå ñòàíåò ðàâíûì 30,54 Ïà.
Ïðèìåð 1.4. Íàéòè ñðåäíåå ÷èñëî âñåõ ïàðíûõ
ñòîëêíîâåíèé â ñåêóíäó ìîëåêóë êèñëîðîäà,
íàõîäÿùèõñÿ â îáúåìå ![]() ïðè òåìïåðàòóðå
ïðè òåìïåðàòóðå ![]() è äàâëåíèè 666,5
è äàâëåíèè 666,5
Ïà.
 Ðåøåíèå.
Ðåøåíèå.
Ñîãëàñíî ÌÊÒ èäåàëüíîãî ãàçà ñðåäíåå ÷èñëî ñòîëêíîâåíèé â ñåêóíäó
îäíîé
ìîëåêóëû
ðàâíî:
| (13) |
ãäå ![]() – ýôôåêòèâíûé äèàìåòð ìîëåêóëû,
– ýôôåêòèâíûé äèàìåòð ìîëåêóëû, ![]() – êîíöåíòðàöèÿ ãàçà,
– êîíöåíòðàöèÿ ãàçà, ![]()
–
ñðåäíÿÿ àðèôìåòè÷åñêàÿ ñêîðîñòü ìîëåêóë.
Åñëè ó÷èòûâàòü òîëüêî ïàðíûå
ñòîëêíîâåíèÿ, ÷èñëî âñåõ ñòîëêíîâåíèé â
ñåêóíäó áóäåò áîëüøå â ![]() ðàç, ãäå
ðàç, ãäå ![]() – îáùåå
– îáùåå
÷èñëî ìîëåêóë.
Òîãäà èñêîìîå ÷èñëî ñòîëêíîâåíèé âûðàçèòñÿ òàê:
| (14) |
Äàëåå ñëåäóåò âûðàçèòü êîíöåíòðàöèþ ãàçà èç îñíîâíîãî óðàâíåíèÿ
êèíåòè÷åñêîé òåîðèè
èäåàëüíîãî ãàçà: ![]() , à ñðåäíþþ àðèôìåòè÷åñêóþ ñêîðîñòü
, à ñðåäíþþ àðèôìåòè÷åñêóþ ñêîðîñòü
— ÷åðåç ïàðàìåòðû ãàçà:
![]() , ãäå
, ãäå ![]() — óíèâåðñàëüíàÿ (ìîëÿðíàÿ) ãàçîâàÿ ïîñòîÿííàÿ.
— óíèâåðñàëüíàÿ (ìîëÿðíàÿ) ãàçîâàÿ ïîñòîÿííàÿ.
Ïîñëå ïîäñòàíîâêè äëÿ èñêîìîé âåëè÷èíû ïîëó÷àåòñÿ:
 | (15) |
 ýòîì âûðàæåíèè âñå, êðîìå äèàìåòðà ìîëåêóëû, èçâåñòíî. Ýòî ÷èñëî
âçÿòî èç òàáëèöû.
Ïðîâåðêà åäèíèöû èçìåðåíèÿ èñêîìîé âåëè÷èíû:
![begin{displaymath}[overline{Z}]={{ì}^2cdot{Í}^2cdot{Ê}^2cdot{ì}^3cdot{Äæ}^... ... 2}over{ñ}cdot{ì}^{3over 2}cdot{êã}^{1over 2}}={ñ}^{-1},.end{displaymath}](https://cito-web.yspu.org/link1/metod/met8/img116.png)
Íàèìåíîâàíèå ![]() ñîîòâåòñòâóåò ÷èñëó ñòîëêíîâåíèé â
ñîîòâåòñòâóåò ÷èñëó ñòîëêíîâåíèé â
ñåêóíäó.
Âû÷èñëåíèÿ:
![]()
Îòâåò: ïðè óêàçàííûõ óñëîâèÿõ ïðîèñõîäèò
![]() ïàðíûõ ñòîëêíîâåíèé ìîëåêóë
ïàðíûõ ñòîëêíîâåíèé ìîëåêóë
â ñåêóíäó. Ýòî ÷èñëî çàâèñèò îò ïàðàìåòðîâ ñîñòîÿíèÿ (![]() ), îáúåìà ãàçà è åãî
), îáúåìà ãàçà è åãî
èíäèâèäóàëüíûõ õàðàêòåðèñòèê: äèàìåòðà ìîëåêóëû è ìîëÿðíîé ìàññû.
Ïðèìåð 1.5. Ðàññòîÿíèå ìåæäó ñòåíêàìè ñîñóäà ðàâíî ![]() . Ïðè êàêîì äàâëåíèè âÿçêîñòü
. Ïðè êàêîì äàâëåíèè âÿçêîñòü
ãàçà, íàõîäÿùåãîñÿ ìåæäó íèìè, íà÷íåò óìåíüøàòüñÿ ïðè îòêà÷êå?
Òåìïåðàòóðà ãàçà ðàâíà
![]() . Äèàìåòð ìîëåêóëû ñîñòàâëÿåò
. Äèàìåòð ìîëåêóëû ñîñòàâëÿåò
![]() .
.
 Ðåøåíèå.
Ðåøåíèå.
Òåîðåòè÷åñêè âÿçêîñòü ãàçà ïðè íå ñëèøêîì íèçêèõ äàâëåíèÿõ
íå çàâèñèò îò íåãî:
| (16) |
òàê êàê ![]() – ñðåäíÿÿ äëèíà ñâîáîäíîãî ïðîáåãà ìîëåêóë îáðàòíî
– ñðåäíÿÿ äëèíà ñâîáîäíîãî ïðîáåãà ìîëåêóë îáðàòíî
ïðîïîðöèîíàëüíà äàâëåíèþ ïðè ïîñòîÿííîé òåìïåðàòóðå:
| (17) |
à ïëîòíîñòü ãàçà ![]() ïðÿìî ïðîïîðöèîíàëüíà äàâëåíèþ.
ïðÿìî ïðîïîðöèîíàëüíà äàâëåíèþ.
Âûðàæåíèå äëÿ ïëîòíîñòè èäåàëüíîãî ãàçà
ìîæíî ïîëó÷èòü èç óðàâíåíèÿ Êëàïåéðîíà – Ìåíäåëååâà:
![]() , ó÷èòûâàÿ,
, ó÷èòûâàÿ,
÷òî ïëîòíîñòü — ýòî ìàññà åäèíèöû îáúåìà:
![]() . Ïîëó÷àåòñÿ, ÷òî
. Ïîëó÷àåòñÿ, ÷òî
![]() .
.
Ïðè íèçêîì äàâëåíèè ñðåäíÿÿ äëèíà ñâîáîäíîãî ïðîáåãà
ïåðåñòàåò
çàâèñåòü îò äàâëåíèÿ è îïðåäåëÿåòñÿ ðàçìåðàìè ñîñóäà:
| (18) |
Ìîëåêóëû äâèæóòñÿ îò ñòåíêè ê ñòåíêå, íå ñòàëêèâàÿñü ìåæäó ñîáîé.
Âÿçêîñòü ãàçà íà÷íåò
óìåíüøàòüñÿ ïðè äàëüíåéøåé îòêà÷êå ñîñóäà çà ñ÷åò óìåíüøåíèÿ
êîíöåíòðàöèè ìîëåêóë
(ïëîòíîñòè ãàçà).
Äëÿ ðåøåíèÿ çàäà÷è íóæíî ïðèðàâíÿòü âûðàæåíèå äëÿ ñðåäíåé äëèíû
ñâîáîäíîãî
ïðîáeãa ìîëåêóë ![]() ðàññòîÿíèþ ìåæäó ñòåíêàìè ñîñóäà:
ðàññòîÿíèþ ìåæäó ñòåíêàìè ñîñóäà:
![]()
è âûðàçèòü äàâëåíèå. Ïîëó÷àåì:
| (19) |
 ýòîì âûðàæåíèè äëÿ äàâëåíèÿ âñå èçâåñòíî.
Ïðîâåðêà íàèìåíîâàíèÿ åäèíèöû èçìåðåíèÿ:
![]()
Âûðàæåíèå äëÿ äàâëåíèÿ â îáùåì âèäå ïîëó÷åíî ïðàâèëüíî.
Âû÷èñëåíèÿ:
![]()
Ïîëó÷åííîå ÷èñëî çíà÷èòåëüíî ìåíüøå âåëè÷èíû àòìîñôåðíîãî äàâëåíèÿ. Äëÿ
äàííîãî ãàçà ïðè íåèçìåííîé
òåìïåðàòóðå îíî îïðåäåëÿåòñÿ òîëüêî ðàçìåðàìè ñîñóäà ![]() .
.
Îòâåò: ïðè äàâëåíèè 1,26 Ïà âÿçêîñòü ãàçà íà÷íåò óìåíüøàòüñÿ
ïðè îòêà÷êå.
Óêàçàíèå: ïîäîáíûì îáðàçîì ðåøàþòñÿ çàäà÷è, ñâÿçàííûå ñ
êîýôôèöèåíòîì òåïëîïðîâîäíîñòè
èäåàëüíîãî ãàçà:
![]()
ãäå ![]() – óäåëüíàÿ òåïëîåìêîñòü
– óäåëüíàÿ òåïëîåìêîñòü
ïðè ïîñòîÿííîì îáúåìå:
![]()
Ïðèìåð 1.6. 10 ë àçîòà, íàõîäÿùåãîñÿ ïîä äàâëåíèåì ![]() , ðàñøèðÿþòñÿ âäâîå.
, ðàñøèðÿþòñÿ âäâîå.
Íàéòè êîíå÷íîå äàâëåíèå è ñîâåðøåííóþ ãàçîì ðàáîòó â ñëó÷àÿõ
èçîáàðè÷åñêîãî,
èçîòåðìè÷åñêîãî è àäèàáàòè÷åñêîãî ïðîöåññîâ. Ìîëåêóëû àçîòà èìåþò ïÿòü
ñòåïåíåé ñâîáîäû.
 Ðåøåíèå.
Ðåøåíèå.
Ïðèìåì àçîò â äàííûõ óñëîâèÿõ çà èäåàëüíûé ãàç.
1. Ïðè èçîáàðè÷åñêîì ïðîöåññå äàâëåíèå ãàçà íå ìåíÿåòñÿ, ïîýòîìó ![]() .
.
Ýëåìåíòàðíàÿ ðàáîòà ðàñøèðåíèÿ ðàâíà â îáùåì ñëó÷àå ![]() , ãäå
, ãäå ![]() – äàâëåíèå,
– äàâëåíèå,
![]() – áåñêîíå÷íî ìàëûé îáúåì. Ïîëíàÿ ðàáîòà íàõîäèòñÿ ïóòåì
– áåñêîíå÷íî ìàëûé îáúåì. Ïîëíàÿ ðàáîòà íàõîäèòñÿ ïóòåì
èíòåãðèðîâàíèÿ, è âåëè÷èíà
eå çàâèñèò îò âèäà ïðîöåññà.
Ïðè èçîáàðè÷åñêîì ïðîöåññå
 | (20) |
Ïðîâåðèì åäèíèöó èçìåðåíèÿ ðàáîòû:
![]()
2.  èçîòåðìè÷åñêîì ïðîöåññå òåìïåðàòóðà îñòàåòñÿ ïîñòîÿííîé, à
äàâëåíèÿ è îáúåìû â äâóõ
ñîñòîÿíèÿõ èäåàëüíîãî ãàçà ñâÿçàíû çàêîíîì Áîéëÿ – Ìàðèîòòà: ![]() , îòêóäà
, îòêóäà
![]() . Âèäíî, ÷òî çäåñü äëÿ åäèíèöû íåèçâåñòíîãî äàâëåíèÿ
. Âèäíî, ÷òî çäåñü äëÿ åäèíèöû íåèçâåñòíîãî äàâëåíèÿ
ïîëó÷àåòñÿ
Ïà (ïàñêàëü).
Ðàáîòà èçîòåðìè÷åñêîãî ðàñøèðåíèÿ ðàññ÷èòûâàåòñÿ òàê:

Çäåñü äàâëåíèå âûðàæåíî èç óðàâíåíèÿ Êëàïåéðîíà – Ìåíäåëååâà.
Òåìïåðàòóðà
íåèçâåñòíà, ïîýòîìó, ïðèìåíèâ åùå ðàç óðàâíåíèå Êëàïåéðîíà –
Ìåíäåëååâà, ïîëó÷èì âûðàæåíèå
äëÿ èñêîìîé ðàáîòû ÷åðåç èçâåñòíûå â óñëîâèè âåëè÷èíû:
| (21) |
Ðåçóëüòàò íå èçìåíèòñÿ, åñëè ïîäñòàâèòü êîíå÷íûå äàâëåíèå è îáúåì ![]() è
è
![]() èëè âìåñòî îòíîøåíèÿ
èëè âìåñòî îòíîøåíèÿ ![]() âçÿòü
âçÿòü ![]() .
.
3. Êîíå÷íîå äàâëåíèå àäèàáàòè÷åñêîãî ðàñøèðåíèÿ âûðàçèì èç óðàâíåíèÿ
Ïóàññîíà:
![]()
(![]() – ÷èñëî ñòåïåíåé ñâîáîäû ìîëåêóëû).
– ÷èñëî ñòåïåíåé ñâîáîäû ìîëåêóëû).
Ðàáîòà â ýòîì ïðîöåññå ñîâåðøàåòñÿ çà ñ÷åò óáûëè âíóòðåííåé ýíåðãèè
ãàçà:
![]()
ãäå ![]() – ìîëÿðíàÿ òåïëîåìêîñòü ïðè ïîñòîÿííîì îáúåìå:
– ìîëÿðíàÿ òåïëîåìêîñòü ïðè ïîñòîÿííîì îáúåìå:
![]()

 ýòîé çàäà÷å òåìïåðàòóðû íå çàäàíû, ïîýòîìó îòíîøåíèå òåìïåðàòóð
ñëåäóåò çàìåíèòü îòíîøåíèåì
îáúåìîâ
 è âîñïîëüçîâàòüñÿ
è âîñïîëüçîâàòüñÿ
óðàâíåíèåì ñîñòîÿíèÿ èäåàëüíîãî ãàçà:

| (22) |
Çäåñü âñå èçâåñòíî, êîíå÷íîå äàâëåíèå ìîæíî ðàññ÷èòàòü îòäåëüíî.
Âû÷èñëåíèÿ:
-
 .
. -


-


Òàêèì îáðàçîì, íàèáîëüøåå èçìåíåíèå äàâëåíèÿ ïðîèñõîäèò ïðè
àäèàáàòè÷åñêîì ðàñøèðåíèè,
à íàèáîëüøàÿ ðàáîòà ñîâåðøàåòñÿ ïðè èçîáàðè÷åñêîì. Êà÷åñòâåííî
ðåçóëüòàòû ïðåäñòàâëåíû
íà ðèñóíêå. Ïëîùàäè ôèãóð ïîä ãðàôèêàìè ïðîöåññîâ ïîçâîëÿþò ñóäèòü î
ñîîòíîøåíèè ñîâåðøåííîé
ðàáîòû.
Îòâåò:
![]()
Ïðèìåð 1.7. Õîëîäèëüíàÿ ìàøèíà, ðàáîòàþùàÿ ïî
îáðàòíîìó öèêëó Êàðíî, ïåðåäàåò òåïëîòó îò
õîëîäèëüíèêà ñ âîäîé ïðè òåìïåðàòóðå ![]()
êèïÿòèëüíèêó ñ âîäîé ïðè òåìïåðàòóðå ![]() C.
C.
Êàêóþ ìàññó âîäû íóæíî çàìîðîçèòü â õîëîäèëüíèêå, ÷òîáû ïðåâðàòèòü â
ïàð 1 êã âîäû â
êèïÿòèëüíèêå? Óäåëüíàÿ òåïëîòà ïàðîîáðàçîâàíèÿ âîäû ïðè ![]() Ñ ðàâíà
Ñ ðàâíà
![]() . Óäåëüíàÿ òåïëîòà ïëàâëåíèÿ ëüäà ðàâíà
. Óäåëüíàÿ òåïëîòà ïëàâëåíèÿ ëüäà ðàâíà
![]() .
.
 Ðåøåíèå.
Ðåøåíèå.
Õîëîäèëüíàÿ ìàøèíà çà ñ÷åò âíåøíåé ðàáîòû îòíèìàåò íåêîòîðîå êîëè÷åñòâî
òåïëîòû ![]()
îò ìåíåå íàãðåòîãî òåëà ïðè òåìïåðàòóðå ![]() è
è
ïåðåäàåò òåïëîòó ![]() áîëåå íàãðåòîìy òåëó
áîëåå íàãðåòîìy òåëó
ïðè òåìïåðàòóðå ![]() .
.
Êîýôôèöèåíò ïîëåçíîãî äåéñòâèÿ åå
![]() .
.
Òàêîå æå ñîîòíîøåíèå ñïðàâåäëèâî è äëÿ òåïëîâîé ìàøèíû, ñîâåðøàþùåé
ðàáîòó çà ñ÷åò ÷àñòè
òåïëîòû, âçÿòîé ó áîëåå íàãðåòîãî òåëà.
Íàèáîëüøèé êîýôôèöèåíò ïîëåçíîãî äåéñòâèÿ ñîîòâåòñòâóåò èäåàëüíîìó
(òåîðåòè÷åñêîìó) öèêëó Êàðíî.
 ýòîì ñëó÷àå
![]() , òî åñòü êïä
, òî åñòü êïä
îïðåäåëÿåòñÿ òîëüêî
òåìïåðàòóðàìè íàãðåâàòåëÿ (òåëà ïðè òåìïåðàòóðå ![]() ) è
) è
õîëîäèëüíèêà (![]() ). Ñ ïîìîùüþ
). Ñ ïîìîùüþ
ýòîãî ñîîòíîøåíèÿ ðåøàåòñÿ áîëüøèíñòâî çàäà÷, ñâÿçàííûõ ñ ðàáîòîé
òåïëîâûõ è õîëîäèëüíûõ ìàøèí.
 ðåàëüíûõ ìàøèíàõ êïä çíà÷èòåëüíî ìåíüøå, ÷åì
![]() .
.
 äàííîé çàäà÷å êîëè÷åñòâî òåïëîòû ![]() , ïåðåäàâàåìîå áîëåå
, ïåðåäàâàåìîå áîëåå
íàãðåòîìó òåëó, ðàâíî ![]() ,
,
à êîëè÷åñòâî òåïëîòû ![]() , âçÿòîå îò ìåíåå íàãðåòîãî òåëà,
, âçÿòîå îò ìåíåå íàãðåòîãî òåëà,
ðàâíî ![]() , ïîýòîìó
, ïîýòîìó
ñïðàâåäëèâî ðàâåíñòâî:
| (23) |
êîòîðîå ìîæíî ïðåîáðàçîâàòü òàê:
![]()
| (24) |
Ïðîâåðêà íàèìåíîâàíèÿ åäèíèöû:
![]()
Âû÷èñëåíèÿ:
![]()
Îòâåò: ÷òîáû èñïàðèòü 1 êã âîäû â êèïÿòèëüíèêå ïðè çàäàííûõ
óñëîâèÿõ, íóæíî
çàìîðîçèòü 4,94 êã âîäû â õîëîäèëüíèêå.
Äàëåå: 1.2.
Çàäà÷è äëÿ ñàìîñòîÿòåëüíîãî
Ââåðõ: 1.
Ìîëåêóëÿðíàÿ ôèçèêà è
Íàçàä: 1.
Ìîëåêóëÿðíàÿ ôèçèêà è
ßÃÏÓ, Öåíòð èíôîðìàöèîííûõ
òåõíîëîãèé îáó÷åíèÿ
2005-09-21
Источник
Задача 28.
При 17°С некоторое количество газа занимает объем 580 мл. Какой объем займет это же количество газа при 100°С, если давление его останется неизменным?
Решение:
По закону Гей – Люссака при постоянном давлении объём газа изменяется прямо пропорционально абсолютной температуре (Т):
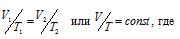
V2 – искомый объём газа;
T2 – соответствующая V2 температура;
V1 – начальный объём газа при соответствующей температуре Т1.
По условию задачи V1 = 580мл; Т1 = 290К (273 + 17 = 290) и Т2 = 373К (273 + 100 = 373). Подставляя эти значения в выражение закона Гей – Люссака, получим:
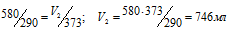
Ответ: V2 = 746мл.
Задача 29.
Давление газа, занимающего объем 2,5л, равно 121,6 кПа (912мм рт. ст.). Чему будет равно давление, если, не изменяя температуры, сжать газ до объема в 1л?
Решение:
Согласно закону Бойля – Мариотта, при постоянной температуре давление, производимое данной массой газа, обратно пропорционально объёму газа:

Обозначив искомое давление газа через Р2, можно записать:
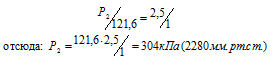
Ответ: Р2 = 304кПа (2280мм.рт.ст.).
Задача 30. На сколько градусов надо нагреть газ, находящийся в закрытом сосуде при 0 °С, чтобы давление его увеличилось вдвое?
Решение:
При постоянном объёме давление газа изменяется прямо пропорционально температуре:

По условию задачи Т1 = 0 °С + 273 = 273К; давление возросло в два раза: Р2 = 2Р1.
Подставляя эти значения в уравнение, находим:
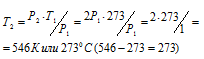
Ответ: Газ нужно нагреть на 2730С.
Задача 31.
При 27°С и давлении 720 мм.рт. ст. объем газа равен 5л. Кой объем займет это же количество газа при 39°С и давлении 104кПа?
Решение:
Зависимость между объёмом газа, давлением и температурой выражается общим уравнением, объединяющим законы Гей-Люссака и Бойля-Мариотта:

где Р и V – давление и объём газа при температуре Т; Р0 и V0 – давление и объём газа при нормальных условиях. Данные задачи: V = 5л; Т = 298К (273 + 25 = 298); Р = 720 мм.рт.ст. (5,99 кПа); Р0 = 104 кПа; Т = 312К (273 + 39 = 312); Т = 273К. Подставляя данные задачи в уравнение, получим:
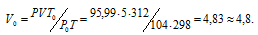
Ответ: V0 = 4,8л
Задача 32.
При 7°С давление газа в закрытом сосуде равно 96,0 кПа. Каким станет давление, если охладить сосуд до —33 °С?
Решение:
При постоянном объёме давление газа изменяется прямо пропорционально абсолютной температуре:

Обозначим искомое давление через Р2, а соответствующую ему температуру через Т2. По условию задачи Р1 = 96,0 кПа; Т1 = 280К (273 + 7 = 280); Т2 = 240К (273 – 33 = 240). Подставляя эти значения в уравнение, получим:
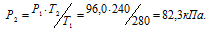
Ответ: Р2 = 82,3кПа.
Задача 33.
При нормальных условиях 1г воздуха занимает объем 773 мл. Какой объем займет та же масса воздуха при 0 °С и )и давлении, равном 93,3 кПа (700мм. рт. ст.)?
Решение:
Зависимость между объёмом газа, давлением и температурой выражается общим уравнением, объединяющим законы Гей-Люссака и Бойля-Мариотта:

где Р и V – давление и объём газа при температуре Т; Р0 и V0 – давление и объём газа при нормальных условиях. Данные задачи: Р0 = 101,325кПа; V0 = 773мл; Т0 = 298К (273 + 25 = 298); Т = 273К; Р = 93,3кПа. Подставляя данные задачи и преобразуя уравнение, получим:
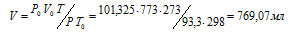
Ответ: V = 769, 07 мл.
Задача 34.
Давление газа в закрытом сосуде при 12°С равно 100 кПа (750мм рт. ст.). Каким станет давление газа, если нагреть сосуд до 30°С?
Решение:
При постоянном объёме давление газа изменяется прямо пропорционально абсолютной температуре:

Обозначим искомое давление через Р2, а соответствующую ему температуру через Т2. По условию задачи Р1 = 100 кПа; Т1 = 285К (273 + 12 = 285); Т2 = 303К (273 + 30 = 303). Подставляя эти значения в уравнение, получим:
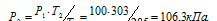
Ответ: Р2 = 106,3кПа.
Задача 35.
В стальном баллоне вместимостью 12л находится при 0°С кислород под давлением 15,2 МПа. Какой объем кислорода, находящегося при нормальных условиях можно получить из такого баллона?
Решение:
Зависимость между объёмом газа, давлением и температурой выражается общим уравнением, объединяющим законы Гей-Люссака и Бойля-Мариотта:

где Р и V – давление и объём газа при температуре Т; Р0 и V0 – давление и объём газа при нормальных условиях. Данные задачи: V = 12л; Т = 273К (273 + 0 = 2273); Р =15,2МПа); Р0 = 101,325кПа; Т0 = 298К (273 + 25 = 298). Подставляя данные задачи в уравнение, получим:
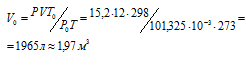
Ответ: V0 = 1,97м3.
Задача 36.
Температура азота, находящегося в стальном баллоне под давлением 12,5 МПа, равна 17°С. Предельное давление для баллона 20,3МПа. При какой температуре давление азота достигнет предельного значения?
Решение:
При постоянном объёме давление газа изменяется прямо пропорционально абсолютной температуре:

Обозначим искомое давление через Р2, а соответствующую ему температуру через Т2. По условию задачи Р1 = 12,5МПа; Т1 = 290К (273 + 17 = 290); Р2 = 20,3МПа. Подставляя эти значения в уравнение, получим:
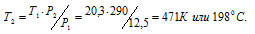
Ответ: Т2 = 1980С.
Задача 37.
При давлении 98,7кПа и температуре 91°С некоторое количество газа занимает объем 680 мл. Найти объем газа при нормальных условиях.
Решение:
Зависимость между объёмом газа, давлением и температурой выражается общим уравнением, объединяющим законы Гей-Люссака и Бойля-Мариотта:

где Р и V – давление и объём газа при температуре Т; Р0 и V0 – давление и объём газа при нормальных условиях. Данные задачи: Р0 = 101,325кПа; V = 680мл; Т0 = 298К (273 + 25 = 298); Т = 364К (273 + 91 = 364); Р = 98,7кПа. Подставляя данные задачи и преобразуя уравнение, получим:
<
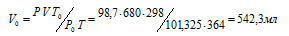
Ответ: V0 = 542,3мл.
Задача 38.
При взаимодействии 1,28г металла с водой выделилось 380 мл водорода, измеренного при 21°С и давлении 104,5кПа (784мм рт.
