Давление газа в закрытом сосуде при 12 равно 100

Опубликовано 1 год назад по предмету
Химия
от perechodko2000
Не тот ответ, который вам нужен?
Найди нужный
Самые новые вопросы
![]()
Математика – 6 месяцев назад
Сколько здесь прямоугольников
![]()
История – 1 год назад
Какое управление было в древнейшем риме? как звали первого и последнего из царей рима?
![]()
Литература – 1 год назад
Уроки французского ответе на вопрос : расскажите о герое по следующему примерному плану: 1.почему мальчик оказался в райцентре ? 2.как он чувствовал себя на новом месте? 3.почему он не убежал в деревню? 4.какие отношения сложились у него с товарищами? 5.почему он ввязался в игру за деньги? 6.как характеризуют его отношения с учительницей ? ответе на эти вопросы пожалуйста ! сочините сочинение пожалуйста
![]()
Русский язык – 1 год назад
Помогите решить тест по русскому языку тест по русскому языку «местоимение. разряды местоимений» для 6 класса
1. укажите личное местоимение:
1) некто
2) вас
3) ни с кем
4) собой
2. укажите относительное местоимение:
1) кто-либо
2) некоторый
3) кто
4) нам
3. укажите вопросительное местоимение:
1) кем-нибудь
2) кем
3) себе
4) никакой
4. укажите определительное местоимение:
1) наш
2) который
3) некий
4) каждый
5. укажите возвратное местоимение:
1) свой
2) чей
3) сам
4) себя
6. найдите указательное местоимение:
1) твой
2) какой
3) тот
4) их
7. найдите притяжательное местоимение:
1) самый
2) моего
3) иной
4) ничей
8. укажите неопределённое местоимение:
1) весь
2) какой-нибудь
3) любой
4) этот
9. укажите вопросительное местоимение:
1) сколько
2) кое-что
3) она
4) нами
10. в каком варианте ответа выделенное слово является притяжательным местоимением?
1) увидел их
2) её нет дома
3) её тетрадь
4) их не спросили
![]()
Русский язык – 1 год назад
Переделай союзное предложение в предложение с бессоюзной связью.
1. океан с гулом ходил за стеной чёрными горами, и вьюга крепко свистала в отяжелевших снастях, а пароход весь дрожал.
2. множество темноватых тучек, с неясно обрисованными краями, расползались по бледно-голубому небу, а довольно крепкий ветер мчался сухой непрерывной струёй, не разгоняя зноя
3. поезд ушёл быстро, и его огни скоро исчезли, а через минуту уже не было слышно шума
![]()
Русский язык – 1 год назад
помогите прошу!перепиши предложения, расставляя недостающие знаки препинания. объясни, что соединяет союз и. если в предложении один союз и, то во втором выпадающем списке отметь «прочерк».пример:«я шёл пешком и,/поражённый прелестью природы/, часто останавливался».союз и соединяет однородные члены.ночь уже ложилась на горы (1) и туман сырой (2) и холодный начал бродить по ущельям.союз и соединяет:1) части сложного предложенияоднородные члены,2) однородные членычасти сложного предложения—.поэт — трубач зовущий войско в битву (1) и прежде всех идущий в битву сам (ю. янонис).союз и соединяет:1) части сложного предложенияоднородные члены,2)
![]()
Физика – 1 год назад
Вокруг прямого проводника с током (смотри рисунок) существует магнитное поле. определи направление линий этого магнитного поля в точках a и b.обрати внимание, что точки a и b находятся с разных сторон от проводника (точка a — снизу, а точка b — сверху). рисунок ниже выбери и отметь правильный ответ среди предложенных.1. в точке a — «от нас», в точке b — «к нам» 2. в точке a — «к нам», в точке b — «от нас» 3. в обеих точках «от нас»4. в обеих точках «к нам»контрольная работа по физике.прошу,не наугад важно
Информация
Посетители, находящиеся в группе Гости, не могут оставлять комментарии к данной публикации.
Источник
Задача 28.
При 17°С некоторое количество газа занимает объем 580 мл. Какой объем займет это же количество газа при 100°С, если давление его останется неизменным?
Решение:
По закону Гей – Люссака при постоянном давлении объём газа изменяется прямо пропорционально абсолютной температуре (Т):
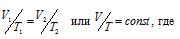
V2 – искомый объём газа;
T2 – соответствующая V2 температура;
V1 – начальный объём газа при соответствующей температуре Т1.
По условию задачи V1 = 580мл; Т1 = 290К (273 + 17 = 290) и Т2 = 373К (273 + 100 = 373). Подставляя эти значения в выражение закона Гей – Люссака, получим:
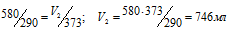
Ответ: V2 = 746мл.
Задача 29.
Давление газа, занимающего объем 2,5л, равно 121,6 кПа (912мм рт. ст.). Чему будет равно давление, если, не изменяя температуры, сжать газ до объема в 1л?
Решение:
Согласно закону Бойля – Мариотта, при постоянной температуре давление, производимое данной массой газа, обратно пропорционально объёму газа:

Обозначив искомое давление газа через Р2, можно записать:
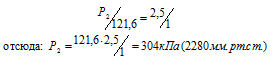
Ответ: Р2 = 304кПа (2280мм.рт.ст.).
Задача 30. На сколько градусов надо нагреть газ, находящийся в закрытом сосуде при 0 °С, чтобы давление его увеличилось вдвое?
Решение:
При постоянном объёме давление газа изменяется прямо пропорционально температуре:

По условию задачи Т1 = 0 °С + 273 = 273К; давление возросло в два раза: Р2 = 2Р1.
Подставляя эти значения в уравнение, находим:
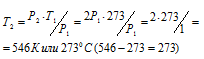
Ответ: Газ нужно нагреть на 2730С.
Задача 31.
При 27°С и давлении 720 мм.рт. ст. объем газа равен 5л. Кой объем займет это же количество газа при 39°С и давлении 104кПа?
Решение:
Зависимость между объёмом газа, давлением и температурой выражается общим уравнением, объединяющим законы Гей-Люссака и Бойля-Мариотта:

где Р и V – давление и объём газа при температуре Т; Р0 и V0 – давление и объём газа при нормальных условиях. Данные задачи: V = 5л; Т = 298К (273 + 25 = 298); Р = 720 мм.рт.ст. (5,99 кПа); Р0 = 104 кПа; Т = 312К (273 + 39 = 312); Т = 273К. Подставляя данные задачи в уравнение, получим:
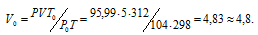
Ответ: V0 = 4,8л
Задача 32.
При 7°С давление газа в закрытом сосуде равно 96,0 кПа. Каким станет давление, если охладить сосуд до —33 °С?
Решение:
При постоянном объёме давление газа изменяется прямо пропорционально абсолютной температуре:

Обозначим искомое давление через Р2, а соответствующую ему температуру через Т2. По условию задачи Р1 = 96,0 кПа; Т1 = 280К (273 + 7 = 280); Т2 = 240К (273 – 33 = 240). Подставляя эти значения в уравнение, получим:
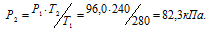
Ответ: Р2 = 82,3кПа.
Задача 33.
При нормальных условиях 1г воздуха занимает объем 773 мл. Какой объем займет та же масса воздуха при 0 °С и )и давлении, равном 93,3 кПа (700мм. рт. ст.)?
Решение:
Зависимость между объёмом газа, давлением и температурой выражается общим уравнением, объединяющим законы Гей-Люссака и Бойля-Мариотта:

где Р и V – давление и объём газа при температуре Т; Р0 и V0 – давление и объём газа при нормальных условиях. Данные задачи: Р0 = 101,325кПа; V0 = 773мл; Т0 = 298К (273 + 25 = 298); Т = 273К; Р = 93,3кПа. Подставляя данные задачи и преобразуя уравнение, получим:
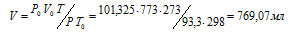
Ответ: V = 769, 07 мл.
Задача 34.
Давление газа в закрытом сосуде при 12°С равно 100 кПа (750мм рт. ст.). Каким станет давление газа, если нагреть сосуд до 30°С?
Решение:
При постоянном объёме давление газа изменяется прямо пропорционально абсолютной температуре:

Обозначим искомое давление через Р2, а соответствующую ему температуру через Т2. По условию задачи Р1 = 100 кПа; Т1 = 285К (273 + 12 = 285); Т2 = 303К (273 + 30 = 303). Подставляя эти значения в уравнение, получим:
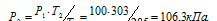
Ответ: Р2 = 106,3кПа.
Задача 35.
В стальном баллоне вместимостью 12л находится при 0°С кислород под давлением 15,2 МПа. Какой объем кислорода, находящегося при нормальных условиях можно получить из такого баллона?
Решение:
Зависимость между объёмом газа, давлением и температурой выражается общим уравнением, объединяющим законы Гей-Люссака и Бойля-Мариотта:

где Р и V – давление и объём газа при температуре Т; Р0 и V0 – давление и объём газа при нормальных условиях. Данные задачи: V = 12л; Т = 273К (273 + 0 = 2273); Р =15,2МПа); Р0 = 101,325кПа; Т0 = 298К (273 + 25 = 298). Подставляя данные задачи в уравнение, получим:
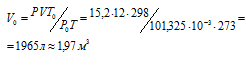
Ответ: V0 = 1,97м3.
Задача 36.
Температура азота, находящегося в стальном баллоне под давлением 12,5 МПа, равна 17°С. Предельное давление для баллона 20,3МПа. При какой температуре давление азота достигнет предельного значения?
Решение:
При постоянном объёме давление газа изменяется прямо пропорционально абсолютной температуре:

Обозначим искомое давление через Р2, а соответствующую ему температуру через Т2. По условию задачи Р1 = 12,5МПа; Т1 = 290К (273 + 17 = 290); Р2 = 20,3МПа. Подставляя эти значения в уравнение, получим:
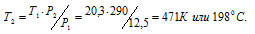
Ответ: Т2 = 1980С.
Задача 37.
При давлении 98,7кПа и температуре 91°С некоторое количество газа занимает объем 680 мл. Найти объем газа при нормальных условиях.
Решение:
Зависимость между объёмом газа, давлением и температурой выражается общим уравнением, объединяющим законы Гей-Люссака и Бойля-Мариотта:

где Р и V – давление и объём газа при температуре Т; Р0 и V0 – давление и объём газа при нормальных условиях. Данные задачи: Р0 = 101,325кПа; V = 680мл; Т0 = 298К (273 + 25 = 298); Т = 364К (273 + 91 = 364); Р = 98,7кПа. Подставляя данные задачи и преобразуя уравнение, получим:
<
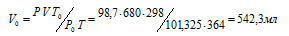
Ответ: V0 = 542,3мл.
Задача 38.
При взаимодействии 1,28г металла с водой выделилось 380 мл водорода, измеренного при 21°С и давлении 104,5кПа (784мм рт. ст.). Найти эквивалентную массу металла.
Решение:
Находим объём выделившегося водорода при нормальных условиях, используя уравнение:

где Р и V – давление и объём газа при температуре Т = 294К (273 +21 = 294); Р0 = 101,325кПа; Т0 = 273К; Р = 104,5кПа. Подставляя данные задачи в уравнение,
получим:
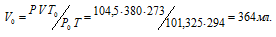
Согласно закону эквивалентов, массы (объёмы) реагирующих друг с другом веществ m1 и m2 пропорциональны их эквивалентным массам (объёмам):
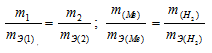
Мольный объём любого газа при н.у. равен 22,4л. Отсюда эквивалентный объём водорода равен 22,4 : 2 = 11,2л или 11200 мл. Тогда, используя формулу закона эквивалентов, рассчитаем эквивалентную массу металла:
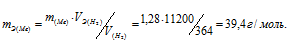
Ответ: mЭ(Ме) = 39,4г/моль.
Задача 39.
Как следует изменить условия, чтобы увеличение массы данного газа не привело к возрастанию его объема: а) понизить температуру; б) увеличить давление; в) нельзя подобрать условий?
Решение:
Для характеристики газа количеством вещества (n, моль) применяется уравнение РV = nRT, или – это уравнение Клапейрона-Менделеева. Оно связывает массу (m, кг); температуру (Т, К); давление (Р, Па) и объём (V, м3) газа с молярной массой (М, кг/моль).
Тогда из уравнения Клапейрона-Менделеева объём газа можно рассчитать по выражению:
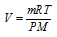
Отсюда следует, что V = const, если при увеличении массы (m) газа на некоторую величину будет соответственно уменьшена температура (T) системы на некоторое необходимое значение. Объём системы также не изменится при постоянной температуре, если при увеличении массы (m) газа на некоторую величину будет соответственно увеличено давление (P) системы на необходимую величину.
Таким образом, при увеличении массы газа объём системы не изменится, если понизить температуру системы или же увеличить давление в ней на некоторую величину.
Ответ: а); б).
Задача 40.
Какие значения температуры и давления соответствуют нормальным условиям для газов: а) t = 25 °С, Р = 760 мм. рт. ст.; б) t = 0 °С, Р = 1,013 • 105Па; в) t = 0°С, Р = 760 мм. рт. ст.?
Решение:
Состояние газа характеризуется температурой, давлением и объёмом. Если температура газа равна 0 °С (273К), а давление составляет 101325 Па (1,013 • 105) или 760 мм. рт. ст., то условия, при которых находится газ, принято считать нормальными.
Ответ: б); в).
Источник
Похожие вопросы:

Химия, 26.02.2019 23:10
Разделите перечисленные в формулы на три равные группы (в каждой группе по 4 элемента), каждую из которых назовите. назовите все вещества. nano2, cu(no3)2, hno2, nh3,n2o3, li3n, n2o5, al(no3)3, mg3n2, na3n, hno3, kno2.
Ответов: 3

Химия, 03.03.2019 16:40
Составить уравнения реакций карбид > > > > > > > > > > > > этиловый > > > каучук буду признательна
Ответов: 3

Химия, 09.03.2019 15:20
Закончите уравнения реакций по следующим схемам: а) naoh + so2 = b) ba(oh)2 + p2o5 = в) koh + sio2 = г) ca(oh)2 + so3 =
Ответов: 3

Химия, 03.03.2019 17:16
(лучше с пошаговым решением, на листке). во вложении
Ответов: 3

Химия, 04.03.2019 10:26
Какой объем h2 выделится при взаимодействии 27.3г калия с серной кислотой
Ответов: 1

Химия, 10.03.2019 14:16
При 38 градусов растворимость соли х равна 60 г на 100 г воды. какова формула соли и как изменится её растворимость при 45 градусов
Ответов: 3

Химия, 12.03.2019 17:40
🙁 свериться нужно. если что, то 25/12 это 25вверху(массовое число) 12 внизу(заряд ядра) №1 опрделите число протонов и нейтронов в атомах изотопа магня 24/12 mg, 25/12 mg,26/12mg и меди – 65/29 cu ,63/29 cu. №2литий имеет 2изотопа: 7/3li b 6/3 li. содержание в природе первого изотопа составляет 92,7% второго-7,3%.вычислите атомную массу лития. .
Ответов: 3

Химия, 12.03.2019 21:00
Вычислите массовые доли элементов в азотной кислоте hno3
Ответов: 1

Химия, 12.03.2019 20:44
1. позначте тип хімічного зв’язку в молекулі s8 а. ковалентний полярний; б. йонний; в. ковалентний неполярний; г. металічний. 2. укажіть кислотний оксид: а. со; б. со2; в. сао; г. zno. 3. укажіть речовини, які взаємодіють з розведеним розчином сульфатної кислоти: а. cao; б. cu; в. mgcl2; г. cu(oh)2; д. cl2. 4. укажіть речовини з однаковим ступенем окиснення фосфору: а p2o3; б k3po4; в p4; г na3p; д p2o5. 5. укажіть речовини з однаковим ступенем окиснення нітрогену: а nh3 ; б no2 ; в hno3 ; г k3n ; д n2. 6. укажіть речовину, яка не є мінеральним добривом: а натрій нітрат; б амоній нітрат; в. кальцій сульфат; г. подвійний суперфосфат. 7. встановіть послідовність сполук за збільшенням ступеня окиснення фосфору в них: а hpo3; б li3p; в p4 ; г ca3(po4)2. 8. встановіть послідовність сполук за збільшенням ступеня окиснення сульфуру в них: а h2so4; б h2s; в h2so3; г s8. 9. розмістіть сполуки в ряд за збільшенням їхніх відносних молекулярних мас: а сульфатна кислота; б нітратна кислота; в вуглекислий газ; г кальцій карбонат. 10. розмістіть сполуки в ряд за збільшенням їхніх відносних молекулярних мас: а хлоридна кислота; б кисень; в амоніак; г сульфатна кислота. 11. встановіть відповідність між хімічним елементом і ступенями окиснення, які він може виявляти в сполуках: а. сульфур; 1 -2; б. карбон; 2 -2, +4, +6; в. оксиген; 3 -2, +2; г. фосфор. 4 -4, +2; +4; 5 -3, +3, +5. 12. встановіть відповідність між реагентами та продуктами реакцій: реагенти: а. so3 + h2o = б. hcl + na2 s = в. h2so4 k + cu = г. ag + hno3 = продукти реакцій: 1 agno3 + no + h2o; 2 nacl + h2 s↑; 3 h2so4 ; 4 cuso4 + h2 ; 5 cuso4 + so2 + h2o; 13. встановіть відповідність між хімічними елементами та електронними формулами їхніх атомів: елементи: а сульфур; б силіцій; в оксиген; г карбон. електронні формули: 1s22s22p63s23p64s24p2 1s22s22p4 1s22s22p63s23p2 1s22s22p63s23p4 1s22s22p2 14. встановіть відповідність між хімічними елементами та електронними формулами їхніх атомів: елементи: а сульфур; б фосфор; в флуор; г нітроген. електронні формули: 11s22s22p63s23p64s24p2 21s22s22p5 31s22s22p63s23p3 41s22s22p63s23p4 51s22s22p3 15. складіть рівняння реакції в молекулярній та йонній формах: барій нітрат + натрій сульфат = 16. складіть рівняння реакції в молекулярній та йонній формах: калій карбонат + нітратна кислота =
Ответов: 1

Химия, 13.03.2019 20:10
Требуется ! ) из формул выпишите отдельно формулы веществ с: а) ионной б)атомной в)молекулярной г)металлической решеткой: na, mgcl2, cao, c6h12o6, ar(тв), hbr(тв), fe, ch4 (тв), k2sо4, sic
Ответов: 2

Химия, 13.03.2019 20:21
Вычислите массу осадка который образуется при взаимодействии 100 грамм раствора содержащего 10 процентов соляной кислоты 5 моль силиката натрия
Ответов: 3

Химия, 14.03.2019 08:20
Существует гидроксид марганца со степень окисления +5? и вообще какие есть с этой степень окисления соеденения?
Ответов: 2
У тебя есть свой ответ?
Давление газа в закрытом сосуде при температуре 12°с равно 100 кпа. каким будет давление газа, если…
Отправлено
Вопросы по другим предметам:

Обществознание, 08.09.2019 00:50

Математика, 08.09.2019 00:50

Математика, 08.09.2019 00:50

Математика, 08.09.2019 00:50

Беларуская мова, 08.09.2019 00:50


Математика, 08.09.2019 00:50

Русский язык, 08.09.2019 00:50


Математика, 08.09.2019 00:50
Источник
Aryuna G.
6 декабря 2019 · 757
Закон Шарля: Давление газа фиксированной массы и фиксированного объёма прямо пропорционально абсолютной температуре газа.
Записываем это уравнением: p₁/p₂ = T₁/T₂.
Подставляем числа: (96 кПа)/p₂ = (273 +7 К)/(273 – 33 К).
Отсюда находите p₂.
273? Что за число? ;
p2=96кПа (273+7)/(273-33) верно составлено уравнение?
Какой объем кислорода требуется для сжигания 56 л пропана?
Книги, звери и еда – это хобби навсегда.
Запишем уравнение горения пропана
С3H8+5*O2->3CO2+4*H2O
Из уравнения видно, что для сжигания 1 моль пропана требуется 5 моль кислорода. Поскольку оба вещества являются газами, то 56 л пропана составляет 56/22.4=2.5 моль, а требуемое количество кислорода составляет 2.5*5 = 12.5 моль, которое будет занимать 12.5*22.4=280 л.
Какой объем занимает водород при давлении в балоне 4 атмосферы если температура газа 27°c, масса 2кг.?
Книги, звери и еда – это хобби навсегда.
Закон Менделеева-Клапейрона p*V=n*R*T, где p=4 атм=4*1.013*10^5 Па=4.052*10^5 Па-давление, V-объем газа, n-количество вещества, R= 8,3 Дж/(моль*К) -газовая постоянная, T=27°С=300°K-температура. Молекулярный вес водорода равен 2, следовательно, масса одного моля μ=2 г, поэтому n=m/μ=2000/2=1000 моль. Теперь можно найти объем:
V=n*R*T/p=1000*8.3*300/(4.052*10^5)=6.15 м^3.
Объясните чайнику: если до Большого взрыва Вселенная была бесконечно мала, то как называлось то пространство, которое ее окружало?
PhD, senior scientist AI, неандерталец
Разум цепляется за привычное. Например, мы привыкли, что все тела падают вниз. Привыкли настолько, что в Англии, на родине Ньютона, еще в девятнадцатом веке огромной общественной популярностью пользовалась книга, в которой «доказывалось», что Земля — плоская, ведь иначе мы бы с нее упали. Раз она плоская, у нее должен быть край. Однако, путешествие Магеллана показало — если плыть все время на запад, то снова приплывешь в Европу, только уже с востока. Итак, Земля — шар, а с тем, что люди на другой стороне ходят «вверх ногами», придется смириться, хоть это и противоречит «здравому смыслу».
Ну, «здравый смысл» с тех пор кое-как примирился с законом всемирного тяготения, но теперь есть новая задача — понять, как Вселенная может быть ограниченной в объеме и при этом не иметь «краев» и чего-то «вне». Что ж, лучшая аналогия — это старые игры, где, выходя за конец экрана, какой-нибудь пэкмен, или диггер, или змейка, или Марио оказывались с противоположного. Для них, таким образом, края экрана не существовало.
Ограниченная по объему трехмерная вселенная — это нечто подобное. Представьте себе: вы находитесь в комнате, у которой как будто две двери в противоположных стенах. Вы открываете дверь и видите такую же комнату и себя со спины, открывающего дверь в следующей стене, за которой видна еще одна комната и еще один вы, и так далее. И за спиной у вас скрипнула дверь — на самом деле та же самая, потому что дверь — одна. И происходит это не потому, что существует бесконечное число вас, а потому что вселенная зациклена сама на себя — просто свет делает несколько кругов по этой вселенной прежде чем достичь ваших глаз. Если в этой нашей вселенной сделать скорость света, к примеру, один метр в секунду, то вы будете видеть себя в другой комнате уже с задержкой в несколько секунд. Теперь добавим еще двери, точнее, одну дверь двум другим стенам комнаты. А теперь — люк в полу и потолке с теми же эффектами.
А теперь — уберем стены, пол и потолок! И увидим многократные копии себя же через равные промежутки пространства. Хотя на самом деле эти копии настолько же реальны, насколько ваше отражение в зеркале — то, что мы видим в зеркале отраженную комнату, отнюдь не значит, что есть еще одна комната.
Поздравляю! Вот вы и очутились во вселенной с ограниченным объемом, но без краев и чего-то «вне». Это лишь один из вариантов, тороидальный. В сферической вселенной вы бы видели размытый образ себя во всем поле зрения — причем, считая, что угол обзора у нас 180°, вы бы видели в упор свой затылок, а в нижнем краю зрения — макушку, в верхнем — подошвы обуви, а по бокам — уши. Но это уже мелочи.
Почему так не происходит в нашей Вселенной? Дело в том, что она расширяется, и достаточно удаленные ее участки улетают от нас быстрее скорости света. В общем, даже если вселенная конечна, свет, испущенный нами или отраженный от нас, просто не имеет возможности к нам возвратиться. Это — большой вариант комнаты.
А теперь рассмотрим противоположный сценарий. Будем сжимать нашу комнату без стен. Вот нам уже в ней неуютно. Вот вы в нее уже не помещаетесь, вас прижимает носом к своему собственному затылку, который вы видите перед собой, и вы чувствуете затылком, как к нему прижало ваш же нос. Вот комната становится размером с атомное ядро… И вот мы приходим в состояние «сразу» после Большого Взрыва. «Сразу» заключено в кавычки, потому что время — это тоже лишь измерение пространства. Так что нет не только «вне» вселенной, но и «до» Большого Взрыва. Ну, то есть, в одной из моделей.
Вот, как-то так.
Прочитать ещё 67 ответов
Источник

Ответ
Ответ дан
Аккаунт удален
t1 = 12°С = 285K
p1 = 100 кПа = 100000 Па
t2 = 30°С = 303K
p2 = ?
p1/t1 = p2/t2 => p2 = (p1*t2)/t1
p2 = (100000 Па*303К)/285К
p2 = 106316,8 Па = 106.3 кПа
Ответ: 106.3 кПа