Давление на стенки сосуда формула для газа
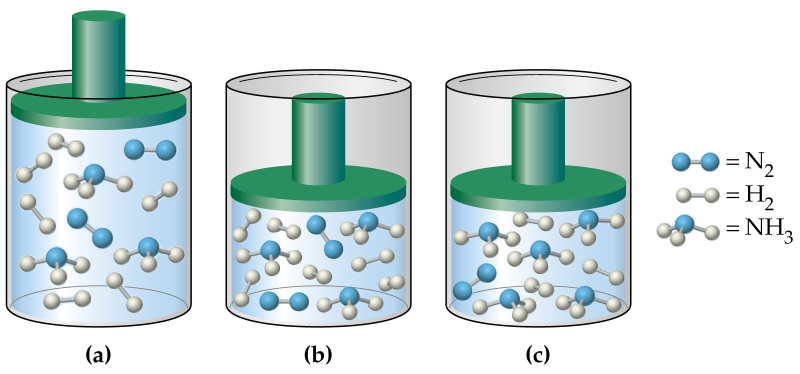
Давление является одним из трех основных термодинамических макроскопических параметров любой газовой системы. В данной статье рассмотрим формулы давления газа в приближении идеального газа и в рамках молекулярно-кинетической теории.
Идеальные газы
Каждый школьник знает, что газ является одним из четырех (включая плазму) агрегатных состояний материи, в котором частицы не имеют определенных положений и движутся хаотичным образом во всех направлениях с одинаковой вероятностью. Исходя из такого строения, газы не сохраняют ни объем, ни форму при малейшем внешнем силовом воздействии на них.
В любом газе средняя кинетическая энергия его частиц (атомов, молекул) больше, чем энергия межмолекулярного взаимодействия между ними. Кроме того, расстояния между частицами намного превышают их собственные размеры. Если молекулярными взаимодействиями и размерами частиц можно пренебречь, тогда такой газ называется идеальным.
В идеальном газе существует лишь единственный вид взаимодействия – упругие столкновения. Поскольку размер частиц пренебрежимо мал в сравнении с расстояниями между ними, то вероятность столкновений частица-частица будет низкой. Поэтому в идеальной газовой системе существуют только столкновения частиц со стенками сосуда.
Все реальные газы с хорошей точностью можно считать идеальными, если температура в них выше комнатной, и давление не сильно превышает атмосферное.
Причина возникновения давления в газах
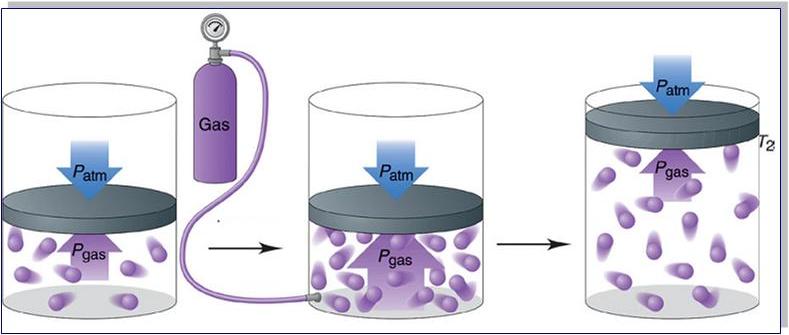
Прежде чем записать формулы расчета давления газа, необходимо разобраться, почему оно возникает в изучаемой системе.
Согласно физическому определению, давление – это величина, равная отношению силы, которая перпендикулярно воздействует на некоторую площадку, к площади этой площадки, то есть:
P = F/S
Выше мы отмечали, что существует только один единственный тип взаимодействия в идеальной газовой системе – это абсолютно упругие столкновения. В результате них частицы передают количество движения Δp стенкам сосуда в течение времени соударения Δt. Для этого случая применим второй закон Ньютона:
F*Δt = Δp
Именно сила F приводит к появлению давления на стенки сосуда. Сама величина F от столкновения одной частицы является незначительной, однако количество частиц огромно (≈ 1023), поэтому они в совокупности создают существенный эффект, который проявляется в виде наличия давления в сосуде.
Формула давления газа идеального из молекулярно-кинетической теории
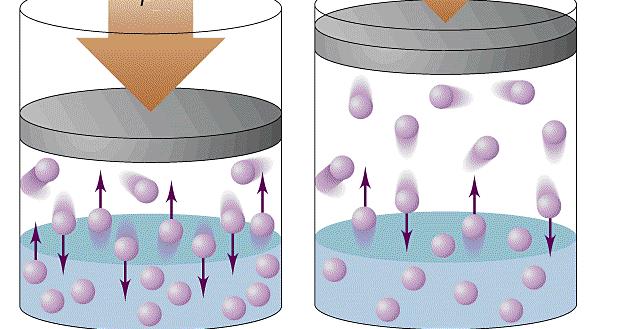
При объяснении концепции идеального газа выше были озвучены основные положения молекулярно-кинетической теории (МКТ). Эта теория основывается на статистической механике. Развита она была во второй половине XIX века такими учеными, как Джеймс Максвелл и Людвиг Больцман, хотя ее основы заложил еще Бернулли в первой половине XVIII века.
Согласно статистике Максвелла-Больцмана, все частицы системы движутся с различными скоростями. При этом существует малая доля частиц, скорость которых практически равна нулю, и такая же доля частиц, имеющих огромные скорости. Если вычислить среднюю квадратичную скорость, то она примет некоторую величину, которая в течение времени остается постоянной. Средняя квадратичная скорость частиц однозначно определяет температуру газа.
Применяя приближения МКТ (невзаимодействующие безразмерные и хаотично перемещающиеся частицы), можно получить следующую формулу давления газа в сосуде:
P = N*m*v2/(3*V)
Здесь N – количество частиц в системе, V – объем, v – средняя квадратичная скорость, m – масса одной частицы. Если все указанные величины определены, то, подставив их в единицах СИ в данное равенство, можно рассчитать давление газа в сосуде.
Формула давления из уравнения состояния

В середине 30-х годов XIX века французский инженер Эмиль Клапейрон, обобщая накопленный до него экспериментальный опыт по изучению поведения газов во время разных изопроцессов, получил уравнение, которое в настоящее время называется универсальным уравнением состояния идеального газа. Соответствующая формула имеет вид:
P*V = n*R*T
Здесь n – количество вещества в молях, T – температура по абсолютной шкале (в кельвинах). Величина R называется универсальной газовой постоянной, которая была введена в это уравнение русским химиком Д. И. Менделеевым, поэтому записанное выражение также называют законом Клапейрона-Менделеева.
Из уравнения выше легко получить формулу давления газа:
P = n*R*T/V
Равенство говорит о том, что давление линейно возрастает с температурой при постоянном объеме и увеличивается по гиперболе с уменьшением объема при постоянной температуре. Эти зависимости отражены в законах Гей-Люссака и Бойля-Мариотта.
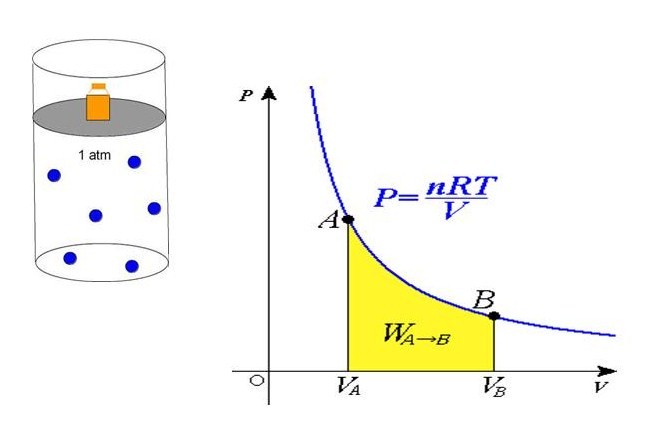
Если сравнить это выражение с записанной выше формулой, которая следует из положений МКТ, то можно установить связь между кинетической энергией одной частицы или всей системы и абсолютной температурой.
Давление в газовой смеси

Отвечая на вопрос о том, как найти давление газа и формулы, мы ничего не говорили о том, является ли газ чистым, или речь идет о газовой смеси. В случае формулы для P, которая следует из уравнения Клапейрона, нет никакой связи с химическим составом газа, в случае же выражения для P из МКТ эта связь присутствует (параметр m). Поэтому при использовании последней формулы для смеси газов становится непонятным, какую массу частиц выбирать.
Когда необходимо рассчитать давление смеси идеальных газов, следует поступать одним из двух способов:
- Рассчитывать среднюю массу частиц m или, что предпочтительнее, среднее значение молярной массы M, исходя из атомных процентов каждого газа в смеси;
- Воспользоваться законом Дальтона. Он гласит, что давление в системе равно сумме парциальных давлений всех ее компонентов.
Пример задачи
Известно, что средняя скорость молекул кислорода составляет 500 м/с. Необходимо определить давление в сосуде объемом 10 литров, в котором находится 2 моль молекул.
Ответ на задачу можно получить, если воспользоваться формулой для P из МКТ:
P = N*m*v2/(3*V)
Здесь содержатся два неудобных для выполнения расчетов параметра – это m и N. Преобразуем формулу следующим образом:
m = M/NA;
n = N/NA;
m*N = M*n;
P = M*n*v2/(3*V)
Объем сосуда в кубических метрах равен 0,01 м3. Молярная масса молекулы кислорода M равна 0,032 кг/моль. Подставляя в формулу эти значения, а также величины скорости v и количества вещества n из условия задачи, приходим к ответу: P = 533333 Па, что соответствует давлению в 5,3 атмосферы.
Источник
Пусть в единице объема сосуда содержатся молекул; тогда число молекул в объеме цилиндра равно υ Δ. Но из этого числа лишь половина движется в сторону стенки, а другая половина движется в противоположном направлении и со стенкой не сталкивается.
Следовательно, число ударов молекул о площадку за время Δ равно
.
Поскольку каждая молекула при столкновении со стенкой изменяет свой импульс на величину 2υ , то полное изменение импульса всех молекул, столкнувшихся за время Δ с площадкой , равно
.
По законам механики это изменение импульса всех столкнувшихся со стенкой молекул происходит под действием импульса силы Δ, где – некоторая средняя сила, действующая на молекулы со стороны стенки на площадке . Но по 3-му закону Ньютона такая же по модулю сила действует со стороны молекул на площадку . Поэтому можно записать:
Разделив обе части на , получим:
где – давление газа на стенку сосуда.
При выводе этого соотношения предполагалось, что все молекул, содержащихся в единице объема газа, имеют одинаковые проекции скоростей на ось . На самом деле это не так. На самом деле в данную формулу должнен входить средний квадрат
проекции υ скорости молекул. С учетом этого формула для давления газа запишется в следующем виде:
Модель может быть использована в режиме ручного переключения кадров и в режиме автоматической демонстрации ( Фильм ).
Источник
Отвечая на первый, из поставленных выше, вопрос, предположим, что давление газов на стенки сосуда объясняется ударами молекул .
Для того, чтобы в процессе поиска расчетной формулы этого давления ограничиться знаниями элементарной математики и физики, введем некоторые упрощения .
- Форма, строение молекул достаточно сложны. Но попробуем представить их в виде маленьких шариков. Это позволит нам применить к описанию процесса удара молекул о стенки сосуда законы механики, в частности, второй закон Ньютона .
- Будем считать, что молекулы газа находятся на достаточно большом расстоянии друг от друга, так, что силы взаимодействия между ними пренебрежимо малы. Если между частицами отсутствуют силы взаимодействия, соответственно, равна нулю и потенциальная энергия взаимодействия . Назовем газ, отвечающий этим свойствам, идеальным .
- Известно, что молекулы газа движутся с разными скоростями . Однако, усредним скорости движения молекул и будем считать их одинаковыми .
- Предположим, что удары молекул о стенки сосуда абсолютно упругие (молекулы ведут себя при ударе подобно резиновым мячикам, а не подобно куску пластилина). При этом скорости молекул изменяются лишь по направлению, а по величине остаются прежними. Тогда изменение скорости каждой молекулы при ударе равно –2υ.
Введя такие упрощения, рассчитаем давление газа на стенки сосуда.
Давление – это физическая величина, равная отношению перпендикулярной составляющей силы, действующей на поверхность, к площади этой поверхности.
Сила действует на стенку со стороны множества молекул. Она может быть рассчитана как произведение силы, действующей со стороны одной молекулы, на число молекул, движущихся в сосуде в направлении этой стенки. Так как пространство трехмерно и каждое измерение имеет два направления: положительное и отрицательное, можно считать, что в направлении одной стенки движется одна шестая часть всех молекул (при большом их числе): .
Сила, действующая на стенку со стороны одной молекулы, равна силе, действующей на молекулу со стороны стенки. Сила, действующая на молекулу со стороны стенки, равна произведению массы одной молекулы на ускорение, которое она получает при ударе о стенку:
Ускорение же – это физическая величина, определяемая отношением изменения скорости ко времени, в течение которого это изменение произошло: .
Изменение скорости равно удвоенному значению скорости молекулы до удара: .
Если молекула ведет себя подобно резиновому мячику, нетрудно представить процесс удара: молекула, ударяясь, деформируется. На процесс сжатия и разжатия затрачивается время. Пока молекула действует на стенку сосуда, о последнюю успевает удариться еще некоторое число молекул, находящихся от нее на расстояниях не дальше . (Например, условно говоря, пусть молекулы имеют скорость 100 м/с. Удар длится 0,01 с. Тогда за это время до стенки успеют долететь и внести свой вклад в давление молекулы, находящиеся от нее на расстояниях 10, 50, 70 см, но не далее 100 см).
Будем рассматривать объем сосуда .
Подставив все формулы в исходную, получаем уравнение:
где:
– масса одной молекулы, – среднее значение квадрата скорости молекул, – число молекул в объеме .
Сделаем некоторые пояснения по поводу одной из величин, входящих в полученное уравнение.
Так как движение молекул хаотично и преимущественного движения молекул в сосуде нет, их средняя скорость равна нулю. Но ясно, что это не относится к каждой отдельной молекуле.
Для вычисления давления идеального газа на стенку сосуда используется не среднее значение -компоненты скорости молекул
а среднее значение квадрата скорости
Чтобы введение этой величины было более понятным, рассмотрим численный пример.
Пусть четыре молекулы имеют скорости 1, 2, 3, 4 усл. ед.
Квадрат среднего значения скорости молекул равен:
Среднее значение квадрата скорости равно:
Если скорости молекул равны +1, –2 , –3 , +4 усл. ед., то квадрат среднего значения скорости равен:
Среднее значение квадрата скорости равно:
Средние значения проекций квадрата скорости на оси связаны со средним значением квадрата скорости соотношением:
Если извлечь квадратный корень из
то получим величину, которая называется средней квадратичной скоростью молекул.
Величина, определяемая отношением числа частиц к объему, в котором они находятся, называется концентрацией (обозначается буквой ).
Величина же
– это средняя кинетическая энергия каждой молекулы газа.
С учетом этого полученное уравнение можно переписать в виде:
Уравнения связывают макропараметры газа – его давление и объем () с микропараметрами – массой молекул и их скоростью (), или энергией
Последнее уравнение читается следующим образом: давление идеального газа на стенки сосуда прямо пропорционально концентрации молекул в сосуде и их средней кинетической энергии .
Источник
➤ Adblock
detector
Источник
Пусть в единице объема сосуда содержатся молекул; тогда число молекул в объеме цилиндра равно υ Δ. Но из этого числа лишь половина движется в сторону стенки, а другая половина движется в противоположном направлении и со стенкой не сталкивается.
Следовательно, число ударов молекул о площадку за время Δ равно
.
Поскольку каждая молекула при столкновении со стенкой изменяет свой импульс на величину 2υ , то полное изменение импульса всех молекул, столкнувшихся за время Δ с площадкой , равно
.
По законам механики это изменение импульса всех столкнувшихся со стенкой молекул происходит под действием импульса силы Δ, где – некоторая средняя сила, действующая на молекулы со стороны стенки на площадке . Но по 3-му закону Ньютона такая же по модулю сила действует со стороны молекул на площадку . Поэтому можно записать:
Разделив обе части на , получим:
где – давление газа на стенку сосуда.
При выводе этого соотношения предполагалось, что все молекул, содержащихся в единице объема газа, имеют одинаковые проекции скоростей на ось . На самом деле это не так. На самом деле в данную формулу должнен входить средний квадрат
проекции υ скорости молекул. С учетом этого формула для давления газа запишется в следующем виде:
Модель может быть использована в режиме ручного переключения кадров и в режиме автоматической демонстрации ( Фильм ).
Источник
Отвечая на первый, из поставленных выше, вопрос, предположим, что давление газов на стенки сосуда объясняется ударами молекул .
Для того, чтобы в процессе поиска расчетной формулы этого давления ограничиться знаниями элементарной математики и физики, введем некоторые упрощения .
- Форма, строение молекул достаточно сложны. Но попробуем представить их в виде маленьких шариков. Это позволит нам применить к описанию процесса удара молекул о стенки сосуда законы механики, в частности, второй закон Ньютона .
- Будем считать, что молекулы газа находятся на достаточно большом расстоянии друг от друга, так, что силы взаимодействия между ними пренебрежимо малы. Если между частицами отсутствуют силы взаимодействия, соответственно, равна нулю и потенциальная энергия взаимодействия . Назовем газ, отвечающий этим свойствам, идеальным .
- Известно, что молекулы газа движутся с разными скоростями . Однако, усредним скорости движения молекул и будем считать их одинаковыми .
- Предположим, что удары молекул о стенки сосуда абсолютно упругие (молекулы ведут себя при ударе подобно резиновым мячикам, а не подобно куску пластилина). При этом скорости молекул изменяются лишь по направлению, а по величине остаются прежними. Тогда изменение скорости каждой молекулы при ударе равно –2υ.
Введя такие упрощения, рассчитаем давление газа на стенки сосуда.
Давление – это физическая величина, равная отношению перпендикулярной составляющей силы, действующей на поверхность, к площади этой поверхности.
Сила действует на стенку со стороны множества молекул. Она может быть рассчитана как произведение силы, действующей со стороны одной молекулы, на число молекул, движущихся в сосуде в направлении этой стенки. Так как пространство трехмерно и каждое измерение имеет два направления: положительное и отрицательное, можно считать, что в направлении одной стенки движется одна шестая часть всех молекул (при большом их числе): .
Сила, действующая на стенку со стороны одной молекулы, равна силе, действующей на молекулу со стороны стенки. Сила, действующая на молекулу со стороны стенки, равна произведению массы одной молекулы на ускорение, которое она получает при ударе о стенку:
Ускорение же – это физическая величина, определяемая отношением изменения скорости ко времени, в течение которого это изменение произошло: .
Изменение скорости равно удвоенному значению скорости молекулы до удара: .
Если молекула ведет себя подобно резиновому мячику, нетрудно представить процесс удара: молекула, ударяясь, деформируется. На процесс сжатия и разжатия затрачивается время. Пока молекула действует на стенку сосуда, о последнюю успевает удариться еще некоторое число молекул, находящихся от нее на расстояниях не дальше . (Например, условно говоря, пусть молекулы имеют скорость 100 м/с. Удар длится 0,01 с. Тогда за это время до стенки успеют долететь и внести свой вклад в давление молекулы, находящиеся от нее на расстояниях 10, 50, 70 см, но не далее 100 см).
Будем рассматривать объем сосуда .
Подставив все формулы в исходную, получаем уравнение:
где:
– масса одной молекулы, – среднее значение квадрата скорости молекул, – число молекул в объеме .
Сделаем некоторые пояснения по поводу одной из величин, входящих в полученное уравнение.
Так как движение молекул хаотично и преимущественного движения молекул в сосуде нет, их средняя скорость равна нулю. Но ясно, что это не относится к каждой отдельной молекуле.
Для вычисления давления идеального газа на стенку сосуда используется не среднее значение -компоненты скорости молекул
а среднее значение квадрата скорости
Чтобы введение этой величины было более понятным, рассмотрим численный пример.
Пусть четыре молекулы имеют скорости 1, 2, 3, 4 усл. ед.
Квадрат среднего значения скорости молекул равен:
Среднее значение квадрата скорости равно:
Если скорости молекул равны +1, –2 , –3 , +4 усл. ед., то квадрат среднего значения скорости равен:
Среднее значение квадрата скорости равно:
Средние значения проекций квадрата скорости на оси связаны со средним значением квадрата скорости соотношением:
Если извлечь квадратный корень из
то получим величину, которая называется средней квадратичной скоростью молекул.
Величина, определяемая отношением числа частиц к объему, в котором они находятся, называется концентрацией (обозначается буквой ).
Величина же
– это средняя кинетическая энергия каждой молекулы газа.
С учетом этого полученное уравнение можно переписать в виде:
Уравнения связывают макропараметры газа – его давление и объем () с микропараметрами – массой молекул и их скоростью (), или энергией
Последнее уравнение читается следующим образом: давление идеального газа на стенки сосуда прямо пропорционально концентрации молекул в сосуде и их средней кинетической энергии .
Источник
➤ Adblock
detector
Источник
