Движение частицы в сосуде

1. В 1827 г. английский ботаник Р. Броун, изучая с помощью микроскопа частички цветочной пыльцы, взвешенные в воде, заметил, что эти частички совершают беспорядочное движение; они как бы дрожат в воде.
Причину движения частиц пыльцы долго не могли объяснить. Сам Броун предположил вначале, что они движутся, потому что они живые. Движение частиц пытались объяснить неодинаковым нагреванием разных частей сосуда, происходящими химическими реакциями и т.д. Лишь значительно позже поняли истинную причину движения частиц, взвешенных в воде. Эта причина – движение молекул.
Молекулы воды, в которой находится частица пыльцы, движутся и ударяются о неё. При этом с разных сторон о частицу ударяется неодинаковое число молекул, что и приводит к её перемещению.
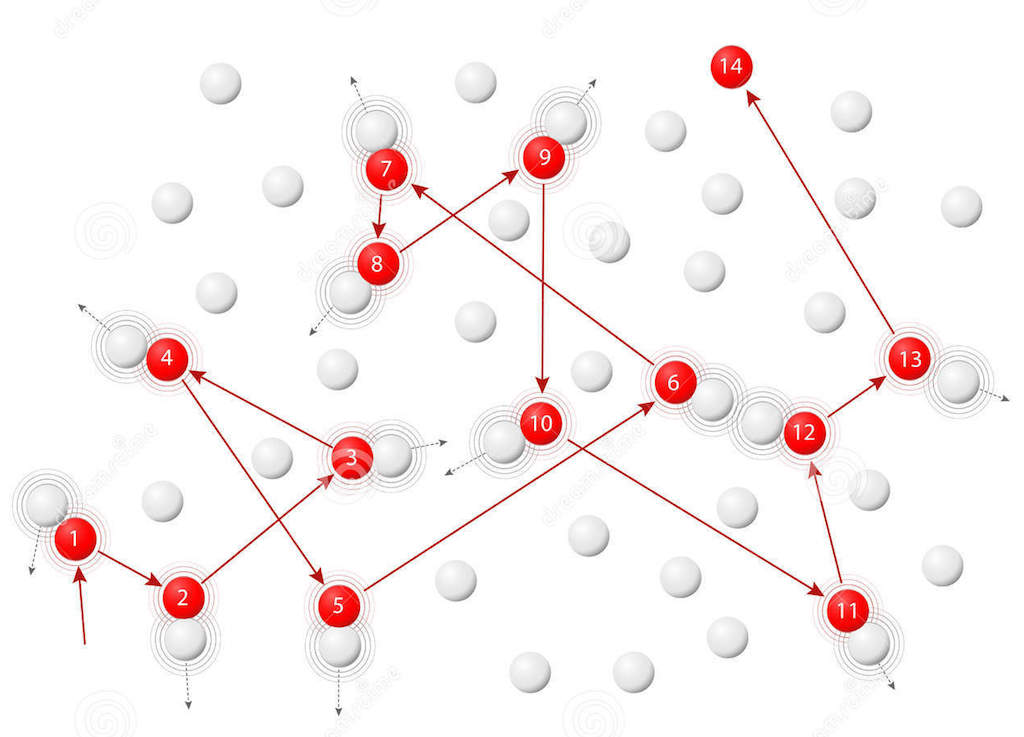
Пусть в момент времени ( t_1 ) под действием ударов молекул воды частица переместилась из т. А в т. В. В следующий момент времени большее число молекул ударяется о частицу с другой стороны, и направление её движения изменяется, она перемещается из т. В в т. С. Таким образом, движение частицы пыльцы является следствием движения и ударов о неё молекул воды, в которой пыльца находится (рис. 65). Подобное явление можно наблюдать, если поместить в воду частицы краски или сажи.
На рисунке 65 показана траектория движения частицы пыльцы. Видно, что нельзя говорить о каком-то определённом направлении её движения; оно всё время меняется.
Поскольку движение частицы – следствие движения молекул, то можно заключить, что молекулы движутся беспорядочно (хаотически). Иными словами, нельзя выделить какое-то определённое направление, в котором движутся все молекулы.
Движение молекул никогда не прекращается. Можно сказать, что оно непрерывно. Непрерывное хаотическое движение атомов и молекул называют тепловым движением. Такое название определяется тем, что скорость движения молекул зависит от температуры тела.
Поскольку тела состоят из большого числа молекул и движение молекул беспорядочно, то нельзя точно сказать, сколько ударов будет испытывать та или иная молекула со стороны других. Поэтому говорят, что положение молекулы, её скорость в каждый момент времени случайны. Однако это не означает, что движение молекул не подчиняется определённым законам. В частности, хотя скорости молекул в некоторый момент времени различны, у большинства из них значения скорости близки к некоторому определённому значению. Обычно, говоря о скорости движения молекул, имеют в виду среднюю скорость ( (v_{ср}) ).
2. С точки зрения движения молекул можно объяснить такое явление, как диффузия.
Диффузией называется явление проникновения молекул одного вещества в промежутки между молекулами другого вещества.
Мы ощущаем запах духов на некотором расстоянии от флакона. Это объясняется тем, что молекулы духов, так же как и молекулы воздуха, движутся. Между молекулами существуют промежутки. Молекулы духов проникают в промежутки между молекулами воздуха, а молекулы воздуха – в промежутки между молекулами духов.
Диффузию жидкостей можно наблюдать, если в мензурку налить раствор медного купороса, а сверху – воду так, чтобы между этими жидкостями была резкая граница. Через два-три дня можно заметить, что граница уже не будет такой резкой; через неделю она совсем размоется. Спустя месяц жидкость станет однородной и во всем сосуде будет окрашена одинаково (рис. 66).
В этом опыте молекулы медного купороса проникают в промежутки между молекулами воды, а молекулы воды – в промежутки между молекулами медного купороса. При этом следует иметь в виду, что плотность медного купороса больше, чем плотность воды.
Опыты показывают, что диффузия в газах происходит быстрее, чем в жидкостях. Это объясняется тем, что газы имеют меньшую плотность, чем жидкости, т.е. молекулы газов расположены на больших расстояниях друг от друга. Ещё медленнее происходит диффузия в твёрдых телах, поскольку молекулы твёрдых тел находятся ещё ближе друг к другу, чем молекулы жидкостей.
В природе, технике, быту можно обнаружить множество явлений, в которых проявляется диффузия: окрашивание, склеивание и др. Диффузия имеет большое значение в жизни человека. В частности, благодаря диффузии кислород в организм человека поступает не только через лёгкие, но и через кожу. По этой же причине питательные вещества проникают из кишечника в кровь.
Скорость диффузии зависит не только от агрегатного состояния вещества, но и от температуры.
Если приготовить два сосуда с водой и медным купоросом для проведения опыта по диффузии и один из них поставить в холодильник, а другой оставить в комнате, то можно обнаружить, что при более высокой температуре диффузия будет происходить быстрее. Это происходит потому, что при повышении температуры быстрее движутся молекулы. Таким образом, скорость движения молекул
и температура тела связаны между собой.
Чем больше средняя скорость движения молекул тела, тем выше его температура.
3. Молекулярная физика в отличие от механики изучает системы (тела), состоящие из большого числа частиц. Эти тела могут находиться в различных состояниях.
Величины, характеризующие состояние системы (тела), называются параметрами состояния. К параметрам состояния относят давление, объём, температуру.
Возможно такое состояние системы, при котором параметры, характеризующие его, остаются неизменными сколь угодно долго при отсутствии внешних воздействий. Это состояние называется тепловым равновесием.
Так, объём, температура, давление жидкости в сосуде, находящейся в тепловом равновесии с воздухом в комнате, не изменяются, если для этого не будет каких-либо внешних причин.
4. Состояние теплового равновесия системы характеризует такой параметр, как температура. Особенностью его является то, что значение температуры во всех частях системы, находящейся в состоянии теплового равновесия, одинаково. Если опустить в стакан с горячей водой серебряную ложку (или ложку из любого другого металла), то ложка будет нагреваться, а вода – остывать. Это будет происходить до тех пор, пока не наступит тепловое равновесие, при котором ложка и вода будут иметь одинаковую температуру. В любом случае, если взять два различно нагретых тела и привести их в соприкосновение, то более нагретое тело будет остывать, а более холодное – нагреваться. Через некоторое время система, состоящая из этих двух тел, придёт в тепловое равновесие, и температура этих тел станет одинаковой.
Так, одинаковой станет температура ложки и воды, когда они придут в тепловое равновесие.
Температура – это физическая величина, которая характеризует тепловое состояние тела.
Так, температура горячей воды выше, чем холодной; зимой температура воздуха на улице ниже, чем летом.
Единицей температуры является градус Цельсия (°С). Температуру измеряют термометром.
В основе устройства термометра и соответственно способа измерения температуры лежит зависимость свойств тел от температуры, в частности свойство тела расширяться при нагревании. В термометрах могут быть использованы разные тела: и жидкие (спирт, ртуть), и твёрдые (металлы) и газообразные. Их называют термометрическими телами. Термометрическое тело (жидкость или газ) помещают в трубку, снабжённую шкалой, её приводят в соприкосновение с телом, температуру которого хотят измерить.
При построении шкалы выбирают две основные (реперные, опорные) точки, которым приписывают определённые значения температуры, и интервал между ними делят на несколько частей. Значение каждой части соответствует единице температуры по данной шкале.
5. Существуют разные температурные шкалы. Одной из наиболее распространённых в практике шкал является шкала Цельсия. Основными точками этой шкалы служат температура таяния льда и температура кипения воды при нормальном атмосферном давлении (760 мм рт. ст.). Первой точке приписали значение 0 °С, а второй – 100 °С. Расстояние между этими точками разделили на 100 равных частей и получили шкалу Цельсия. За единицу температуры по этой шкале принят 1 °С. Помимо шкалы Цельсия широко используется температурная шкала, названная абсолютной (термодинамической) шкалой температур, или шкалой Кельвина. За ноль по этой шкале принята температура -273 °С (точнее -273,15 °С). Эта температура названа абсолютным нулём температур и обозначается 0 К. Единицей температуры является один кельвин (1 К); он равен 1 градусу Цельсия. Соответственно температура таяния льда но абсолютной шкале температур – 273 К (273,15 К), а температура кипения воды – 373 К (373,15 К).
Температуру по абсолютной шкале обозначают буквой ( T ). Связь между температурой по абсолютной шкале ( (T) ) и температурой по шкале Цельсия ( ({t}^circ) ) выражается формулой:
[ T=t^circ+273 ]
ПРИМЕРЫ ЗАДАНИЙ
Часть 1
1. Броуновское движение частиц краски в воде является следствием
1) притяжения между атомами и молекулами
2) отталкивания между атомами и молекулами
3) хаотического и непрерывного движения молекул
4) перемещения слоёв воды из-за разности температуры нижних и верхних слоёв
2. В какой из приведённых ниже ситуаций речь идёт о броуновском движении?
1) беспорядочное движение пылинок в воздухе
2) распространение запахов
3) колебательное движение частиц в узлах кристаллической решётки
4) поступательное движение молекул газа
3. Что означают слова: «Молекулы движутся хаотически» ?
А. Отсутствует выделенное направление движения молекул.
Б. Движение молекул не подчиняется никаким законам.
Правильный ответ
1) только А
2) только Б
3) и А, и Б
4) ни А, ни Б
4. Положение молекулярно-кинетической теории строения вещества о том, что частицы вещества участвуют в непрерывном хаотическом движении, относится
1) только к газам
2) только жидкостям
3) только к газам и жидкостям
4) к газам, жидкостям и твёрдым телам
5. Какое (-ие) положение (-я) молекулярно-кинетической теории строения вещества подтверждает явление диффузии?
А. Молекулы находятся в непрерывном хаотическом движении
Б. Между молекулами существуют промежутки
Правильный ответ
1) только А
2) только Б
3) и А, и Б
4) ни А, ни Б
6. При одинаковой температуре диффузия в жидкостях происходит
1) быстрее, чем в твёрдых телах
2) быстрее, чем в газах
3) медленнее, чем в твёрдых телах
4) с той же скоростью, что и в газах
7. Укажите пару веществ, скорость диффузии которых наименьшая при прочих равных условиях
1) раствор медного купороса и вода
2) пары эфира и воздух
3) железная и алюминиевая пластины
4) вода и спирт
8. Вода кипит и превращается в пар при температуре 100 °С. Средняя скорость движения молекул пара
1) равна средней скорости движения молекул воды
2) больше средней скорости движения молекул воды
3) меньше средней скорости движения молекул воды
4) зависит от атмосферного давления
9. Тепловое движение молекул
1) прекращается при 0 °С
2) прекращается при 100 °С
3) непрерывно
4) имеет определённое направление
10. Воду нагревают от комнатной температуры до 80 °С. Что происходит со средней скоростью движения молекул воды?
1) уменьшается
2) увеличивается
3) не изменяется
4) сначала увеличивается, а начиная с некоторого значения температуры, остаётся неизменной
11. Один стакан с водой стоит на столе в тёплом помещении, другой – в холодильнике. Средняя скорость движения молекул воды в стакане, стоящем в холодильнике
1) равна средней скорости движения молекул воды в стакане, стоящем на столе
2) больше средней скорости движения молекул воды в стакане, стоящем на столе
3) меньше средней скорости движения молекул воды в стакане, стоящем на столе
4) равна нулю
12. Из перечня приведённых ниже высказываний выберите два правильных и запишите их номера в таблицу
1) тепловое движение молекул происходит только при температуре большей 0 °С
2) диффузия в твёрдых телах невозможна
3) между молекулами одновременно действуют силы притяжения и силы отталкивания
4) молекула – это наименьшая частица вещества
5) скорость диффузии увеличивается с повышением температуры
13. В кабинет физики принесли ватку, смоченную духами, и сосуд, в который налили раствор медного купороса (раствор голубого цвета), а поверх осторожно налили воду (рис. 1). Было замечено, что запах духов распространился по объёму всего кабинета за несколько минут, тогда как граница между двумя жидкостями в сосуде исчезла только через две недели (рис. 2).
Выберите из предложенного перечня два утверждения, которые соответствуют результатам проведённых экспериментальных наблюдений. Укажите их номера.
1) Процесс диффузии можно наблюдать в газах и жидкостях.
2) Скорость диффузии зависит от температуры вещества.
3) Скорость диффузии зависит от агрегатного состояния вещества.
4) Скорость диффузии зависит от рода жидкостей.
5) В твёрдых телах скорость диффузии наименьшая.
Ответы
Тепловое движение атомов и молекул. Связь температуры вещества со скоростью хаотического движения частиц. Броуновское движение. Диффузия. Тепловое равновесие
3.8 (76%) 5 votes
Источник
Кинетическая энергия молекулы
В газе молекулы совершают свободное (изолированное от других молекул) движение, лишь время от времени сталкиваясь друг с другом или со стенками сосуда. До тех пор, пока молекула совершает свободное движение, у нее имеется только кинетическая энергия. Во время столкновения у молекул появляется и потенциальная энергия. Таким образом, полная энергия газа представляют сумму кинетической и потенциальной энергий ее молекул. Чем разреженное газ, тем больше молекул в каждый момент времени пребывает в состоянии свободного движения, имеющих только кинетическую энергию. Следовательно, при разрежении газа уменьшается доля потенциальной энергии в сравнении с кинетической.
Средняя кинетическая энергия молекулы пpи равновесии идеального газа обладает одной очень важной особенностью: в смеси различных газов средняя кинетическая энергия молекулы для различных компонентов смеси одна и та же.
Например, воздух представляет собой смесь газов. Средняя энергия молекулы воздуха для всех его компонентов пpи нормальных условиях, когда воздух еще можно рассматривать как идеальный газ, одинакова. Данное свойство идеальных газов может быть доказано на основании общих статистических соображений. Из него вытекает важное следствие: если два различных газа (в разных сосудах) находятся в тепловом равновесии друг с другом, то средние кинетические энергии их молекул одинаковы.
В газах обычно расстояние между молекулами и атомами значительно больше, чем размеры самих молекул, силы взаимодействия молекул не велики. Вследствие чего газ не имеет собственной формы и постоянного объема. Газ легко сжимается и может неограниченно расширяться. Молекулы газа движутся свободно (поступательно, могут вращаться), лишь иногда сталкиваясь с другими молекулами и стенками сосуда, в котором находится газ, причем движутся с очень большими скоростями.
Движение частиц в твердых телах
Строение твёрдых тел принципиально отлично от строения газов. В них межмолекулярные расстояния малы и потенциальная энергия молекул сравнима с кинетической. Атомы (или ионы, или целые молекулы) нельзя назвать неподвижными, они совершают беспорядочное колебательное движение около средних положений. Чем больше температура, тем больше энергия колебаний, а следовательно, и средняя амплитуда колебаний. Тепловыми колебаниями атомов объясняется и теплоемкость твёрдых тел. Рассмотрим подробнее движения частиц в кристаллических твердых телах. Весь кристалл в целом представляет собой очень сложную связанную колебательную систему. Отклонения атомов от средних положений невелики, и поэтому можно считать, что атомы подвергаются действию квазиупругих сил, подчиняющихся линейному закону Гука. Такие колебательные системы называются линейными.
Существует развитая математическая теория систем, подверженных линейным колебаниям. В ней доказана очень важная теорема, суть которой состоит в следующем. Если система совершает малые (линейные) взаимосвязанные колебания, то путем преобразования координат ее формально можно свести к системе независимых осцилляторов (у которых уравнения колебаний не зависят друг от друга). Система независимых осцилляторов ведет себя подобно идеальному газу в том смысле, что атомы последнего тоже можно рассматривать как независимые.
Именно используя представление о независимости атомов газа, мы приходим к закону Больцмана. Этот очень важный вывод представляет простую и надежную основу для всей теории твёрдого тела.
Закон Больцмана
Число осцилляторов с заданными параметрами (координаты и скорости) определяется так же, как и число молекул газа в заданном состоянии, по формуле:
[n_a=Ce^{-frac{E_a}{kT}} (1),]
где
[E_a=frac{mv^2}{2}+frac{kx^2}{2}(2)]
— энергия осциллятора.
Закон Больцмана (1) в теории твёрдого тела не имеет ограничений, однако формула (2) для энергии осциллятора взята из классической механики. Пpи теоретическом рассмотрении твёрдых тел нужно опираться на квантовую механику, для которой характерна дискретность изменения энергии осциллятора. Дискретность энергии осциллятора становится несущественной только пpи достаточно высоких значениях его энергии. Это значит, что (2) можно пользоваться лишь пpи достаточно высоких температурах. Пpи высоких температурах твёрдого тела, близких к температуре плавления, из закона Больцмана вытекает закон равномерного распределения энергии по степеням свободы. Если в газах на каждую степень свободы в среднем приходится количество энергии, равное (1/2) kT, то у осциллятора одна степень свободы, кроме кинетической, имеет потенциальную энергию. Поэтому на одну степень свободы в твёрдом теле пpи достаточно высокой температуре приходится энергия, равная kT. Исходя из этого закона, нетрудно рассчитать полную внутреннюю энергию твердого тела, а вслед за ней и его теплоемкость. Моль твердого тела содержит NA атомов, а каждый атом имеет три степени свободы. Следовательно, в моле содержится 3 NA осцилляторов. Энергия моля твердого тела
[E_{mu }=3N_AkT=3RT(3)]
а молярная теплоемкость твердого тела пpи достаточно высоких температурах
[c=frac{dE_{mu }}{dT}=3R (4)]
Закон Дюлонга и Пти
Это закон Дюлонга и Пти: все простые (одноатомные) твёрдые тела в области высоких температур имеют одну и ту же, не зависящую от температуры, молярную теплоемкость, равную 3R.
Опыт подтверждает этот закон.
Жидкости занимают промежуточное положение между газами и твердыми телами. Молекулы жидкости не расходятся на большие расстояния, и жидкость в обычных условиях сохраняет свой объем. Но в отличие от твердых тел молекулы не только совершают колебания, но и перескакивают с места на место, то есть совершают свободные движения. При повышении температуры жидкости кипят (существует так называемая температура кипения) и переходят в газ. При понижении температуры жидкости кристаллизуются и становятся твердыми веществами. Существует такая точка в поле температур, в которой граница между газом (насыщенным паром) жидкостью исчезает (критическая точка). Картина теплового движения молекул в жидкостях вблизи температуры затвердевания очень похожа на поведение молекул в твердых телах. К примеру, коэффициенты теплоемкости прочти совпадают. Так как теплоемкость вещества при плавлении изменяется слабо, то можно сделать вывод, что характер движения частиц в жидкости близок движению в твердом теле (при температуре плавления). При нагревании свойства жидкости постепенно изменяются, и она становится более похожа на газ. У жидкостей средняя кинетическая энергия частиц меньше потенциальной энергии их межмолекулярного взаимодействия. Энергия межмолекулярного взаимодействия в жидкости и твердых телах отличаются несущественно. Если сравнить теплоту плавления и теплоту испарения, то увидим, что при переходе из одного агрегатного состояния в другое теплота плавления существенно ниже, теплоты парообразования. Адекватное математическое описание структуры жидкости может быть дано лишь с помощью статистической физики. Например, если жидкость состоит из одинаковых сферических молекул, то ее структуру можно описать радиальной функцией распределения g(r), которая дает вероятность обнаружения какой-либо молекулы на расстоянии r от данной, выбранной в качестве точки отсчета. Экспериментально эту функцию можно найти, исследуя дифракцию рентгеновских лучей или нейтронов, можно провести компьютерное моделирование этой функции, используя механику Ньютона.
Кинетическая теория жидкости была разработана Я.И. Френкелем. В этой теории жидкость рассматривается, как и в случае твердого тела, как динамическая система гармонически осцилляторов. Но в отличие от твердого тела положение равновесия молекул в жидкости имеет временный характер. Поколебавшись около одного положения, молекула жидкости перескакивает в новое положение, расположенное по соседству. Такой перескок происходит с затратой энергии. Среднее время «оседлой жизни» молекулы жидкости можно рассчитать как:
[leftlangle trightrangle =t_0e^{frac{W}{kT}}left(5right),]
где $t_0 $- период колебаний около одного положения равновесия. Энергия, которую должна получить молекула, чтобы из одного положения перейти в другое, называется энергией активации W, а время нахождения молекулы в положении равновесия — временем «оседлой жизни» t.
У молекулы воды, например, при комнатной температуре, одна молекула совершает около 100 колебаний и перескакивает в новое положение. Силы притяжения между молекулам жидкости велики, чтобы сохранялся объем, но ограниченность оседлой жизни молекул ведет к возникновению такого явления, как текучесть. Во врем колебаний частицы около положения равновесия они непрерывно соударяются друг с другом, поэтому даже малое сжатие жидкости приводит к резкому «ожесточению» соударений частиц. Это означает резкое повышение давления жидкости на стенки сосуда, в котором ее сжимают.
Пример 1
Задание: Определить удельную теплоёмкость меди. Считать, что температура меди близка к температуре плавления. (Молярная масса меди $mu =63cdot 10^{-3}frac{кг}{моль})$
Решение:
Согласно закону Дюлонга и Пти моль химически простых веществ при температурах, близких к температуре плавления, имеет теплоемкость:
[c=frac{dE_{mu }}{dT}=3R left(1.1right)]
Удельная теплоемкость меди:
[С=frac{с}{mu }to С=frac{3R}{mu }left(1.2right),] [С=frac{3cdot 8,31}{63cdot 10^{-3}}=0,39 cdot 10^3(frac{Дж}{кгК})]
Ответ: Удельная теплоёмкость меди $0,39 cdot 10^3left(frac{Дж}{кгК}right).$
Пример 2
Задание: Объясните упрощённо с точки зрения физики процесс растворения соли (NaCl) в воде.
Решение:
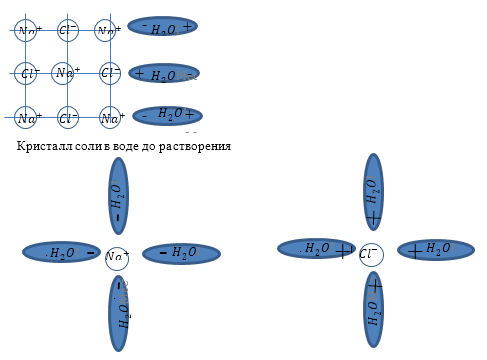
Рис. 1
Основу современной теории растворов создал Д.И. Менделеев. Он установил, что при растворении протекают одновременно два процесса: физический — равномерное распределение частиц растворяемого вещества по всему объему раствора, и химический — взаимодействие растворителя с растворяемым веществом. Нас интересует физический процесс. Молекулы соли не разрушают молекулы воды. В этом случае нельзя было бы выпарить воду. Если бы молекулы соли присоединялись бы к молекулам воды — мы получали бы некое новое вещество. И внутрь молекул волы молекулы соли проникнуть не могут.
Между ионами Na+ и Cl– хлора и полярными молекулами воды возникает ионно-дипольная связь. Она оказывается прочнее, чем ионные связи в молекулах поваренной соли. В результате этого процесса связь между ионами, расположенными на поверхности кристаллов NaCl, ослабляется, ионы натрия и хлора отрываются от кристалла, а молекулы воды образуют вокруг них так называемые гидратные оболочки. Отделившиеся гидратированные ионы под влиянием теплового движения равномерно распределяются между молекулами растворителя.
Источник
