Гибридная операция на сосудах это
Сегодня уже невозможно представить сосудистую хирургию без так называемых «гибридных операций». Что же такое гибридная хирургия или гибридная операция? В основу термина «гибридный» положено латинское слово «hybrida» — смесь, помесь.
В случае сосудистой хирургии, гибридными называются операции, которые сочетают в себе два различных лечебных подхода:
- классический хирургический подход, когда воздействие на сосуд осуществлеяется прямым путём с помощью хирургических инструментов под контролем глаза;
- рентгенэндоваскулярный подход, когда сосуд подвергается воздействию дистанционно с помощью специальных проводников, катетеров, баллонов и т. д. под рентгеновским контролем.
Каждый из этих двух подходов имеет свои неоспоримые преимущества. Классическая «открытая» хирургия ассоциируется с радикальностью и высокой степенью надёжности вмешательства, в то время как эндоваскулярная — с малотравматичностью и быстротой. Сочетая эти подходы в одной операции, сосудистый хирург, с одной стороны, добивается её радикальности, а с другой — скорости и малотравматичности. Это первое преимущество гибридного подхода к операциям на артериях.
Вторым большим преимуществом гибридной хирургии является возможность выполнения нескольких лечебных воздействий в рамках одной операции. Таким образом, вместо нескольких оперативных пособий пациенту выполняется одно с сопоставимым конечным результатом.
Третьим бесспорным преимуществом гибридной операции является её контролируемость. Практически на любом этапе гибридного вмешательства возможен ангиографический контроль, что повышает надёжность и качество выполненной операции.
С внедрением в лечебный процесс гибридных операций перед сосудистыми хирургами открылись новые возможности в лечении сложных пациентов, которые ранее были обречены на страдания, связанные с их недугом.
Гибридные операции чаще всего используются в лечении заболеваний подвздошных артерий в сочетании с поражением общей или глубокой бедренных артерий. В этом случае первым этапом гибридной операции выполняется эндартерэктомия — удаление атеросклеротической бляшки из бедренных сосудов, а вторым — стентирование подвздошных артерий.
Другим самым распространённым случаем применения гибридной хирургии является вмешательства при многоуровневом поражении магистральных артерий бедра и голени. Первым этапом в таких операциях выполняется бедренно-подколенное или бедренно-берцовое шунтирование (создаётся обходной путь для кровотока путём соединения к поражённому сосуду выше и ниже закупорки дополнительного сосуда — шунта; в качестве шунта может использоваться синтетический протез или собственная вена пациента), а вторым — эндоваскулярная ангиопластика (расправление стенок закупоренных сосудов специальным баллоными катетерами) артерий голени.
Гибридная хирургия также находит своё применение в лечении аневризм аорты. Так, например, аневризмы дуги аорты почти всегда требуют гибридного подхода. То же самое касается аневризм брюшного отдела аорты, сочетающиеся с выраженным стенозом одной из двух общих подвздошных артерий, отходящих от неё. В таких случаях после основного этапа эндопротезирования аорты выполняется перекрёстное бедренно-бедренное шунтирование.
Таким образом, гибридные операции в практике сосудистого хирурга являются чрезвычайно полезным инструментом, позволяющим добиться следующих важных преимуществ:
- Малотравматичность в сочетании с радикальностью,
- Возможность избежать дополнительных операций,
- Высокая степень надёжности выполняемого вмешательства,
- Возможность хирургической помощи у пациентов крайне высокого риска,
- Сокращение сроков лечения и реабилитации.
Источник
Закарян Н.В., Панков А.С.
Эндоваскулярные методы лечения продолжают свое победное шествие по планете, постоянно расширяя свое влияние на коррекцию сосудистой патологии. Тем не менее, некоторые проблемы до сих пор остаются серьезным вызовом как для открытых, так и для эндоваскулярных хирургов. Например, при тяжелых многоэтажных поражениях артерий нижних конечностей не всегда удается выполнить их полноценную коррекцию только рентгенохирургическим либо открытым способом [1-7, 9,12,14,16-20]. При использовании исключительно эндоваскулярных методов часто увеличивается время облучения и объем используемого рентгеноконтрастного вещества [1,3,8,10-15]. С другой стороны, продолжительные открытые сосудистые вмешательства сопровождаются увеличением частоты осложнений и летальных исходов, особенно у пожилых пациентов и у больных с тяжелыми сопутствующими заболеваниями [1-3,6,8,12-15]. Для решения этой проблемы в современных условиях активно развивается концепция гибридной хирургии, которая заключается в одновременном использовании как эндоваскулярных, так и открытых хирургических методов лечения сложных поражений сосудов [1-20].
В некоторых клиниках частота выполнения гибридных операций при многоэтажных поражениях достигает 25%, и эти цифры продолжают расти. [3-6,9,11]. Обычно данные операции проводятся в специальной гибридной операционной, оснащенной прозрачным для рентгеновских лучей операционным столом и ангиографической установкой (стационарной или передвижной С-дугой).
Выделяют одномоментные и двухэтапные гибридные вмешательства, когда открытый и эндоваскулярный этапы разделяются по времени. Большинство специалистов в последнее время склоняются к тому, что термин “гибридная хирургия” более правильно использовать только в случаях одномоментных вмешательств [2].
Наиболее частыми гибридными периферическими вмешательствами в настоящее время являются эндартерэктомия из общей бедренной артерии в сочетании с ангиопластикой/стентированием нижележащих и/или вышележащих сегментов, бедренно-подколенное шунтирование в сочетании с эндоваскулярными вмешательствами на артериях голени, ангиопластика/стентирование поверхностной бедренной артерии (ПБА) с одномоментным выполнением бедренно-дистального шунтирования артерий голени, а также различные операции на брахиоцефальных артериях [1-23].
Вероятно, самой распространенной гибридной операцией на периферических сосудах является одномоментное стентирование подвздошных артерий в сочетании с эндартерэктомией из общей бедренной артерии (ОБА) и возможным бедренным шунтированием/стентированием. Dosluoglu с коллегами в 2006 году разработали технику PAGA (“pre-arteriotomy guidewire access”, или “эндоваскулярная установка проводника до артериотомии”) для оптимизации подобных операций [5]. В последние годы техника получила широкое распространение во всем мире. Описание методики в классическом варианте представлено ниже.
Вначале хирурги выполняют открытое выделение общей (ОБА), глубокой (ГБА) и поверхностной бедренных артерий (ПБА), а также наружной подвздошной артерии (НПА), если это необходимо. Затем пунктируют общую бедренную артерию; в случае окклюзии или сильного кальциноза ОБА проводят пункцию дистального отдела НПА. Рекомендуется выполнять микропункцию с проведением 0,018-дюймового проводника для предотвращения травмы артерии. В случае окклюзии подвздошных артерий осуществляется реканализация с использованием стандартных методик или с помощью специальных устройств (например, “Frontrunner” (“Cordis”)). После доставки проводника в брюшную аорту эндоваскулярный этап прерывается. Затем после гепаринизации выполняется артериотомия ОБА (с распространением на ПБА и ГБА, если это необходимо). Далее хирурги проводят стандартную эндартерэктомию из ОБА с наложением заплаты, при этом швы в области пункции артерии оставляют незатянутыми. На линию швов по желанию хирурга может быть нанесен биологический клей (например, “Bioglue” (“CryoLife, Inc”)), для предотвращения подтекания крови. Когда гемостаз полностью завершен, по проводнику в ОБА устанавливают интродьюсер размером 6-11 F для продолжения эндоваскулярного этапа (интродьюсеры большого размера обеспечивают хороший гемостаз в ходе операции, кроме того, через них можно проводить стент-графты, если это необходимо). Затем последние швы в области пункции затягиваются, зажимы с артерий снимают, запускают кровоток и заканчивают эндоваскулярный этап, который обычно заключается в выполнении ангиопластики и стентирования подвздошных артерий [3,5,11].
Как известно, пункция артерии и проведение проводника после выполненной эндартерэктомии может сопровождаться риском развития кровотечений и диссекций в ОБА и НПА. Одним из главных достоинств методики PAGA является устранение данных рисков, т.к. артерия пунктируется перед эндартерэктомией. Также при использовании этой техники можно относительно безопасно выполнить пункцию НПА в случае необходимости, т.к. в конце операции эта область тщательно ушивается и риск забрюшинной гематомы практически отсутствует (при традиционном эндоваскулярном подходе пункция НПА является нежелательной процедурой).
В качестве примера использования методики PAGA можно привести опыт корейских специалистов Joh et al [11]. Они использовали данную методику с некоторыми изменениями. Так, в случае, если на начальном этапе не удавалось выполнить реканализацию окклюзии подвздошных артерий ретроградным доступом, выполнялась антеградная реканализация (доступом через контралатеральную ОБА, либо через плечевую артерию), затем проводник захватывался и выводился через артериотомическое отверстие в ходе эндартерэктомии или шунтирования (т.н. “экстернализация” проводника).
Вышеуказанными корейскими авторами также применялась антеградная методика PAGA при сочетанных поражениях ОБА и ПБА: сначала выполнялась антеградная реканализация ПБА доступом через пораженную ОБА, затем эндартерэктомия из ОБА и потом финальная ангиопластика/стентирование ПБА [11].
Также часто выполняется наложение бедренно-дистального шунта с одномоментным стентированием вышележащих сегментов (бедренной и/или подвздошных артерий). Данный вид вмешательств используется достаточно давно. Так, в 2001 году Schneider с соавт. впервые описали технику выполнения одномоментной ангиопластики сужений ПБА в сочетании с наложением бедренно-берцового шунта у больных с критической ишемией нижних конечностей [12]. В госпитальном периоде ни у одного из 12 пациентов не было отмечено окклюзии шунта, ампутаций также удалось избежать. Через 2 года частота первичной проходимости артерий составила 76%. Пример гибридного стентирования левой ОПА в сочетании с наложением бедренно-берцового шунта представлен на рис. 1.
До сих пор дискутабельным остается вопрос о схеме введения антикоагулянтов и антиагрегантов во время и после гибридных вмешательств на периферических артериях. Наиболее признанной схемой у большинства специалистов является следующая: в ходе вмешательства вводится 70-100 ЕД/кг гепарина (в среднем 5000-7000 ЕД), также в дальнейшем пациент получает клопидогрель 75 мг/день в течение 3-6 месяцев и 100 мг/день ацетилсалициловой кислоты пожизненно [1-23]. Вопреки мнению некоторых сосудистых хирургов, риск кровотечения при подобной схеме остается невысоким как во время операции, так и в ближайшем послеоперационном периоде [1-12, 14, 18].
Эффективность гибридных операций, по данным разных авторов, является достаточно высокой [1-16, 19-23]. В работе Antoniou показано, что проходимость артерий после гибридных вмешательств через 1 год составила 98%, причем исходно группа пациентов была достаточно тяжелой (47% больных с критической ишемией нижних конечностей) [1]. Matsagkas с соавт. доложили, что у пациентов с критической ишемией первичная и вторичная проходимость оперированных сегментов через 2 года составила 93,2% и 95,5% соответственно [10]. В исследовании Cotroneo были изучены результаты гибридных вмешательств у 44 пациентов (24 были с хронической и 20 – с критической ишемией). Через 2 года первичная и вторичная проходимость составила 79,1% и 86,1% соответственно [4]. Nishibe с коллегами доложили, что у пациентов с мультифокальными поражениями TASC D через 2 года после гибридных операций первичная проходимость оперированных сегментов составила 94%, а частота спасения конечности – 100% [13].
В работе Schanzer с соавт. также доложено о хороших результатах гибридной ангиопластики/стентирования сужений в поверхностной бедренной артерии (ПБА) в сочетании с шунтированием артерий голени у 23 больных с критической ишемией. Проксимальный анастомоз шунта вшивался в дистальный отдел ПБА или в подколенную артерию, дистальный – в артерию голени или стопы. В ближайшем послеоперационном периоде не было отмечено случаев ампутации или тромбозов оперированных сегментов. Через 5 лет ампутации удалось избежать 70% пациентов, эндоваскулярная коррекция рестенозов в ПБА потребовалась только 1 больному [8].
Многие авторы отмечают сокращение времени нахождения в клинике и снижение стоимости лечения у пациентов с гибридными одномоментными вмешательствами по сравнению с теми, кто перенес двухэтапные операции [1-8, 10, 12-16, 22]. Так, в работе Ebaugh с соавт. показано, что при одноэтапных операциях больничные расходы снижаются почти в 2 раза по сравнению с двухэтапными [7]. Кроме того, при гибридных вмешательствах практически отсутствуют осложнения в области пункции, так как в конце операции эта зона тщательно ушивается. Безусловно, при гибридных процедурах, по сравнению с тотальной эндоваскулярной коррекцией, снижается расход рентгеноконтрастного вещества, что очень важно у пациентов, находящихся в группе риска развития контраст-индуцированной нефропатии [2-7, 17, 19].
Интересны данные, полученные Dosluoglu с соавт.: в группе гибридных вмешательств, проведенных в их клинике, частота выполнения эндоваскулярного этапа сосудистым хирургом составляла 0% в 2004 году и на порядок выше – 86,3% в 2010 году [6]. Показано, что сосудистые хирурги моложе 50 лет активно осваивают эндоваскулярные методики и регулярно посещают специальные обучающие курсы, что позволяет им самостоятельно, без помощи эндоваскулярных хирургов, проводить гибридные операции. Все это способствует дальнейшему активному распространению гибридной хирургии при патологии периферических артерий.
Список литературы:
- Antoniou GA, Sfyroeras GS, Karathanos C, et al. Hybrid endovascular and open treatment of severe multilevel lower extremity arterial disease // Eur J Vasc Endovasc Surg. – 2009. – Vol. 38(5). – P. 616–622.
- Balaz P, Rokosny S, Bafrnec J, Björck M. The role of hybrid procedures in the management of peripheral vascular disease // Scand J Surg. – 2012. – Vol. 101(4). – P. 232–237.
- Chang RW, Goodney PP, Baek JH, Nolan BW, Rzucidlo EM, Powell RJ. Long-term results of combined common femoral endarterectomy and iliac stenting/stent grafting for occlusive disease // J Vasc Surg. – 2008. – Vol. 48(2). – P. 362–367.
- Cotroneo AR, Iezzi R, Marano G, Fonio P, Nessi F, Gandini G. Hybrid therapy in patients with complex peripheral multifocal steno-obstructive vascular disease: two-year results // Cardiovasc Intervent Radiol. – 2007. – Vol. 30(3). – P. 355–361.
- Dosluoglu HH, Cherr GS. Pre-arteriotomy guidewire access (PAGA): a crucial maneuver for securing infow and/or outfow in patients with bulky iliofemoral occlusive disease undergoing combined (open/endovascular) procedures // Eur J Vasc Endovasc Surg. – 2006. – Vol. 32(1). – P. 97–100.
- Dosluoglu HH, Lall P, Cherr GS, Harris LM, Dryjski ML. Role of simple and complex hybrid revascularization procedures for symptomatic lower extremity occlusive disease // J Vasc Surg. – 2010. – Vol. 51(6). – P. 1425–1435.
- Ebaugh JL, Gagnon D, Owens CD, Conte MS, Raffetto JD. Comparison of costs of staged versus simultaneous lower extremity arterial hybrid procedures // Am J Surg. – 2008. – Vol. 196(5). – P. 634–640.
- Schanzer A, Owens CD, Conte MS, Belkin M. Superficial femoral artery percutaneous intervention is an effective strategy to optimize inflow for distal origin bypass grafts // J Vasc Surg. – 2007. – Vol. 45. – P. 740–743.
- Lyden SP, Smouse HB. TASC II and the endovascular management of infrainguinal disease // J Endovasc Ther. – 2009. – Vol. 16(2). – P. II5–II18.
- Matsagkas M, Kouvelos G, Arnaoutoglou E, Papa N, Labropoulos N, Tassiopoulos A. Hybrid procedures for patients with critical limb ischemia and severe common femoral artery atherosclerosis // Ann Vasc Surg. – 2011. – Vol. 25(8). – P. 1063–1069.
- Joh J. et al. Simultaneous hybrid revascularization for symptomatic lower extremity arterial occlusive disease // Experimental and therapeutic medicine. – 2014. – P. 804-810.
- Schneider P., Caps M., Ogawa D. Intraoperative superficial femoral artery balloon angioplasty and popliteal to distal bypass graft: an option for combined open and endovascular treatment of diabetic gangrene // J Vasc Surg. – 2001. – Vol. 33. – P. 955–962.
- Nishibe T, Kondo Y, Dardik A, Muto A, Koizumi J, Nishibe M. Hybrid surgical and endovascular therapy in multifocal peripheral TASC D lesions: up to three-year follow-up // J Cardiovasc Surg (Torino). – 2009. – Vol. 50(4). – P. 493–499.
- Piazza M, Ricotta JJ II, Bower TC, et al. Iliac artery stenting combined with open femoral endarterectomy is as effective as open surgical reconstruction for severe iliac and common femoral occlusive disease // J Vasc Surg. – 2011. – Vol. 54(2). – P. 402–411.
- Reed AB. Endovascular as an open adjunct: use of hybrid endovascular treatment in the SFA // Semin Vasc Surg. – 2008. – Vol. 21(4). – P. 200–203.
- Van Den Berg J, Waser S, Trelle S, Diehm N, Baumgartner I. Lesion characteristics of patients with chronic critical limb ischemia that determine choice of treatment modality // J Cardiovasc Surg (Torino). – 2012. – Vol. 53(1). – P. 45–52.
- Scali ST, Rzucidlo EM, Bjerke AA, et al. Long-term results of open and endovascular revascularization of superfcial femoral artery occlusive disease // J Vasc Surg. – 2011. – Vol. 54(3). – P. 714–721.
- Schrijver AM, Moll FL, De Vries JP. Hybrid procedures for peripheral obstructive disease // J Cardiovasc Surg (Torino). – 2010. – Vol. 51(6). – P. 833–843.
- Reed AB. Hybrid procedures and distal origin grafts // Semin Vasc Surg. – 2009. – Vol. 22(4). – P. 240–244.
- Fernandez N, McEnaney R, Marone LK, et al. Multilevel versus isolated endovascular tibial interventions for critical limb ischemia // J Vasc Surg. – 2011. – Vol. 54(3). – P. 722–729.
- Karathanos C, Sfyroeras GS, Stamoulis K, Drakou A, Vretzakis G, Giannoukas AD. Hybrid procedures for the treatment of multi-focal ipsilateral internal carotid and proximal common carotid or innominate artery lesions // Vasa. – 2011. – Vol. 40. – P. 241–245
- Bazan H, Sheahan M, Dardik A. Carotid endarterectomy with simultaneous retrograde common carotid artery stenting: Technical considerations // Catheter Cardiovasc Interv. – 2008. – Vol. 72. – P. 1003–1007.
- Zhang L., Xing T. et al. Preliminary application of hybrid operation in the treatment of carotid artery stenosis in patients with complex ischemic cerebrovascular diseases // Int J Clin Exp Pathol. – 2014. – Vol. 7(8). – P. 5355–5362.
Статья добавлена 20 февраля 2016 г.
Источник
В настоящее время лечение пациентов с сердечно-сосудистыми заболеваниями становится всё более сложным в связи с общим старением населения и распространённостью сопутствующей патологии, что заставляет вести поиски альтернативных методов терапии. Стратегии гибридной реваскуляризации сочетают преимущества открытой хирургии и транскатетерных вмешательств. Методики, доступные как хирургу, так и кардиологу, могут быть с успехом применены в лечении широкого круга пациентов, страдающих сердечно-сосудистыми заболеваниями. Результаты гибридных вмешательств во всех областях кардиохирургии не уступают результатам традиционных методик и заслуживают пристального внимания. Будущее кардиохирургии и интервенционной кардиологии связано с дальнейшим развитием “гибридного мышления”.
Гибридные операции представляют собой комбинацию коронарного шунтирования (открытая хирургическая операция на работающем сердце из мини-доступа) со стентированием (рентгенэндоваскулярное вмешательство).
Гибридные методики реваскуляризации миокарда были включены в рекомендации Американской Ассоциации Сердца (American Heart Association) в 2012 году. На текущий момент стратегии гибридной реваскуляризации получают всё более широкое распространение.
Чрескожное коронарное вмешательство (ЧКВ) с последующим миниинвазивным коронарным шунтированием (MIDCABG)
К преимуществам данного подхода можно отнести снижение риска ишемии миокарда в ходе MIDCABG. При этом традиционное аортокоронарное шунтирование может стать альтернативой в случае субоптимальных результатов ЧКВ. К недостаткам данной методики можно отнести недостаточность ангиографического контроля анастомоза между левой внутренней грудной артерией (ЛВГА) и передней межжелудочковой артерией (ПМЖА), риск увеличения кровопотери в ходе MIDCABG, выполняемого на фоне двойной антиагрегантной терапии, и возможность тромбоза стента.
Миниинвазивное коронарное шунтирование (MIDCABG) с последующим чрескожным коронарным вмешательством (ЧКВ)
Преимущества данного подхода: начало агрессивной антиагрегантной терапии после ЧКВ, выполняемой вторым этапом, защита миокарда функционирующим шунтом к ПМЖА при выполнении ЧКВ высокого риска. К недостаткам относятся следующие моменты: MIDCABG выполняется на фоне значимого поражения коронарных артерий, а альтернатива в виде традиционного аортокоронарного шунтирования ведет к росту осложнений после субоптимального или неудачного ЧКВ.
Симультанное выполнение MIDCABG и ЧКВ (одновременное)
К положительным моментам данной стратегии относятся единовременный ангиографический контроль анастомоза ЛВГА с ПМЖА и ЧКВ пораженных коронарных артерий. К отрицательным сторонам можно отнести риск кровотечения на фоне двойной антиагрегантной терапии, а также экономические и логистические затруднения.
В большинстве случаев пациентам с нестабильной стенокардией, обусловленной поражением правой или огибающей коронарных артерий, первым этапом выполняется ЧКВ. Напротив, при критическом поражении ПМЖА первым этапом выполняется MIDCABG.
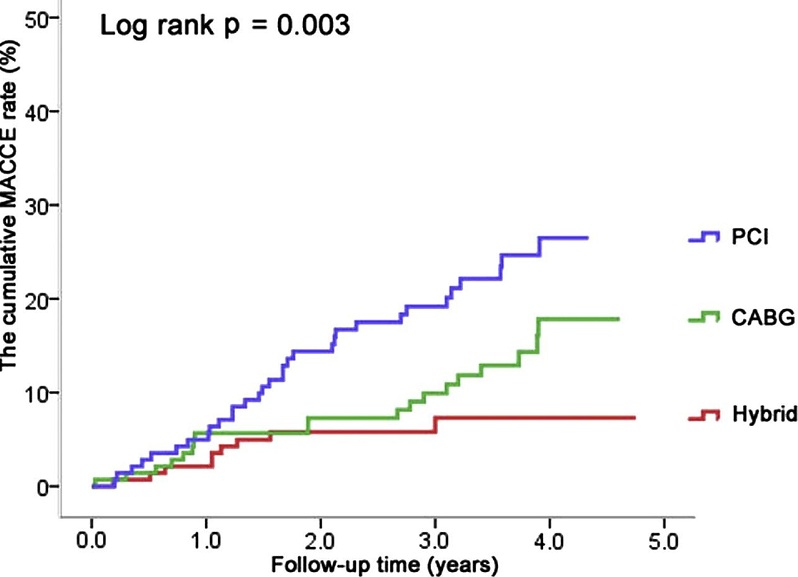
Ключевым моментом, определяющим превосходство АКШ перед ЧКВ, является формирование анастомоза между левой внутренней грудной артерией (ЛВГА) и передней межжелудочковой артерией (ПМЖА), что позволяет обеспечить до 75% потребности в кровоснабжении миокарда левого желудочка (и до 100% потребности в случае левого типа коронарного кровообращения). Отдаленная работоспособность маммарокоронарного шунта ЛВГА-ПМЖА составляет более 95% в течение 10 лет после операции, что позволяет существенно снизить риск нежелательных событий, частоту эпизодов стенокардии, а также улучшить качество жизни.Риск нежелательных сердечно-сосудистых событий у пациентов, перенесших.

– интервенционное вмешательство,
– традиционное аортокоронарное шунтирование,
– гибридную операцию.
Liuzhong Shen, Shengshou Hu, Haoran Wang, Hui Xiong, Zhe Zheng, Lihuan Li, Bo Xu, Hongbing Yan, Runlin Gao. One-Stop Hybrid Coronary Revascularization Versus Coronary Artery Bypass Grafting and Percutaneous Coronary Intervention for the Treatment of Multivessel Coronary Artery Disease. 3-Year Follow-Up Results From a Single Institution. Journal of the American College of Cardiology, Volume 61, Issue 25, June 2013. DOI: 10.1016/j.jacc.2013.04.007.
Источник
