Идеальный газ находящийся в сосуде переводят
5.4. Практическое применение уравнения состояния идеального газа
5.4.1. Уравнение состояния для идеального газа в открытом сосуде
При рассмотрении идеального газа, находящегося в открытом сосуде, необходимо учитывать, что вследствие изменения термодинамических параметров часть газа выходит из сосуда. При этом уравнение состояния записывается только для той части газа, которая остается в сосуде.
Для идеального газа, находящегося в открытом сосуде, необходимо учитывать следующее:
- масса газа изменяется в результате изменения его термодинамических параметров:
m ≠ const;
- рассматривается газ, оставшийся в сосуде определенного объема, т.е. объем газа фиксирован:
V = const;
- давление газа может изменяться или оставаться постоянным (в зависимости от условия задачи), причем на изменение давления в условии задачи обычно бывает четкое указание.
Если давление идеального газа в открытом сосуде по условию задачи изменяется (p ≠ const), то уравнение Менделеева – Клапейрона записывается для двух состояний газа в виде системы (рис. 5.7):Рис. 5.7
p 1 V = m 1 M R T 1 , p 2 V = m 2 M R T 2 , }
где p 1, m 1, T 1 – давление, масса и температура газа в начальном состоянии; p 2, m 2, T 2 – указанные параметры газа в конечном состоянии; V – объем сосуда; M – молярная масса газа; R – универсальная газовая постоянная, R ≈ 8,31 Дж/(моль ⋅ К).
Если давление идеального газа в открытом сосуде по условию задачи остается постоянным (p = const), то изменения некоторых характеристик газа в открытом сосуде можно вычислить по следующим формулам:
- изменение массы
Δ m = m 1 − m 2 = m 1 ( 1 − T 1 T 2 ) ,
где m 1 – первоначальная масса газа; m 2 – масса газа в конце процесса; T 1 – термодинамическая (абсолютная) температура газа в начале процесса; T 2 – термодинамическая (абсолютная) температура газа в конце процесса;
- изменение плотности
Δ ρ = ρ 1 − ρ 2 = ρ 1 ( 1 − T 1 T 2 ) ,
где ρ1 – первоначальная плотность газа; ρ2 – плотность газа в конце процесса;
- изменение количества вещества
Δ ν = ν 1 − ν 2 = ν 1 ( 1 − T 1 T 2 ) ,
где ν1 – первоначальное количество вещества (газа) в сосуде; ν2 – количество вещества (газа) в сосуде в конце процесса.
Пример 11. В открытом сосуде объемом 450 дм3 содержится некоторое количество идеального газа. Температуру газа увеличивают от 27 до 177 °С. Давление газа остается постоянным и равным 166 кПа. Сколько моль газа выйдет из сосуда?
Решение. Запишем уравнение Менделеева – Клапейрона для двух состояний газа, находящегося в открытом сосуде, при нагревании:
- для начального состояния
pV = ν1RT 1;
- для конечного состояния
pV = ν2RT 2;
где p – давление газа, p = const; V – объем газа (сосуда), V = const; ν1, ν2 – количество вещества (газа) в начале и в конце процесса; R – универсальная газовая постоянная, R = 8,31 Дж/(моль ⋅ К); T 1, T 2 – температура газа в начале и в конце процесса.
Первое уравнение позволяет получить формулу для расчета количества вещества (газа) в начале процесса:
ν 1 = p V R T 1 .
Подстановка полученной формулы в уравнение
Δ ν = ν 1 ( 1 − T 1 T 2 )
дает искомую разность
Δ ν = p V R T 1 ( 1 − T 1 T 2 ) = p V ( T 2 − T 1 ) R T 1 T 2 .
Для вычисления искомой величины необходимо перевести температуру из градусов Цельсия в кельвины:
T 1 = t 1 + 273 = 27 + 273 = 300 К,
T 2 = t 2 + 273 = 177 + 273 = 450 К.
Произведем вычисление:
Δ ν = 166 ⋅ 10 3 ⋅ 450 ⋅ 10 − 3 ( 450 − 300 ) 8,31 ⋅ 450 ⋅ 300 = 10 моль.
При нагревании из сосуда вышло 10 моль газа.
Пример 12. В баллоне при температуре 15 °С находится идеальный газ. Из баллона выходит 40 % газа, а температура при этом понижается на 8,0 °С. Во сколько раз уменьшится давление газа в баллоне?
Решение. Запишем уравнение Менделеева – Клапейрона для двух состояний газа, находящегося в открытом сосуде:
- для начального состояния
p 1V = ν1RT 1;
- для конечного состояния
p 2V = ν2RT 2;
где p 1 – давление газа в начальном состоянии; p 2 – давление газа в конечном состоянии; V – объем газа (сосуда), V = const; ν1, ν2 – количество вещества (газа) в начале и в конце процесса соответственно; R – универсальная газовая постоянная, R = 8,31 Дж/(моль ⋅ К); T 1, T 2 – температура газа в начале и в конце процесса соответственно.
Искомой величиной является отношение давлений p 1/p 2, которое определим из отношения уравнений:
p 1 V p 2 V = ν 1 R T 1 ν 2 R T 2 , т.е. p 1 p 2 = ν 1 T 1 ν 2 T 2 .
В результате процесса из баллона выходит 40 % газа, поэтому количество вещества (газа) ν2, оставшегося в баллоне, составляет 60 % от количества вещества (газа) ν1, которое было в начале процесса:
ν2 = 0,6ν1.
Для вычисления искомой величины необходимо сделать перевод температуры, заданной в градусах Цельсия, в кельвины:
T 1 = t 1 + 273 = 15 + 273 = 288 К,
T 2 = t 2 + 273 = (t 1 − Δt) + 273 = (15 − 8,0) + 273 = 280 К.
Подстановка температур и количества вещества (газа), оставшегося в баллоне, в выражение для искомой величины дает
p 1 p 2 = ν 1 T 1 0,6 ν 1 T 2 = T 1 0,6 T 2 = 288 0,6 ⋅ 280 = 1,7 .
Давление газа в баллоне понизится в 1,7 раза.
Источник
2011 год 109 вариант СЗ
В сосуде лежит кусок льда. Температура льда t1 = 0°С. Если сообщить ему количество теплоты Q = 50 кДж, то 3/4 льда растает. Какое количество теплоты q надо после этого сообщить содержимому сосуда дополнительно, чтобы весь лёд растаял и образовавшаяся вода нагрелась до температуры t2 = 20°С? Тепловыми потерями на нагрев сосуда пренебречь. (Решение)
2011 год. 01-2 вариант. С3
В бутылке объемом V = 1 л находится гелий при нормальном атмосферном давлении. Горлышко бутылки площадью S = 2 см2 заткнуто короткой пробкой, имеющей массу m = 20 г. Если бутылка лежит горизонтально, то для того, чтобы медленно вытащить из ее горлышка пробку, нужно приложить к пробке горизонтально направленную силу F = 1 Н. Бутылку поставили на стол вертикально горлышком вверх. Какое количество теплоты нужно сообщить гелию в бутылке для того, чтобы он выдавил пробку из горлышка? (Решение)
2011 год. 01-1 вариант. С3
Один моль идеального одноатомного газа переводят из состояния 1 с температурой Т1 = 300 К в состояние 2 таким образом, что в течение всего процесса давление газа возрастает прямо пропорционально его объему. В ходе этого процесса газ получает количество теплоты Q = 14958 Дж. Во сколько раз n уменьшается в результате этого процесса плотность газа? (Решение)
 2010 год. 11 вариант. С1
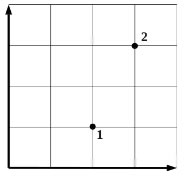
2010 год. 11 вариант. С1
В кабинете физики проводились опыты с разреженным газом постоянной массы. По невнимательности ученик, отметив на графике начальное и конечное состояния газа (см. рисунок), не указал, какие две величины из трёх (давление р, объём V, температура Т) отложены по осям. В журнале осталась запись, согласно которой названные величины изменялись следующим образом: p1 < р2, V1 > V2, Τ1 < Ί2. Пользуясь этими данными, определите, какие величины были отложены на горизонтальной и вертикальной осях. Ответ поясните, указав, какие физические закономерности вы использовали. (Решение)
 2010 год 304 вариант СЗ
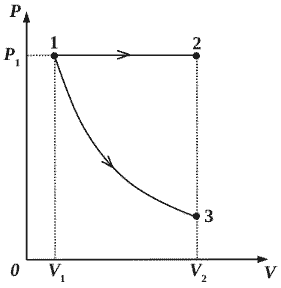
2010 год 304 вариант СЗ
Некоторое количество одноатомного идеального газа расширяется из одного и того же начального состояния (p1, V1) до одного и того же конечного объёма V2 первый раз по изобаре, а второй – по адиабате (см. рисунок). Отношение количества теплоты Q12, полученного газом на изобаре от нагревателя, к модулю изменения внутренней энергии газа |U3 – U1| на адиабате k = Q12/|U3 – U1| = 6 . Чему равно отношение х работы газа на изобаре А12 к работе газа на адиабате А13? (Решение)
 2010 год. 135 вариант. С5
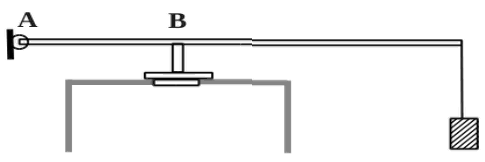
2010 год. 135 вариант. С5
В цилиндр закачивается воздух со скоростью 0,002 кг/с. В верхнем торце цилиндра есть отверстие площадью 5·10-4 м2, закрытое предохранительным клапаном. Клапан удерживается в закрытом состоянии невесомым стержнем длиной 0,5 м, который может свободно поворачиваться вокруг оси в точке А (см. рисунок). Расстояние АВ равно 0,1 м. К свободному концу стержня подвешен груз массой 2 кг. Клапан открывается через 580 с работы насоса, если в начальный момент времени давление воздуха в цилиндре было равно атмосферному. Температура воздуха в цилиндре и снаружи не меняется и равна 300 К. Определите объём цилиндра. (Решение)
2009 год. 133 вариант. С1
В цилиндрическом сосуде под поршнем длительное время находятся вода и ее пар. Поршень начинают вдвигать в сосуд. При этом температура воды и пара остается неизменной. Как будет меняться при этом масса жидкости в сосуде? Ответ поясните. (Решение)
 2009 год. 133 вариант. С3
2009 год. 133 вариант. С3
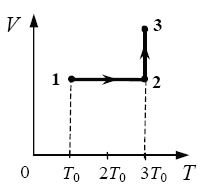
Один моль одноатомного идеального газа переходит из состояния 1 в состояние 3 в соответствии с графиком зависимости его объёма V от температуры T (T0 = 100 К). На участке 2 − 3 к газу подводят 2,5 кДж теплоты. Найдите отношение работы газа А123 ко всему количеству подведенной к газу теплоты Q123. (Решение)
 2009 год. 304 вариант. С3
2009 год. 304 вариант. С3
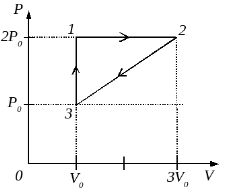
Постоянная масса одноатомного идеального газа совершает циклический процесс, показанный на рисунке. За цикл от нагревателя газ получает количество теплоты QH = 8 кДж. Какую работу совершают внешние силы при переходе газа из состояния 2 в состояние 3? (Решение) 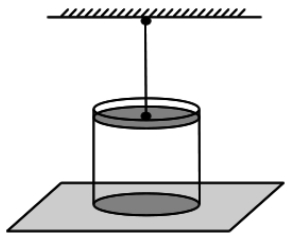 2008 год. 131 вариант. С2
2008 год. 131 вариант. С2
Разогретый сосуд прикрыли поршнем, который с помощью вертикальной нерастяжимой нити соединили с потолком. На сколько процентов от начальной понизится температура воздуха в сосуде к моменту, когда сосуд оторвется от поверхности, на которой он расположен? Масса сосуда 5 кг. Поршень может скользить по стенкам сосуда без трения. Площадь дна сосуда 125 см2. Атмосферное давление 105 Па. Тепловым расширением сосуда и поршня пренебречь. (Решение)
2008 год. 5941 вариант. С2
В калориметре находился m1 = 1 кг льда при температуре t1 = -5°С. После добавления в калориметр m2 = 25 г воды в нем установилось тепловое равновесие при температуре t = 0°С. Какова температура t2 добавленной в калориметр воды, если в калориметре оказался в итоге только лёд? Теплоёмкостью калориметра пренебречь. (Решение)
2008 год. 05205939 вариант. С2
В горизонтально расположенной трубке постоянного сечения, запаянной с одного конца, помещен столбик ртути длиной 15 см, который отделяет воздух в трубке от атмосферы. Трубку расположили вертикально запаянным концом вниз. На сколько градусов следует нагреть воздух в трубке, чтобы объём, занимаемый воздухом, стал прежним? Температура воздуха в лаборатории 300 К, а атмосферное давление составляет 750 мм рт.ст. (Решение)
 2008 год. 2 вариант. С2
2008 год. 2 вариант. С2
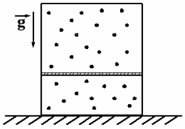
Вертикально расположенный замкнутый цилиндрический сосуд высотой 50 см разделен подвижным поршнем весом 110 Н на две части, в каждой из которых содержится одинаковое количество водорода при температуре 361 К. Какая масса газа находится в каждой части цилиндра, если поршень находится на высоте 20 см от дна сосуда? Толщиной поршня пренебречь. (Решение)
2007 год. 19 вариант. С2
В сосуде находится одноатомный идеальный газ, масса которого 12 г, а молярная масса 0,004 кг/моль. Вначале давление в сосуде было равно 4•105 Па при температуре 400 К. После охлаждения газа давление понизилось до 2•105 Па. Какое количество теплоты отдал газ? (Решение)
2006 год. 61 вариант. С2
В водонепроницаемый мешок, лежащий на дне моря на глубине 73,1 м, закачивается сверху воздух. Вода вытесняется из мешка через нижнее отверстие, и когда объём воздуха в мешке достигает 28,0 м3- мешок всплывает вместе с прикреплённым к нему грузом. Масса оболочки мешка 2710 кг. Определите массу груза. Температура воды равна 7°С, атмосферное давление на уровне моря равно 105 Па. Объёмом груза и стенок мешка пренебречь. (Решение)
2006 год. 86 вариант. С2
Теплоизолированный сосуд объемом V = 2 м3 разделен теплоизолирующей перегородкой на две равные части. В одной части сосуда находится 2 моль гелия, а в другой – такое же количество молей аргона. Начальная температура гелия равна 300 К, а температура аргона 600 К. Определите давление смеси после удаления перегородки. Теплоемкостью сосуда пренебречь. (Решение)
2006 год. 33 вариант. С2
Воздушный шар объемом 2500 м3 с массой оболочки 400 кг имеет внизу отверстие, через которое воздух в шаре нагревается горелкой. Температура окружающего воздуха 7°С, его плотность 1,2 кг/м3. При какой минимальной разности температур воздуха внутри шара и снаружи шар взлетит вместе с грузом (корзиной и воздухоплавателем) массой 200 кг? Оболочку шара считать нерастяжимой. (Решение)
 2006 год. 222 вариант. С2
2006 год. 222 вариант. С2
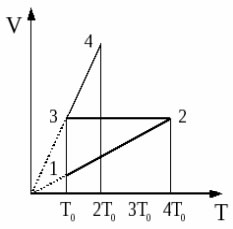
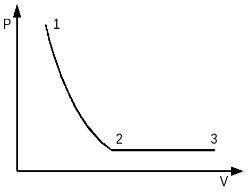
С одним молем идеального одноатомного газа совершают процесс 1-2-3-4, показанный на рисунке в координатах V-Т. Во сколько раз количество теплоты, полученное газом в процессе 1-2-3-4, больше работы газа в этом процессе? (Решение)
 2005 год. 58 вариант. С2
2005 год. 58 вариант. С2
Идеальный одноатомный газ в количестве 1 моль сначала изотермически расширился при температуре T1 = 300 К. Затем газ изобарно нагрели, повысив температуру в 3 раза. Какое количество теплоты получил газ на участке 2-3? (Решение)
 2004 год. 92 вариант. С2
2004 год. 92 вариант. С2
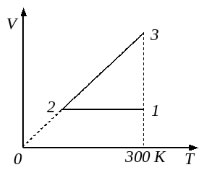
10 моль одноатомного идеального газа сначала охладили, уменьшив давление в 3 раза, а затем нагрели до первоначальной температуры 300 К (см. рисунок). Какое количество теплоты получил газ на участке 2-3? (Решение)
 2004 год. 77 вариант. С5
2004 год. 77 вариант. С5
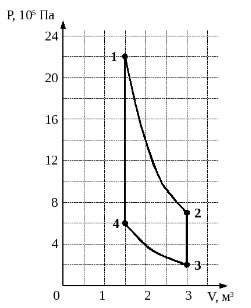
Идеальный одноатомный газ используется в качестве рабочего тела в тепловом двигателе. В ходе работы двигателя состояние газа изменяется в соответствии с циклом, состоящим из двух адиабат и двух изохор (см. рисунок). Вычислите КПД такого двигателя. (Решение)
2004 год. 49 вариант. С5
При электролизе воды образуется кислород О2 и водород Н2. Газы отводят в сосуд объёмом 100 л, поддерживая в нём температуру 300 К. Чему равна масса воды, которая разложилась в результате электролиза, чтобы суммарное давление в сосуде достигло 0,1 атм? Считать, что ничего не взрывается. (Решение)
2004 год. 35 вариант. С5
Смесь одинаковых масс гелия, водорода и азота помещена в сосуд и нагрета до температуры 350 К. Плотность смеси оказалась равной 50 г/м3. Чему равно давление в сосуде? (Решение)
Источник
Задача 8.
Скопировать ссылку на задачу
Скопировать ссылку на задачу
Задача 8.1
В результате некоторого процесса средняя кинетическая энергия поступательного теплового движения молекул идеального газа уменьшилась в 3 раза, а давление возросло в 2 раза. Во сколько раз изменилась концентрация молекул газа, если число молекул осталось неизменным?
Показать ответ
Скопировать ссылку на задачу
Задача 8.2
В сосуде находится некоторое количество идеального газа. Во сколько раз изменится температура газа, если он перейдёт из состояния 1 в состояние 2 (см. рисунок)?
Показать ответ
Скопировать ссылку на задачу
Задача 8.3
В закрытом сосуде находится идеальный газ. При некоторой температуре среднеквадратичная скорость теплового хаотического движения молекул равна 526 м/с, а давление газа равно 101450 Па. Чему равна плотность этого газа? Ответ выразите в кгм3 к г м 3 и округлите до десятых долей.
Показать ответ
Скопировать ссылку на задачу
Задача 8.4
В баллоне емкостью 20 л находится кислород при температуре 16°C под давлением 107 Па Какой объем займет этот газ при нормальных условиях? Ответ выразите в кубических метрах с точностью до сотых.
Показать ответ
Скопировать ссылку на задачу
Задача 8.5
При неизменной концентрации молекул идеального газа средняя квадратичная скорость теплового движения его молекул уменьшилась в 2 раза. Чему равно отношение конечного давления к начальному?
Показать ответ
Скопировать ссылку на задачу
Задача 8.6
В сосуде находится некоторое количество идеального газа. Он переходит из состояния 1 в состояние 2 (см. рисунок). Чему равно отношение температур T2T1?
Показать ответ
Скопировать ссылку на задачу
Задача 8.7
В сосуде постоянного объёма 16,62 л находится идеальный газ при неизменной температуре. Через маленькое отверстие в стенке сосуда газ очень медленно выпускают наружу. На графике показана зависимость давления p газа в сосуде от количества ν газа в нём. Чему равна температура газа? Ответ выразите в К.
Показать ответ
Скопировать ссылку на задачу
Задача 8.8
В результате нагревания идеального газа средняя кинетическая энергия теплового движения его молекул увеличилась в 4 раза. Во сколько раз изменилась абсолютная температура газа?
Показать ответ
Скопировать ссылку на задачу
Задача 8.9
В сосуде находится некоторое количество идеального газа. Во сколько раз изменится температура газа, если он перейдёт из состояния 1 в состояние 2 (см. рисунок)?
Показать ответ
Скопировать ссылку на задачу
Задача 8.10
Кислород и водород находятся в закрытом сосуде в состоянии термодинамического равновесия друг с другом. Во сколько раз среднеквадратичная скорость молекул водорода отличается от среднеквадратичной скорости молекул кислорода?
Показать ответ
Скопировать ссылку на задачу
Задача 8.11
На графике изображена диаграмма «объём – температура» (VT-диаграмма). Неизменное количество идеального газа переводят из состояния 1 в состояние 2 (см. рисунок). Определите, во сколько раз давление газа в состоянии 2 отличается от давления газа в состоянии 1.
Показать ответ
Скопировать ссылку на задачу
Задача 8.12
В результате некоторого процесса концентрация молекул идеального газа уменьшилась в 2 раза, а давление возросло в 4 раза. Во сколько раз изменилась средняя кинетическая энергия поступательного теплового движения молекул идеального газа, если число молекул было неизменным?
Показать ответ
Скопировать ссылку на задачу
Задача 8.13
В сосуде находится некоторое количество идеального газа. Во сколько раз изменится температура газа, если он перейдёт из состояния 1 в состояние 2 (см. рисунок)?
Показать ответ
Скопировать ссылку на задачу
Задача 8.14
Чему равно соотношение давлений в сосудах с кислородом и водородом ркрв если концентрации газов и среднеквадратичные скорости одинаковы?
Показать ответ
Скопировать ссылку на задачу
Задача 8.15
Объём 3 моль водорода в сосуде при температуре 300 К и давлении р1 равен V1 Во сколько раз отличается от него объём 3 моль кислорода при той же температуре и том же давлении?
Показать ответ
Скопировать ссылку на задачу
Задача 8.16
На графике показана зависимость давления от концентрации для двух идеальных газов при фиксированных температурах. Чему равно отношение температур T2T1 этих газов?
Показать ответ
Скопировать ссылку на задачу
Задача 8.17
При неизменной плотности одноатомного идеального газа давление этого газа увеличивают в 4 раза. Во сколько раз изменяется при этом среднеквадратичная скорость движения его атомов?
Показать ответ
Скопировать ссылку на задачу
Задача 8.18
На рисунке изображено изменение состояния постоянной массы разреженного аргона. Температура газа в состоянии 1 равна 27 °С. Какая температура соответствует состоянию 2? Ответ выразите в градусах Кельвина.
Показать ответ
Скопировать ссылку на задачу
Задача 8.19
В сосуде находится некоторое количество идеального газа. Он переходит из состояния 1 в состояние 2 (см. рисунок). Чему равно отношение объёмов V1V2?
Показать ответ
Скопировать ссылку на задачу
Задача 8.20
В закрытом сосуде находится идеальный газ при давлении 105750 Па и температуре, соответствующей среднеквадратичной скорости теплового хаотического движения молекул 494 м/с. Чему равна плотность этого газа? Ответ выразите в кг/м3 и округлите до десятых долей.
Показать ответ
Скопировать ссылку на задачу
Задача 8.21
В сосуде объёмом 1 л находится 10 г идеального газа при давлении 1 атм и температуре 300 К. Во втором сосуде объёмом 3 л находится 30 г того же газа при давлении 2 атм. Чему равна температура (в К) газа во втором сосуде?
Показать ответ
Скопировать ссылку на задачу
Задача 8.22
В результате охлаждения разреженного аргона его абсолютная температура уменьшилась в 4 раза. Во сколько раз уменьшилась при этом средняя кинетическая энергия теплового движения молекул аргона?
Показать ответ
Скопировать ссылку на задачу
Задача 8.23
При температуре T0 и давлении 40 кПа 2 моль идеального газа занимают объём V0. Каково давление 1 моль этого газа в объёме V0 при температуре 2T0? Ответ выразите в кПа.
Показать ответ
Скопировать ссылку на задачу
Задача 8.24
В ходе эксперимента давление разреженного газа в сосуде снизилось в 5 раз, а средняя энергия теплового движения его молекул уменьшилась в 2 раза. Во сколько раз уменьшилась при этом концентрация молекул газа в сосуде?
Показать ответ
Скопировать ссылку на задачу
Задача 8.25
Газообразный азот находится в сосуде объёмом 33,2 литра. Давление газа 100 кПа, его температура 127 °С. Определите массу газа в этом сосуде. Ответ выразите в граммах и округлите до целого числа.
Показать ответ
Скопировать ссылку на задачу
Задача 8.26
Конечная температура газа в некотором процессе – 373 °С. В ходе этого процесса объём идеального газа увеличился в 2 раза, а давление не изменилось. Какова была начальная абсолютная температура газа?
Показать ответ
Скопировать ссылку на задачу
Задача 8.27
Давление идеального газа при постоянной концентрации увеличилось в 2 раза. Во сколько раз изменилась его абсолютная температура?
Показать ответ
Скопировать ссылку на задачу
Задача 8.28
В сосуде объёмом 2 л находится 20 г идеального газа при давлении 2 атм и температуре 300 К. Во втором сосуде объёмом 3 л находится 30 г того же газа при температуре 450 К. Чему равно давление газа (в атм) во втором сосуде?
Показать ответ
Скопировать ссылку на задачу
Задача 8.29
На графиках приведены зависимости давления p и объёма V от времени t для 0,2 молей идеального газа. Чему равна температура газа в момент t = 30 минут? Ответ выразите в градусах Кельвина с точностью до 10 К.
Показать ответ
Скопировать ссылку на задачу
Задача 8.30
Температура порции идеального газа уменьшилась на 773 К. На сколько уменьшилась средняя энергия хаотического теплового движения одной молекулы, входящей в состав этой порции газа? Ответ выразите в электронвольтах и округлите до десятых долей.
Показать ответ
Источник
