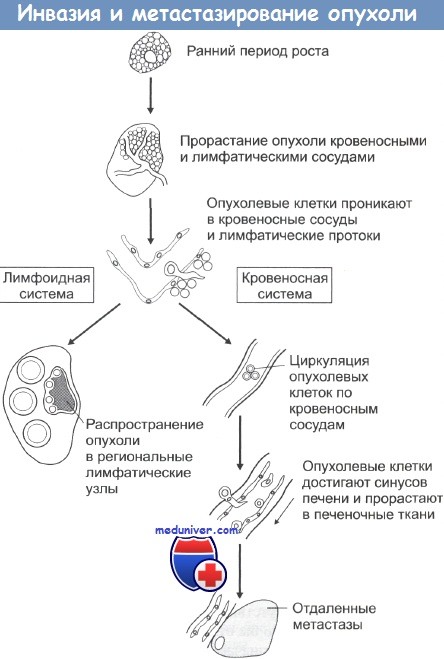
Инвазия в онкологии в сосуды
Каждый пациент на приёме у врача больше всего боится, что у него заподозрят или, что хуже, найдут новообразование. Однако мало кто знает о механизме развития опухоли и за счет чего конкретно данный диагноз является настолько страшным. В этой статье мы разберёмся, что именно делает онкологические заболевания такими опасными для жизни.
Строение тканей с точки зрения формирования опухолевого процесса
Чтобы разобраться в механизме образования и развития опухоли, необходимо иметь представление о принципе строения тканей в организме. Большинство тканей, независимо от места их расположения, имеют сходный план строения:
- Базальная мембрана — это неклеточная структура, отграничивающая ткани друг от друга;
- Ростковый слой — группа активно делящихся клеток, расположенных на базальной мембране, которые обеспечивают обновление ткани. Именно изменение генетического материала клеток росткового слоя влечёт за собой развития опухоли;
- Слой созревающих клеток — клетки ростового слоя, которые постепенно продвигаются в верхние слои в процессе дифференцировки (приобретения формы и свойств, характерных для данной ткани);
- Поверхностный слой — группа клеток, которая и обеспечивает выполнение тканью определённой функции.
Между ростковым и поверхностным могут располагаться дополнительные слои в зависимости от конкретного вида ткани. Но принцип строения всегда один и тот же: клетки, способные делиться, находятся на базальной мембране. В процессе созревания они перемещаются в верхние слои, утрачивая способность к делению и приобретая специфические свойства.
Доброкачественные и злокачественные опухоли: в чем разница?
Исходя из того, клетки какого слоя подверглись мутации, выделяют два типа неоплазий — доброкачественные и злокачественные. Их отличия заключаются в том, что первый тип формируется из высоко дифференцированных клеток созревающего слоя. При доброкачественных опухолях клетки не будут сильно отличаться от здоровых клеток данной ткани. Такая неоплазия считается неагрессивной и растет медленно, а также не даёт метастазы. Патогенное действие доброкачественного новообразования заключается главным образом в сдавлении окружающих её тканей. Иногда такие опухоли полностью или частично закрывают просвет какого-либо полого органа.
Злокачественные новообразования возникают из-за мутаций клеток низкодифференцированного росткового слоя. Опухолевый рост происходит стремительно, из-за чего новообразование нуждается в активном питании. Эта потребность удовлетворяется за счет собственных ресурсов организма: новообразование обкрадывает своего носителя. Именно злокачественные неоплазии принято называть «раком». К доброкачественным образованиям этот термин не относится. При злокачественных опухолях происходит инвазия раковых клеток.
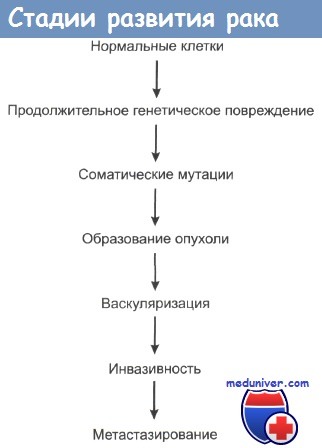
В процессе развития рака выделяют 4 стадии:
- Стадия предопухоли. В этот период наблюдается изменение клеток росткового слоя: они могут увеличиваться в размерах и приобретать нетипичные формы.
- Стадия неинвазивной опухоли. Ещё одно название этой стадии — «рак на месте» (или «рак in situ»). Клетки росткового слоя всё также созревают и продвигаются наверх, хотя теперь их структура и свойства изменены. Поэтому в стадии неинвазивной опухоли мы будем видеть изменения не только в самом глубоком слое.
- Стадия инвазивного роста — прорастание через базальную мембрану.
- Стадия метастазирования.

Что такое инвазия опухоли?
Данный термин происходит от латинского слова «invasio», что переводится как «нашествие» или «нападение». Инвазия — это процесс распространения раковых клеток посредством прорастания опухоли через базальную мембрану.
Инвазия обуславливает способность опухолей давать метастазы — вторичные очаги онкологического процесса вдали от материнской опухоли, возникшие из-за миграции раковых клеток. Обязательное условие метастазирования — наличие у опухоли собственной капиллярной сети. Она формируется, когда количество неопластических клеток достигает 103 (1-2 мм).
Этапы инвазии:
- Разрыв межклеточных связей, соединяющих раковые клетки между собой;
- Прикрепление клеток опухоли к базальной мембране;
- Разрушение базальной мембраны лизирующими (расщепляющими) ферментами;
- Миграция клеток в соседние ткани и органы.
Раковые клетки, находящиеся в процессе инвазии, более устойчивы к облучению и химеотерапии, чем стационарные. Во многом это связано с временной утратой мигрирующими клетками способности к делению. Также движущиеся опухолевые клетки проявляют повышенную активность антиапоптотических генов (гены, препятствующие запрограммированной смерти клетки — апоптозу). И, поскольку химиотерапевтические препараты направлены на стимуляцию апопоза, их устойчивость к лечению возрастает.
Инвазивный рост опухоли не только способствует её распространению по всему организму, но и обеспечивает раковым клеткам интенсивное питание. Поэтому можно сказать, что инвазия является фактором «укоренения» новообразования.
Факторы, определяющие степень инвазивности опухоли
Чтобы злокачественная опухоль проросла сквозь базальную мембрану, необходимо наличие следующих факторов:
- Быстрое деление и давление. Механическое воздействие опухолевой массы на базальную мембрану способствует её разрушению и, как следствие, инвазии раковых клеток;
- Подвижность клеток. Клетки новообразования способны к миграции, причем их движение не является хаотичным. Они движутся в направлении большей концентрации кислорода, питательных веществ, а также в сторону более нейтрального показателя кислотности (рН);
- Межклеточные связи. Чем прочнее эти контакты, тем меньше шансов, что опухоль начнет инвазивный рост. У злокачественных клеток связи слабые, поэтому клетки легко отрываются от новообразования и попадают в кровоток или в лимфатическую систему;
- Действие лизосомальных ферментов. Злокачественная опухоль вырабатывает вещества, способные разрушать здоровые клетки и межклеточное вещество, что будет способствовать инвазии;
- Иммунная система человека. В организме существует собственная противоопухолевая защита, которую обеспечивает наш иммунитет. Её активность у каждого человека индивидуальна. Она зависит от генетической предрасположенности и состояния всего организма в конкретный момент. Так, при заболеваниях, сопровождающихся угнетением иммунной системы (например, при ВИЧ), пациенты могут погибать от онкологических заболеваний, возникших из-за отсутствия противоопухолевой активности.
Инвазия раковых клеток в сосуды
Вслед за прорастанием в базальную мембрану наступает интравазальная (внутрисосудистая) инвазия опухоли. Чаще раковые клетки мигрируют в артерии. Это связано с тем, что стенки артерий более упругие и эластичные, в то время как у вен они тонкие и легко спадаются в опухолях. Однако раковые клетки могут быть занесены в вены из лимфатических сосудов.

Способствует интравазации также «неполноценность» сосудов, снабжающих злокачественное новообразование. Их базальная мембрана имеет щели, дефекты и истончения, что позволяет раковым клеткам с лёгкостью ее преодолеть. Такая структура обусловлена снижением продукции компонентов базальной мембраны или повышенной активностью разрушающих ее протеаз.
Циркуляция раковых клеток в системе кровотока и экстравазация
При попадании в кровоток опухолевая клетка покрывается фибрином и тромбоцитами, формируя микротромбоэмбол с опухолевой «сердцевиной». Не все они переживают движение в кровяном русле. Разрушение раковых клеток может быть обусловлено иммунными механизмами, а также турбулентностью кровяного потока и механическим повреждением во время циркуляции. Но около 80% деформированных клеток всё-таки сохраняют способность к размножению.
Экстарвазация представляет собой выход опухолевых клеток из сосудов для формирования метастатического очага. В этом процессе задействованы те же ферменты, что и в инвазии через базальную мембрану.
Резюме
Вот что следует знать об инвазии опухолей:
- Инвазия — это проникновение раковых клеток через базальную мембрану ткани, из которой развилась опухоль;
- Инвазия свойственна только злокачественным новообразованиям;
- В инвазии участвуют лизирующие ферменты, которые способны разрушать как неклеточные структуры, так и связи между здоровыми клетками (например, выстилка сосудов);
- Явление инвазии лежит в основе метастазирования;
- Инвазия бывает индивидуальной и групповой, и последняя чаще обуславливает появление метастазов,
- Самые распространенные виды инвазивных опухолей — рак шейки матки и рак молочной железы.
Источник
Инвазия, ангиогенез и метастазирование опухолевых клеток – ракаМожно сказать, что раковые клетки в определенной степени не реагируют на механизмы, контролирующие рост и развитие нормальной ткани. При пролиферации нормальной ткани непосредственный контакт клетки со своими соседями обычно служит сигналом к прекращению размножения. Это контактное торможение отсутствует в опухолевых тканях. При подкожном введении раковых клеток иммунодефицитным мышам происходит рост и развитие опухоли, что никогда не случается при введении здоровых клеток. Раковые клетки отличаются от здоровых по составу мембранных гликопротеинов, по микропотенциалам на клеточной мембране, а также характеризуются повышенным содержанием сиаловой кислоты. Локомоторный клеточный аппарат (микротрубочки и микрофиламенты) раковых клеток деградирует, клетка теряет присущие ей формы, отмечается миграция цитоплазмы раковой клетки в зону контакта со здоровыми клетками. Одновременно раковые клетки становятся локально инвазивными, хотя биохимические основы этого свойства до сих пор четко не выявлены. Опухолевые клетки часто демонстрируют пониженную адгезивность в сравнении с нормальными клетками. Важным моментом механизма инвазии является секреция определенных ферментов. Некоторые ферменты играют ключевую роль в протеолизе внутриклеточного матрикса, который всегда сопровождает инвазию раковых клеток. К таким ферментам относится семейство матричных металлопротеиназ (ММП), которое включает в себя колллагеназы, желатиназы и стромолизины. Эти ферменты экскретируются в неактивной форме. Последующий разрыв сульфгидрильной группы и присоединение атома металла (чаще всего цинка) приводят к изменению конформации фермента и переводят его в активное состояние. Тканевые ингибиторы металлопротеиназ (ТИМП) прекращают действие этих ферментов. Некоторые типы тканей изначально обладают повышенной устойчивостью к инвазии. Это, например, компактная костная ткань, ткани крупных сосудов и хрящевая ткань. Предположительно способность к инвазии у опухолевых клеток появляется в результате трансформации нормальных процессов реконструкции и восстановления здоровых тканей. Тем не менее к настоящему моменту неизвестно, какие конкретно изменения генетической структуры раковых клеток ответственны за инвазивный рост. По мере роста опухоли она выделяет в кровь ангиогенные факторы, которые стимулируют прорастание опухоли кровеносными сосудами и формирование сети капилляров. Сосудистая система кровоснабжения опухоли может стать мишенью для различных видов противораковой терапии. Опухоль стимулирует пролиферацию эндотелиальных клеток, выделяя ангиогенные цитокины, такие как эндотелиальный фактор роста сосудов (ЭФРС), ТФР и факторы роста фибробластов. Эндотелиальные же клетки в свою очередь могут стимулировать рост клеток опухоли. В одном грамме опухолевой ткани может находиться до 10-20 млн эндотелиальных клеток, которые не являются неопластическими.
Антигены нормальных эндотелиальных клеток, включая и профакторы свертываемости крови, могут быть разрегулированы в активно пролиферирующей под действием опухоли эндотелиальной ткани. В дополнение к действию цитокинов, гипоксия, развивающаяся в сети опухолевого кровоснабжения, может стимулировать выбросы ЭФРС и других факторов. В ходе ангиогенеза эндотелиальные клетки внедряются в строму опухоли, активно делятся там с образованием зачатков новых капилляров, которые затем развиваются в сосудистую систему опухоли. Как и в случае инвазии опухолевых клеток, этот процесс идет с участием продуцируемых эндотелием ММП и их естественных ингибиторов. При локальной инвазии рака опухолевые клетки могут попадать в сосудистую систему и давать начало метастазам. Последовательность событий при метастазировании показана на рисунке. Распространение раковых клеток по лимфатической системе, что особенно характерно при карциномах, происходит при попадании опухолевых клеток в лимфатические протоки с последующим оседанием их в местах разветвления протоков и в ближайших лимфатических узлах. Вслед за этим обычно происходит инфильтрация опухолевыми клетками и отдаленных лимфоузлов. Распространение через кровяное русло проходит при проникновении раковых клеток в кровеносные сосуды рядом с местом первичной локализации опухоли либо через грудные протоки. Подхваченные током крови раковые клетки затем захватываются ближайшими капиллярными сетями, чаще всего сетями печени и легких, и оседают в них. При оценке направлений метастазирования очень важно учитывать первичную локализацию опухоли. Например, опухоли пищеварительного тракта обычно метастазируют через воротную вену в печень. Опухоли также могут метастазировать непосредственно сквозь прилегающие ткани. Так возникающие в брюшной полости новообразования могут очень быстро рассеяться по всему внутрибрюшинному пространству, а клетки рака легкого могут мигрировать через плевру. Некоторые опухоли метастазируют в определенные органы и ткани, другие — бессистемно. Саркомы, например, почти всегда метастазируют в легкие, рак молочной железы поражает также ткани осевого скелета. Тем не менее биологических механизмов, объясняющих такую избирательность, пока не найдено. Региональные лимфоузлы могут осуществлять барьерную функцию, предотвращая распространение метастазов за пределы области первичной локализации опухоли. До сих пор четко не выяснено, каким образом и за счет каких специфических иммунных механизмов лимфатические узлы создают барьер на пути распространения опухоли.
Проникая в кровеносное русло в районе первичной опухоли, раковые клетки затем могут достигать других органов и тканей. Для того чтобы дать начало новым очагам опухоли, эти клетки на новом месте должны, во-первых, проникнуть в ткани через эндотелий капилляров, а во-вторых, выжить при атаках местных иммунных систем защиты, таких как фагоцитирующие клетки и так называемые естественные киллеры (ЕК). Способность к инвазированию и расселению в отдаленных органах и тканях у различных видов опухолей сильно варьирует. Эта способность, по-видимому, определяется степенью экспрессии того участка генома, который и обусловливает злокачественный рост клеток. Действительно, со временем почти все раковые опухоли накапливают все больше и больше генетических изменений в своих клетках и приобретают способности к инвазии и метастазированию. Но даже при клиническом обнаружении опухоли метастазы и инвазия могут проявиться лишь спустя несколько лет. Типичным примером является карцинома низкой степени злокачественности. Следует отметить, что даже однотипные виды рака с одинаковой степенью дифференцированности опухолевых клеток по-разному метастазируют у разных больных. Все это говорит о необходимости поиска молекулярных маркеров, которые смогли бы предсказывать исход течения онкологического заболевания более точно, чем диагностика по гистологическому типу опухоли (хотя последний метод в настоящее время является наиболее точным из всех возможных). Кроме того, даже конкретная опухоль может быть в значительной степени гетерогенной и состоять из клеток, различных по своему метастатическому потенциалу, что было показано на клонированных субпопуляциях, выделенных из одной опухоли. Биологические причины такой вариабельности в настоящее время неизвестны. Совершенно ясно, что для успешного лечения онкологических пациентов необходимо проводить масштабные исследования в области нахождения механизмов тканевой инвазии, метастатического роста и поиска биологических причин гетерогенности опухолей. Отсутствие гомогенности в опухолях, сходство опухолевых клеток со здоровыми клетками породившей ее ткани, и отсутствие четкого единичного критерия, по которому можно было бы отличить раковую клетку от здоровой, — все это вместе означает, что наши рассуждения о противоопухолевом иммунитете или о механизмах действия лекарственных цитостатических препаратов должны приниматься с изрядной долей скептицизма, особенно если они базируются на экспериментах с гомогенными опухолевыми культурами. – Также рекомендуем “Иммунный ответ на опухолевые клетки – рак” Оглавление темы “Механизмы роста и развития рака”:
|
Источник
Диагностика инвазии сосудов средостения опухолью на рентгене, КТ, МРТ
а) Определение:
• Наличие опухоли или опух:олевых клеток в стенке кровеносных сосудов или в их просвете:
о Сосуды легких:
– Легочные артерии и вены
о Сосуды большого круга кровообращения:
– Полые вены
– Непарная/полунепарнаявены
– Аорта
– Крупные артерии: плечеголовной ствол, левая общая сонная, левая подключичная и позвоночные
• Типы инвазии сосудов:
о Микроскопическая:
– Выявляется при гистологическом исследовании
о Макроскопическая:
– Обнаруживается при КТ, МРТ или ангиографии:
Дефект наполнения в просвете сосуда, являющийся продолжением опухоли
Циркулярный рост опухоли и стенозирование просвета сосуда
Облитерация просвета сосуда опухолью
б) Лучевые признаки:
1. Основные особенности инвазии сосудов средостения:
• Оптимальный диагностический ориентир:
о Контрастирующийся дефект наполнения в просвете сосуда:
– Является продолжением объемного образования, расположенного в легких, средостении или пищеводе
• Локализация:
о Поражение легочных и полых вен наблюдается чаще, чем легочных артерий и артерий большого круга кровообращения
• Размер:
о Микроскопический:
– Выявляется при гистологическом исследовании
– Дифференцирование с инвазией лимфатических сосудов затруднено
о Макроскопический:
– Различная протяженность поражения
– Инвазия сосудов выявляется при хирургическом вмешательстве или патологоанатомическом исследовании
• Морфологические особенности:
о Дефект наполнения в просвете сосуда, являющийся продолжением опухоли
о Циркулярный рост опухоли и стенозирование просвета сосуда о Облитерация просвета сосуда опухолью
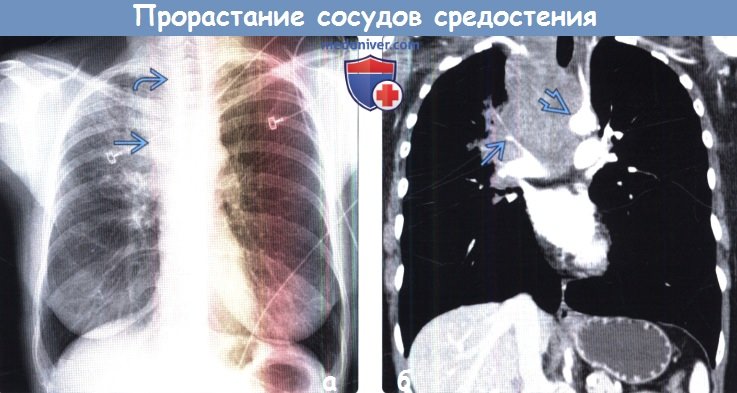
(а) Женщина 52 лет с жалобами на одышку, хрипы и отечность лица в течение трех недель. При рентгенографии органов грудной клетки в ПП проекции в верхней доле правого легкого определяется участок консолидации гетерогенной структуры. Также в правой паратрахеальной области выявляется объемное образование, распространяющееся на область шеи
(б) У этой же пациентки при КТ с контрастным усилением на реконструкции в коронарной плоскости в средостении визуализируется крупное инфильтративное объемное образование, которое циркулярно прорастает задние отделы дуги аорты правую легочную артерию и ее ветви. КТ с контрастным усилением является методом выбора для оценки инвазии сосудов опухолью.
2. Рентгенография инвазии сосудов средостения:
о Объемное образование в легких или средостении центральной локализации:
– Расположено в корне легкого или в прикорневой зоне
– Прилежит к центральным отделам легочных сосудов
– Примыкает к сердцу, средостению или крупным сосудам
о При рентгенографии оценить инвазию сосудов не представляется возможным
3. КТ инвазии сосудов средостения:
• Нативная КТ:
о Без контрастного усиления оценка поражения затруднена
о Объемное образование, примыкающее к сосудам
о Прилежащие к опухоли сосуды расширены
о Коллатеральные сосуды при обструкции верхней полой вены
• КТ с контрастным усилением:
о Оптимальный метод для оценки сосудов:
– Для исследования определенных сосудов следует выбирать соответствующий интервал введения контрастного вещества
– Выявление границы между сосудами и прилежащей опухолью
о Инвазия сосудов:
– Дефект наполнения в просвете сосуда, являющийся продолжением опухоли:
Может накапливать контрастное вещество
– Циркулярный рост опухоли и стенозирование просвета сосуда
– Облитерация просвета сосуда опухолью
о Распространение в грудную полость злокачественной опухоли органов брюшной полости:
– Следует заподозрить при наличии в правом предсердии дефекта наполнения
– Печеночноклеточный, почечноклеточный рак и адренокор-тикальная карцинома
о Косвенные признаки:
– Визуализация коллатеральных сосудов грудной клетки и средостения при обструкции верхней полой вены
– Контакт опухоли с аортой на протяжении >90° ее окружности (угол Пикуса) и отсутствие периаортальной жировой клетчатки свидетельствуют в пользу инвазии
о Осложнения:
– Опухолевые эмболы:
Чередование расширенных и суженных участков в легочной артерии в виде бус
– Псевдоаневризма легочной артерии
4. МРТ инвазии сосудов средостения:
• Т1ВИ с контрастным усилением:
о Дефект наполнения в просвете сосуда лучше визуализируется при контрастном усилении:
– Отличить опухолевый тромб от неопухолевого можно в отсроченную фазу исследования
• Кино-режим SSFP:
о Позволяет обнаруживать дефект наполнения в просвете сосуда без контрастного усиления:
– Не позволяет оценить особенности контрастирования образования
• Отсроченная фаза контрастирования:
о Опухоль может контрастироваться спустя некоторое время после введения контрастного вещества
– Позволяет отличить опухолевый тромб от неопухолевого
5. Ангиография инвазии сосудов средостения:
• Дефект наполнения в просвете сосуда
• Сдавление сосуда извне опухолью, стенозирование его просвета
• Симптоматическое лечение: стентирование верхней полой вены при ее обструкции
6. Рекомендации к проведению лучевых исследований:
• Оптимальный метод лучевой диагностики:
о КТ с контрастным усилением: метод выбора для выявления инвазии сосудов
о МРТ: может выполняться при наличии противопоказаний к внутривенному введению контрастного вещества
• Рекомендации по выбору протокола:
о КТ: исследование в отсроченную фазу позволяет исключить артефакт смешивания в качестве этиологии дефекта наполнения в просвете сосуда
о МРТ: субтракция позволяет лучше выявлять особенности контрастирования опухоли
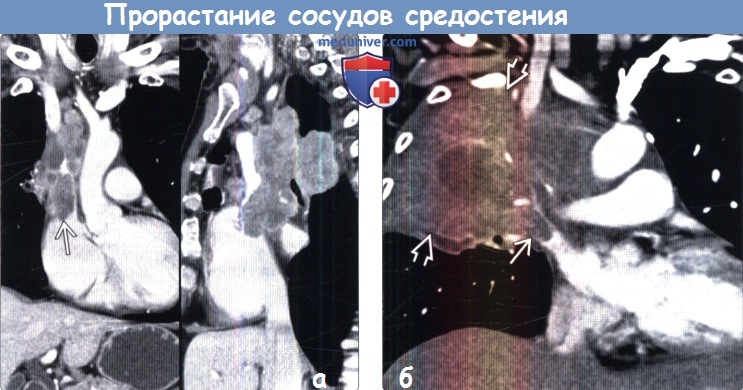
(а) При КТ с контрастным усилением на реконструкциях в коронарной (слева) и сагиттальной (справа) плоскостях в верхней доле правого легкого определяется образование гетерогенной структуры с дольчатым контуром. Отмечается инвазия верхней полой вены, приводящая к сужению ее просвета. Данная картина соответствует стадии Т4.
(б) Пациент, страдающий раком легких. При КТ с контрастным усилением на реконструкции в коронарной плоскости в верхней доле правого легкого визуализируется крупное новообразование гетерогенной структуры, накапливающее контрастное вещество. Выявляется инвазия средостения и циркулярный охват сосудов. Следует отметить наличие в правой верхней легочной вене контрастирующегося дефекта наполнения, являющегося продолжением опухоли, что служит признаком инвазии сосуда.
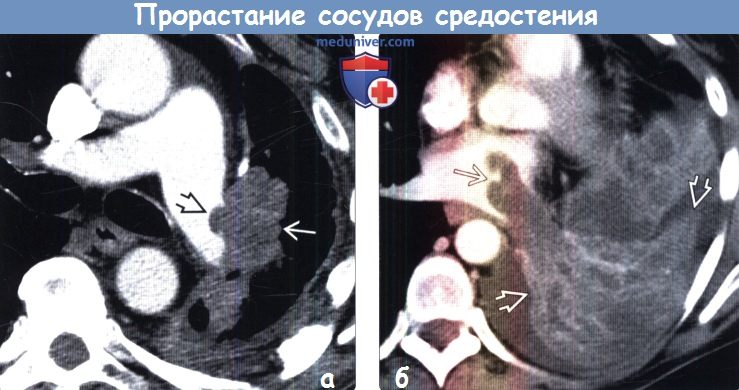
(а) Пациент с распространенным раком легких. При КТ с контрастным усилением в прикорневой зоне левого легкого определяется мягкотканное объемное образование, продолжением которого является дефект наполнения с дольчатым контуром в левой легочной артерии. Следует отметить наличие небольшого левостороннего плеврального выпота.
(б) Пациент, страдающий раком нижней доли левого легкого. При КТ с контрастным усилением в левом легком визуализируется крупное новообразование гетерогенной структуры, прорастающее левое предсердие через левую нижнюю легочную вену: дефект наполнения в левом предсердии является продолжением крупной опухоли легкого. Следует отметить наличие небольшого левостороннего плеврального выпота.
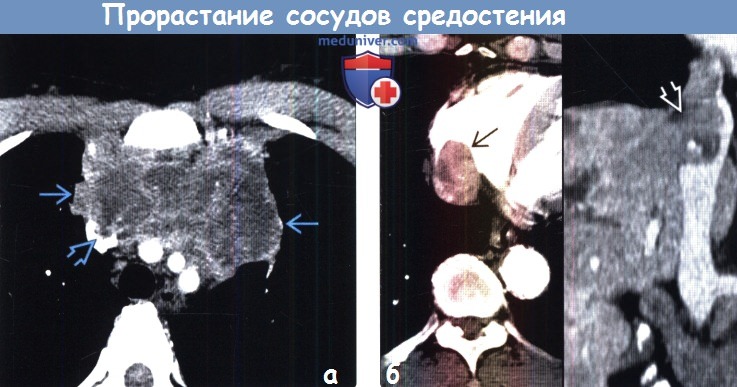
(а) Женщина 44 лет с первичной В-крупноклеточной лимфомой средостения. При КТ с контрастным усилением в преваскулярном отделе средостения определяется крупное объемное образование, гетерогенно накапливающее контрастное вещество. Продолжением образования является дефект наполнения в просвете верхней полой вены, что соответствует прямой инвазии.
(б) На совмещенных изображениях при КТ с контрастным усилением в аксиальной (слева) и коронарной (справа) плоскостях в полости правого предсердия и нижней полой вене визуализируется контрастирующееся образование, которое является продолжением гепа-тоцеллюлярной карциномы, растущей по печеночным венам.
в) Дифференциальная диагностика:
1. Дефект наполнения в просвете сосуда:
• Артефакт смешивания контрастного вещества:
о Дефект наполнения в просвете вен или артерий
о В отсроченную фазу не визуализируется
• Тромб:
о Неконтрастирующийся дефект наполнения в просвете сосуда
о При наличии злокачественной опухоли существует высокий риск развития тромбоэмболии легочной артерии
• Саркома легочной артерии:
о Дефект наполнения в просвете легочной артерии
о Антикоагуляционная терапия неэффективна
о Может контрастироваться
• Саркома аорты
2. Циркулярный рост опухоли вокруг сосуда:
• Ангиоинвазивная грибковая инфекция:
о Может выявляться консолидация легочной ткани, напоминающая объемное образование
• Медиастинальный фиброз:
о В структуре могут выявляться кальцификаты
о Циркулярный рост, обструкция сосудов
– Легочные артерии и вены
– Верхняя полая вена
г) Патоморфология:
1. Основные особенности:
• Этиология:
о Объемное образование в легкихя:
– Рак легких
– Метастаз
о Объемное образование в средостении:
– Лимфома
– Метастаз
– Эпителиальная опухоль тимуса
– Рак щитовидной железы
– Рак пищевода
• Генетические особенности:
о Рак легких:
– Существует корреляция между микроскопической инвазией лимфатических и кровеносных сосудов и следующими особенностями:
Амплификация гена KRAS и его мутация
Размер опухоль и стадия
• Сопутствующие патологические изменения:
о Инвазия лимфатических сосудов:
– Дифференцирование кровеносных и лимфатических сосудов затруднено
2. Стадирование, определение степени дифференцировки и классификация опухолей:
• Рак легких:
о Т4:
– Макроскопическая инвазия:
Интраперикардиальные отделы легочных артерий, вен
Интраперикардиальные/экстраперикардиальные отделы полых вен, аорты
• Эпителиальная опухоль тимуса:
о Циркулярный рост опухоли вокруг сосуда позволяет заподозрить его инвазию
– Согласно классификации Масаока-Кога инвазия сосуда соответствует распространенной стадии опухоли
3. Макроскопические патоморфологические и хирургические особенности:
• Опухолевые клетки в просвете сосуда
д) Клинические аспекты инфазии сосудов средостения:
1. Проявления:
• Наиболее частые признаки:
о Постепенное нарастание тяжести симптомов
о Одышка и кашель
о Симптомы могут отсутствовать
• Другие симптомы:
о Синдром верхней полой вены:
– Отечность лица, шеи и верхней половины тела + цианоз
– В редких случаях охриплость, боли в груди, дисфагия и гемофтиз
о Дисфагия обусловлена распространенным раком пищевода
2. Естественное течение заболевания и прогноз:
• Рак легких:
о Прогностическая значимость микроскопической инвазии сосудов опухолью I стадии не установлена
• Эпителиальная опухоль тимуса:
о При наличии в переднем средостении объемного образования, инвазирующего сосуды, следует заподозрить рак тимуса
3. Лечение инвазии сосудов средостения:
• Варианты, риски, осложнения:
о В некоторых случаях при раке легких выполняется резекция инвазированных сосудов:
– Инвазия крупных сосудов обычно является противопоказанием к выполнению резекции
– Резекция верхней полой вены; является одним из наиболее распространенных расширенных хирургических вмешательств на сосудах при опухоли на стадии Т4
е) Диагностические пункты инвазии сосудов средостения:
1. Следует учитывать:
• При наличии в просвете сосуда дефекта наполнения, являющегося продолжением объемного образования легких/средостения, либо при выявлении циркулярного охвата, окклюзии или облитерации сосуда следует заподозрить его инвазию
• При наличии в сосуде контрастирующегося дефекта наполнения и отсутствии за пределами сосуда объемного образования следует заподозрить первичную злокачественную опухоль сосуда
2. Ключевые моменты при интерпретации изображений:
• При макроскопической инвазии легочной артерии следует исключить наличие опухолевых эмболов и псевдоаневризм
• Дефект наполнения в правом предсердии может являться результатом распространения злокачественной опухоли органов брюшной полости через нижнюю полую вену:
о Печеночноклеточный, почечноклеточный рак и адренокортикальная карцинома
3. Ключевые моменты диагностического заключения:
• В заключении следует отразить наличие циркулярного охвата верхней полой вены, поскольку оно потенциально может привести к ее обструкции
ж) Список литературы:
1. Mollberg NM et al: Lymphovascular invasion as a prognostic indicator in stage I non-small cell lung cancer: a systematic review and meta-analysis. Ann Thorac Surg. 97(3) 965-71, 2014
2. Detterbeck FC et al: The stage classification of lung cancer: Diagnosis and management of lung cancer, 3rd ed: American College of Chest Physicians evidence-based clinical practice guidelines. Chest. 143(5 Suppl): e191S-210S, 2013
3. Benveniste MF et al: Role of imaging in the diagnosis, staging, and treatment of thymoma. Radiographics. 31 (7): 1847-61; discussion 1861-3, 2011
4. DiPerna CA et al.: Surgical management of T3 and T4 lung cancer. Clin Cancer Res. 11(13 Pt 2):5038s-5044s, 2005
– Также рекомендуем “Саркома аорты на КТ, МРТ”
Редактор: Искандер Милевски. Дата публикации: 13.2.2019
Оглавление темы “Лучевая диагностика опухоли сердца.”:
- Диагностика метастаза в сердце и перикард на рентгене, КТ, МРТ, ПЭТ
- Прорастание сосудов средостения опухолью на рентгенограмме, КТ, МРТ
- Диагностика инвазии сосудов средостения опухолью на рентгене, КТ, МРТ
- Саркома аорты на КТ, МРТ
- Диагностика саркомы аорты на КТ, МРТ
- Саркома легочной артерии на КТ, МРТ
- Диагностика саркомы легочной артерии на рентгене, КТ, МРТ
Источник