Эмболия сосудов системы воротной вены
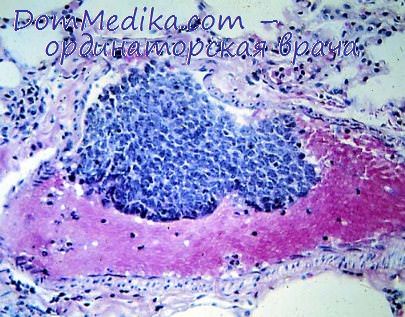
Эмболы
закрывают просвет легочных артерий. В
легочные артерии инородные частицы
поступают из венозных сосудов большого
круга кровообращения и правой половины
сердца. Последствия зависят от состава,
размеров эмболов, их общей массы. Особенно
опасна множественная эмболия мелких
легочных артерий. Нарушается кровоток.
Повышается давление крови в сосудах
малого круга кровообращения, поступление
крови в левое предсердие и желудочек
ограничено, уменьшается ударный и
минутный объемы сердца, резко снижается
артериальное давление. Гипотензия –
характерный признак массивной эмболии
сосудов малого круга кровообращения.
Снижение артериального давления
негативно сказывается на функциональной
активности самого сердца вследствие
гипоксии миокарда. Падение артериального
давления сочетается со значительным
повышением системного венозного давления
с развитием острой правожелудочковой
недостаточности (синдром острого
легочного сердца).
Эмболия
легочных сосудов сопровождается
изменениями газового состава крови.
Возникает одышка как рефлекторная
реакция на раздражение хеморецепторов
рефлексогенных зон большого круга
кровообращения и как реакция с рецепторных
полей системы малого круга кровообращения.
Одышка способствует усилению оксигенации
крови и освобождению ее от СО2.
Эмболия большого круга кровообращения.
Эмболы
поступают в сосуды большого круга
кровообращения различными путями. Один
из них – прохождение пузырьков воздуха
через легочную сеть капилляров. Они
вытягиваются, принимают форму сосуда
и из малого круга кровообращения
поступают в большой. Аналогичным путем
в ток крови большого круга кровообращения
могут проникать капли жира. Поражения
левой половины сердца, его клапанного
аппарата способны порождать тромбоэмболию,
тканевую эмболию. Образование тромбов
в артериях большого круга кровообращения,
возникающих у животных после внедрения
личинок паразитов, служит причиной
тромбоэмболии. Артерии большого круга
кровообращения могут быть местом
локализации опухолевых клеток.
Наиболее
часто эмболии подвергаются брыжеечные
артерии, артерии почек, селезенки,
головного мозга, сердечной мышцы.
Эмболия воротной вены.
В
портальную систему печени эмболы
поступают из большого числа венозных
сосудов органов брюшной полости.
Закупорка воротной вены эмболами
сопровождается тяжелыми расстройствами
гемоциркуляции. Возникает портальная
гипертония с венозной гиперемией органов
брюшной полости – желудка, тонкого и
толстого кишечника, почек, селезенки.
Это вызывает нарушение пищеварения и
основных функций печени – белково – и
желчеобразовательной, дезинтоксикационной.
Венозная гиперемия органов брюшной
полости, повышение гидродинамического
давления в венах и снижение онкотического
давления сопровождаются выходом
транссудата в брюшную полость, развитием
асцита. Портальная гипертензия
характеризуется общими расстройствами
кровообращения: ограничивается приток
крови к полостям сердца, снижаются
ударный и минутный объемы выбрасываемой
крови, артериальное давление. Рефлекторно
в ответ на гипоксемию и гиперкапнию
развивается одышка, за которой в тяжелых
случаях следует остановка дыхания.
Тяжесть
состояния больного определяется тем,
что русло воротной вены способно вместить
до 90 % объема циркулирующей крови и
неспособностью оставшейся части
обеспечить нормальное кровоснабжение
животного организма.
Последствия
эмболии различного происхождения
зависят от:
–
функциональной значимости органа, в
котором произошла закупорка сосудов,
для жизнедеятельности организма. Эмболия
венечных, мозговых, брыжеечных, легочных
артерий может привести к быстрому
летальному исходу, чего не наблюдается
при эмболии сосудов поперечнополосатых
мышц, костной, некоторых других тканей;
состава инородных частиц. Воздух
сравнительно легко рассасывается, жир
эмульгируется и омыляется, клетки
опухолей формируют метастазы, гнойные
тельца провоцируют образование нового
очага воспаления, инородные предметы
инкапсулируются и т.д;
–
величины эмбола. Чем она больше, тем
более крупный сосуд будет закупорен;
–
рефлекторного спазма близлежащих и
отдаленных сосудов, провоцирующего
системную патологию;
–
развитости анастомозов в области
закупоренного сосуда. Чем их больше,
тем быстрее будет восстановлено
кровообращение по коллатералям.
Источник
Эмболия воротной вены встречается значительно реже, чем эмболия малого и большого кругов кровообращения. Вместе с тем она может приводить к весьма тяжелым расстройствам кровообращения. При полной закупорке эмболом воротной вены или основных ее ветвей развивается портальная гипертензия, сопровождающаяся венозным застоем в органах брюшной полости и асцитом. Отток крови из портальной системы в полые вены может осуществляться через вены передней брюшной стенки и пищевода, которые в этих условиях значительно расширяются.
В развитии асцита при закупорке воротной вены имеют значение не только увеличение в ней гидродинамического давления, но и ряд других факторов. Среди них — увеличение выработки альдостерона (вторичный альдостеронизм), задержка натрия в тканях и их гиперосмия вследствие уменьшения объема циркулирующей крови, гипопротеинемия и гипоонкия крови в результате повреждения печеночных клеток, повышение проницаемости мембран капилляров портального русла вследствие действия гипоксии и другие факторы.
При эмболии воротной вены существенные расстройства возникают в сфере центрального кровообращения. Именно они чаще всего являются причиной гибели больных. Уменьшение возврата крови к сердцу (а в портальной системе может депонироваться до 90 % всей циркулирующей крови) приводит к сердечной недостаточности. Ослабление сердечной деятельности, снижение объема циркулирующей крови и сосудистая недостаточность определяют тяжесть состояния больных при эмболии воротной вены.

Тромбообразование
Процесс тромбообразования — физиологическое явление, без которого существование животного мира невозможно. В здоровом организме животных и человека кровеносные сосуды постоянно подвергаются травматизации в результате растяжения тканей, перепадов гидродинамического давления, мелких травм, физиологической гипоксии и ишемии и многих других причин. В таких случаях в результате местной активации системы гемостаза образуются гемостатические тромбы, которые не только закрывают место повреждения, но и стимулируют регенеративный процесс в эндотелиальной сети, восстанавливая целостность стенки сосуда.
Тромбоциты и плазменные компоненты гемостаза непосредственно участвуют в поддержании резистентности сосудистой стенки к разного рода повреждениям в норме и патологии. Под влиянием соответствующих сигналов, исходящих от элементов стенки сосуда, тромбоциты совершают адгезию, образуют тромбоцитарную пробку в месте повреждения, а их биологически активные вещества включаются в процесс распластывания тромбоцитов и регенерации эндотелиоцитов. Около 15 % тромбоцитов крови расходуется на эту ангиотрофическую функцию, а тромбоцитопения приводит к дистрофии и гибели эндотелиоцитов, резкому повышению проницаемости микрососудов и диапедезу эритроцитов. Кроме того, в процессе нормального завершения родов происходит естественное тромбирование сосудов матки, что предупреждает кровотечение, а у здорового новорожденного — тромбирование сосудов пупочного канатика.
На ранних этапах эволюции остановка кровотечений обеспечивалась первоначальным, практически мгновенным, спазмом мелких сосудов. Позднее появились кровяные клетки — амебоциты, способные совершать адгезию к поврежденному участку стенки сосуда и закрывать место его повреждения. Последующее развитие животного мира привело к формированию системы гемостаза, включающей специализированные клетки — тромбоциты, или кровяные пластинки, и большую совокупность связанных с ними и между собой белков крови.
Система гемостаза состоит из прокоагулянтов и антикоагулянтов; необходимость локализации и устранения тромба привела к тому, что в процессе естественно-исторического развития сформировалась еще одна система — фибринолиза. После завершения репарации сосуда она предупреждает избыточное образование тромботических масс, обеспечивает элиминацию остатков тромба, а также его рост и распространение по сосудистой системе.
– Читать “Тромбоз. Причины формирования тромбоза”
Оглавление темы “Эмболии и гемостаз”:
1. Эмболия сосудов и сердца. Воздушная и газовая эмболия
2. Тромбоэмболия. Жировая и клеточная эмболия
3. Эмболия околоплодными водами. Значение эмболии для организма
4. Эмболия воротной вены. Тромбообразование
5. Тромбоз. Причины формирования тромбоза
6. Сосудисто-тромбоцитарный гемостаз. Значение тромбоцитов
7. Свойства тромбоцитов. Биохимия тромбоцитов
8. Плазменная фаза тромбообразования. Факторы свертывания крови в плазме
9. Функциональная активность тромбоцитов. Регуляция тромбообразования и проявления ее расстройства
10. Антикоагулянты. Система фибринолиза
Источник
Эмболия системы воротной вены возникает в результате патологических процессов, развивающихся в бассейне воротной вены. Чаще всего она образуется вследствие тромбоэмболии при воспалительных процессах стенок как вен, так и кишок, особенно при кишечной непроходимости. В итоге развиваются венозная гиперемия, стаз, дистрофические изменения, паранекроз, некробиоз и некроз различных отделов кишечника.
Кроме названных видов, выделяют также ретроградную и парадоксальную эмболии.
• При ретроградной эмболии крупные тромбоэмболы движутся в больших венах нижней половины тела, особенно нижних конечностей, не в соответствии с законами гемодинамики, а в силу тяжести эмболов и земного притяжения. Последнее обнаруживают чаще при замедлении тока венозной крови и ослаблении присасывающего действия грудной клетки.
• При парадоксальной эмболии эмболы из левой половины сердца могут попадать в правую и (очень редко) наоборот. Это происходит при незаращении межпредсердной или межжелудочковой перегородки, а также боталлова протока сердца.
Проявления и исходы эмболии
Проявления и исходы эмболии, так же, как и тромбозов, могут быть самыми различными. Они определяются следующими факторами:
• локализацией, видом, объёмом, количеством эмболов и тромбов;
• размерами, строением и функциональной значимостью закупоривающихся сосудов;
• состоянием коллатерального кровообращения;
• соотношением активности свёртывающей, противосвёртывающей и фибринолитической систем крови;
• скоростью и интенсивностью нарушения регионарного кровотока;
• реактивностью и резистентностью вовлечённых в патологический процесс тканей, органов, систем и организма в целом.
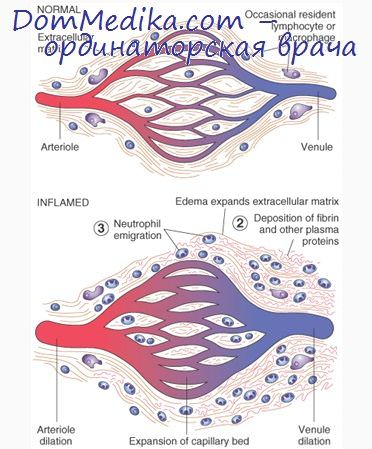
Воспаление
Термин «воспаление» происходит от латинского слова inflammatio и греческого слова phlogosis, что условно означает воспламенение, жар.
Известный русский патофизиолог В.В. Воронин, глубоко и всесторонне изучавший воспаление, писал: «Изучать литературу о воспалении — значило бы писать историю всей медицины».
Воспаление — одна из наиболее частых типовых форм реакций организма на действие разнообразных патогенных факторов.
Аналоги воспаления встречают на различных ступенях развития животного мира, но особой сложности и совершенства воспаление достигло у высших животных и человека.
Воспаление — основное проявление многих заболеваний, а локализация и характер воспалительного процесса в том или ином органе нередко определяет нозологическую форму и специфику болезни.
Для обозначения воспаления ткани или органа принято добавлять окончание «-ит» (-itis) к греко-латинскому названию ткани или конкретного органа (например, гепатит, миокардит, нефрит, колит, энцефалит, менингит, ринит, конъюнктивит, дерматит и т.д.). Реже воспалению дают специальное название (например, пневмония, абсцесс, флегмона и т.д.).
Важно отметить, что при воспалении организм жертвует местным (частью своих повреждённых клеточно-тканевых структур в очаге воспаления) ради сохранения целого (всего организма).
– Читать далее “Теории воспаления. Признаки воспаления”
Оглавление темы “Тромбз и эмболия. Воспаление”:
1. Нарушения проницаемости сосудов. Повреждение сосудистой стенки
2. Развитие отёка сосудов. Микрокровоизлияния
3. Внесосудистые расстройства микроциркуляции. Нормализация микроциркуляции
4. Тромбоз. Причины образования тромбов и тромбообразования
5. Эмболия. Формы эмболии сосудов
6. Эндогенная эмболия. Формы эндогенной эмболии
7. Эмболия системы воротной вены. Воспаление
8. Теории воспаления. Признаки воспаления
9. Характеристика воспаления. Классификация воспаления
10. Исходы и причины воспаления. Механизмы развития воспаления
Источник
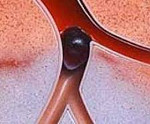
Тромбоз воротной вены – это полная или частичная окклюзия ствола воротной вены и ее ветвей тромботическими массами. Патология проявляется абдоминальным синдромом, рвотой, диареей, признаками портальной гипертензии (асцит, спленомегалия, расширение венозных коллатералей), осложняется кровотечением из верхних отделов пищеварительного тракта, инфарктом кишечника и другими состояниями. Основу диагностики составляют методы визуализации – УЗДС, МР- и КТ-ангиография, венография пораженных участков. Лечебная тактика предполагает антикоагулянтную терапию, тромболизис, хирургическую коррекцию.
Общие сведения
Тромбоз воротной вены (пилетромбоз) считается достаточно редким явлением, риск возникновения которого не превышает 1% в общей популяции. Его распространенность среди пациентов с циррозом печени варьируется от 0,6 до 26%, что, по-видимому, связано с различием в критериях выборки и диагностических методах. Заболевание называют причиной 5–10% случаев портальной гипертензии у жителей развитых стран и до 40% – в азиатском регионе (из-за более высокой частоты инфекционной патологии). Распространенность первичного тромбоза у взрослых и детей одинакова. Гендерных отличий в развитии болезни не выявлено, кроме цирротической обструкции, чаще диагностируемой у мужчин.
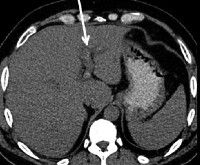
Тромбоз воротной вены
Причины
Заболевание имеет мультифакторную природу. Тромбоз развивается под влиянием системных и локальных нарушений, участвующих в повреждении сосудистой стенки, усилении коагуляции, замедлении венозного кровотока. Среди наиболее значимых причин отмечают следующие:
- Цирроз печени. Является основным этиологическим фактором, составляя 24–32% случаев тромботической окклюзии. Вероятность тромбоза повышается на поздних стадиях болезни, при необходимости трансплантации органа. Переход цирроза в гепатоцеллюлярную карциному увеличивает частоту внепеченочных пилетромбозов.
- Новообразования. Злокачественные новообразования печеночного или панкреатического происхождения являются причиной 21–24% случаев тромбоза. Развитие патологии опосредовано компрессией или прямой опухолевой инвазией, сопутствующей гиперкоагуляцией, гормональными сдвигами.
- Тромбофилии. Системные нарушения вызваны врожденными дефектами коагуляции – генетическими мутациями (фактора V Лейдена, протромбина, ингибитора активатора плазминогена), дефицитом протеинов C и S, антитромбиновой недостаточностью. К приобретенным факторам относят хроническую миелопролиферативную патологию, антифосфолипидный синдром, пароксизмальную ночную гемоглобинурию.
- Воспалительные заболевания. Патологический процесс может возникать на фоне абдоминальной воспалительной патологии (панкреатита, холецистита, гепатита), инфекционных заболеваний (малярии, брюшного тифа, амебиаза). У детей и новорожденных половина случаев тромбоза приходится на долю омфалита, пупочного сепсиса, аппендицита.
- Травмы и оперативные вмешательства. Воротная вена подвергается повреждению при травмах живота и хирургических вмешательствах на органах брюшной полости (спленэктомии, холецистэктомии, трансплантациии печени). Патология возникает после портосистемного шунтирования, тонкоигольной аспирационной биопсии печени, склеротерапии вен пищевода.
К другим факторам риска тромбоза воротной вены относят беременность, прием пероральных контрацептивов, гиперхолестеринемию. Отмечена роль внутрибрюшной аденопатии, синдрома системного воспалительного ответа. В детском возрасте окклюзия возникает при врожденных аномалиях сосудистой системы (дефектах межжелудочковой и межпредсердной перегородок, деформации полой вены) и желчевыводящих путей. Причина 10–30% тромботических стенозов остается невыясненной.
Патогенез
Исходя из современных представлений, пилетромбоз является результатом системных коагулопатий (наследственных, приобретенных) и действия локальных факторов. Повреждение стенки сосуда опухолью, инвазивными процедурами или травмами характеризуется выработкой цитокинов, активацией тромбоксана A2 и тромбина, усилением адгезии и агрегации тромбоцитов. Венозный застой при наружной компрессии сопровождается гипоксией эндотелия, накоплением активированных факторов свертывания. Все это запускает формирование пристеночного кровяного сгустка с дальнейшим его увеличением.
Сосудистая окклюзия сопровождается портальной гипертензией, что ведет к изменению системной и внутриорганной гемодинамики. Печень теряет около 2/3 своего кровоснабжения, но это компенсируется дилатацией печеночной артерии и быстрым развитием сети коллатералей. Вокруг тромбированной вены формируется кавернома, а сама она превращается в фиброзный тяж. Новообразованные сосуды расположены в пределах желчных протоков и пузыря, поджелудочной железы, антрального отдела желудка, двенадцатиперстной кишки.
Патогенез тромбоза при печеночном циррозе до конца не ясен. Важное значение отводят портальной гипертензии с замедлением кровотока по воротной вене, периферическому лимфангииту, перипортальному фиброзу. Системное шунтирование крови провоцирует гемосидероз, гепатоциты в зонах гипоперфузии подвергаются апоптозу. В тонком и толстом кишечнике выше уровня окклюзии определяются застойные явления, в желудке – гастропатия. Брыжеечная ишемия может привести к переходу тромботического процесса на мезентериальные сегменты.
Классификация
Формальной классификации тромбоза воротной вены не существует. Согласно клиническим рекомендациям по портальной гипертензии, при постановке диагноза учитывают участок тромбоза и его проявления, наличие и характер основного заболевания, степень окклюзии (частичную, полную), вовлеченность внепеченочных сегментов. В зависимости от локализации тромба различают несколько форм патологии:
- Стволовая (трункулярная). Участок окклюзии расположен в стволе воротной вены, дистальнее слияния селезеночной и верхней мезентериальной. Возникает первично или путем распространения из корешкового сегмента.
- Радикулярная (корешковая). Характеризуется поражением корешковых ветвей – селезеночной вены и брыжеечных сосудов.
- Терминальная. Пилетромбоз распространяется на внутрипеченочные разветвления и капилляры, сопровождаясь мелкими или развитыми коллатералями.
Представленная классификация позволяет оценить последствия тромботической обструкции и трудоспособность пациента. При поражении сначала интерстициальных сосудов, а затем крупных стволов констатируют восходящий (первичный) процесс. Мезентериальный тромбоз, возникающий из-за обструкции воротной или селезеночной вен, называют нисходящим (вторичным). В клинической флебологии также различают острую, подострую и хроническую стадии, последовательно сменяющие друг друга.
Симптомы
Клиническая картина тромбоза воротной вены определяется происхождением, степенью, протяженностью, локализацией, темпами нарастания окклюзии, выраженностью коллатералей. Частичное тромбирование протекает бессимптомно, выявляясь лишь при инструментальной диагностике, полной обструкции (90–100% просвета) присуще бурное развитие за несколько суток. Подострая форма прогрессирует на протяжении 4–6 недель, а хронический процесс характеризуется медленным нарастанием симптоматики (от нескольких месяцев до года).
Стволовой тромбоз
Острый стволовой пилетромбоз проявляется резкими болями в правом подреберье и эпигастрии, сочетающимися с метеоризмом, частой рвотой, диареей (нередко с примесью крови). Быстро нарастают признаки портальной гипертензии – расширение подкожных, пищеводных, геморроидальных вен, асцит. Зачастую выявляют желтуху, недостаточность печеночной функции. Общее состояние пациентов быстро становится тяжелым, что в основном обусловлено рецидивирующими кровотечениями из желудочно-кишечного тракта.
Радикулярный тромбоз
Радикулярный тромбоз на уровне селезеночного сегмента начинается остро, с боли в левом подреберье, кровавой рвоты и дегтеобразного стула. Увеличение селезенки и субфебрильная лихорадка сочетаются с обычными размерами печени. В подостром периоде постепенно нарастают спленомегалия, асцит, расширяется венозная сеть на животе. Терминальная форма патологии выявляется только при распространенном поражении – у таких пациентов обычно определяют увеличенную селезенку, широкие подкожные коллатерали.
Хронический тромбоз
Хронический пилетромбоз не имеет специфических проявлений. Отсутствие аппетита и общая слабость – иногда единственные симптомы болезни. У большинства пациентов выявляют подкожные анастомозы, умеренный асцит. В 20–40% случаев патология манифестирует кровотечением из варикозных расширений пищевода. Вялотекущие варианты тромбоза воротной вены характеризуются нерезким болевым синдромом, субфебрилитетом, чувствительностью печении при пальпации. Отмечаются спленомегалия с признаками гиперспленизма, тяжестью в подреберье, исхуданием.
Осложнения
Наиболее опасное следствие острой окклюзии мезентериальных сосудов – инфаркт кишечника с развитием перитонита и полиорганной недостаточности (характерно для 5% случаев). Большинство осложнений длительного пилетромбоза обусловлено портальной гипертензией. Расширение пищеводных вен у многих пациентов сопровождается кровотечением, риск которого в 100 раз выше при циррозе печени. Выраженное портосистемное шунтирование приводит к печеночной энцефалопатии, вторичным изменениям в желчевыводящих путях (портальной билиопатии, холангиопатии). При сохраняющихся факторах риска тромбозы могут рецидивировать, осложняться эмболизацией.
Диагностика
Отсутствие специфических признаков тромбоза, необходимость определения предпосылок, уровня, степени и последствий поражения создают потребность в комплексном обследовании пациента. Основой диагностической программы выступают методы инструментальной визуализации:
- УЗАС воротной вены. Обладая высокой специфичностью (60–100%), признано методом выбора при первичной диагностике. УЗДС определяет неоднородный очаг повышенной эхогенности с нечеткими контурами, частично или полностью перекрывающий сосудистый просвет. Допплеровское картирование дает возможность выявить отсутствие кровотока в вене и ее притоках, наличие портосистемных шунтов, каверноматозную трансформацию.
- КТ и МР-ангиография сосудов. КТ с контрастированием дает точную информацию о состоянии венозных стенок, протяженности тромбированных участков, наличии перивисцеральных коллатералей, варикозных вен в забрюшинном пространстве. Магнитно-резонансную ангиографию используют для выяснения состоятельности портального кровотока, оценки просвета шунтов – ее результаты более надежны, чем УЗДС.
- Портальная венография. Используется в случаях, когда неинвазивными методами подтвердить или исключить тромботическое поражение не удается. Контрастная венография выявляет не только стенозы, но и дефекты наполнения от сдавления извне. Однако при установленной проходимости сосуда в ней нет необходимости.
Проводя диагностику пилетромбоза, врачи-флебологи обращают внимание на показатели коагулограммы (увеличение фибриногена, протромбинового индекса, замедление времени свертывания крови), низкий уровень антитромбина. Выявить варикозно-расширенные вены пищевода позволяет ФГДС, исключить цирроз удается благодаря эластографии и биопсии печени. Дифференциальная диагностика осуществляется с печеночным шистосомозом, тромбозом нижней полой вены, сдавливающим перикардитом, рестриктивной кардиомиопатией.
Лечение тромбоза воротной вены
Задачами лечебной коррекции являются восстановление проходимости сосуда, предотвращение прогрессирования патологии, устранение осложнений венозной гипертензии. Исходя из остроты процесса, возраста пациента, этиологических и прочих факторов, применяют комбинацию консервативных и радикальных методов:
- Антикоагулянтная терапия. Является лучшим способом для реканализации венозного просвета, но единого мнения о ее применении нет. Длительность лечения антикоагулянтами (низкомолекулярными гепаринами, пероральными средствами) у лиц с острым пилетромбозом составляет от 3 до 6 месяцев, а при хроническом решается в индивидуальном порядке.
- Введение тромболитиков. Регионарный тромболизис (введение стрептокиназы, альтеплазы, тенектеплазы) транспеченочным или трансъюгулярным доступом позволяет обеспечить реканализацию, избежав побочных эффектов антикоагулянтной терапии. При острой тотальной или субтотальной окклюзии может выполняться системный тромболизис.
- Хирургические методы. При неэффективности консервативных мероприятий операцией выбора является дистальное спленоренальное шунтирование. В условиях нарушенной проходимости селезеночного участка накладывают мезентерикопортальный или мезентерикокавальный анастомоз с применением сосудистых протезов.
Варикозные расширения пищевода лечат с помощью лигирования, эндоскопической склеротерапии. В ургентных ситуациях при кровотечении могут производить операции азигопортального разобщения (гастротомию с прошиванием нижней трети пищевода, деваскуляризацию желудка). Тяжелый гиперспленизм требует спленэктомии.
Прогноз и профилактика
В целом прогноз при заболевании относительно благоприятный. Сгустки могут подвергаться асептическому аутолизу, организации, васкуляризации. Десятилетняя выживаемость для взрослых достигает 60%, а общий уровень смертности составляет менее 10%. При наличии цирроза и злокачественных новообразований прогноз ухудшается. Иногда тромбы превращаются в эмболы, становятся источником сепсиса. Но своевременное и интенсивное лечение приводит к реканализации сосуда, что сопровождается полным клиническим выздоровлением. Профилактика рецидивов проводится путем назначения антикоагулянтов.
Источник
