Эмбриональный источник развития сосудов
Занятие №9.
ТЕМА : ОРГАНОГЕНЕЗ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ
Контрольные вопросы.
1. Источники развития сердечно-сосудистой системы (мезенхима, висцеральная мезодерма).
2. Развитие сосудов. Первичный ангиогенез, вторичный ангиогенез.
3. Сердце, источники развития и этапы эмбриогенеза.
4. Развитие рабочей и проводящей сердечной мышечной ткани.
5. Кровоснабжение плода.
6. Циркуляция крови в сердце.
7. Врожденные пороки сердца.
– .
Занятие №9.
ТЕМА : ОРГАНОГЕНЕЗ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ
ЦЕЛЬ ЗАНЯТИЯ :изучить морфогенетические процессы в развитии органов сердечно-сосудистой системы, рассмотреть источники развития и тканевой состав. Дать представление о сроках закладки сосудов и сердца, а также врожденных пороках сердца.
СТУДЕНТ ДОЛЖЕН ЗНАТЬ :
– источники эмбрионального развития кровеносных сосудов и сердца;
– этапы эмбриогенеза;
– развитие рабочей и проводящей сердечной мышечной ткани;
– развитие сосудов;
– кровоснабжение плода;
– врожденные пороки сердца
СТУДЕНТ ДОЛЖЕН УМЕТЬ :
– диагностировать на схемах и таблицах этапы ангиогенеза;
– зарисовать по памяти тканевые компоненты и клеточные компоненты стенки сосудов и сердца;
– составлять схемы последовательных этапов эмбриогенеза сердца;
– объяснить основные принципы кровоснабжения плода;
– объяснить причину возникновения врожденных пороков сердца.
Контрольные вопросы.
1. Источники развития сердечно-сосудистой системы (мезенхима, висцеральная мезодерма).
2. Развитие сосудов. Первичный ангиогенез, вторичный ангиогенез.
3. Сердце, источники развития и этапы эмбриогенеза.
4. Развитие рабочей и проводящей сердечной мышечной ткани.
5. Кровоснабжение плода.
6. Циркуляция крови в сердце.
7. Врожденные пороки сердца.
ИСТОЧНИКИ РАЗВИТИЯ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ.
Сердечно-сосудистая система – это замкнутая разветвленная сеть, представленная сердцем и кровеносными сосудами
В эмбриональном развитии сердечно-сосудистой системы участвует мезенхима , висцеральные и париетальные листки спланхнотома.
1. Мезенхима. На 2-3 недели эмбриогенеза первые кровеносные сосуды появляются в мезенхиме желточного мешка и ворсинках хориона
Из мезенхимы на 17ые сутки справа и слева образуются эндокардиальные сердечные трубки , которые впячиваются в висцеральные листки спланхнотома.
2. Висцеральные листки спланхнотома . утолщённые участки спланхнотома – миоэпикардиальные пластинки , дадут начало миокарду и эпикарду. Из слившихся мезенхимных трубок формируется эндокард . Клетки миоэпикардиальных пластинок дифференцируются в 2х направлениях : из наружной части образуюется мезотелий , выстилающий эпикард . Клетки внутренней части дифференцируются в 3х направлениях . Из них образуются : сократительные кардиомиоциты ; проводящие кардиомиоциты ; эндокринные кардиомиоциты.
3. Париетальные листки спланхнотома . Из париетального листка спланхнотома развивается перикард. Перикард также выстлан мезотелием. В процессе развития сердца имеет место три этапа :
1)дифференцировка ;
2)стадия стабилизации ;
3)стадия инволюции.
Дифференцировка начинается в эмбриогенезе и продолжается сразу после рождения. Стадия стабилизацииначинается в двадцатилетнем возрасте и заканчивается в сорок лет. После сорока лет начинается стадия инволюции , сопровождаемая уменьшением толщины кардиомиоцитов засчёт уменьшения толщины миофибрилл. Увеличивается толщина прослоек соединительной ткани . Снижается частота и сила сокращений сердечной мышцы . Впоследствии это приводит к ишемической болезни сердца и инфаркту миокарда.
Источник
Развитие сосудов плода. Первичная система кровообращения эмбриона
Приблизительно в конце пятой недели уже начинает функционировать первичная система кровообращения эмбриона, основными составными компонентами которой являются следующие образования.
1. Эмбриональное сердце, описанное при разборе его начальных стадий развития в предыдущей статье.
2. Артериальный ствол (truncus arteriosus), отходящий от сердца и расширяющийся в его близости в аортальный мешок.
3. Две короткие восходящие (вентральные) аорты (aortae ascendentes), которые отходят от артериального ствола в краниальном направлении, вернее из аортального мешка, и на переднем конце эмбрионального тела образуют дугу, обращенную выпуклостью кпереди. Затем эти аорты поворачиваются на дорсальную сторону тела.
4. Здесь они продолжаются в виде так называемых нисходящих (дорсальных) аорт (aortae descendentes), которые направляются вниз.
Обе аорты затем сливаются в единую нисходящую аорту (aorta descendes), причем это слияние происходит сначала посередине тела и продолжается краниально вплоть до области жаберной кишки (фарингеальной, или глоточной, кишки), а каудально вплоть до хвостовой области в виде так называемой каудальной, хвостовой, артерии (arteria caudalis).
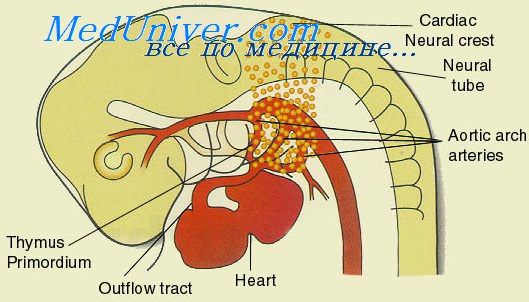
5. От аортального мешка, точнее от коротких восходящих аорт, отходит шесть пар первичных аортальных дуг, которые окружают фарингеальную кишку с боков и идут затем в жаберных дугах; пятая дуга уже с самого начала является рудиментарной и очень скоро полностью исчезает.
Из нисходящей аорты к различным органам эмбрионального тела отходят сначала идущие сегментно дорсальные, латеральные ветви (rami dorsales, laterales et ventrales). Одна из вентральных ветвей представлена пупочно-брыжеечной артерией (arteria omphalomesentrica), являющейся вначале парной и идущей к вентральной стенке тела эмбриона, где она присоединяется к пупочно-кишечному протоку и идет далее в желточный мешок. Из каудального отдела дорсальной аорты берут начало две пупочные артерии (arteriae umbilicales), которые проходят вместе с протоком аллантоиса (ductus allantoideus), направляясь в пуповину.
Первичная венозная система собирает кровь, лишенную кислорода из эмбрионального тела и из экстраэмбриональных областей. Из краниальных отделов тела кровь оттекает по двум идущим параллельно передним кардинальным венам, из каудальных областей — по двум задним кардинальным венам.
На каждой стороне тела задняя кардинальная и передняя кардинальная вены соединяются в общий короткий ствол — общую кардинальную вену, или кувиеров проток, а оба ствола затем, в свою очередь, впадают в венозную пазуху. В эту же венозную пазуху впадают также и пупочно-брыжеечные вены (venae vitellinae), приводящие кровь из желточного кровообращения, а также обе пупочные вены (venae umbilicales), которые на данной стадии развития еще существуют.
Затем эти закладки сосудистой системы в течение шестой и седьмой недель претерпевают сложные изменения, причем возникают взаимоотношения, наблюдаемые у взрослого человека. Основные изменения касаются прежде всего аортальных дуг жаберной области.
– Также рекомендуем “Развитие артериальной сосудистой системы. Этапы формирования аорты плода”
Оглавление темы “Формирование сердечно-сосудистой системы плода”:
1. Формирование предсердий и желудочков сердца. Развитие камер сердца плода
2. Область венозной пазухи сердца плода. Вены сердца эмбриона
3. Область желудочков сердца плода. Формирование луковицы аорты эмбриона
4. Формирование клапанов сердца плода. Развитие перикарда эмбриона
5. Развитие сосудов плода. Первичная система кровообращения эмбриона
6. Развитие артериальной сосудистой системы. Этапы формирования аорты плода
7. Формирование артерий плода. Развитие артериального круга – Вилизиева круга
8. Развитие венозной системы плода плода. Формирование вен эмбриона
9. Ключевые вены эмбриона. Пупочно-брыжеечные вены плода
10. Пупочные вены. Желточное кровообращение плода
Источник
Развитие кровеносных сосудов
В стенке желточного мешка и хориона в конце 2-й и в начале 3-й недели внутриутробного развития появляются кровяные островки. По периферии этих островков мезенхимные клетки обособляются от центральных клеток и превращаются в эндотелиальные клетки кровеносных сосудов. Сосуды туловища также образуются из кровяных островков и на 3-й неделе развития вступают в связь с внезародышевыми кровеносными сосудами (сосуды желточного мешка и хориона).
Развитие артерий. У трехнедельного зародыша от зачатка сердца берет начало артериальный ствол, который разделяется на правую и левую дорсальные аорты (рис. 427). Дорсальные аорты в средней части туловища сливаются в один ствол брюшной аорты. На головном конце тела в это время (3-4-я неделя) закладывается 6 жаберных дуг, в мезензиме которых залегают артерии (дуги аорты), соединяющие вентральные и дорсальные аорты. Такая схема строения артерий эмбриона напоминает строение сосудистой системы животных, имеющих жаберный аппарат. У эмбриона человека нельзя одновременно видеть все 6 жаберных артерий, так как их развитие и перестройка совершаются в различное время: 1-я и 2-я жаберные дуги атрофируются прежде, чем появятся 5-я и 6-я дуги; 5-я дуга существует недолго. Полного развития достигают 3-я, 4-я и 6-я дуги и корни дорсальных и вентральных аорт.

427. Перестройка дуг артерий у эмбрионов (по Петтену). А – схема расположения всех дуг аорты: 1 – корень аорты; 2 – дорсальная часть аорты; 3 – наружная сонная артерия; 4 – внутренняя сонная артерия; I – IV – дуги аорты; Б – ранняя стадия перестройки дуг аорты: 1-общая сонная артерия; 2 – ветвь от шестой дуги к легкому; 3 – левая подключичная артерия; 4 – грудные сегментарные артерии; 5 – правая подключичная артерия; 6 – шейные сегментарные артерии; 7 – наружная сонная артерия; 8 – внутренняя сонная артерия; В – окончательная картина перестройки сосудов: 1 – передняя мозговая артерия; 2 – средняя мозговая артерия; 3 – задняя мозговая артерия; 4 – базилярная артерия; 5 – внутренняя сонная артерия; 6 – задняя нижняя мозжечковая артерия; 7, 11 – позвоночная артерия; 8 – наружная сонная артерия; 9 – общая сонная артерия; 10 – артериальный проток; 12 – подключичная .артерия; 13 – внутренняя грудная артерия; 14 – дорсальная аорта; 15 – легочный ствол; 16 -плечеголовной ствол; 17 – верхняя щитовидная артерия; 18 – язычная артерия; 19 – верхнечелюстная артерия; 20 – передняя нижняя мозжечковая артерия; 21 – артерия мозга; 22 – верхняя мозжечковая артерия; 23 – глазная артерия; 24 – гипофиз; 25-артериальный круг на основании мозга
В дальнейшем 3-я пара жаберных дуг, правая и левая дорсальные аорты на расстоянии от 3-й до 1-й жаберных дуг преобразуются во внутренние сонные артерии. Из 4-й пары дуг формируются различные кровеносные сосуды; 4-я левая жаберная дуга вместе с левой вентральной и частью дорсальной аорты превращается у плода в дугу аорты; 6-я пара аортальных дуг дает производное для развития правой и левой легочных артерий. Левая артерия у плода имеет анастомоз с дугой аорты (см. Кровообращение плода).
В этот период в начальной части общего ствола вентральных аорт возникает фронтальная перегородка, разделяющая ее на переднюю и заднюю части. Из передней части образуется легочный ствол, а из задней – восходящая часть будущей аорты. Эта часть аорты соединяется с 4-й левой жаберной артерией и формирует дугу аорты.
Конечная часть правой вентральной аорты и 4-я правая жаберная артерия дают начало правой подключичной артерии. Правая и левая вентральные аорты, находящиеся между 4-й и 3-й жаберными дугами, преобразуются в общие сонные артерии.
От правой и левой дорсальных аорт и единой дорсальной аорты отходят между сомитами, а затем склеротомами сегментарные артерии в латеральном направлении для кровоснабжения соответствующего сегмента спинного мозга и окружающих его тканей. Позднее в шейном отделе сегментарные артерии редуцируются и остаются только позвоночные артерии, которые являются ветвями подключичных артерий. В грудном и поясничном отделах отходят соответственно межреберные и поясничные сегментарные артерии.
Вентральная группа кровеносных сосудов отходит от досальной аорты, связана с сосудами желточного мешка и кишечной трубки. После обособления кишечника от желточного мешка три артерии (чревная, верхняя брыжеечная, нижняя брыжеечная) вступают в кишечную брыжейку.
Развитие начальной части правой подключичной артерии рассмотрено выше. Левая подключичная артерия берет начало каудальнее артериального протока и представляет 7-ю межсегментарную артерию. После опускания сердца межсегментарная артерия превращается в левую подключичную артерию, которая врастает в почку верхней конечности.
Почки зачатков задних конечностей появляются только после развития плацентарного кровообращения. Парная артерия зачатка ноги берет начало от пупочной артерии в том месте, где она ближе всего проходит от основания зачатка конечности. В почке конечности сосуд занимает осевое положение, располагаясь около седалищного и бедренного нервов.
Развитие вен. Развитие вен начинается с зачатков, имеющих билатеральную симметрию (рис. 428). Парные передние и задние кардинальные вены на правой и левой сторонах тела эмбриона соединяются в общие кардинальные вены, которые впадают в венозный синус простого трубчатого сердца. У взрослого человека парные вены сохраняются только в периферических частях тела. Крупные вены развиваются как непарные образования, расположенные в правой половине тела. Они вливаются в правую половину сердца.

428. Развитие вен у эмбриона 4 нед (по McClur, Batler) 1 – передняя кардинальная вена; 2 – общая кардинальная вена; 3 – пупочная вена; 4 – желточно-брыжеечная вена; 5 – субкардинальная вена; 6 – задняя кардинальная вена; 7 – развивающееся субкардиальное сплетение в средней почке; 8 – печень
Дальнейшая перестройка в венозной системе происходит с образованием четырехкамерного сердца и его смещением. Оказалось, что с образованием правого предсердия обе общие кардинальные вены впадают в правое предсердие. В связи с тем, что кровь по правой общей кардинальной вене протекает беспрепятственно в правое предсердие, в дальнейшем из него формируется верхняя полая вена. Левая общая кардинальная вена частично редуцируется, за исключением ее конечной части, которая превращается в венечный синус сердца.
Появление задних кардинальных вен связано главным образом с развитием средней почки (мезонефрос). С редукцией средней почки исчезают задние кардинальные вены. Вместо них появляются субкардинальные вены, расположенные параллельно задним кардинальным венам эмбриона. Субкардинальные вены на уровне окончательной почки (метанефрос) соединяются венозным анастомозом, который называется субкардинальным (медиальным) синусом (рис. 429). Кровь из нижних частей тела в это время течет уже не по задним кардинальным венам, а вливается в сердце через субкардинальный (медиальный) синус. Выше медиального синуса субкардинальные вены (краниальные их части) превращаются в непарную и полунепарную вены, а ниже (каудальные их части) – в подвздошные вены, по которым кровь оттекает от таза и нижних конечностей.

429. Образование субкардинального синуса и превращение его в нижнюю полую вену у эмбриона 7 нед (по Mellur, Batler) 1 – плечеголовная вена; 2 – субкардинально-субкардинальный анастомоз; 3 – вена гонады; 4 – подвздошный анастомоз; 5 – межсубкардинальный анастомоз; 6 – субкардинальная вена; 7 – нижняя полая вена; 8 – подключичная вена; 9 – наружная яремная вена
На формирование воротной вены оказывает влияние отток венозной крови из первичной кишки через желточные вены желточного мешка. Желточные вены впадают в венозный синус сердца сзади. На пути к печени желточные брыжеечные вены проходят ее зачаток, где они распадаются на несколько ветвей, образуя синусоиды и печеночные вены, которые в дальнейшем устанавливают связь с нижней полой веной. С исчезновением желточного мешка и ростом кишечника желточные вены атрофируются, а брыжеечная часть их развивается лучше и преобразуется в воротную вену. В дальнейшем их развитию способствует венозный ток крови от кишечника, желудка, селезенки и поджелудочной железы.
Источник
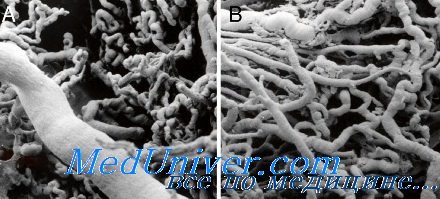
Эмбриогенез гемомикроциркуляции. Развитие внутриорганной кровеносной системыСледовательно, морфология зрелой системы гемомикроциркуляции исследована довольно полно, чего нельзя сказать о полноте изучения ее развития в эмбриогенезе. Более того, можно с уверенностью утверждать, что в морфологической науке до сих пор нет четких представлений о том, за счет каких исходных структур, в какой последовательности и с помощью каких механизмов формируются сосудистые звенья системы гемомикроциркуляции в пренатальном онтогенезе человека. Современная биология располагает большим набором методических приемов, обеспечивающих успешное изучение многих проявлений эмбрионального морфогенеза. В исследованиях, касающихся построения кровеносного русла, особую ценность представляют методы, позволяющие выявлять сосуды всех блоков системы гемомикроциркуляции в их топографической взаимосвязи. Наш опыт показал, что в наибольшей степени этим требованиям отвечает пленочный морфологический метод. К сожалению, эмбриологами в работах по изучению ангиогенеза он почти не применяется, хотя высокая его информативность доказана. При изучении морфогенеза внутриорганной кровеносной системы в эмбриогенезе человека в качестве тест-объекта выбран большой сальник. Использован трупный материал 42 плодов с гестационным возрастом от 12-14 до 28 недель (масса тела от 60 до 1000 г), 108 недоношенных детей, родившихся с I (30 аутопсий), II (41), III (28) и IY (9) степенью незрелости (масса тела от 900 до 2500 г) и 48 доношенных зрелых детей, умерших от различных заболеваний в возрасте от 1-6 дней до 3 лет.
Сосуды в пленочных препаратах выявляли импрегнацией нитратом серебра (В.В.Куприянов, 1969) и гистохимическими методами с применением судана черного В или реактива Шиффа с докраской пленок толуидиновым синим (Н.Е.Ярыгин, С.В.Панченко, 1980). В ряде случаев исследование микрососудов проводили в серийных полутонких срезах, окрашенных метиленовым синим. Принято считать (Б.М.Пэттен, 1959; А.Г.Кнорре, 1967; В.В.Куприянов, 1969; О.В.Волкова, М.И.Пекарский, 1976; И.Станек, 1977; Б.Карлсон, 1983; И.И.Бобрик, В.Г.Черкасов, Е.А.Шевченко, А.И.Парахин, 1986; В.В.Куприянов, 1986; В.В.Куприянов, В.А.Миронов, А.А.Миронов, О.Ю.Гурина, 1993; Wagner, 1980; Merlen, 1983; Hudlicka, Tyler, 1986), что васкуляризация развивающихся органов в эмбриогенезе человека начинается с преобразования вазоформативных клеток мезенхимы в эндотелиоциты. Так, в эмбриональном зачатке органа образуются изолированные друг от друга островки из примордиального эндотелия, превращающиеся вскоре в первичные (презумптивные) кровеносные сосуды, получившие название протокапилляров, при анастомозирований которых формируются первичные капиллярные сети. В последующем первичное диффузное протокапиллярное русло ремоделируется во вторичное, органоспецифическое гемомикроциркуляторное русло. Этот переход проявляется редукцией части протокапилляров и конструированием в презумптивных сосудистых сетях артериолярного и венулярного звеньев за счет морфофункциональной перестройки сохранившихся первичных капилляров и новообразующихся на их основе вторичных (окончательных) капилляров. По мнению некоторых сторонников излагаемой концепции центральные и периферические звенья кровеносного русла в раннем пренатальном онтогенезе конструируются раздельно, а затем при «встречном» (от центра к периферии и от периферии к центру) росте сосудов соединяются. Однако убедительных доказательств в пользу возможного раздельного формирования центральных и периферических отделов кровеносной системы и реальности последующей их интеграции в эмбриологической литературе не приводится. – Также рекомендуем “Эмбриональный ангиогенез. Петлевидный ангиогенез” Оглавление темы “Микроциркуляция и мироциркуляторное русло”: |
Источник