Как молекулярная теория объясняет давление газа на стенки сосуда
Рассмотрим подробнее, что представляет собой один из основных параметров состояния – давление P. Ещё в XVIII веке Даниил Бернулли предположил, что давление газа есть следствие столкновения газовых молекул со стенками сосуда. Именно давление чаще всего является единственным сигналом присутствия газа. Итак, находящиеся под давлением газ или жидкость действуют с некоторой силой на любую поверхность, ограничивающую их объем. В этом случае сила действует по нормали к ограничивающей объем поверхности. Давление на поверхность равно:
где ΔF – сила, действующая на поверхность площадью ΔS. Можно также говорить о давлении внутри газа или жидкости. Его можно измерить, помещая в газ или жидкость небольшой куб с тонкими стенками, наполненный той же средой (рис. 1.1). Рис. 1.1 Поскольку среда покоится, на каждую грань куба со стороны среды действует одна и та же сила ΔF. В окрестности куба давление равно ΔF/ΔS, где ΔS – площадь грани куба. Из этого следует, что внутреннее давление является одним и тем же во всех направлениях и во всем объеме независимо от формы сосуда. Этот результат называется законом Паскаля: если к некоторой части поверхности, ограничивающей газ или жидкость, приложено давление P0, то оно одинаково передается любой части этой поверхности. Допустим, автомобиль поднимается гидравлическим домкратом, состоящим, как показано на рисунке 1.2, из двух соединенных трубкой цилиндров с поршнями. Диаметр большого цилиндра равен 1 м, а диаметр малого – 10 см. Автомобиль имеет вес F2. Найдем силу давления на поршень малого цилиндра, необходимую для подъема автомобиля. Рис. 1.2 Поскольку оба поршня являются стенками одного и того же сосуда, то в соответствии с законом Паскаля они испытывают одинаковое давление. Пусть – давление на малый поршень, а – давление на большой поршень. Тогда, т.к. P1 = P2, имеем:
Отсюда F1=F2(S1/S2)=0,01F2 Таким образом, для подъема автомобиля достаточно давить на малый поршень с силой, составляющей лишь 1 % веса автомобиля. Вычислим давление, оказываемое газом на одну из стенок сосуда (рис. 1.3).
Рис. 1.3 Обозначим: n – концентрация молекул в сосуде; m0 – масса одной молекулы. Движение молекул по всем осям равновероятно, поэтому к одной из стенок сосуда площадью S, подлетает в единицу времени (1/6)nvx молекул, где vx – проекция вектора скорости на направление, перпендикулярное стенке. Каждая молекула обладает импульсом m0υx, но стенка получает импульс 2m0υx(при абсолютно-упругом ударе m0υx- (-m0υx)=2m0υx). За время dt о стенку площадью S успеет удариться число молекул, которое заключено в объёме V:
Общий импульс, который получит стенка S:
Разделив обе части равенства на S и dt, получим выражение для давления:
Таким образом, мы определили давление как силу, действующую в единицу времени на единицу площади:
Наивно полагать, что все молекулы подлетают к стенке S с одной и той же скоростью vx (рис. 1.3). На самом деле молекулы имеют разные скорости, направленные в разные стороны, то есть скорости газовых молекул – случайные величины. Более точно случайную величину характеризует среднеквадратичная величина. Поэтому под скоростью vx2понимаем среднеквадратичную скорость <vx2> . Вектор скорости, направленный произвольно в пространстве, можно разделить на три составляющих:
Ни одной из этих проекций нельзя отдать предпочтение из-за хаотичного теплового движения молекул, то есть в среднем . Следовательно, на другие стенки будет точно такое же давление. Тогда можно записать в общем случае: или
где <Ek>- средняя энергия одной молекулы. Это и есть основное уравнение молекулярно-кинетической теории газов. Итак, давление газов определяется средней кинетической энергией поступательного движения молекул. Уравнение (1.2.3) называют основным уравнением, потому что давление Р – макроскопический параметр системы здесь связан с основными характеристиками – массой и скоростью молекул. Иногда за основное уравнение принимают выражение Рассмотрим единицы измерения давления. По определению, , поэтому размерность давления Н/м2. 1 Н/м2 = 1 Па; 1 атм. = 9,8 Н/см2 = 98066 Па ≈105 Па, 1 мм рт.ст. = 1 тор = 1/760 атм. = 133,3 Па, 1 бар = 105 Па; 1 атм. = 0,98 бар. |
Источник
Давление газа – что это за параметр
Определение
Давление в физике представляет собой один из трех ключевых термодинамических макроскопических характеристик для измерения любой газовой системы.
Определение
Газ – это одно из четырех, включая плазму, агрегатных состояний материи, характеризующееся очень слабыми связями между составляющими его частицами, а также их большой подвижностью.
В газообразной среде частицы в определенной концентрации расположены не упорядоченно и перемещаются в хаотичном порядке в разных направлениях с одинаковой вероятностью. Подобное строение не позволяет газам сохранять стабильность объема и формы даже при малом внешнем силовом воздействии. Для любого газа, включая одноатомный, значение средней кинетической энергии его частиц в виде атомов и молекул будет превышать энергию межмолекулярного взаимодействия между ними.
Кроме того, расстояние, на которое удалены частицы, значительно превышает их собственные размеры. В том случае, когда молекулярными взаимодействиями и габаритами частиц допускается пренебрегать, газ считают идеальным. Для такой формы материи характерен только один тип внутреннего взаимодействия в виде упругих столкновений. Так как размер частиц пренебрежимо мал по сравнению с расстоянием, на которое они удалены, вероятность столкновений частиц между собой будет низкой.
Примечание
По этой причине в идеальной газовой среде можно наблюдать лишь столкновения частиц со стенками сосуда. Какой-либо реальный газ с хорошей точностью можно отнести к идеальному, когда их температура выше, чем комнатная, а давление несущественно больше, чем атмосферное.
Причина возникновения давления в газах
Давление газа нельзя объяснить теми же причинами, что и давление твердого тела на опору. Расстояние, на которое удалены молекулы газообразной среды, существенно больше. В результате хаотичного движения они сталкиваются между собой и со стенками сосуда, который они занимают. Давление газа на стенки сосуда и вызвано ударами его молекул.
Данный параметр увеличивается по мере того, как нарастает сила ударов молекул о стенки. Газ характеризуется одинаковым давлением во всех направлениях, которое является следствием хаотичного движения огромного числа молекул.
Примечание
Важно отметить, что газ оказывает давление на дно и стенки сосуда, объем которого он занимает, во всех направления равномерно. В связи с этим, воздушный шарик сохраняет форму, несмотря на то, что его оболочка достаточно эластична.
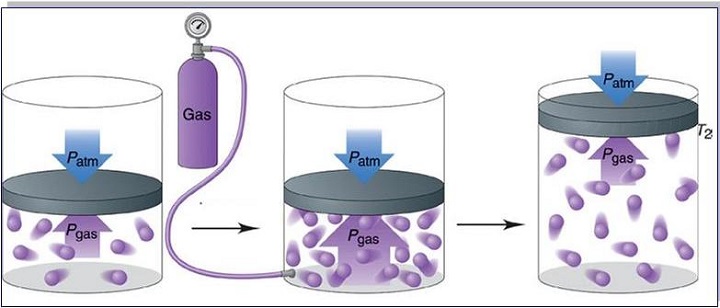
Перед тем как транспортировать или отправить на хранение газообразные вещества, их сильно сжимают. В этом случае давление газа увеличивается. Его помещают в специальные баллоны из стали высокой прочности. Такие емкости необходимы для хранения сжатого воздуха на подводных лодках и кислорода, предназначенного для сварки металлов.
Свойства давления газа:
- Если объем уменьшается, то давление газа возрастает, а во время увеличения объема, давление будет снижаться при постоянных величинах массы и температуры вещества.
- Газ, находящийся в закрытом сосуде, характеризуется давлением, которое возрастает по мере увеличения температуры вещества при условии постоянства его массы и объема.
- В том случае, когда масса газа увеличивается, его давление также будет возрастать и наоборот.
Запись формул для определения давления газа начинают с выяснения причин, по которым оно возникает в рассматриваемой системе. Исходя из физического смысла, давление представляет собой величину, равную отношению силы, перпендикулярно воздействующей на некоторое основание, к площади этого основания:
(P=frac{F}{S})
Как было отмечено ранее, для идеальной газовой системы характерен лишь один тип взаимодействия – это абсолютно упругие столкновения. В процессе частицы передают количество движения Δp стенкам сосуда в течение времени соударения Δt. В данном случае применим второй закон Ньютона:
(F*Δt = Δp)
Таким образом, конкретно сила F является причиной формирования давления на стенки сосуда. Данная величина F, производимая одной частицей, незначительна. Однако, когда количество частиц огромно, они в совокупности создают ощутимый эффект, проявляемый в виде наличия давления в сосуде.
Формула давления идеального газа из молекулярно-кинетической теории
Объяснение концепции идеального газа построено на основных положениях молекулярно-кинетической теории, которая вытекает из принципов статистической механики. Наука получила активное развитие во второй половине XIX, благодаря таким ученым, как Джеймс Максвелл и Людвиг Больцман. Основы дисциплины были заложены еще Бернулли в первой половине XVIII века.
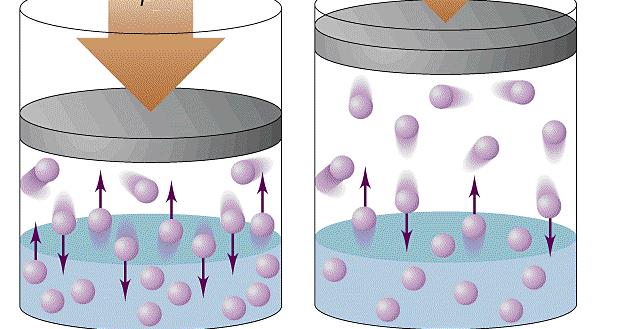
Исходя из статистики Максвелла-Больцмана, все частицы в системе обладают разными скоростями движения. При этом можно наблюдать небольшой процент частиц со скоростями, приближенными к нулю, и малую долю частиц, обладающих огромной скоростью. Средняя квадратичная скорость в этом случае будет соответствовать некоторой величине, не изменяющейся с течением времени.
Средняя квадратичная скорость частиц однозначно характеризует температуру газа. Используя приближения молекулярно-кинетической теории в виде невзаимодействующих безразмерных и хаотично движущихся частиц, получают формулу для расчета давления газа в сосуде:
(P=frac{N*m*v^{2}}{3*V})
где N является количеством частиц в системе; V обозначает объем; v представляет собой среднюю квадратичную скорость; m является массой одной частицы.
При наличии указанных в формуле параметров, выраженных в единицах СИ, можно вычислить давление газа в сосуде.
Второй способ записи основного уравнения МКТ
Определение
В середине 30-х годов XIX столетия французскому инженеру Эмилю Клапейрону удалось обобщить накопленный до этого времени экспериментальный опыт изучения поведения газов во время разнообразных изопроцессов и получить формулу, которую в будущем назвали универсальным уравнением состояния идеального газа:
(P*V = n*R*T )
n является количеством вещества в молях; T представляет собой температуру по абсолютной шкале и обозначается в кельвинах.
Величина R является универсальной газовой постоянной. Этот термин был введен в уравнение русским химиком Д.И. Менделеевым. Исходя из этого, запись уравнения называют законом Клапейрона-Менделеева.
Определение
С помощью данного выражения можно определить формулу для расчета давления газа:
(P=frac{n*R*T}{V})
Полученное уравнение объясняет линейный рост давления при увеличении температуры в условиях стабильности объема. Если объем уменьшается с сохранением температуры, то давление увеличивается по гиперболе. Данные закономерности явления отражены в законах Гей-Люссака и Бойля-Мариотта.
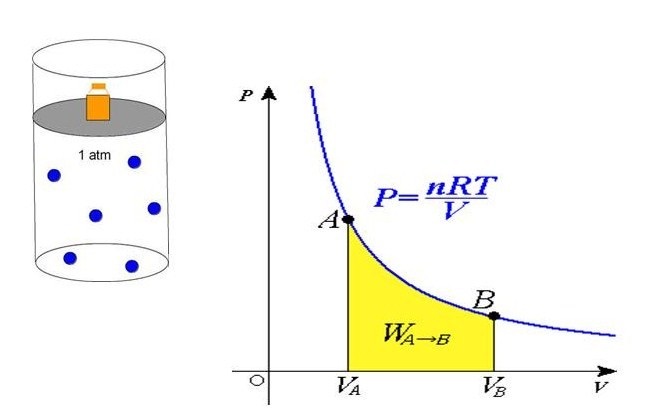
Сравнивая представленное выражение с записью формулы, которая вытекает из положений молекулярно-кинетической теории, можно установить связь кинетической энергии одной частицы, либо системы в общем, и абсолютной температуры.
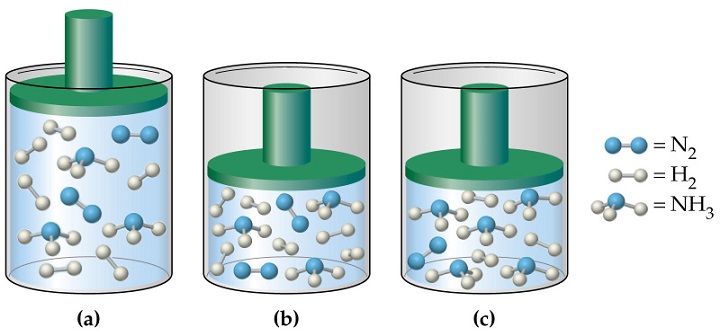
Важно отметить, что при расчетах с использованием формулы для Р, вытекающей из уравнения Клапейрона, связь с химическим составом газа отсутствует. Если давление определяют с помощью выражения, согласно понятию молекулярно-кинетической теории, то данную связь следует учитывать в виде параметра m. В том случае, когда определяют давление смеси идеальных газов, применяют один из следующих методов:
- Расчет средней массы частиц m, либо среднего значения молярной массы М с учетом атомных процентов каждого газа в смеси.
- Применение закона Дальтона, согласно которому давление в системе равно сумме парциальных давлений всех ее компонентов.
Пример
Предположим, что молекулы кислорода движутся со средней скоростью в 500 м/с. Требуется рассчитать, каково давление в сосуде, объем которого равен 10 литров, содержащий 2 моль молекул.
Для того чтобы найти ответ, следует применить формулу для Р из молекулярно-кинетической теории:
(P=frac{N*m*v^{2}}{3*V})
Из-за неизвестных параметров m и N требуется выполнить некоторые преобразования формулы:
(m=frac{M}{NA})
(n=frac{N}{NA})
(m*N= M*n)
(P=frac{M*n*v^{2}}{3*V})
Таким образом, удельный объем сосуда в кубических метрах равен 0,01. Молярная масса молекулы кислорода М составляет 0,032 кг/моль. Данные параметры можно подставить в уравнение вместе со скоростью и количеством вещества. Тогда Р = 533333 Па, что представляет собой давление в 5,3 атмосферы.
Источник
В жизни мы встречаем газообразное состояние вещества, когда чувствуем запахи. Запах очень легко распространяется, потому что газ не имеет ни формы, ни объема (он занимает весь предоставленный ему объем), состоит из хаотично движущихся молекул, расстояние между которыми больше, чем размеры молекул.
Агрегатных состояния точно три?
На самом деле, есть еще четвертое – плазма. Звучит, как что-то из научной фантастики, но это просто ионизированный газ – газ, в котором помимо нейтральных частиц, есть еще и заряженные. Ионизаторы воздуха как раз строятся на принципе перехода из газообразного вещества в плазму.
Давление газа
Мы только что выяснили, что молекулы газа беспорядочно движутся. Во время движения они сталкиваются друг с другом, а также со стенками сосуда, в котором этот газ находится. Поскольку молекул много, ударов тоже много.
Например, в комнате, в которой вы сейчас находитесь, на каждый квадратный сантиметр за 1 с молекулами воздуха наносится столько ударов, что их количество выражается двадцати трехзначным числом.
Хотя сила удара отдельной молекулы мала, действие всех молекул о стенки сосуда приводит к значительному давлению. Это как если бы один комар толкал машину, то она бы и не сдвинулась с места, а вот пару сотен миллионов комаров вполне себе способны эту машину сдвинуть.
Зависимость давления от других величин
Зависимость давления от объема
В механике есть формула давления, которая показывает: давление прямо пропорционально силе и обратно пропорционально площади, на которую эта сила оказывается.
Давление
p = F/S
p – давление [Па]
F – сила [Н]
S – площадь [м^2]
То есть, если наши двести миллионов комаров будут толкать легковую машину, они распределятся по меньшей площади, чем если бы они толкали грузовой автомобиль (просто потому что легковая меньше грузовика).
Из формулы давления следует, что давление на легковой автомобиль будет больше из-за меньшей площади.
Давайте рассмотрим аналогичный пример с двумя сосудами разной площади.
Давление в левом сосуде будет больше, чем во втором, по аналогичной схеме – потому что площадь меньше. Но если площадь основания меньше, то и объем меньше. Это значит, что давление будет зависеть от объема следующим образом: чем больше объем, тем меньше давление – и наоборот.
При этом зависимость будет не линейная, а примет вот такой вид (при условии, что температура постоянна):
Такая зависимость называется законом Бойля-Мариотта.
Она экспериментально проверяется с помощью такой установки.
Объем шприца увеличивают с помощью насоса, а манометр измеряет давление. Эксперимент показывает, что при увеличении объема давление действительно уменьшается.
Зависимость давления от температуры
Рассмотрим зависимость давления газа от температуры при условии неизменного объема определенной массы газа. Эти исследования были впервые произведены в Жаком Шарлем.
Газ нагревался в большой колбе, соединенной с ртутным манометром в виде узкой изогнутой трубки. Пренебрегая ничтожным увеличением объема колбы при нагревании и незначительным изменением объема при смещении ртути в узкой манометрической трубке.
Таким образом, можно считать объем газа неизменным. Подогревая воду в сосуде, окружающем колбу, измеряли температуру газа по термометру, а соответствующее давление – по манометру.
Этот эксперимент показал, что давление газа увеличивается с увеличением температуры. Это связано с тем, что при нагревании молекулы газа движутся быстрее, из-за чего чаще ударяются о стенки сосуда.
С температурой все проще. Зависимость давления от температуры при постоянных объеме и массе будет линейно:
Эта зависимость называется законом Шарля.
Хранение и транспортировка газов
Если нужно перевезти значительное количество газа из одного места в другое, или когда газы необходимо длительно хранить – их помещают в специальные прочные металлические сосуды. Из-за того, что при уменьшении объема увеличивается давление, газ можно закачать в небольшой баллон, но он должен быть очень прочным.
Сосуды, предназначенные для транспортировки газов, выдерживают высокие давления. Поэтому с помощью специальных насосов (компрессоров) туда можно закачать значительные массы газа, которые в обычных условиях занимали бы в сотни раз больший объем.
Поскольку давление газов в баллонах даже при комнатной температуре очень велико, их ни в коем случае нельзя нагревать. Например, держать под прямыми лучами солнца или любым способом пытаться сделать в них отверстие, даже после использования.
Понимать и любить этот мир проще, когда разбираешься в физике. В этом помогут небезразличные и компетентные преподаватели онлайн-школы Skysmart.
Чтобы формулы и задачки ожили и стали более дружелюбными, на уроках мы разбираем примеры из обычной жизни современных подростков. Приходите на бесплатный вводный урок по физике и начните учиться в удовольствие уже завтра!
Источник
Это уравнение устанавливает связь между давлением и средней энергией теплового движения молекул. Давление, оказываемое газом на стенки сосуда, является результатом передачи стенке импульса сталкивающихся с ней молекул. При расчетах учтем, что движение молекул хаотично, и удары молекул об стенку являются абсолютно-упругими. Рассмотрим одноатомный газ, занимающий объем (рис. 1). Выделим на стенке сосуда элементарную поверхность и вычислим давление, оказываемое на эту поверхность. При соударении со стенкой молекула с

Рис.1
массой , движущаяся со скоростью перпендикулярно стенке, передает ей импульс . За время поверхности стенки достигнут только те молекулы которые заключены в объеме цилиндра с основанием и высотой .Это число молекул равно , где – число молекул в единице объема. Здесь мы упростили рассмотрение движения молекул. На самом деле молекулы к площадке движутся под разными углами, имея различные скорости. Для упрощения расчета хаотическое движение молекул по всем направлениям обычно заменяют движением вдоль трех взаимно перпендикулярных координатных осей так, что в любой момент времени вдоль каждой из них (например, оси х) движется 1/3 общего числа молекул, причем одна половина из этого числа, т.е. 1/6 часть молекул, движется вдоль положительной оси, другая половина – в противоположном направлении. Тогда число ударов о поверхность за время будет равно /6 При столкновении с поверхностью молекулы передают ей импульс . Воспользовавшись вторым законом Ньютона , можем выразить силу давления на поверхность
.
Давление газа на стенку выразится в виде
. (2.8)
Молекулы в сосуде движутся с самыми различными скоростями . Их общее число . Поэтому вместо скорости в эту формулу следует подставлять среднюю квадратичную скорость, которая характеризует всю совокупность молекул
. (2.9)
Поэтому
(2.10)
Здесь – средняя кинетическая энергия поступательного движения молекул. Тогда уравнение (2.10) перепишется в виде
. (2.11)
Таким образом, давление газа пропорционально средней кинетической энергии теплового движения молекул газа, заключенных в единице объема. Полученное выражение носит название основного уравнения молекулярно-кинетической теории газов.
Следствия из основного уравнения молекулярно-кинетической теории газов
Так как , то получаем
, (2.12)
где – средняя энергия поступательного движения всех молекул газа.
Отсюда (2.13)
С помощью уравнения Клапейрона-Менделеева
легко получаем
,
откуда
. (2.14)
Энергия поступательного движения одного моля газа будет равна
.
Поделив это уравнение на число Авогадро , получаем
.
Формула
(2.15)
имеет глубокий физический смысл – она выражает, что термодинамическая температура зависит толь от средней энергии поступательного движения молекул.
Существенно также, что средняя кинетическая энергия молекул зависит только от температуры и не зависит от массы молекул. При абсолютно нулевой температуре Т = 0 поступательное движение молекул прекращается. Подставив
в (2.15), получаем выражение для среднеквадратичной скорости в виде
(2.16)
Умножая числитель и знаменатель дроби под корнем на число Авогадро, получим
(2.17)
Источник

