Как найти число молекул газа в сосуде
1
Сколько молекул содержится в 1 см3 воды? Какова масса молекулы воды? Каков приблизительный размер молекулы воды?
Ответ и решение
n = 3,33·1022 1/см3; m = 2,99·10-26 кг; a = 3,11·10-10 м.
Масса 1 моля воды составляет 18 г, а его объем V — 18 см3. В 1 моле воды содержится число молекул, равное постоянной Авогадро NА = 6·1023. Число молекул в 1 см3n = NА/V = 3,33·1022. Масса одной молекулы m = 18/NА = 3·10-26 кг. Объем V0 одной молекулы приблизительно равен 1/n см3. Тогда размер молекулы составит
.
2
Хорошо откачанная лампа накаливания объемом 10 см3 имеет трещину, в которую ежесекундно проникает миллион частиц газа. Сколько времени понадобится для наполнения лампы до нормального давления, если скорость проникновения газа остается постоянной? Температура 0 °С.
Ответ и решение
t ≈ 8,5 млн. лет.
Найдем число частиц газа, необходимое для наполнения лампы:
N = VNЛ = 10·2,69·1019 см3·см-3 = 2,69·1020,
где V – объем лампы, NЛ – постоянная Лошмидта.
Время, необходимое для наполнения лампы со скоростью v = 106 с-1, равно:
t = N/v = 2,69·1020/(106·с-1) = 2,69·1014 c ≈ 8,5 млн. лет.
3
За 10 суток полностью испарилось из стакана 100 г воды. Сколько в среднем вылетало молекул с поверхности воды за 1 с?
Ответ и решение
≈ 3,8·1018 молекул в секунду.
Переведем время t испарения воды из суток в секунды:
t = 10 сут. = 8,64·105 с.
Поскольку 1 моль воды имеет массу 18 г, то, используя постоянную Авогадро, можно найти число N молекул в 100 г воды:
N = NА·100/18 = 3,3·1024 шт.
Теперь найдем скорость v испарения воды:
v = N/t ≈ 3,8·1018 c-1.
4
В озеро средней глубиной 10 м и площадью 10 км2 бросили кристаллик поваренной соли NaCl массой 0,01 г. Сколько ионов хлора оказалось бы в наперстке воды объемом 2 см3, зачерпнутом из этого озера, если считать, что соль, растворившись, равномерно распределилась в озере?
Ответ и решение
≈ 2·106 ионов.
1 моль поваренной соли имеет массу 58,5 г, из которых 23 г — масса натрия, а 35,5 г — масса хлора. Чтобы рассчитать массу хлора в брошенном кристаллике хлора, решим систему из двух уравнений:
m(Na) + m(Cl) = 0,01
m(Na)/m(Cl) = 0,65
Из системы получим, m(Cl) = 6·10-3 г.
Теперь можно вычислить число частиц хлора N(Cl):
N(Cl) = NA· 6·10-3/35,5 ≈ 1020 ионов хлора.
Число ионов хлора в наперстке будет меньше полученного числа во столько раз, во сколько раз объем наперстка меньше объема озера. Найдем это число:
N = 1020·2·10-6/108 = 2·106 ионов хлора в наперстке.
5
Кристаллы поваренной соли NaCl кубической системы состоят из чередующихся атомов (ионов) Na и Cl.

Определить наименьшее расстояние между их центрами. Молярная масса поваренной соли ν = 58,5 г/моль, а ее плотность ρ = 2,2 г/см3.
Ответ и решение
r = 2,83·10-8 см.
Найдем сторону a куба, который занимает объем одного моля поваренной соли:
a =  = 3 см.
= 3 см.
Найдем, какое число ионов натрия и хлора приходится на одно ребро куба (общее число ионов натрия и хлора в 1 моле поваренной соли равно удвоенному числу молекул NaCl, т.е. 2NА):
n = 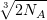 ≈ 108 ионов.
≈ 108 ионов.
Теперь найдем расстояние между ионами:
l = a/n = 2,83·10-8 см.
6
Кубическая кристаллическая решетка железа содержит один атом железа на элементарный куб, повторяя который, можно получить всю решетку кристалла. Определить расстояние между ближайшими атомами железа, если плотность железа ρ = 7,9 г/см3, атомная масса А = 56.
Ответ и решение
2,3·10-8 см.
Найдем сторону a куба, который занимает объем одного моля железа:
a =  = 1,9 см.
= 1,9 см.
Найдем, какое число атомов железа приходится на одно ребро куба (общее число атомов железа в 1 моле равно NА):
n = ≈ 8,4·107 атомов.
≈ 8,4·107 атомов.
Теперь найдем расстояние между атомами железа:
l = a/n = 2,3·10-8 см.
7
На пути молекулярного пучка стоит «зеркальная» стенка. Найти давление, испытываемое этой стенкой, если скорость молекул в пучке v = 103 м/с, концентрация n = 5·1017 1/м3, масса m = 3,32·10-27 кг. Рассмотреть три случая: а) стенка расположена перпендикулярно скорости пучка и неподвижна; б) пучок движется по направлению, составляющему со стенкой угол α = 45°; в) стенка движется навстречу молекулам со скоростью u = 50 м/с.
Ответ
а) pа ≈ 3,3·10-3 Па; б) pб ≈ 2,4·10-3 Па; в) pв ≈ pа.
8
Как изменилось бы давление в сосуде с газом, если бы внезапно исчезли силы притяжения между его молекулами?
Ответ
Источник
Тема. Решение задач по теме «Скорости газовых молекул. Распределение молекул по скоростям »
Цели
На примерах решения задач познакомить учащихся с основными типами задач и методами их решения.
Ход занятия
Вспомните основные свойства модели идеального газа. Повторите понятие размера молекул и длины свободного пробега. Выведите формулу для длины свободного пробега. Покажите, что длина свободного пробега зависит от давления, под которым находится газ. Подсчитайте число молекул, находящихся в единице объема при нормальных условиях. Обсудите насколько велико это число.
Качественные вопросы
1. Какие гипотезы положены в основу вывода основного уравнения молекулярно-кинетической теории газа?
2. Как правильно сформулировать вопрос о распределении молекул по скоростям?
3. Какой физический смысл имеет функция распределения молекул по скоростям?
4. Чему равна ограниченная кривой распределения молекул по скоростям площадь?
5. Как изменяются с температурой положение максимума кривой функции распределения молекул по скоростям и его высота?
Примеры решения задач
Задача 1.Найти среднюю длину свободного пробега молекул воздуха при нормальных условиях. Эффективный диаметр молекул принять равным м.
Решение
Средняя длина свободного пробега определяется формулой , где r – радиус молекулы. Так как d = 2r, то , где – число молекул в единице объема, Р – давление и Т – температура. Подставляя значение в формулу для длины свободного пробега, получим
м.
Ответ: м.
Задача 2. Найти среднюю длину свободного пробега атомов гелия в условиях, когда плотность гелия ρ = 2,1·10–2 кг/м3, а эффективный диаметр атома гелия d = 1,9·10–2 м.
Решение
Для определения средней длины свободного пробега необходимо знать концентрацию молекул n при данных условиях. Найдем n0. Из уравнения Клапейрона–Менделеева следует, что
.
Следовательно,
.
И для средней длины свободного пробега l получаем расчетную формулу
м.
Ответ: м.
Задача 3. Какое предельное число молекул азота может находиться в сферическом сосуде диаметром D = 1 см, чтобы молекулы не сталкивались друг с другом? Диаметр молекул азота d = 3,1·10–10 м.
Решение
Для того чтобы столкновений молекул друг с другом не было, необходимо чтобы средняя длина свободного пробега λ была не меньше диаметра сосуда D, то есть λ ≥ D. Известно, что
,
где d – эффективный диаметр молекул азота, n – число молекул в единице объема, то есть концентрация молекул. Зная d, можно найти допустимую концентрацию молекул.
.
Максимальное число молекул в сосуде, объем которого , определится следующим образом
.
Ответ: .
Задача 4. Азот находится под давлением Па при температуре Т = 300 К. Найти относительное число молекул азота, скорости которых лежат в интервале скоростей, отличающихся от наиболее вероятной на Δv = 1 м/с.
Решение
Так как интервал скоростей Δv мал, то изменением функции распределения в этом интервале скоростей можно пренебречь, считая ее приближенно постоянной.
.
Подставляем значение наиболее вероятной скорости
;
.
Это и есть решение задачи. Производим вычисления: масса молекулы азота кг, постоянная Больцмана Дж/К. Подставляя численные значения, получим
.
При подсчете необходимо учесть, что определяется относительное число молекул, отличающихся по скорости от наиболее вероятной в обе стороны, то есть интервал равен Δv = 2 м/с.
Ответ: .
Задача 5. Найти температуру газообразного азота, при которой скоростям молекул v1 = 300 м/с и v2 = 600 м/с соответствуют одинаковые значения функции распределения Максвелла молекул по скоростям.
Решение
Запишем функцию распределения для указанных скоростей. По условию задачи значения функции должны быть одинаковы.
;
;
;
;
.
Масса молекулы азота кг.
Постоянная Больцмана Дж/К.
К.
Ответ: = 300 К.
Задача 6. Найти отношение средних квадратичных скоростей молекул гелия и азота при одинаковых температурах.
Решение
Воспользуемся формулой для определения средней квадратичной скорости
,
где – молярная масса газа. Тогда отношение средних квадратичных скоростей молекул гелия и азота при одинаковых температурах будет равно
,
где- молярная масса неона, – молярная масса гелия. Подставляя численные значения, получим
Ответ: .
Задача 7. Определить: 1) число молекул в 1 мм3 воды, 2) массу молекулы воды, 3) диаметр молекулы воды, считая условно, что молекулы воды шарообразны и соприкасаются.
Решение
Число молекул, содержащихся в массе вещества равно числу Авогадро , умноженному на число молей (- молярная масса вещества)
,
где r – плотность, V – объем вещества. После подстановки числовых значений получим
.
Массу m1 одной молекулы можно определить, разделив массу одного моля на число Авогадро:
кг.
Считая, что молекулы соприкасаются, объем, занимаемый одной молекулой , где d – диаметр молекулы. Отсюда . Так как , где – объем одного моля, то
м.
Ответ: ; кг; м.
Задача 8. Зная, что диаметр молекулы кислорода d = 3·10–10 м подсчитать, какой длины S получилась бы цепочка из молекул кислорода, находящихся в объеме V = 2 см2 при давлении Р = 1,01·105 Н/м2 и температуре Т = 300 К, если эти молекулы расположить вплотную в один ряд. Сравнить длину этой цепочки со средним расстоянием от Земли до Луны м.
Решение
Число молекул кислорода, содержащихся в единице объема, согласно основному уравнению молекулярно-кинетической теории, равно
,
Число молекул в объеме V будет равно . Следовательно, м.
Тогда .
Ответ: м; раз.
Задача 9. Средняя квадратичная скорость молекул некоторого газа vc.к. = 450 м/с. Давление газа р = 7 · 104 Н/м2. Найти плотность газа ρ при этих условиях.
Решение
Из уравнения Клайперона–Менделеева следует: . Учитывая, что , получаем .
Ответ: .
Задания для самостоятельной работы
1. В опыте Штерна источник атомов серебра создает пучок, который падает на внутреннюю поверхность неподвижного цилиндра радиуса R = 30 см и образует на ней пятно. Цилиндр начинает вращаться с угловой скоростью ω = 100 рад/с. Определить скорость атомов серебра, если пятно отклонилось на угол φ = 0,314 рад от первоначального положения.
Ответ: м/с.
2. Сколько молекул газа содержится в баллоне емкостью V = 60 л при температуре Т = 300 К и давлении P= 5·103 Н/м2?
Ответ: .
3. Определить температуру газа, для которой средняя квадратичная скорость молекул водорода больше их наиболее вероятной скорости на Δv = 400 м/с. Масса молекулы водорода т = 3,35·10–27 кг.
Ответ: = 380 К.
4. Вычислить среднее расстояние между центрами молекул идеального газа при нормальных условиях.
Ответ: м.
5. В помещении площадью S = 100 м2 и высотой h = 4 м разлито V1 = 1 л ацетона (СН3)2СО. Сколько молекул ацетона содержится в 1 м3 воздуха, если весь ацетон испарился? Плотность r ацетона 792 кг/м3.
Ответ:
6. Найти число столкновений z, которые произойдут за 1 с в 1 см3 кислорода при нормальных условиях. Эффективный радиус молекулы кислорода принять равным
1,5·10–10 м.
Ответ: .
7. Найти среднюю длину свободного пробега молекул азота при давлении P = 133 Па и температуре t = 27°C.
Ответ: м.
8. Доказать, что средняя арифметическая и средняя квадратичная скорости молекул газа пропорциональны , где P – давление газа; ρ – плотность газа.
Ответ: .
9. Два одинаковых сосуда, содержащие одинаковое число молекул кислорода, соединены краном. В первом сосуде средняя квадратичная скорость молекул равна , во втором – . Какой будет эта скорость, если открыть кран, соединяющий сосуды (теплообмен с окружающей средой отсутствует)?
Ответ: .
Рекомендуемая литература
1. Бутиков Е.И., Кондратьев А.С. Физика. Т.3. Строение и свойства вещества – Москва – Санкт-Петербург. Физматлит. Невский диалект. Лаборатория Базовых Знаний, 2001. С. 170-194.
2. Белолипецкий С.Н., Еркович О.С., Казаковцева В.А., Цвецинская Т.С. Задачник по физике – Москва. Физматлит, 2005.
3. Готовцев В.В. Лучшие задачи по механике и термодинамике. Москва-Ростов-на-Дону, Издательский центр «Март», 2004. С. 215-219.
Источник
3.1. Распределение молекул между двумя половинками сосуда.
Применим теперь элементы теории вероятности для описания одноатомного идеального газа, заключенного в сосуд объемом . Рассмотрим сначала распределение молекул между двумя половинками сосуда.
Введем следующую терминологию:
Макросостояние – состояние, определяемое только известным количеством частиц в каждой из половин сосуда (без уточнения их номеров и, полагая частицы неразличимыми);
Микросостояние – состояние, определяемое нахождением конкретных (по номерам) частиц в каждой из половин сосуда (известно, частицы с какими номерами находятся в левой и правой половинах сосуда).
Статистический вес (статвес)– это число равновероятных микросостояний, посредством которых реализуется данное макросостояние.
1). Если имеется всего одна молекула, то вероятность найти ее в любой половине сосуда равна
(4.1).
2). Возьмем две молекулы, пронумеруем их и будем размещать их всеми возможными способами двум по половинкам сосуда. Очевидно, что всего возможны 4 (четыре) способа размещения:
Вероятность каждой из молекул оказаться в какой-либо половине сосуда равна . Поскольку положения молекул никак не зависят друг от друга, т.е. это независимые события, то, вероятность определенного размещения двух молекул сразу равна .
3). Пусть мы теперь имеем 4 молекулы. Пронумеруем эти частицы: 1, 2, 3, 4, считая, что это возможно сделать.
Итак, каждое “номерное” размещение частиц по половинкам сосуда – это микросостояние. Понятно, что
вероятность каждого микросостояния одинакова и в случае 4-х частиц равна: .
Построим таблицу:
| N | Макросостояние (число частиц в половинках сосуда) левая правая | Микросостояние (частицы с разными номерами в половинках сосуда) левая правая | Статистический вес (число микросостояний, соответствующих определенному макросостоянию) | Вероятность макросостояния |
| 0 4 | – 1,2,3,4 | 1/16 | ||
| 1 3 | 1 2,3,4 2 1,3,4 3 1,2,4 4 1,2,3 | 4 ×1/16 = 1/4 | ||
| 2 2 | 1,2 3,4 1,3 2,4 1,4 2,3 2,3 1,4 2,4 1,3 3,4 1,2 | | 6 ×1/16 = 3/8 | |
| 3 1 | 1,2,3 4 1,2,4 3 1,3,4 2 2,3,4 1 | 1/4 | ||
| 4 0 | 1,2,3,4 – | 1/16 |
Полная вероятность макросостояний равна, как и следует ожидать, единице:
.
Из данных таблицы видно, что наиболее вероятное макросостояние – это симметричное распределение молекул.
4). Рассмотрим, наконец, общий случай, когда в сосуде находится молекул.
Будем искать вероятность реализации макросостояния, при котором находятся: слева – частиц, справа– частиц. Выберем одно из микросостояний: слева – частицы с номерами ; справа – с номерами . Переставляя частицы местами, учтем, что макросостояние не изменяется (число частиц остается постоянным в каждой половинке сосуда), а микросостояние изменяется, если переставляются частицы из левой половины в правую, и не изменяется, если перестановки происходят только внутри каждой половины.
Сосчитаем статвес в рассматриваемого макросостояния. Полное число возможных перестановок в системе, содержащей частиц, равно . Чтобы получить число разных микросостояний в данном макросостоянии, исключим из них число перестановок внутри каждой половины, т.е., соответственно, и перестановок. Получаем, что статистический вес выбранного макросостояния равен числу сочетаний из по :
(3.2)
Очевидно, что вероятность каждого микросостояния равна
(3.3)
Тогда, вероятность рассматриваемого макросостояния ( молекул слева, а молекул справа) есть
. (3.4)
Из полученного выражения следует, что наиболее вероятным является макросостояние, соответствующее максимальному статистическому весу, который достигается при .
Пример: Пусть в сосуде находятся молекулы. Вероятность того, что все молекулы соберутся в одной половине сосуда, легко вычисляется:
статвес этого макросостояния и ,
т.е. вероятность такого события крайне мала уже при молекулах.
3.2. Распределение молекул в случае произвольных объемов.
Пусть в объеме находится молекул. Выделим в объеме меньший объем . Будем интересоваться макросостоянием, при котором в объеме находится частиц, а в остальной части объема содержится молекул. Вероятность того, что в объеме находится одна молекула находится равна отношению . Вероятность, что объем содержит две частицы: .
Если объем содержит частиц, то вероятность такого события – .
В то же время остальные молекул должны попасть в объем , вероятность чего равна
Т. о., вероятность реализации интересующего нас “микросостояния” (это условное микросостояние, т.к. клеточки пространства не одинаковы!):
(3.5)
Число способов такого распределения молекул газа в сосуде – это число соответствующих микросостояний, или статистический вес тот же, как в случае деления сосуда на равные половинки:
Итак, полная вероятность данного макросостояния записывается:
(3.6)
Итак, вероятность того, что в объеме будет обнаружено частиц из , определяется формулой (3.6).
Удобно ввести обозначения: , при этом .
Полученное распределение вероятностей называется биномиальным распределением:
. (3.7)
Биномиальное распределение (распределение Бернулли) – распределение вероятностей числа появлений некоторого события при повторных независимых испытания если вероятность появления этого события равна , .
Название распределения произошло от алгебраического бинома Ньютона:
. (3.8)
3.3. Свойства биномиального распределения.
1). Нормировка
Поскольку , то
, (3.9)
т.е. полная вероятность – вероятность обнаружения в малом объеме какого-либо числа частиц (от нуля до включительно) – нормирована на единицу.
2). Максимум вероятности.
Сразу же возникает резонный вопрос – какое из всех возможных состояний системы (макросостояний) будет реализовываться с максимальной вероятностью? Ясно, что вероятность состояния с очень малыми или при фиксированных и очень мала, т.к. при этом
или .
Т.е. максимум вероятности должен находиться при некоторых промежуточных значениях .
Вычисление максимума вероятности биномиального распределения.
Пусть нас интересуют достаточно большие и , такие что переход от вероятности к вероятности осуществляется непрерывным образом и – бесконечно малая величина. Чтобы найти максимум вероятности, вычислим разность вероятностей двух соседних состояний (при сделанных допущениях проведенная операция равносильна вычислению производной ) и приравняем ее нулю,:
(3.10)
Из равенства нулю выражения в скобках имеем
,
.
Т.к. и , получаем что
. (3.11)
Вспомним, что при ( , см. пункт 3.1), максимальная вероятность достигается тогда, когда максимален статвес , т.е. при равномерном распределении ( ) молекул газа по половинкам сосуда.
В общем случае, когда , как показывает расчет, максимум вероятности достигается при .
Из полученного результата вытекает исключительно важное следствие. Поскольку – концентрация молекул в объеме, то наиболее вероятным является состояние системы, когда число молекул в объеме равно , т.е. когда осуществляется равномерное заполнение (или распределение) молекулами всего объема сосуда.
Схематически картина распределения вероятности при достаточно больших значениях числах частиц и выглядит как показано на рисунке (дискретные точки соединены сплошной линией): в виде острого в пика окрестности c очень маленькой шириной . Условие нормировки может быть записано как
(3.12)
Если за газом наблюдать достаточно большое время, то окажется, что более вероятные распределения молекул возникают чаще, чем менее вероятные. Поэтому с течением времени газ именно и переходит в наиболее вероятные состояния, причем, достигнув наиболее вероятного состояния, газ в нем практически всегда и остается.
Такое состояние называется стационарным или равновесным.
Существенно, что равновесное состояние газа не зависит от предыстории (или начального состояния), т.е. от “пути”, которым газ шел к равновесию. Независимость от предыстории и постоянство во времени свойств газа в равновесии имеют своим следствием то, что равновесный газ можно описать небольшим числом макроскопических величин, характеризующих газ в целом (для идеального газа – ).
Определение: равновесным состоянием системы является ее наиболее вероятное состояние.
Итак, вероятность того, что число частиц в объеме будет отклоняться даже незначительно от ничтожна и быстро убывает с величиной этого отклонения. Но, тем не менее, число молекул в не всегда строго равно , а колеблется около этой величины. Отклонения числа частиц в объеме от наиболее вероятного значения – это флуктуации.
Приложение. Вычисление максимума вероятности биномиального распределения (традиционный способ).
.
Надо решить уравнение . Будем решать это уравнение для случая, когда и малы, т.е. , но при этом объем не слишком мал, так чтобы не было ничтожно мало. В этом случае максимум вероятности биноминального распределения достигается при достаточно больших и можно воспользоваться формулой Стирлинга для факториалов: .
Примечание. Формула Стирлинга получается следующим образом.
Возьмем логарифм от :
, где Dn = 1.
При больших можно считать . Тогда можно проинтегрировать полученное выражение
.
Теперь потенцируем и получаем формулу Стирлинга:
.
Используем полученное выражение:
Проводя преобразования, мы воспользовались тем, что велико (причем ) и известным пределом
.
Тогда имеем
.
Возьмем производную и приравняем её нулю , при этом вспоминая, что
.
Получаем
,
и тогда
.
Итак, развивая статистический (вероятностный) подход, мы нашли закон распределения частиц (молекул) по некоторому произвольно выбранному объему, предполагая, что в интересующем нас объеме находится газ невзаимодействующих частиц.
Среднее число частиц в произвольном объеме.
Вычислим теперь, используя распределение Бернулли, среднее число частиц в объеме по правилу, определяемому выражением (2.16)
, (3.13)
где .
Т.к. сумма, входящая в (3.13), согласно условию нормировки, равна единице, то
. (3.14)
Заменяя в (3.6) на , можем записать
. (3.15)
Сравнивая (3.11) и (3.14) сделаем ещё один важный вывод, вытекающий из статистического рассмотрения макроскопических систем. Из полученных выражений вытекает, что в состоянии равновесия наиболее вероятным числом молекул в некотором произвольно выбранном объеме является их среднее значение, что соответствует равномерному заполнению сосуда.
Источник
