Как найти константу сосуда
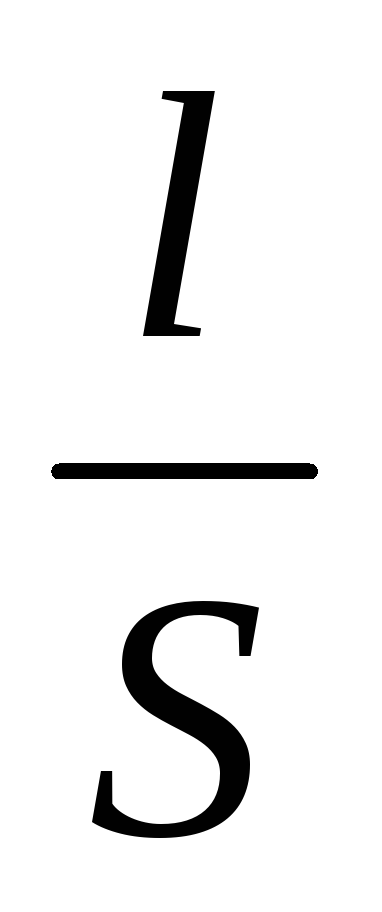
Определение константы диссоциации слабой кислоты.
Цель работы: определение электропроводности растворов уксусной кислоты различной концентрации и определение ее константы электролитической диссоциации.
Расчет постоянной сосуда.
Если измерения проводились на кондуктометре, то расчет производится следующим образом.
Удельная электропроводность рассчитывается по формуле: Х=k/R
Где R-сопротивление, k-коэффициент пропорциональности.
k=βL/S-называется постоянной сосуда.
Откуда k=xR.
Кондуктометр показывает не сопротивление R, а величину ей обратную I/R, назовем ее условно общей электропроводностью (хоб). Следовательно, постоянная сосуда через общую электропроводность выразится: K=x/ хоб Удельную электропроводность раствора КCl находим из справочных данных учитывая температуру.
Если измерения проводились на реохордном мосте, то в форму определения постоянной сосуда подставляем найденное по прибору сопротивление раствора КСl.
2. Измерение электропроводности растворов СН3СООН различной концентрации и расчет удельной и эквивалентной электропроводности.
Измерив электропроводность (сопротивление), рассчитываем и эквивалентную электропроводности растворов.
Расчет удельной электропроводности растворов СН3СООН
производим по формуле: Х=k/R
Т.к. кондуктометр показывает общую электропроводность, то удельная электропроводность будет равна х=k/ хоб. Постоянная сосуда известна из первой части работы, следовательно находим удельную электропроводность.
Эквивалентную электропроводность определяем по формуле: λ=х*1000/С
Где х – удельная электропроводность, С-концентрация раствора. Рассчитанные значения удельной и эквивалентной электропроводностей растворов СН3СООН заносим в таблицу:
| Концентрация раствора, С | Общая электропроводность, хоб, | Сопротивление сосуда, R | Хс | λ с | αс | К дис |
3. Расчет константы диссоциации уксусной кислоты.
Для того, чтобы рассчитать константу диссоциации, надо вычислить λ 0 –эквивалентную электропроводность при бесконечном разбавлении. Т.к. уксусная кислота-электролит слабый,
то λ 0 находим по уравнению λ 0=е0А + е0в
Подвижности ионов находим по справочнику.
Для слабых электролитов, диссоциирующих по схеме
АВ→
←А+ +В-
Константа электролитической диссоциации равна:
Кдис= (α2 *С)/(+1-α)
Т.к. для слабых электролитов: α= λ / λ 0
То константа диссоциации Кдис=( λ 2 *С)/( λ 0 *( λ 0- λ)
Величины λ 0 и Кдис можно определить и графическим путем. Для этого последнее уравнение можно свести к линейному виду:
I/ λ = I/ λ 0 +(1/(Кдис* λ 02))* λ *С
Прямая, построенная в координатах I/ λ – λ *С
, даст возможность определить величину I/ λ 0 посредством ее экстраполяции на ось ординат I/ λ 0 . А из I/ λ 0 определяем λ 0 . По тангенсу угла наклона прямой вычислить значение I/Кдис. λ 02. А из нее вычисляем Кдис.
Значения λ 0 и Кдис, полученные графическим путем сравним с их значениями, полученными соответственно по уравнениям.
4. Оформление работы
1. Краткое изложение теории данного вопрос.
2. Расчет для каждой концентрации кислоты:
А) удельная электропроводность
Б) эквивалентная электропроводность
В) степени диссоциации
Г) константы диссоциации
3. Расчет постоянной сосуда
4. Найти в справочнике табулированную величину константы диссоциации уксусной кислоты.
5. Рассчитать относительную ошибку опыта.
Решить задачу
Экспериментальная часть (замеры на приборе)
| Концентрация р-ра, С | Сопротивление в См |
| 1 | 1,15*10-3 |
| 0,5 | 862,0*10-6 |
| 0,25 | 682,0*10-6 |
| 0,125 | 511,0*10-6 |
| 0,0625 | 388,0*10-6 |
Сопротивление сосуда 2,09*10-3
Задача №12.
Эквивалентная электрическая проводимость 1,59*10-4 М уксусной кислоты при 298 К равна 109,78 Ом-1 *см2*г-экв-1. Вычислите константу диссоциации и рН раствора, данные о подвижностях ионов возьмите из справочника [М.].
Расписать все подробно, с текстовыми объяснениями.
Источник
Измерению
электропроводности растворов предшествует
определение константы электролитического
сосуда. Если бы расстояние между
электродами точно равнялось 1 см, а
площадь каждого электрода была 1 см2
и в проведении тока участвовал бы только
раствор, заключенный между этими
электродами, то измеренная в таких
условиях электропроводность была бы
удельной. В действительности измерение
электропроводности производят в сосудах
различной формы с электродами, площадь,
форма которых, а также расстояние
между ними могут быть различными.
Сопротивление
проводника прямо пропорционально его
длине и обратно пропорционально сечению
R
= ρ·![]() .
.
(2)
Отношение
![]()
для данного электролитического сосуда
есть величина постоянная и называется
константой
сосуда С,
откуда
R
= ρ·
С
и С=R
/ ρ.
(3)
Константу
сосуда С
можно легко определить, измерив
сопротивление раствора, удельная
электропроводность которого известна.
Для определения постоянной сосуда
обычно используют 1/50 н. и 1/100 н. растворы
стандартного электролита—КСl.
Величина удельной электропроводности
этих растворов при различных
температурах приведена в табл. 1.
Раствор
готовят из химически чистого КСl,
прокаленного при температуре темно-красного
каления и сохраняемого в эксикаторе
над серной кислотой. Воду, используемую
для приготовления растворов, очищают
двойной дистилляцией.
Таблица
1
Удельная электропроводность водных растворов кСl при концентрации 1/50 и 1/100 моль/л
t°, | χ | t°, | χ | ||
1/50 | 1/100 | 1/50 | 1/100 | ||
15 | 0,002243 | 0,001147 | 21 | 0,002553 | 0,001305 |
16 | 0,002294 | 0,001173 | 22 | 0,002606 | 0,001332 |
17 | 0,002345 | 0,001199 | |||
18 | 0,002397 | 0,001225 | 23 | 0,002659 | 0,001359 |
19 | 0,002449 | 0,001251 | 24 | 0,002712 | 0.001386 |
20 | 0,002501 | 0,001278 | 25 | 0,002765 | 0,001413 |
Константа сосуда рассчитывается по уравнению
С
= R·χКCl.
(4)
Следовательно,
величина удельной электропроводности
раствора любого электролита равна
χ= С /Rx.
(5)
Лабораторная работа № 15. Определение коэффициента электропроводности сильного электролита.
Цель
работы:
Определить:
1) константу электролитического
сосуда; 2) удельную электропроводность
воды, которую используют для приготовления
растворов электролита; 3) удельную
электропроводность растворов электролита.
Приборы и посуда:
Прибор
для определения электропроводности
растворов электролитов;Мерный
цилиндр на 100 мл;Пипетка;
Коническая
колба;Термостат.
Реактивы
и материалы:
Дистиллированная
вода;Раствор
хлорида калия (С
= 0,02 моль/л);Раствор
хлорида калия (С
= 0,01 моль/л);Раствор
сильного электролита заданной
концентрации;
Методика выполнения работы
Определение
константы сосуда и измерение
электропроводности проводят в
растворах различной (убывающей)
концентрации. Такие растворы готовят
путем последовательного разбавления
вдвое исходных растворов.
Как
указано выше, константу сосуда находят
измерением сопротивления растворов
КСl,
удельная электропроводность которого
табулирована. Тщательно промытый
дистиллированной водой электролитический
сосуд дважды споласкивают 1/50 н. раствором
КСl.
Затем мерным цилиндром или пипеткой
наливают в сосуд определенный объем
этого раствора так, чтобы уровень
жидкости был выше верхнего края электродов
на 5—10 мм (например, 50 мл).
При
всех измерениях электропроводности
объем жидкости в сосуде должен быть
одним и тем же,
он определяется объемом электролитического
сосуда. Устанавливают сосуд в термостат
и выдерживают там 10—15 мин при заданной
температуре или проводят определение
при комнатной температуре. Повышение
температуры на 1° С вызывает увеличение
удельной электропроводности водных
растворов на 2—2,5 %, поэтому при измерениях
необходимо следить за постоянством
температуры.
Сосуд
подключают к мосту и измеряют сопротивление
раствора, не вынимая из термостата, если
определение ведется при заданной
температуре. Затем 1/50 н. раствор КСl
разбавляют вдвое.
Разбавление
растворов проводят в мерном цилиндре
на 100 мл с притертой пробкой, для чего в
него наливают 50 мл дистиллированной
воды, затем туда вливают 50 мл раствора
электролита из электролитического
сосуда, т.е. разбавляют исходный раствор
вдвое. Мерный цилиндр закрывают пробкой,
и раствор энергично перемешивают
встряхиванием.
Разбавление
растворов можно осуществлять и с помощью
пипетки, объем которой равен объему
электролитического сосуда, т. е. 50 мл
при объеме сосуда 50 мл. Этой пипеткой
заполняют электролитический сосуд
исследуемым раствором. После измерения
сопротивления раствор выливают в
коническую колбу на 150—200 мл, другой
пипеткой добавляют туда 50 мл
дистиллированной воды, т.е. раствор
разбавляют вдвое. При разбавлении одна
пипетка на 50 мл должна быть использована
только для исследуемого раствора, другая
(также на 50 мл) — для добавления воды.
Колбу энергично встряхивают для
перемешивания раствора.
Полученным
разбавленным раствором споласкивают
2—3 раза электролитический сосуд,
вносят 50 мл раствора и измеряют
сопротивление. Если измерение
электропроводности растворов проводится
при заданной температуре, то
электролитический сосуд должен постоянно
находиться в термостате. Перед первым
измерением сосуд в термостате выдерживают
10—15 мин.
Вода,
используемая для разбавления растворов,
должна иметь температуру раствора, т.
е. комнатную, или температуру термостата
(колба с водой находится в термостате).
Результаты
измерений сопротивления растворов КСl
заносят в табл. I (см. форму отчета).
После
определения постоянной сосуда приступают
к измерению сопротивления растворов
электролита. Исследуемый раствор
1-1-валентного электролита (какого-либо
галогенида щелочного металла) и его
исходная концентрация указываются
преподавателем. Измеряют сопротивление
растворов электролита при убывающей
концентрации. Операцию разбавления
повторяют 6 раз. Результаты измерения
заносят в табл. II.
Для сильных
электролитов отношение λ/λ∞, характеризует
коэффициент электропроводности fλ.
При обработке
экспериментальных данных рассчитать
константу диссоциации по закону
разведения Оствальда для первого,
третьего и пятого разбавления раствора
и показать, что закон разведения Оствальда
к сильным электролитам не приложим.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
Если бы расстояние между электродами точно равнялось 1 см, а площадь каждого электрода – 1 см2 и в прохождении тока участвовал только один объем раствора, заключенный между электродами, то электропроводность, измеренная в таких условиях, представляла бы собой удельную электропроводность раствора. Практически
Причем все ионы остаются между электродами, участвуя в переносе электричества. Следовательно, возрастание эквивалентной электропроводности раствора данного электролита при разбавлении определяется степенью электролитической диссоциации и вместе с ней, по мере разбавления, стремится к пределу, после которого остается постоянной. Это предельное значение электропроводности называется электропроводностью при бесконечном разведении и обозначается . Электропроводность при бесконечном разведении вычисляется как сумма подвижностей ионов (катионов – и анионов – ):
Определив эквивалентную электропроводность раствора и, зная подвижность ионов, можно вычислить степень диссоциации по формуле:
.
Степень диссоциации слабого электролита в водном растворе с разбавлением V определяется частным от деления значения эквивалентной электропроводности при этом разбавлении на значение электропроводности при бесконечном разведении.
В растворах слабых электролитов имеются недиссоциированные молекулы, а также катионы и анионы, образовавшиеся вследствие электролитической диссоциации некоторой части молекул. Между ними в растворе устанавливается динамическое (подвижное равновесие, характеризуемое при данной температуре и данной общей концентрации электролита постоянной величиной – константой электролитической диссоциации, которую можно вычислить на основании закона действующих масс. Для молекул, способных диссоциировать на два иона, КА Û К+ + А-:
, где /4/
К – константа электролитической диссоциации;
– концентрация катионов;
– концентрация анионов;
– концентрация недиссоциированных молекул.
Если концентрацию электролита в объеме V принять равной С:
= = a . С, тогда концентрация недиссоциированных молекул определяется по формуле:
= (1 – a) . С , учитывая это, получим для константы диссоциации:
. /5/
Учитывая, что V = 1/С, получим:
. /6/
Подставим значение степени диссоциации в /6/:
= /7/
Последние два уравнения носят название закона разведения Оствальда. Целью данной работы является проверка настоящего закона.
Экспериментальная часть
Методика измерений
Так как электропроводность – это величина, обратная сопротивлению, то, практически, определение электропроводности сводится к определению сопротивления. Наиболее пригодным в этом случае является метод, основанный на применении переменного тока по схеме мостика Уитстона. Допустим, ток идет из источника Е к точке А (рис.1), где он разветвляется и часть тока идет через D к С, а другая – через В к С. От точки С ток идет обратно к источнику тока.
Рис.1
Сопротивления частей цепи будут:
АВ = R1, BC = R2, AD = R3, DC = R4.
Если точки D и В соединить проводником, то по нему может пойти ток. По закону Кирхгофа, в проводнике ВD тока не будет в том случае, когда будет соблюдаться следующее соотношение:
.
Зная три из этих сопротивлений, можно вычислить четвертое. На опыте в качестве R2 берется определенное сопротивление магазина; R1 – сосуд с электролитом, электропроводность которого нужно определить; R3 и R4 – берется реохорд, плечи которого будут соответственно a и b. Для измерения сопротивления жидкостей применяют переменный ток, а не постоянный, чтобы избежать электролиза и поляризации.
Очень чувствительным прибором, обнаруживающим присутствие или отсутствие тока в мостике, является низкоомный телефон, вибрационный гальванометр или осциллограф. В качестве источника переменного тока применяется звуковой генератор ЗГ-1. Схема присоединения приборов для измерения сопротивления жидкостей изображена на рис. 2.
Лабораторная работа № 16
Дата добавления: 2016-11-20; просмотров: 757 | Нарушение авторских прав | Изречения для студентов
Читайте также:
Рекомендуемый контект:
Поиск на сайте:
© 2015-2021 lektsii.org – Контакты – Последнее добавление
Источник
