Как рассчитать давление в сосуде после реакции
Задачи и упражнения по химической кинетике
Скорость химической реакции. Закон действующих масс (закон Гульдберга и Вааге)
1. Как изменится скорость образования диоксида азота в реакции оксида азота(II) с кислородом, если давление в системе увеличить в 3 раза, а температуру оставить неизменной?
Ответ. Возрастет в 27 раз.
2. Как изменится скорость элементарной реакции А2 + 2В2 = 2АВ2, протекающей в газовой фазе в закрытом сосуде, если увеличить давление в 6 раз?
Для реакции, описываемой уравнением:
1= k•[A2]•[B2] 2 .
При увеличении давления в сосуде в 6 раз концентрации всех веществ также возрастут в 6 раз. Выражение для скорости реакции примет вид:
2= k•6[A2]•(6[B2]) 2 = 216k•[A2]•[B2] 2 .
Ответ. Возрастет в 216 раз.
3. Определить среднюю скорость химической реакции восстановления углекислого газа водородом до угарного газа и воды, если через 80 с после начала реакции молярная концентрация воды была равна 0,24 моль/л, а через 2 мин 7 с стала равна 0,28 моль/л.
Ответ. 0,051 моль/(л•мин).
4. Как изменится скорость реакции получения аммиака из простых веществ, если при неизменной температуре уменьшить объем газовой смеси в 3 раза?
Ответ. Увеличится в 81 раз.
5. Во сколько раз изменится скорость химической реакции 2А + В = А2В, если концентрацию вещества А увеличить в 2 раза, а концентрацию вещества В уменьшить в 2 раза?
Ответ. Возрастет в 2 раза.
1. Во сколько раз увеличится скорость химической реакции образования йодоводорода из простых веществ при повышении температуры от 20 °С до 170 °С, если при повышении температуры на каждые 25 °С скорость реакции увеличивается в 3 раза?
Ответ. Увеличится в 716 раз.
2. Коэффициент Вант-Гоффа для некоторой реакции равен 2,5. Во сколько раз увеличится скорость этой реакции при повышении температуры от 10 °С до 55 °С?
Выражение для скорости реакции
2по сравнению со скоростью реакции 1при изменении температуры Тимеет вид:
Ответ. Возрастет в 61,76 раза.
3. Скорость некоторой реакции возрастает в 3,5 раза при повышении температуры на каждые 20 °C. Как изменится время протекания данной реакции при повышении температуры от 20 °C до 85 °С?
Ответ. Уменьшится в 58,475 раза.
4. Растворение образца цинка в соляной кислоте при 20 °С заканчивается через 27 мин, а при 40 °С такой же образец металла растворяется за 3 мин. За какое время данный образец цинка растворится при 55 °С?
5. Растворение образца железа в серной кислоте при 20 °С заканчивается через 15 мин, а при 30 °С такой же образец металла растворяется за 6 мин. За какое время данный образец железа растворится при 35 °С?
Состояние равновесия. Равновесные концентрации
1. Равновесие реакции образования йодоводорода из простых веществ установилось при следующих концентрациях: [H2] = 0,4 моль/л, [I2] = 0,5 моль/л, [HI] = 0,9 моль/л. Определить исходные концентрации водорода и йода и рассчитать константу равновесия данной реакции.
Для реакции образования йодоводорода:
[H2] = 0,4 моль/л, [I2] = 0,5 моль/л, [HI] = 0,9 моль/л.
Прореагировало в объеме: 0,45 моль/л Н2 и 0,45 моль/л I2, получилось 0,9 моль/л HI.
2. В реакции А + В = С + D смешали по 1 моль всех веществ A-D. После установления равновесия в смеси оказалось 1,5 моль вещества С. Определить константу равновесия данной реакции.
3. Равновесие реакции образования аммиака из простых веществ устанавливается при следующих концентрациях: [N2] = 0,01 моль/л, [Н2] = 2 моль/л, [NН3] = 0,4 моль/л. Вычислить константу равновесия и исходные концентрации азота и водорода.
4. Равновесие реакции образования диоксида азота из монооксида и кислорода установилось при следующих концентрациях реагирующих веществ: оксида азота(II) – а моль/л, кислорода – в моль/л, оксида азота(IV) – с моль/л. Как изменятся скорости прямой и обратной реакций, если уменьшить объем, занимаемый газами, в 2 раза? Сместится ли при этом равновесие?
Ответ. Возрастут в 8 и 4 раза,
равновесие сместится вправо.
5. Исходные концентрации азота и водорода в реакционной смеси для получения аммиака составляли 4 и 10 моль/л соответственно. Вычислить равновесные концентрации компонентов смеси и константу равновесия данной реакции, если к моменту наступления равновесия прореагировало 50% азота.
Принцип Ле Шателье
1. Какие факторы способствуют смещению равновесия в эндотермической реакции восстановления углекислого газа до угарного с помощью углерода в сторону образования продукта реакции?
СО2 (г.) + С (тв.)
2СО (г.) – Q
смещению равновесия вправо способствуют:
а) нагревание; б) понижение давления;
в) увеличение концентрации СО2;
г) вывод СО из сферы реакции.
2. Какие факторы способствуют смещению равновесия в эндотермической реакции восстановления оксида железа(III) с помощью водорода в сторону прямой реакции?
Fe2О3 (тв.) + 3Н2 (г.)
2Fe (тв.) + 3Н2О (г.) – Q
смещению равновесия вправо способствуют:
а) нагревание; б) увеличение концентрации Н2; в) вывод Н2О из реакции.
3. Какие факторы способствуют смещению равновесия в экзотермической реакции образования сероводорода из простых веществ в сторону образования продукта реакции?
Н2 (г.) + S (тв.)
Н2S (г.) + Q
смещению равновесия в сторону образования Н2S способствуют:
а) охлаждение; б) увеличение концентрации Н2; в) вывод Н2S из реакции.
4. Для каких из указанных реакций повышение давления приведет к смещению равновесия в том же направлении, что и понижение температуры?
а) N2 + O2
2NO – Q;
б) CO2 + C
2CO – Q;
в) 2CO + O2
2CO2+ Q;
г) CO + H2O (г.)
CO2+ H2+ Q.
Комбинированные задачи повышенной сложности
1. Один моль смеси пропена с водородом, имеющей плотность по водороду 15, нагрели в замкнутом сосуде с платиновым катализатором при 320 °С, при этом давление в сосуде уменьшилось на 25%. Рассчитать выход продукта гидрирования в процентах от теоретического.
2. Пары этаналя смешали с водородом в молярном отношении 1:2 при давлении 300 кПа и температуре 400 °С в замкнутом реакторе, предназначенном для синтеза этанола. После окончания процесса давление газов в реакторе при неизменной температуре уменьшилось на 20%. Определить объемную долю паров этанола в реакционной смеси и процент превращения уксусного альдегида в этанол.
Ответ. Объемная доля паров этанола
в конечной реакционной смеси – 25%,
степень превращения альдегида в этанол – 60%.
3. При нагревании до некоторой температуры 36 г уксусной кислоты и 7,36 г безводного этанола в присутствии серной кислоты получена равновесная смесь. Эта смесь при действии избытка раствора хлорида бария образует 4,66 г осадка, а при действии избытка раствора гидрокарбоната калия выделяет 12,1 л углекислого газа (н.у.). Найти количество сложного эфира в равновесной смеси.
4. Угарный газ смешали с водородом в молярном соотношении 1:4 при давлении 10 МПа и температуре 327 °С в замкнутом реакторе, предназначенном для синтеза метанола. После окончания процесса давление газов в реакторе при неизменной температуре уменьшилось на 10%. Определить объемную долю паров метанола в реакционной смеси и процент превращения угарного газа в метанол.
Источник
➤Adblock
detector
| в | в | а | б | а | в, г | б, в, г | б | г |
Источник
Химическое равновесие – состояние химической системы, при котором скорость прямой реакции равна скорости обратной.
В большом количестве заданий, которые мне довелось увидеть, я ни один раз видел, как коверкают это определение. Например, в заданиях верно-неверно предлагают похожий вариант, однако говорят о “равенстве концентраций исходных веществ и продуктов” – это грубая ошибка. Химическое равновесие – равенство скоростей.
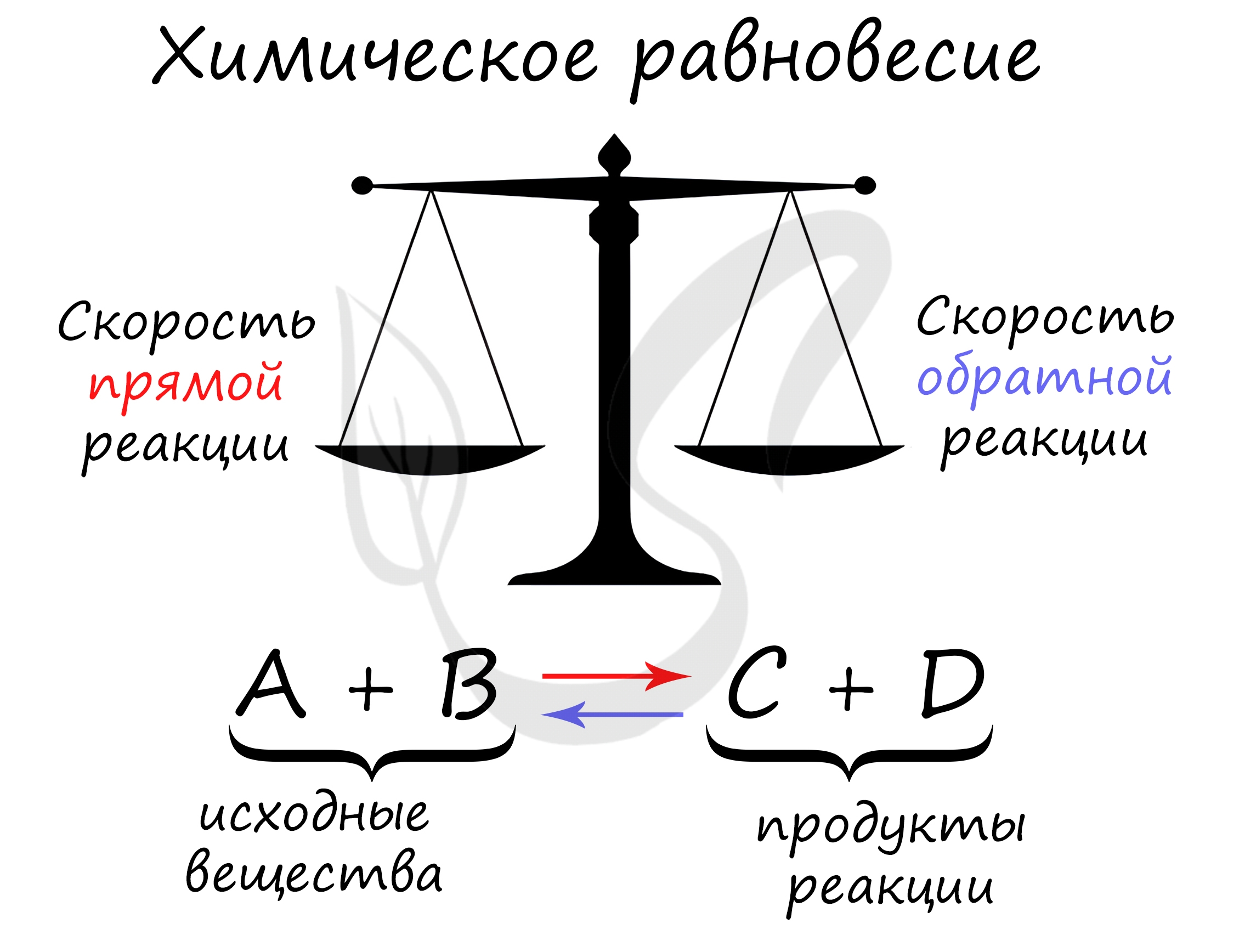
Принцип Ле Шателье
В 1884 году французским химиком Анри Ле Шателье был предложен принцип, согласно которому, если на систему, находящуюся в состоянии равновесия, оказать внешнее воздействие (изменить температуру, давление, концентрацию), то система будет стремиться компенсировать внешнее воздействие.

Это принцип обоснован термодинамически и доказан. Однако в такой абстрактной формулировке его сложно применить для решения конкретных задач по химическому равновесию. В этой статье я покажу конкретные примеры и обозначу алгоритм действия, чтобы вы могли успешно справляться с заданиями.
Влияние изменения концентрации на химическое равновесие
При увеличении концентрации какого-либо компонента химической реакции, система будет стремиться восстановить равновесие: равновесие будет смещаться в сторону расходования добавленного компонента.
Объясню проще: если вы увеличиваете концентрацию вещества, которое находится в левой части, равновесие сместится в правую сторону. Если добавляете вещество из левой части (продуктов реакции) – смещается в сторону исходных веществ. Посмотрите на пример ниже.

Если мы попытаемся удалить какое-либо вещество из системы (уменьшить его концентрацию), то система будет стремиться заполнить “пустое” место, которые мы создали. Наглядно демонстрирую на примере:
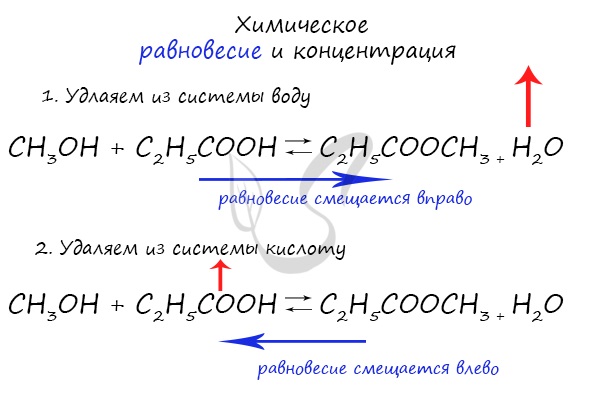
Можно подвести итог полученным знаниям таким образом: “Куда добавляем – оттуда смещается, откуда берем – туда смещается”. Воспользуйтесь этой или придумайте свое правило для запоминания этой закономерности 😉
Изменения давления и химическое равновесие
Если речь в задании идет об изменении давления, то первое, что нужно сделать, это посчитать количество газов в уравнении слева и справа. Твердые вещества и жидкости считать не нужно. Например:
CO2(г) + С(тв) ⇄ 2CO(г) – Q
В приведенном уравнении количество молекул газа в левой части – 1, в правой – 2.
Запомните правило: “При увеличении давления равновесие смещается в сторону меньших газов, при уменьшении давления – в сторону больших газов”. Для нашей системы правило действует таким образом:

В случае, если слева и справа количество молекул газа одинаково, например, в реакции:
H2(г) + I2(г) ⇄ 2HI(г) – Q
Слева – 2 газа, и справа – 2. В такой реакции увеличение или уменьшение давления не повлияет на химическое равновесие.
Изменение температуры и химическое равновесие
Если в задании увеличивают или уменьшают температуру, то первое, что вы должны оценить: экзотермическая это реакция или эндотермическая.
Следуйте следующему правилу: “При увеличении температуры равновесие смещается в сторону эндотермической реакции, при уменьшении – в сторону экзотермической реакции”. У любой обратимой реакции есть экзо- и эндотермические части:
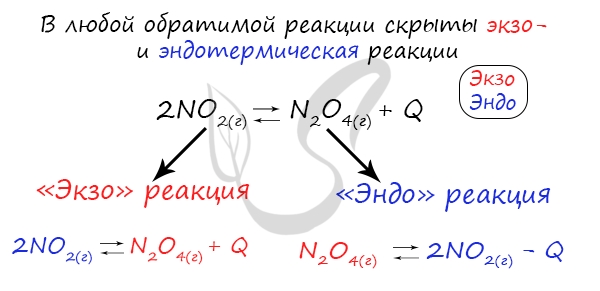
Поэтому данное правило универсально и применимо для всех реакций. Для примера разберем следующие задачи:

Чтобы не осталось белых пятен, возьмем экзотермическую реакцию и повторим с ней подобный эксперимент.
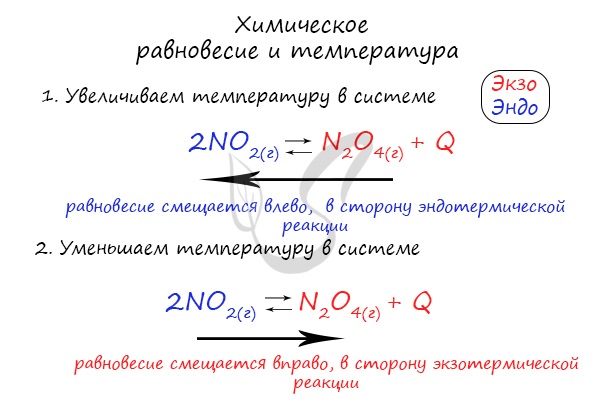
Катализатор и ингибитор
Действие катализатора и ингибитора соответственно касается только ускорения и замедления химической реакции. Они никоим образом не влияют на равновесие.
Константа равновесия
Константой равновесия называют отношения скоростей прямой и обратной реакции. Для реакции типа aA + bB = cC + dD константа равновесия будет записана следующим образом:

Решим задачу. Дана реакция: 2NO + Cl2 ⇄ 2NOCl . Вычислите константу равновесия, если равновесные концентрации веществ для данной реакции: c(NO) = 1.8 моль/л , c(Cl2) = 1.2 моль/л , c(NOCl) = 0.8 моль/л.

Константу равновесия для данной задачи можно представить в виде 1.64 * 10-1.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Источник
ЛЕКЦИЯ 6
Химическое равновесие
План лекции:
1. Закон действующих масс. Различные способы выражения константы равновесия для идеальных систем.
2. Связь константы равновесия с применением энергии Гиббса. Уравнение изотермы химической реакции.
3. Зависимость константы равновесия от температуры. Уравнение изобары химической реакции.
4. Понятия для активности и летучести (фугитивности).
Большинство химических реакций протекают одновременно в двух направлениях: в сторону образования продуктов реакции (прямая реакция) и в сторону разложения последних (обратная реакция). Вследствие химической обратимости реакции не доходят до конца. Скорость прямой реакции уменьшается, а скорость обратной, напротив, возрастает. Когда эти скорости выравниваются наступает состояние химического равновесия.
Так как химически обратимые реакции до перехода в равновесное состояние протекают с конечными скоростями, то с точки зрения термодинамики они не обратимы. Однако можно мысленно представить, что эти реакции идут бесконечно медленно через смежные равновесные состояния. Тогда к ним можно применить общие условия термодинамического равновесия.
Для гомогенных обратимых реакций экспериментально Гульбергом и Ваге был установлен закон действующих масс. При постоянной температуре отношение произведения равновесных концентраций (или парциальных давлений) продуктов реакции к произведению равновесных концентраций (или парциальных равновесий) исходных веществ есть величина постоянная.
Этот экспериментально установленный закон может быть получен методом термодинамических потенциалов. Рассмотрим реакцию в газовой фазе:
аА(г) + bВ ↔ сС + dD
Когда система достигает термодинамического равновесия, то термодинамический потенциал при фиксированных естественных переменных достигает минимума. Равновесие, таким образом, можно охарактеризовать выражением химических потенциалов, когда потенциалы продуктов реакции сравняются с потенциалами исходных веществ:
с μ (с) + d μ (D) – a μ (a) – b μ (b) = 0 (6 – 1)
Если естественными переменными являются p и T, то = , а = V
Отсюда для систем, подчиняющихся закону идеальных газов, можно получить выражения для μi
μi = μi° + RTlnCi (6 – 2)
где μi° – стандартный химический потенциал.
Подставляется (6 – 2) в (6 – 1) и перенося постоянные величины в левую часть, получаем
сμC° + dμD° – aμA° – bμB° = -RTln (6 – 3)
Поскольку в левой части выражение не зависит от концентраций, то выражение под логарифмом является постоянной величиной при постоянной температуре:
Для идеального газа парциальные давления пропорциональны концентрациям, поэтому константа равновесия может быть всегда выражена через равновесные парциальные давления:
Аналогично может быть записано выражение через мольные доли:
Для идеальных газов эти константы связаны между собой соотношением:
где
Следует обратить внимание, что в полученных соотношениях только KN зависит от общего давления. Она позволяет нам оценивать сдвиг равновесия в газовых реакциях при изменении общего давления. Следует иметь в виду, что давление в этих выражениях складывается из парциальных давлений компонентов системы и не учитывает влияние инертных газов, если они присутствуют в реакционной смеси. Естественно инертный газ «разбавляет» компоненты реакционной смеси и поэтому влияет на KN.
Из уравнения (6 – 3) вытекает связь константы равновесия с ∆rG°:
(6 – 4)
Это уравнение было впервые получено Вант – Гофором методом циклов и получило название уравнения изотермической химической реакции. Очевидно, в этом уравнении ∆rGT° относится к этой температуре, при которой определена Кр. Уравнение изотермической химической реакции позволяет определить константу равновесия при заданных условиях не прибегая к исследованию равновесия. Величина ∆rGT° может быть рассчитана на основе термических констант для индивидуальных веществ.
Если заданы концентрации (парциальные давления) отличные от равновесных, то можно записать более общий вид уравнения изотермической химической реакции:
Это выражение позволяет определить направление самопроизвольного процесса.
Уравнение изотермы химической реакции позволяет получить выражение для температурной зависимости константы равновесия.
Запишем уравнение Гиббса – Гельмгольца:
Подставим выражение для из (6 – 4)
(6 – 5)
Дифференцируем уравнение (6 – 5)
(6 – 5´)
Из уравнения (6 – 5´) получаем уравнение изобары химической реакции:
(6 – 6)
Если проинтегрировать уравнение (6 – 6) в предположении, что ∆rHT° не зависит от температуры, то получим уравнение:
где С – константа интегрирования.
Уравнение (6 – 7) хорошо выполняется в узких интервалах температур и позволяет определить ∆rGT°.
Для широких интервалов температур ln Kр представляют в виде степенных рядов или других аналитических формах:
Например:
Такие выражения позволяют рассчитать все термодинамические функции для процессов, для которых данные зависимости получены.
Выражения для термодинамических потенциалов, полученные для идеального газа. Для реальных газов, а особенно для газовых растворов возникают затруднения. Это связано с тем, что расчет концентраций и давлений должен быть проведен исходя из уравнения состояния. Однако для реальных систем единое достаточно простое уравнение состояния получить не удалось.
В связи с этим в термодинамике реальных систем применяется эмпирический метод, предложенный Льюисом. Льюис предложил в уравнениях термодинамики, полученных для идеальных систем заменить давления p на величину летучести f, а концентрации С на активности a.
При такой замене выражения для констант равновесия не меняются по форме. Но этот прием позволяет связать экспериментально найденные свойства реального газа с термодинамическими параметрами.
Летучести и активности – это экспериментальные величины, которые находятся из условия, что для раствора при бесконечном разбавлении или газа при давлении стремящимся к 0 активность приближается к аналитической концентрации, а летучесть к реальному давлению идеального газа. Исходя из этой посылки рассчитываются активности и летучести.
Пример 6 – 1.
При 1273 К и общем равновесии 30 атм. В равновесной системе
содержится 17% (по общему) . Сколько процентов будет содержаться в газе при общем давлении 20 атм.? При каком давлении в газе будет содержаться 25% ? (Газ считать идеальным).
Решение.
В соответствии с законом Авогадро, объёмный процент равен мольному проценту. Следовательно, при 30 атм. будет равен:
Отсюда находим
В отличие от , для идеальных газов не зависит от давления. На основании этого находим при 20 атм.
= 0,125 или 12,5%
Для 25%
Следовательно,
Пример 6 – 2.
При 2000°С и общем давлении 1 атм. 2% воды диссоцииовано на водород и кислород. Рассчитайте константу равновесия реакции при этих условиях.
Решение.
Исходное количество | 1 | ||
Равновесное количество | |||
Равновесная мольная доля |
Следовательно,
Пример 6 – 3
Константа равновесия реакции
При 500°С равна Смесь, состоящую из 1 моля СО и 5 моль нагрели до этой температуры. Рассчитайте мольную долю в равновесной смеси.
Решение.
Исходное количество | 1 | 5 | ||
Равновесное количество | 1 – х | 5 – х | х | х |
Поскольку , то
, следовательно, Х = 0.96
Следовательно,
Пример 6 – 4.
Рассчитайте стандартную энтальпию реакции, для которой константа равновесия
а) увеличивается в 2 раза,
б) уменьшается в 2 раза,
при изменении температуры от 298 К до 308 К.
Решение.
, после интегрирования получаем
или
а) Дж∙мольˉ¹
б) Дж∙мольˉ¹
Пример 6 – 5.
Оксид ртути диссоциирует до реакции
При 420°С давление газов Па, а при 450°С Па. Рассчитайте константы равновесия при этих температурах и энтальпию диссоциации HgO.
В соответствии с уравнением реакции.
Исходное количество газообразных продуктов | – | ||
Равновесное количество газообразных продуктов | – | 2 | 1 |
Мольные доли газообразных продуктов | – |
Парциальные давления газообразных продуктов при 420°С, Па | |
Парциальные давления газообразных продуктов при 450°С, Па |
За стандарт принят , поэтому
Рассчитываем
С учетом того, что диссоциирует 2 моля HgO, энтальпия диссоциации HgO составляет 154 кДж∙мольˉ¹.
Следует обратить внимание на то, что если рассчитывать исходя из ранее принятого стандартного давления = 1атм., то их значения будут отличаться:
Пример 6 – 6:
Зависимость константы равновесия реакции от температуры между 300К и 600К описывается уравнением:
Рассчитайте , и реакции при 400 К.
Решение:
По уравнению изотермы химической реакции:
Отсюда находим непосредственно температурную зависимость
Для расчета удобнее продифференцировать по . В этом случае . Отсюда
Расчет проводим на основании уравнения Гиббса – Гельмгольца:
Пример 6 – 7:
Рассчитайте константу равновесия реакции , если известно, что при получении жидкого формальдегида при 198 К, а давление пара формальдегида при этой температуре равно 1500 Торр.
Решение:
Имеем следующие данные:
Из этого следует, что при получение газообразного формальдегида складывается из этих величин:
Отсюда
Пример 6 – 8:
Константа равновесия реакции при 25°С равна , рассчитайте давление, которое установится в сосуде 1л, содержанием 1г. при этой температуре.
Решение:
Исходные концентрации моль∙¹ | ||
Равновесные концентрации моль∙¹ | 2Х |
Х = 0,00330 | |
∑=0,01417 |
Источник
