Как соединяют сосуды при операции
ШУНТИРОВАНИЕ КРОВЕНОСНЫХ СОСУДОВ – хирургическая операция по созданию с помощью различных сосудистых трансплантатов нового пути кровотока в обход пораженного патологическим процессом сегмента артериального или венозного сосуда при частичном или полном нарушении его проходимости. В отличие от протезирования кровеносных сосудов при их шунтировании патологически измененные участки сосуда не резецируют и анастомозы трансплантата с шунтируемым сосудом накладывают по способу конец в бок. При шунтировании создают новый путь кровотока, который не соответствует анатомическому кровеносному руслу, но вполне полноценен в гемодинамическом и функциональном отношении.
Впервые шунтирование кровеносных сосудов в эксперименте выполнил Егер (E. Jeger) в 1913 году, а в клинике – Кюнлен (J. Kunlin) в 1949 году.
Показаниями к шунтированию кровеносных сосудов являются тромбоз и стеноз артерий и вен различной этиологии, когда обширность поражения, технические трудности или общее состояние больного не позволяют восстановить кровоток по естественному анатомическому пути.
Операции по шунтированию кровеносных сосудов выполняют в плановом и экстренном порядке. Примером экстренной операции может служить аортокоронарное шунтирование (см. Артериализация миокарда) при предынфарктном состоянии с целью предупреждения развития инфаркта миокарда. При инфаркте миокарда эта операция способствует ограничению распространения некроза и ускоряет процесс рубцевания миокарда (см. Инфаркт миокарда, хирургическое лечение). Экстренное шунтирование кровеносных сосудов производят также при нагноении в области ранее имплантированного трансплантата или протеза сосуда, осложненном аррозионным кровотечением, при остром тромбозе и травмах крупных сосудов.
Шунтирование кровеносных сосудов выполняют с помощью аутотрансплантатов, аллотрансплантатов или ксенотрансплантатов (см. Трансплантат). В качестве аутотрансплантата используют вены пациента, чаще большую подкожную вену ноги в виде свободного трансплантата или трансплантата «на ножке». Например, при окклюзии подколенной и бедренной вен накладывают анастомоз между дистальной частью большой подкожной вены ноги и глубокими венами голени. При односторонней окклюзии подвздошных вен можно использовать метод, предложенный в 1960 году Пальмой и Эспероном (E. Palma, В. Esperon), заключающийся в том, что дистальный конец большой подкожной вены здоровой ноги перемещают на противоположную сторону через тоннель в подкожной клетчатке над лонным сочленением и анастомозируют с бедренной веной больной ноги. Перемещение большой подкожной вены «на ножке» иногда применяют и при гипертензионном синдроме верхней полой вены (см. Полые вены), например при ее тромбозе или сдавлении злокачественной опухолью. В этом случае большую подкожную вену ноги после мобилизации ее дистального отдела проводят через тоннель в подкожной клетчатке переднебоковой поверхности брюшной и грудной стенок и соединяют с яремной или подключичной веной.
Для создания шунтов «на ножке» используют также малую подкожную вену ноги, наружную яремную вену, латеральную и медиальную вены плеча, а также внутреннюю грудную артерию при подключичнокоронарном шунтировании. Перечисленные вены применяют и в качестве свободных шунтов-трансплантатов при самых различных окклюзионных поражениях магистральных венозных стволов системы верхней и нижней полых вен, в частности при болезни Педжета – Шреттера (см. Педжета – Шреттера синдром), при односторонних окклюзиях подвздошных вен, окклюзиях бедренной, подколенной вен и глубоких вен голени.
Аутовенозное шунтирование широко применяют при реконструктивных операциях на артериях верхних и нижних конечностей. Эта операция является методом выбора при закупорках сравнительно мелких артерий предплечья и голени. При формировании сосудистых анастомозов в этих случаях желательно использовать микрохирургическую технику (см. Микрохирургия).
При стенозах и окклюзиях чревной, верхней брыжеечной, почечных артерий производят шунтирование кровеносных сосудов непосредственно с брюшным отделом аорты. Для шунтирования артерий небольшого диаметра, кроме аутовен, используют аллотрансплантаты и ксенотрансплантаты, например вену пуповины человека, обработанную глутаровым альдегидом с целью снижения антигенных свойств. Подобная обработка способствует ослаблению нейтрофильной и макрофагальной реакции и улучшает результаты операции. Иногда снаружи пупочную вену укрепляют сетчатым синтетическим каркасом. Шунтирование кровеносных сосудов осуществляют также трансплантатами из бычьих и свиных сосудов (ксенотрансплантаты). Их с целью удаления чужеродных белков предварительно обрабатывают протеолитическими ферментами (фицином, папаином, химотрипсином, террилитином и др.), а затем дубят глутаральдегидом и диальдегидом крахмала.
При шунтировании кровеносных сосудов широко применяют трансплантаты из синтетических материалов (лавсана, дакрона, политетрафторэтилена и др.). Эти трансплантаты применяют для шунтирования при окклюзиях ветвей дуги аорты и подключичных артерий. При окклюзиях подвздошных артерий и брюшного отдела аорты стандартными стали аортоподвздошное и аортобедренное шунтирование кровеносных сосудов. Использование синтетических материалов позволяет создать шунты необходимой длины и конфигурации (см. Атеросклероз, хирургическое лечение окклюзионных поражений).
Рис. 1. Схематическое изображение отдельных этапов операции удаления мешковидной аневризмы дуги аорты с применением временного шунтирования: а – наложен синтетический шунт (1), через который осуществляется кровоток в обход отключенной с помощью зажимов восходящей части аорты; начато удаление мешковидной аневризмы (2); б – наложены швы на стенку аорты в области иссеченной мешковидной аневризмы и в местах подключения временного шунта, восстановлен обычный кровоток по аорте.
Различают временное и постоянное шунтирование кровеносных сосудов. Временное шунтирование кровеносных сосудов обычно применяют для создания обходного пути кровотока только на время основного этапа операции, требующего полного перекрытия кровотока в сегменте крупного сосуда. Например, при операциях по поводу аневризм дуги и нисходящей части грудного отдела аорты (см. Аневризма аорты) прибегают к наложению временного шунта (рис. 1). Временное шунтирование может осуществляться не только с помощью сосудистых трансплантатов. Иногда для этого используют специальные канюли или иглы, соединенные между собой полиэтиленовой или силиконовой трубкой. Канюли (иглы) вводят в сосуд прок-симальнее и дистальнее места его реконструкции. При этом кровь из центрального сегмента пережатой артерии по соединительной трубке поступает в его периферический отдел. Преимущество канюльного метода временного шунтирования заключается в его простоте. Небольшие отверстия, остающиеся в стенке сосуда после удаления канюль, ушивают одним-двумя швами. Однако серьезным недостатком указанного метода является то, что сравнительно небольшой калибр канюль и игл не всегда обеспечивает необходимый объем кровотока через их просвет. Временное шунтирование кровеносных сосудов с помощью канюль и силиконовых трубок показано также при острой травме магистральных сосудов для сохранения кровотока в них на время транспортировки раненого в специализированное лечебное учреждение.
Наибольшее распространение в сердечно-сосудистой хирургии получило постоянное шунтирование кровеносных сосудов. В некоторых случаях оно является менее травматичной, а в техническом отношении более простой операцией, чем протезирование сосудов. Принципиальное значение при постоянном шунтировании кровеносных сосудов имеет сохранение коллатерального кровообращения (см. Коллатерали сосудистые). Постоянное шунтирование кровеносных сосудов наиболее часто применяют при облитерациях или стенозах аорты различной природы, например при синдроме Лериша (см. Лериша синдром), а также при облитерирующих заболеваниях магистральных артерий и вен.
Для постоянного шунтирования кровеносных сосудов в зависимости от типа сосуда (артерия или вена), а также его диаметра применяют различные трансплантаты (см.). При шунтировании венозных стволов, как правило, используют аутовены.

Рис. 2. Аортограмма больного со стенозирующим атеросклерозом подвздошных артерий после правостороннего линейного аортобедренного шунтирования: кровоток осуществляется одновременно по шунту (1) и по стенозированным общей (2) и внутренней (3) подвздошным артериям.
Шунтирование кровеносных сосудов одним линейным трансплантатом (рис. 2) называют одиночным, или линейным, шунтированием. Если применяют бифуркационный трансплантат, шунтирование называют бифуркационным (например, бифуркационное аортобедренное шунтирование). Если шунтируются одновременно несколько сосудов, то говорят о двойном, тройном или множественном шунтировании (например, множественное аортокоронарное шунтирование). В последнее время стали использовать так называемое последовательное шунтирование. Выполняют его главным образом при аортокоронарном шунтировании и реконструкциях артерий голени. Принцип этой операции заключается в формировании нескольких последовательных анастомозов одного трансплантата с двумя или тремя близлежащими артериями или проходимыми сегментами одной артерии.
При шунтировании кровеносных сосудов необходимо учитывать некоторые технические особенности. Канал, в котором проводят трансплантат, должен быть достаточно широким, чтобы предупредить сдавление шунта окружающими тканями. При использовании длинного шунта во время его проведения необходимо избегать перекручивания последнего по продольной оси. Избыточная длина шунта может привести к его перегибу и последующему тромбозу (см.). Шунт должен находиться в слегка натянутом состоянии. Диаметр трансплантата должен быть больше диаметра шунтируемых сосудов в 1,5-2 раза. Соединение трансплантата с сосудами должно осуществляться под максимально острым углом, желательно не более 15°. В этом случае гемодинамическая характеристика соустья почти аналогична таковой при соединении сосудов конец в конец. Желательно, чтобы длина анастомоза (конец в бок) в 1,5-2 раза превышала диаметр шунта. Это особенно важно, когда шунт и шунтируемые сосуды имеют примерно одинаковый калибр. Для наложения анастомозов выбирают обычно неизмененные участки стенок сосудов. Если стенка аорты или артерии уплотнена, необходимо перед наложением анастомоза экономно иссечь участок стенки сосуда, чтобы в нем образовалось овальное отверстие. При шунтировании вен этот прием следует выполнять по возможности всегда.
Сшивание трансплантата с шунтируемым сосудом обычно производят обвивным атравматическим швом между двумя швами-держалками, предварительно наложенными на верхний и нижний углы анастомоза. Перед включением шунта в кровоток удаляют образовавшиеся в нем пристеночные тромбы и воздух.
При шунтировании кровеносных сосудов большое значение имеют морфологические особенности системы вновь сформированного сосудистого анастомоза, связанные с многими причинами, в том числе и с применяемыми трансплантатами. Сосудистый трансплантат (шунт) нередко вызывает асептическое воспаление в окружающих тканях. Вокруг него образуется грануляционная ткань (см.), которая в течение 2-3 недель превращается в наружную фиброзную (соединительнотканную) капсулу. В дальнейшем наружная капсула меняется мало, наблюдается лишь ее истончение, а иногда гиалиноз (см.) и петрификация (см. Петрификат).
При использовании для шунтирования кровеносных сосудов аутовен в их стенке уже в первые дни отмечаются частичная десквамация эндотелия, рексис ядер гладких мышечных клеток, отек и умеренная нейтрофильная инфильтрация, что связано с нарушением кровообращения и метаболизма венозной стенки. Затем происходит пролиферация эндотелия, гладких мышечных клеток и фибробластов с синтезом коллагена и гликозаминогликанов, что обусловливает репарацию сосудистой стенки. В поздние сроки после шунтирования кровеносных сосудов происходит утолщение стенки вены за счет фиброза и гиперэластоза всех ее слоев, особенно адвентиции. У больных пожилого возраста через несколько лет после шунтирования могут развиться периваскулярный фиброз, утолщение внутренней оболочки сосуда и атеросклероз (см.). В результате наступает сужение или облитерация просвета периферических аутовенозных шунтов.
Морфологические изменения трансплантата вены из пуповины человека менее выражены. Внутренняя оболочка трансплантированной вены покрывается тонкой пленкой фибрина (см.), в области анастомоза образуется прослойка из клеток эндотелия, нейтрофилов и макрофагов, что создает благоприятные условия для функционирования трансплантата. В результате тканевой несовместимости (см. Несовместимость иммунологическая) эндотелий, гладкие мышцы и частично эластические волокна разрушаются макрофагальным, лимфоплазмоклеточным и нейтрофильным инфильтратом. Дистрофические изменения ведут к изъязвлению, поздним тромбозам, кальцинозу (см.), уменьшению прочности, образованию аневризм (см. Аневризма) и разрывам стенки трансплантата.
При использовании консервированных ксенотрансплантатов (бычьих, свиных сосудов и др.) морфологические изменения не существенны, а нейтрофильная и лимфоплазмоклеточная реакции на пересадку таких сосудов минимальны.
Морфологические изменения в синтетических трансплантатах особенно выражены на внутренней поверхности, которая покрывается фибринной выстилкой с формированием так называемые неоинтимы. Источником ее образования являются фибробласты и капилляры, прорастающие через поры синтетического каркаса, а также клетки сосудистой стенки, мигрирующие через анастомозы (обычно на расстояние, не превышающее 2-3 см). Нельзя исключить и участия в этом процессе предшественников фибробластов, находящихся в кровотоке. У человека полной эндотелизации нового сосудистого русла часто не происходит.
Функционирование шунтов зависит от диаметра шунтируемых сосудов, характера используемого пластического материала и др. Чем больше диаметр шунтируемого сосуда и короче трансплантат, тем лучше отдаленный результат операции. Отдаленные результаты шунтирования артериальных сосудов зависят от многих факторов, в частности имеет значение этиология поражения аорты и артерий (атеросклероз, аортит, артериит). Наиболее неблагоприятные результаты наблюдаются после операции при неспецифическом аортите (см.) и артериите (см.). Основной причиной неблагоприятных отдаленных результатов при шунтировании артериальных стволов является прогрессирование основного заболевания. Поэтому после различных видов шунтирования необходимо постоянное диспансерное наблюдение за больными и лечение основного заболевания.
Отдаленные результаты шунтирования магистральных вен значительно хуже, чем при шунтировании магистральных артериальных стволов. Однако в последнее время появились сообщения о многолетнем функционировании аутовенозных шунтов, созданных по поводу окклюзии вен самой различной локализации. Это связано с развитием терапии, улучшающей реологические свойства крови, и внедрением микрохирургической техники.
См. также Кровеносные сосуды, операции; Облитерирующие поражения сосудов конечностей.
Библиогр.: Веденский А. Н. Пластические и реконструктивные операции на магистральных венах, Д., 1979; Князев М. Д., Белорусов О. С. и Савченко А. Н. Хирургия аортоподвздошных окклюзий, Минск, 1980; Лебедев Л. В., Плоткин Л. Л. и Смирнов А. Д. Протезы кровеносных сосудов, Л., 1975, библиогр.; Петровский Б. В., Беличенко И. А. и Крылов B.C. Хирургия ветвей дуги, М., 1970; Сычеников И. А. Шов и пластика артерий, М., 1980; E sato К., Shintani К. a. Yasutake S. Modification and morphology of human umbilical cord vein as canine arterial bypass grafts, Ann. Surg., v. 191, p. 443, 1980; Leu H. J. u. Brunner U. Zur Pathogenese der degenerati ven Veranderungen an autologen des Venetransplantaten, Dtsch. med. Wschr., S. 2433, 1973; Palma E. a. Esperon R. Vein transplants and grafts in the surgical treatment of the postphlebitic syndrome, J. cardiovasc. Surg., v*. 1, p. 94, 1960; Szilagyi D. E. a. o. The laws of fluid flow and arterial grafting, Surgery, v. 47, p. 55, 1960; We so low A. The healing of arterial prosthesis, Thorac. cardiovasc. Surg., v. 30, p. 196, 1982.
О. С. Белорусов; А. Б. Шехтер (пат. ан.).
Источник
Сегодня существует несколько неинвазивных методик, эффективно используемых при сужении сосудов.
К самым популярным в современной эндоваскулярной (сосудистой) хирургии методам относятся ангиопластика и стентирование.
Малоинвазивные операции на сосудах производятся через небольшой прокол или разрез на коже пациента. В сделанное  отверстие хирург вводит сначала иглу со специальной сердцевиной – стилетом, а затем катетер – тонкую полую трубочку. Ход процедуры контролируется с помощью рентгеновского монитора. Продвигая катетер вверх по руслу сосуда, его подводят к локализованному заранее посредством ангиографии месту сужения артерии. В зависимости от специфики процедуры, на конце катетера прикреплен стент или баллон.
отверстие хирург вводит сначала иглу со специальной сердцевиной – стилетом, а затем катетер – тонкую полую трубочку. Ход процедуры контролируется с помощью рентгеновского монитора. Продвигая катетер вверх по руслу сосуда, его подводят к локализованному заранее посредством ангиографии месту сужения артерии. В зависимости от специфики процедуры, на конце катетера прикреплен стент или баллон.
Просвет здоровой артерии равномерно широкий, а стенки гладкие. Возраст и атеросклероз провоцируют появление на стенках сосудов отложений, состоящих из фиброзной ткани, кальция и холестерина. Это так называемые атеросклеротические бляшки. Чем больше на стенках артерий таких бляшек, тем сильнее сужается просвет сосуда и ухудшается кровоток. В конечном итоге сужение достигает критической степени, и нормальный кровоток становится невозможен. Развивается ишемия (недостаточное кровоснабжение) и, как следствие, боль и даже некроз (омертвение) тканей.
Ангиопластика (балонная) чаще всего используется для лечения заболеваний периферических сосудов, иногда – для восстановления функциональной проходимости вен. Кроме того, она бывает единственной медицинской альтернативой коронарного шунтирования, в частности, потому что не требует разреза для проведения манипуляций, выполняется под местной анестезией, а период реабилитации после операции достаточно короткий.
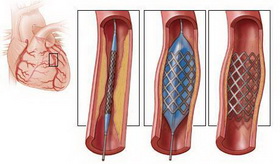
Стентирование применяется в случае, если нужно не просто расширить просвет сосуда, но и армировать его постановкой стента – миниатюрного проволочного каркаса.
Показания к операции
Традиционно операция на сосудах показана всем пациентам с умеренным или тяжелым сужением сосудов.
Противопоказанием может служить значительная закупорка сосуда (кончик катетера не проходит через место сужения).
Осложнения, возникающие после стентирования
Нельзя исключать возможность возникновения осложнения после стентирования:
- кровотечение в точке введения катетера;
- образование канала между веной и артерией;
- высокий риск образования тромбов вокруг стента (в первые месяцы после операции);
- возникновение рестеноза;
- закупорка просвета артерии ниже места сужения;
- образование тромба в артерии;
- почечная недостаточность;
- ослабление или разрыв стенки сосуда;
- аллергия на контраст;
- расслоение стенки артерии
Операция по коронарной ангиопластике
Предоперационная подготовка к коронарной ангиопластике (транслюминальной реконструкции) заключается в полном обследовании пациента, в ходе которого обязательно проводятся:
- рентгенографическое исследования грудной клетки;
- электрокардиограмма;
- лабораторные анализы мочи и крови;
- тест на переносимость рентгеноконтраста (в случае, если перед операцией назначено ангиографическое исследование сосудов сердца)
Перед операцией рекомендовано воздерживаться от приема пищи. Касательно приема лекарств (особенно, противодиабетических препаратов) необходимо проконсультироваться у кардиолога.
Специфика процедуры
Через бедренную артерию пациента вводится катетер и проводится к суженному участку артерии для интраоперационной коронарографии, в ходе которой выявляется место и стадия сужения артериального просвета.
На основании полученных данных, кардиохирург выбирает баллон соответствующего размера и подходящий катетер-проводник. Для того чтобы предупредить тромбообразование и дополнительно разжижить кровь, пациенту назначается гепарин.
Катетер-проводник – это тончайшая проволока, имеющая рентгеноконтрастный наконечник, которая вводится в пораженную коронарную артерию пациента. Получив полную картину, кардиохирург направляет проводник в нужное место.
Наконечник выводится за место сужения просвета артерии.
После этого через проводник вводится баллонный катетер, который доставляет баллон на место сужения. После надувания, баллон расширяет просвет артерии, расплющивая бляшку. Если целью операции является постановка стента, то он при раздувании баллона вдавливается в стенку сосуда, армируя пораженный участок и не давая ему сужаться.
Эффект и реабилитация
Как правило, в результате успешно проведенной операции по коронарной ангиопластике значительно улучшается кровоток в коронарных сосудах и значительно сокращается вероятность проведения аортокоронарного шунтирования.
Чтобы минимизировать проявления основного заболевания, следует придерживаться предписанной врачом диеты, воздерживаться от курения и исключить стрессовые моменты.
Уже через шесть часов после успешной операции пациенту разрешают вставать и ходить, но первые два дня он проводит в стационаре кардиоцентра.
Реабилитационный период длится в среднем неделю.
Источник
