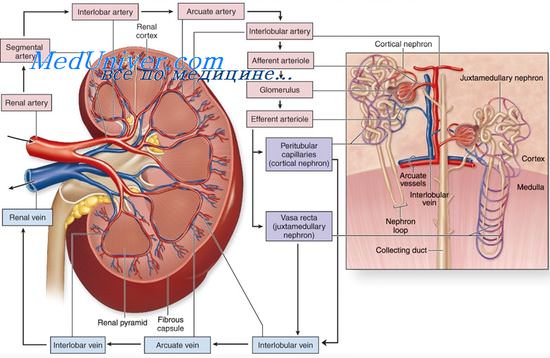
Как вырастить новые сосуды

Васкуляризация тканей. Формирование и рост новых кровеносных сосудовОсновным механизмом долговременной регуляции местного кровотока является изменение количества кровеносных сосудов в тканях. Так, длительная активизация метаболических процессов в данной ткани вызывает усиленную васкуляризацию ткани; если же уровень метаболизма снижается, количество кровеносных сосудов в ткани уменьшается. Так происходит изменение васкуляризации тканей в зависимости от их метаболических потребностей. Эта реконструкция сосудистой системы развивается быстро (через несколько дней) у очень молодых животных, а также в быстрорастущих тканях зрелого организма (например, в рубцовой ткани или в растущей опухоли). И наоборот, в зрелых, высокодифференцированных тканях подобный процесс протекает медленно. Таким образом, на долговременную регуляцию кровотока требуется всего несколько дней у новорожденных, и более месяца — у лиц старшего возраста. Кроме того, результат перестройки сосудистого русла оказывается гораздо лучшим в молодых тканях. Так, у новорожденных сосудистая сеть способна практически полностью удовлетворять возросшие потребности тканей, в то время как в зрелых тканях васкуляризация зачастую намного отстает от потребностей ткани. Роль кислорода в долговременной регуляции. Кислород имеет большое значение не только в быстрой краткосрочной регуляции местного кровотока, но и в долговременной регуляции. Одним из примеров является усиленная васкуляризация тканей у животных, обитающих на больших высотах, где содержание кислорода в атмосфере низкое. Другим примером может быть наблюдение за куриными зародышами, развивающимися в условиях гипоксии, у которых число кровеносных сосудов в 2 раза превышает нормальную плотность сосудов в тканях. Подобный эффект может иметь самые неблагоприятные последствия у недоношенных детей, помещенных в кислородную палатку с лечебными целями. Избыток кислорода немедленно прекращает рост сосудов сетчатки глаза у недоношенного ребенка и даже вызывает дегенерацию уже имеющихся сосудов. Затем, когда ребенка извлекают из кислородной палатки, начинается бурный рост сосудов в тканях глазного яблока, и кровеносные сосуды прорастают в стекловидное тело глаза, что приводит к слепоте. Такое явление называют ретроленталъной фиброплазией.
Формирование и рост новых кровеносных сосудовОбнаружены более 10 факторов, которые усиливают рост новых кровеносных сосудов. Почти все они являются короткими пептидами, из них 3 фактора изучены лучше других: сосудистый эндотелиальный фактор роста, фактор роста фибробластов и ангиогенин. Каждый из них был выделен из тканей с неадекватно низким кровоснабжением. По-видимому, дефицит кислорода или питательных веществ (или и того, и другого) приводит к образованию сосудистых факторов роста (так называемых ангиогенных факторов). В сущности, все ангиогенные факторы вызывают рост новых сосудов одинаковым способом: они способствуют появлению новых сосудов путем разрастания и ветвления старых сосудов. Первым этапом этого процесса является растворение базальной мембраны эндотелия в точке ветвления. Затем начинается быстрое образование новых эндотелиальных клеток, которые мигрируют через сосудистую стенку, образуя сосудистый росток, направленный к источнику ангиогенных факторов. Клетки продолжают быстро делиться и свертываются в трубку. Трубка соединяется с другой такой же, формирующейся от другого сосуда (артериолы или венулы), — и появляется капиллярная петля, в которой начинается кровоток. Если кровоток достаточно велик, в стенку нового сосуда переселяются гладкомышечные клетки, сосуд становится артериолой или венулой, а иногда и более крупным сосудом. Так, ангиогенез объясняет механизм, с помощью которого метаболические факторы тканей способствуют росту новых сосудов. Ряд других веществ, таких как некоторые стероидные гормоны, оказывают на мелкие кровеносные сосуды противоположное действие. При этом происходит разрушение сосудистых клеток и исчезновение сосудов. Следовательно, количество кровеносных сосудов может уменьшаться, когда необходимость в них отпадает. Васкуляризация зависит от максимальной потребности тканей в кровоснабжении, а не от среднего уровня кровоснабжения. Исключительно важной характеристикой долговременной регуляции кровоснабжения является то, что васкуляризация тканей обусловлена главным образом максимальным уровнем кровотока, необходимого тканям, а не средним уровнем их потребностей. Необходимость в таком максимальном кровотоке может возникать не более чем на несколько минут в день. Тем не менее, даже такой кратковременной предельной нагрузки достаточно для выделения эндотелиальных факторов роста в мышечной ткани, чтобы усилить ее васкуляризацию. Если этого не происходит, каждый раз, когда человеку приходится выполнять тяжелую физическую нагрузку, его мышцы не могут развить необходимую силу сокращения, т.к. они не получают достаточного количества кислорода и питательных веществ. Однако если избыточная васкуляризация произошла, большая часть кровеносных сосудов обычно пребывает в состоянии сужения. Они открываются только под действием местных факторов, таких как недостаток кислорода, влияние сосудорасширяющих нервов и других факторов, свидетельствующих о необходимости резко увеличить кровоток. – Также рекомендуем “Коллатеральное кровообращение. Гуморальная регуляция кровообращения” Оглавление темы “Регуляция кровоснабжения”: |
Источник
Новые сосуды
Российские ученые научились выращивать новые сосуды взамен поврежденных. Что это за методика и в каких случаях она применяется?
Отвечает член-корреспондент РАМН, профессор, член Международного союза ангиологов, заведующий отделением хирургии сосудов Российского научного центра хирургии им. академика Б. В. Петровского РАМН в столице Александр Васильевич Гавриленко.
— Вырастить новые сосуды — это звучит фантастически. Но не очень понятно, зачем понадобилась такая методика. Ведь уже сейчас существует множество способов восстановить сосуды: реконструктивная операция, установка стента…
— К сожалению, с помощью этих методик далеко не всегда можно получить хороший результат. Если сосуд имеет множественные повреждения или поражение успело распространиться, поставить стент или выполнить восстанавливающую операцию — задача почти нереальная. Такое нередко случается при атеросклерозе или артрите. Наиболее сложен случай, если эти проблемы сочетаются еще и с сахарным диабетом. Раньше в таких ситуациях перспектива была фактически одна — ампутация. А сейчас мы можем сохранить ногу. У человека появляется возможность жить полноценно. Все — благодаря уникальным генным технологиям, с помощью которых можно вырастить новые сосуды.
— Когда речь заходит о генной инженерии, на ум сразу приходят стволовые клетки. Вы применяете их?
— Сейчас речь идет о другой методике, которую мы считаем более перспективной. К тому же она имеет ряд преимуществ перед стволовыми технологиями.
Из «чудо-клеток» действительно можно получить многие ткани, в том числе и сосуды. Но при их использовании теоретически не исключено появление новообразований. А наша методика не приводит к развитию онкологии.
Суть ее такова. В организм вводят специальный генно-инженерный комплекс. Он был разработан ведущими генетиками нашей страны под руководством академика Николая Павловича Бочкова. Комплекс активизирует гены, которые отвечают за рост сосудов.
В течение жизни у здорового человека новые вены и артерии не образуются. Но иногда, если сосуд поврежден, может появиться новая кровеносная «сеточка». Она «обходит» проблемный участок, и кровообращение частично восстанавливается.
К сожалению, этот процесс возможен далеко не всегда. А уж если имеющиеся сосуды поражены атеросклеротическими бляшками, ждать естественного восстановления просто бессмысленно. Организму нужно помочь.
Для этого и предназначен новый генно-инженерный комплекс. Он стимулирует рост мелких сосудов. Они берут на себя обязанности пораженных артерий и капилляров. Кровоснабжение улучшается, и нога может нормально функционировать.
— Как много времени требуется, чтобы вырастить сосуд?
— Уже через 2–3 недели после того, как мы ввели наш комплекс, начинают образовываться новые мелкие сосуды. Их рост достигает пика через 2–6 месяцев.
Как долго сохранится хороший результат, зависит от состояния человека, от его образа жизни и того, насколько тщательно он соблюдает рекомендации врача. Но на несколько лет проблема точно отступает — это факт.
— Как проходит лечение? Генно-инженерный комплекс надо вводить как-то по-особому?
— Это обычный укол. По ощущениям — не больнее любой прививки. Его могут делать и в вену, и под кожу. Но наилучший эффект отмечается, если состав вводят внутримышечно, и именно в проблемную зону. Чаще всего это икры ног — участок, кровоснабжение которого особенно страдает. Как правило, уколы делают трижды, на весь курс уходит несколько дней.
Никаких особенных побочных эффектов нет. Если противопоказаний к использованию генно-инженерного комплекса у вас изначально выявлено не было, проблем быть не должно.
— А каковы противопоказания?
— Скажем, системные болезни или онкологические проблемы. Но делать уколы с нашим комплексом нельзя, например, и людям с гепатитом.
Чтобы исключить все риски, мы обязательно проводим тщательное обследование. В него входит и компьютерная томография, и доплерография, и ряд анализов крови. В общем, без строгих показаний лечение назначено не будет.
— Какие правила нужно соблюдать после лечения, чтобы эффект был максимальным?
— Просто придерживайтесь здорового образа жизни. Так, ни в коем случае нельзя курить.
Из-за курения резко, практически молниеносно, прогрессирует атеросклероз. А если у человека уже есть эта проблема, значительно увеличивается риск инфаркта и инсульта. При диабете сигареты еще сильнее ухудшают обмен веществ. Даже у относительно здоровых людей сосуды из-за этой вредной привычки становятся менее эластичными.
Кстати, тут есть интересная тенденция, которую я заметил за долгие годы работы. Делать операции и лечиться с помощью новой генной методики к нам приходят и мужчины, и женщины. Но первых значительно больше. У представителей сильного пола атеросклероз бывает в шесть раз чаще, чем у дам. Однако по статистике, далеко не все курящие мужчины имеют проблемы с сосудами. Если же курит женщина, подобные неприятности ей гарантированы почти на 100%.
Поэтому отказ от сигарет очень важен как для профилактики, так и для лечения. Если после введения генно-инженерного комплекса вы не избавились от вредной привычки, значит, попусту тратили время и силы. Положительный эффект быстро исчезнет, и проблема вернется.
После того как вырастут новые сосуды, очень важно также не употреблять крепкие алкогольные напитки. Бокал сухого красного вина изредка, по праздникам, выпить можно.
Обязательно соблюдайте режим труда и отдыха. Следите за питанием — в нем не должно быть много жирной пищи: мяса, масла, маргарина. Обязательный пункт меню — рыба и морепродукты. По возможности нужно есть чеснок и морскую капусту. А также следовать другим принципам средиземноморской диеты.
В принципе, все это можно посоветовать и любому здоровому человеку. Из особых рекомендаций выделю лишь две. Во-первых, людям с «выращенными» сосудами нужно избегать сырости и переохлаждения. Во-вторых, им не стоит носить синтетическую одежду.
— А как быть с фитнесом? Реально ли сохранить былую активность? Скажем, бегать по утрам.
— Раньше ни о чем подобном люди после лечения даже не спрашивали. Было огромным достижением уже то, что они получили возможность ходить.
Но сейчас и атеросклероз, и диабет заметно «молодеют». А чтобы избежать осложнений при этих болезнях, важно не набирать лишний вес. Поэтому вопрос о фитнесе периодически возникает.
Я против бега. На мой взгляд, он вреден даже для тех, кто здоров.
В такой ситуации сильно увеличивается нагрузка на сердце, позвоночник, легкие. Для многих она чрезмерна, поэтому организм скорее изнашивается, чем получает какую-то пользу.
Если же у человека есть проблемы с сосудами, неприятностей может быть еще больше. В своей массе люди не имеют ни малейшего представления о правильной технике бега. И поэтому рискуют травмировать едва вылеченную ногу. Устраивать пробежки в большом городе практически негде. Даже рядом с парками ездят машины, там слишком много выхлопных газов. А дышать грязным воздухом — значит, увеличивать нагрузку на сердце и сосуды.
В общем, утреннему бегу после «генного» лечения придется сказать категорическое нет. Но это не значит, что человек не может пробежать пару десятков метров, если опаздывает на трамвай. Это небольшое усилие, особого вреда не будет.
А вообще после лечения стоит взять за правило: любая нагрузка должна быть эмоционально окрашенной. Катаясь на велосипеде, вы можете любоваться пейзажем, — это удовольствие. Плавая в бассейне или тем более в море, тоже получаете хорошие впечатления. Вот этим и нужно заниматься.
Также можно поиграть в футбол с друзьями на пикнике. После лечения очень хороший эффект дает ходьба, терренкур. Главное — относиться к активности без излишнего фанатизма, не изнурять себя. Если вы почувствовали дискомфорт, занятия надо прекратить. Тогда сосудам ног это пойдет только на пользу.
Наталия ФУРСОВА
Источник

 Наши эксперты – доктор медицинских наук, профессор кафедры госпитальной хирургии медицинского факультета РУДН Алексей Зудин и сердечно-сосудистый хирург Ярославской областной клинической больницы, доктор медицинских наук, профессор кафедры хирургии ИПДО Ярославского государственного медицинского университета Юрий Червяков.
Наши эксперты – доктор медицинских наук, профессор кафедры госпитальной хирургии медицинского факультета РУДН Алексей Зудин и сердечно-сосудистый хирург Ярославской областной клинической больницы, доктор медицинских наук, профессор кафедры хирургии ИПДО Ярославского государственного медицинского университета Юрий Червяков.
Масштаб проблемы
Два миллиона россиян страдают ишемией нижних конечностей. Болезнь проявляется перемежающей хромотой – болью в голенях во время ходьбы, которая не позволяет человеку пройти без остановки – кому больше 1 км, а кому и больше 25 м. И если не лечиться, состояние будет только ухудшаться.
У 40% тех, кто страдает перемежающей хромотой, в перспективе – ампутация ноги, инвалидность, у многих гибель в ближайшие 5 лет после операции. Причём такие перспективы не только у российских больных, но и у пациентов из других стран. Частота ампутаций на 1 млн населения в год по причине ишемии ног: 400 – в Швеции, 300 – в Великобритании, 280 – в США, 500 – в России.
40 тысяч человек у нас остаются без ноги ежегодно. А потери для бюджета страны на одного обезножившего пациента – 700 тысяч рублей. Вот как в цифрах выглядит эта проблема.
В чём причина?
Отчего в ногах ухудшается кровоснабжение? В основе заболевания – тот же атеросклероз, который приводит к инсультам и инфарктам. Только в случае ишемии ног холестериновые бляшки забивают не крупные артерии, а мелкие капилляры. Мышцы не получают достаточно кислорода, начинают болеть при ходьбе, ноги мёрзнут, кожа на них становится бледной, голень из-за плохого питания утончается, ногти на ногах медленно растут, ломаются…
При этом ишемия нижних конечностей встречается чаще других сосудистых заболеваний, таких, например, как ишемическая болезнь сердца или инсульт. 42 тысячи новых пациентов с таким диагнозом появляются у нас ежегодно.
Как до недавнего времени лечили, да и сейчас ещё во многих местах лечат, ишемию ног?
Назначают сосудорасширяющие препараты. Но так как у них есть опасный побочный эффект – риск инфаркта, – такое лечение теперь признано неэффективным.
В 30% случаев ишемии ног кровоток пытаются восстановить хирургическим путём. Удаляют из крупных сосудов бляшки, ставят стенты, которые расширяют артерии, заменяют старые сосуды на искусственные… Но в мелкие сосуды со скальпелем не заберёшься и стент в них не поставишь. Так что для 30% больных с ишемией ног медицина ещё совсем недавно была бессильна.
Новый метод
Но недавно появился новый метод: генно-терапевтический, который позволяет вырастить новые капилляры.
Это всего лишь 2 курса уколов, когда в мышцы вводится ген, который приводит в действие фактор роста сосудов ног, и этот фактор заставляет периферические сосуды расти. Рост может продолжаться до трёх лет.
Безопасность метода была подтверждена во время клинических исследований, проходивших в 33 медицинских учреждениях России и Украины. С этого года препарат, созданный нашими учёными, зарегистрированный и производимый в России, входит в список жизненно необходимых лекарств.

Шесть лет прошло с того времени, как первые пациенты получили генную терапию и у них выросли новые капилляры. Так они и остались, снабжают ткани ног кровью и позволяют бывшим больным ходить без боли.
Факторы риска развития ишемической болезни ног:
1. Возраст: атеросклероз сосудов ног у мужчин начинает проявляться после 45 лет, у женщин – после 55 лет;
2. Мужской пол;
3. Курение: 90% больных ишемией ног – злостные курильщики;
4. Сахарный диабет: у пациентов с этим заболеванием вероятность ампутации возрастает в 10 раз;
5. Ожирение: риск атеросклероза повышается, если объём талии у мужчины больше 102 см, у женщины – больше 88 см;
6. Гипертония;
7. Повышенный уровень холестерина в крови: это фактор риска появления бляшек, закупоривающих сосуды;
8. Наследственность: в группе риска те, у чьих родственников были инфаркты и инсульты.
Смотрите также:
- Встать в строй. Отечественный препарат помогает пациентам ходить без боли →
- Академик РАН Амиран Ревишвили: «Аритмию необходимо контролировать» →
- Разрыв аорты: где возникают аневризмы и как их избежать →
Источник
05.11.2014
Группа ученых из шведского Гетеборга опубликовала статью, в которой рассказывается, как им удалось вырастить и трансплантировать двум пациентам новый кровеносный сосуд, используя донорский сосуд и 25 миллилитров крови реципиента. Ну и немного лабораторных реактивов.
Плохое состояние сосудов и недостаточное кровоснабжение оказываются причиной или заметно снижающим качество жизни следствием при многих патологиях.
Во-первых, сужение просвета коронарных (снабжающих кровью сердце) сосудов приводит к сердечной недостаточности, стенокардии и т. п. Попадание или образование в них тромба и вовсе влечет инфаркт миокарда. Сейчас для улучшения коронарного кровоснабжения применяются аорто-коронарное шунтирование и стентирование. Аорто-коронарное шунтирование в 2011 году оказалось самой частой операцией, проводимой в США (1,4% от общего числа). При шунтировании откуда-нибудь, как правило, из ноги, вырезается фрагмент вены, имеющей дублеров, и пришивается одним концом к аорте, а другим – к коронарным сосудам ниже того места, где в них образовалась непроходимость. После этого часть обогащенной кислородом крови, попадающей из сердца в аорту, будет сразу попадать в коронарные сосуды и питать сердечную мышцу. Стентирование – это манипуляция, при которой в просвет сужающегося сосуда вводится полый цилиндр-расширитель, который не дает сосуду сузиться окончательно. В отличие от аорто-коронарного шунтирования – сложной полостной операции на открытом сердце со всеми ее рисками и трудностью последующего восстановления, стент устанавливается через бедренную артерию, и пациенту даже не обязательно давать наркоз.
Другая болезнь, связанная с недостаточностью кровоснабжения, – сахарный диабет. При диабетической ангиопатии сосуды делаются более ломкими, повышается вероятность атеросклероза и тромбоза. Ухудшается кровоснабжение. Все это особенно характерно для мелких сосудов нижних конечностей. В сочетании с другими проявлениями диабета это приводит к развитию синдрома так называемой диабетической стопы, часто заканчивающегося ампутацией.
В целом, для стареющего и полнеющего населения развитых стран проблемы плохого кровоснабжения очень актуальны по самым разным причинам.
В работе, о которой идет речь у нас, протезировали воротную вену печени. Воротная вена – это не вена в прямом смысле слова, кровь по ней не идет к сердцу. Воротная вена собирает кровь, идущую от органов желудочно-кишечного тракта и селезенки, и направляет ее в печень. В некоторых случаях из-за тромбоза или аномалий развития воротная вена может оказаться непроходимой или просто отсутствовать.
Пациенты, участвовавшие в исследовании, попадали в больницу с жалобами на усталость, боль в животе. Обе девочки (одна четырех, другая полутора лет) отставали в росте и наборе веса. У одной из них болезненные ощущения были явно связаны с приемом пищи. При анализе крови обнаруживались анемия, тромбоцитопения, нейтропения, но диагноз оказался не гематологическим. Компьютерная томография показала у обеих девочек отсутствие воротной вены.
Иногда в таких случаях новую вену делают из пуповинной артерии. Пуповинная артерия во время внутриутробного развития соединяет организм ребенка с организмом матери, после рождения она становится ненужной и постепенно редуцируется, ее просвет зарастает. В некоторых случаях ее остатки можно использовать для протезирования воротной вены, но в данном случае от пуповинных артерий ничего не осталось. Также можно пытаться трансплантировать донорские сосуды, а в редких тяжелых случаях и печень целиком, но это будет означать риск отторжения и пожизненный прием иммуносупрессивных препаратов.
Поскольку эти варианты не исчерпывают всех случаев патологии, стали разрабатываться методики изготовления искусственных персонализированных сосудов. На ранних этапах развития технологии пытались использовать трубки из неорганических материалов, заселяя их внутри клетками или ожидая, пока сосудистый эндотелий в местах контакта прорастет в искусственный сосуд. Этот подход не увенчался успехом.
В предыдущей своей работе авторы предложили более перспективный подход. Пересадить донорский сосуд нельзя – он вызовет иммунный ответ. Сделать новый сосуд из клеток в пробирке тоже нельзя – клетки так просто не уговорить сформировать трехмерную структуру сосуда или любого другого органа. Но в последние годы активно исследуется новый подход, заключающийся в использовании бесклеточного матрикса. Мы раньше писали о сердечном клапане и упоминали мышиную почку, созданные таким образом. Специальными растворами из донорской ткани или органа вымываются клетки, и разрушается вся ДНК. Остается только трехмерный каркас из межклеточного вещества. Этот каркас заселяется новыми клетками. Такая конструкция не должна вызывать иммунного ответа, потому что содержит только клетки реципиента.
В первом эксперименте каркас будущей воротной вены заселялся с помощью стволовых клеток из костного мозга. Они могут дифференцироваться и в мышечные клетки сосудов, и в эндотелиальные клетки, выстилающие сосуд изнутри. У такого подхода есть минусы. Во-первых, пункция костного мозга болезненная процедура. Во-вторых, стволовые клетки надо долго размножать в культуре. Это требует времени и повышает риск генетических аберраций. В-третьих, среди стволовых клеток могут остаться не до конца дифференцированные. Их трансплантация сопряжена с минимальным, но все же риском образования опухоли.
Авторы работы обнаружили, что без стволовых клеток можно обойтись. Циркулирующая кровь несет в себе достаточное количество эндотелиальных клеток, и 25 миллилитров хватило для первичного заселения сосудов. Сосуды были трансплантированы двум пациенткам, и еще одной пациентке ранее был трансплантирован сосуд, заселенный клетками, полученными из стволовых.
Только в одном из трех случаев возникли осложнения, у одной из девочек в новом сосуде образовался тромб. Операцию пришлось повторить.
К настоящему моменту после вмешательства прошло более полутора лет. Кровоток восстановился, самочувствие по оценкам родителей и объективным показателям улучшилось. Эксперимент можно признать вполне успешным.
Кровеносный сосуд и сердечный клапан обладают относительно простой трехмерной структурой и состоят из небольшого числа типов клеток. Однако есть надежда, что в будущем технология бесклеточного матрикса позволит создавать из клеток реципиента и более сложные органы. Это очень сильно продвинет вперед всю трансплантологию, сильно ограниченную на сегодняшний день дефицитом донорских органов и проблемой совместимости.
Александра Брутер
Источники:
- polit.ru
Источник