Какие самые упругие сосуды это
Растяжимость сосудов. Емкость сосудов
Важной характеристикой сосудистой системы является растяжимость сосудов. Увеличение давления крови приводит к расширению сосудов и, следовательно, к уменьшению их сопротивления. В результате объемный кровоток увеличивается в гораздо большей степени, чем можно было ожидать, потому что он растет за счет не только увеличения давления, но и уменьшения сосудистого сопротивления.
Растяжимость сосудов имеет и другое важное значение. Например, растяжимость артерий позволяет им приспосабливаться к пульсирующему характеру кровотока и сглаживать периодические систолические колебания давления. Это обеспечивает постоянный и непрерывный ток крови в мельчайших сосудах периферических тканей.
Наиболее растяжимыми из всех сосудов являются вены. Даже небольшое увеличение венозного давления позволяет венам вмещать дополнительно от 0,5 до 1 л крови. Таким образом, вены выполняют емкостную (резервуарную) функцию. Они способны депонировать большое количество крови и выбрасывать ее в общий кровоток в любой момент, как только потребуется.
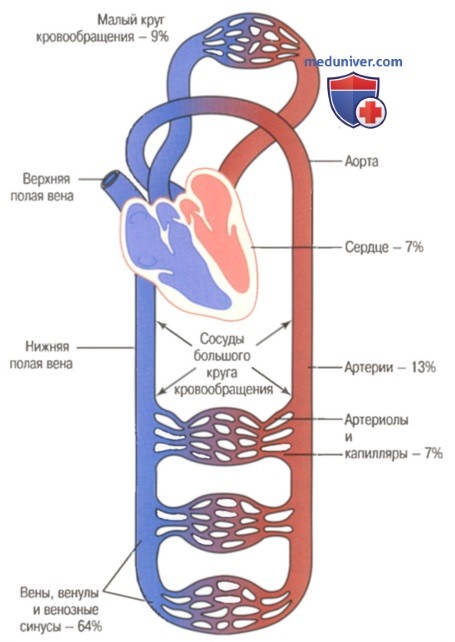 Распределение крови (% общего объема) в различных отделах сердечно-сосудистой системы
Распределение крови (% общего объема) в различных отделах сердечно-сосудистой системы
Единицы растяжимости сосудов. Обычно способность сосудов растягиваться характеризуется как степень увеличения объема сосуда при повышении давления на 1 мм рт. ст. в соответствии со следующей формулой: Растяжимость сосуда = увеличение объема / увеличение давления*исходный объем.
Например, если сосуд исходно содержит 10 мл крови, а при увеличении давления на 1 мм рт. ст. объем крови увеличивается на 1 мл, то растяжимость сосуда оценивается как 0,1 на 1 мм рт. ст. или 10% на 1 мм рт. ст.
Различия в растяжимости артерий и вен. Благодаря анатомическому строению стенки упругость артерии гораздо выше, чем упругость вен, поэтому артерии примерно в 8 раз менее растяжимы, чем вены. Это означает, что рост давления вызывает увеличение объема крови в венах в 8 раз большее, чем в артериях соответствующего калибра.
В малом круге кровообращения легочные вены имеют такую же растяжимость, как и вены большого круга. Что касается легочных артерий, то давление в них обычно составляет 1/6 величины системного артериального давления, и растяжимость их, соответственно, в 6 раз выше, чем растяжимость артерий большого круга кровообращения.
Емкость сосудов
При исследовании гемодинамики иногда гораздо важнее знать общий объем крови, который может дополнительно вместиться в тот или иной отдел сосудистой системы при увеличении давления на 1 мм рт. ст., чем растяжимость отдельных сосудов. Способность сосуда, растягиваясь, вмещать дополнительный объем крови, можно назвать резервной емкостью сосуда (или податливостью сосудистой стенки).
Резервная емкость выражается следующей формулой: Резервная емкость = увеличение объема / увеличение давления.
«Резервная емкость» и «растяжимость» – разные понятия. Хорошо растяжимый сосуд, наполненный небольшим объемом крови, имеет гораздо меньшую резервную емкость, чем менее растяжимый сосуд, наполненный большим объемом крови, т.к. резервная емкость равна растяжимости, умноженной на объем.
Резервная емкость вены большого круга кровообращения в 24 раза больше, чем резервная емкость соответствующей артерии, потому что вена в 8 раз более растяжима и объем вены в 3 раза больше, чем объем соответствующей артерии (8×3 = 24).
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
– Также рекомендуем “Кривые объем-давление артериальных и венозных сосудов. Релаксация сосудистой стенки”
Оглавление темы “Давление крови. Венозный кровоток”:
1. Гематокрит. Зависимость кровотока от давления
2. Растяжимость сосудов. Емкость сосудов
3. Кривые объем-давление артериальных и венозных сосудов. Релаксация сосудистой стенки
4. Пульсовые колебания артериального давления. Изменения пульсового давления
5. Пульсовая волна. Аускультативный метод измерения давления
6. Среднее артериальное давление. Вены и венозное давление
7. Сопротивление венозных сосудов. Влияние гравитации на венозное давление
8. Клапаны вен и венозный насос. Несостоятельность венозных клапанов
9. Методы измерения венозного давления. Емкостная функция вен
10. Депо эритроцитов – селезенка. Обновление крови
Источник
3. Свойства кровеносных сосудов.
Кровеносные сосуды по своим свойствам и функциям подразделяются на четыре типа: артерии эластичного типа, артерии мышечного типа, капилляры и вены.
l Артерии эластичного типа можно назвать аккумуляторами давления крови: благодаря им поддерживается непрерывный ток крови во время диастолы, когда сердце отдыхает. Стенки таких сосудов содержат значительное количество эластических волокон, благодаря чему в ходе функционирования артерий этого типа их радиус способен при упругих деформациях увеличиваться в 1,1 раза (на 10%), что соответствует увеличению площади сечения на 20%.
В ходе нарастания давления крови в процессе сокращения желудочков, информация об этом передается вдоль системы сосудов со скоростью звука (это порядка 1000 м/с). Вследствие этого все артерии эластического типа слегка увеличиваются в диаметре; их стенки слегка напрягаются (закон Гука); создается некоторый запас крови повышенного давления.
Помимо этого, начиная с аорты, вдоль всей системы артерий начинает распространяться пульсовая волна, расходясь по разветвлениям и постепенно затухая. В возникновении и распространении этой волны, помимо эластичности сосудов, играет роль инерционность жидкости. Благодаря инерционности, для жидкости легче образовать вздутие сосуда (благо он это позволяет), чем устремляться вдоль сосуда. Вздутие развивается до той поры, пока возрастающие силы упругости не уравновесят внутренние силы статического давления. Далее – кровь выдавливается из зоны вздутия упругими силами стенок, с тем, чтобы образовать вздутие в соседних сечениях; и т.д.
Упругие и инерционные свойства системы «кровь – аорта» определяют скорость распространения пульсовой волны:
(8)
Здесь Е – модуль упругости стенки; r – плотность крови; r – внутренний радиус сосуда; b – толщина его стенки.
С возрастом, по мере уменьшения эластичности сосудов, растет модуль упругости Е, что отслеживается ростом скорости распространения пульсовой волны.
Измерить скорость пульсовой волны можно следующим образом. Можно установить два датчика пульсовых колебаний на некотором расстоянии Dl друг от друга, и записать две кривые артериального пульса. Такие записи называются санмограммами. По двум таким записям легко определяется временной сдвиг Dt одной из них по отношению к другой. Скорость пульсовой волны:
Зная Vп, можно с помощью формулы (8) вычислить модуль упругости Е как показатель состояния сосудистой стенки. А можно обойтись и без вычислений, сравнивая измеренные значения Vп со значениями, характерными для нормы.
Наряду с эластичными волокнами, стенки сосудов данного типа имеют значительное количество коллагеновых волокон, природное предназначение которых – обеспечение прочности тканей. Однако прочностные способности этих волокон способны проявиться лишь при значительных деформациях стенок сосудов. Это объясняется рыхлой укладкой коллагеновых волокон. Они как бы спутаны, и начинают проявлять прочность только когда распрямляются при больших деформациях стенок.
Наличие прочных нитей коллагеновых волокон обеспечивает возможность работы сосудов в условиях очень больших нагрузок на систему кровообращения, вплоть до десятикратного роста артериального давления.
l Артерии мышечного типа, меняя тонус, меняют распределение давления крови по органам и тканям. В системе кровообращения нет кранов и задвижек, но есть артерии мышечного типа – артериолы. Их численность – несколько сот тысяч; суммарная площадь сосудистого русла получается весьма внушительной, а потому перепад давлений на системе артериол достаточно велик, несмотря на параллельную работу их ветвей. Так, если давление в аорте во время систолы достигает 115-130 мм рт.ст., то у начала артериол оно составляет 70-80 мм, а у начала капилляров – 20-40 мм рт.ст. Природная логика здесь примерно такова: артериола должна иметь заметное гидравлическое сопротивление, и тогда она может своим мышечным тонусом менять его в обе стороны: как в сторону понижения, так и в сторону повышения. Будь у нее очень малое сопротивление, она могла бы работать, регулируя систему только на повышение давления, что было бы гораздо менее эффективно.
Изменения тонуса в отдельных звеньях системы артериол обеспечивают повышенный кровоток в тех органах, которые в данный момент в этом нуждаются, как в связи с физическими нагрузками, так и в ходе регулирования теплообмена организма с окружающей средой.
Помимо изложенного, система артериол передает пульсовую волну, которая окончательно затухает лишь на входе в капилляры.
Примеры системных нарушений в работе этого участка кровеносной системы – гипертония и гипотония.
l Капилляры – та часть системы кровообращения, ради которой эта система существует.
Гидравлическое сопротивление всей системы капилляров невелико: если на входе в капилляры давление крови 20-40 мм рт.ст., то на выходе – 8-15 мм рт.ст., и это несмотря на впечатляющую суммарную их протяженность. Объяснение тому – очень малая скорость движения крови в этих сосудах: порядка 0,5 мм/с.
Система капилляров – та часть кровеносной системы, которая выходит из строя при декомпрессии. Имеется в виду ситуация, когда резко уменьшается давление воздуха, который окружает человека (и которым он дышит). Например, если водолаз, в нарушение инструкций, будет быстро всплывать с больших глубин на поверхность, то давление воздуха в его скафандре будет автоматически уменьшаться вслед за уменьшением внешнего гидростатического давления, и при этом воздух, растворившийся в его крови при больших давлениях в скафандре, начинает выделяться в виде микроскопических пузырьков как в самих капиллярах, так и в потоке крови, поступающей к ним. Эти пузырьки способны закупорить капилляры.
Дело в том, что в связи с явлением поверхностного натяжения под изогнутой поверхностью жидкости возникает избыточное давление (давление Лапласа), величина которого, где s – коэффициент поверхностного натяжения; r – радиус пузырька или капилляра, в котором он обосновался.
При радиусе капилляра r = 5 мкм = 5×10-6м и при s = 0,05 Н/м давление в пузырьке: p = 20 кПа = 150 мм рт.ст., т.е. превосходит «рабочее» давление крови в капиллярах и вполне годится в качестве пробки для них. Такой пузырек, вместе с его внутренним давлением, будет постепенно вытолкнут из капилляра, но навредить он успеет, поскольку ток в капилляре будет существенно замедлен. А дальше что? Спустя небольшое время значительная часть этих пузырьков вернется, пройдя сердце, в систему капилляров на повторное вредительство.
Радикальным выходом из подобных ситуаций, приводящих к кессонной болезни, является помещение пострадавших в барокамеры с повышенным давлением воздуха, выдерживание их в камерах в течение долгих часов, пока воздух из пузырьков опять растворится в крови, затем – медленное поэтапное снижение давления в барокамере до нормального атмосферного давления. Чем раньше начинается такая восстановительная процедура, тем меньше остаточные явления.
Чтобы оказаться в обозначенном круге проблем, не обязательно быть водолазом или космонавтом. В медицинской практике – камеры гипербарической оксигенации: пациента помещают в герметичную камеру, в которой воздух заменен кислородом высокого давления. Это предпринимается для эффективного насыщения крови кислородом в случаях, когда обычное легочное дыхание плохо справляется с этой задачей.
Вывод пациента из барокамеры должен быть растянут во времени, с медленным снижением избыточного давления, во избежание кессонной болезни.
l Вены – сложная разветвленная сеть сосудов, замыкающая выход капилляров с предсердиями. Эта система работает в условиях низкого давления; оно достигает нулевой отметки, и даже, как уже говорилось, может быть отрицательным. В этих условиях, в правом предсердии возникает еще более низкое давление, чтобы всасывать кровь, если она поступает слабо.
Если же организм работает в режиме повышенных физических нагрузок, то давление на входе в предсердия – повышенное, и имеет место хорошая заполняемость предсердий и желудочков. Это означает, что мышечные волокна миокарда растянуты значительно. Для сердца это является указанием на то, что от него требуется сократительная деятельность повышенной мощности. В этом проявляется закон Старлинга: сила сердечного сокращения прямо пропорциональна исходной длине миокардиальных волокон перед началом систолы. Таким путем, не дожидаясь команд из «центра» – ЦНС, сердце автоматически регулирует свою деятельность. Способность сердца автономно выполнять сократительную деятельность, даже находясь вне организма, поражала еще древних медиков.
Разумеется, сказанное не означает, что сердце работает совершенно независимо от центральной нервной системы. Хорошо известно, что эмоциональные перегрузки способны оказывать сильнейшее влияние, как положительное, так и отрицательное, на работу сердца и всей сердечно-сосудистой системы.
l Автоматическое регулирование собственных параметров системой кровообращения просто обязано быть под контролем центральной нервной системы. Без этого система может «далеко зайти».
В самом деле, легко представима такая ситуация: работая по закону Старлинга, сердце начинает, в ответ на хорошую заполненность предсердий, совершать более энергичные сокращения; это приводит к еще более хорошему заполнению предсердий, сердце начинает работать еще энергичнее, и т.д., – сердце «пошло в разнос».
Нечто подобное можно представить себе и в работе системы артериол: давление крови повысилось – артериолы зажались – сердце вынуждено повысить давление еще больше – артериолы зажались еще сильнее, и т.д.
Следовательно, центральная нервная система по отношению к системе кровообращения должна тонко проводить принцип: «ты саморегулируйся, но знай меру». Это очень деликатная и тонкая работа ведется нервной системой непрерывно, в том числе и тогда, когда мы спим. Одно из двух: либо ЦНС справляется с этой работой, либо – нет, и тогда встают задачи, самые сложные для медика – устранение неполадок в работе ЦНС.
l Памятник – пародия на дурную систему автоматического регулирования установлен в Стокгольме перед музеем техники: на столбе висит фонарь; его включение и выключение осуществляет фотоэлемент. А дальше так: стемнело – фотоэлемент включил фонарь – стало светло – фотоэлемент выключил фонарь – стало темно – и т.д.
l В отношении венозной части системы кровообращения, работающей в условиях низкого давления, а что гораздо важнее – низких перепадов давления (см. закон Пуазейля), природа распорядилась не полагаться полностью на эти перепады. Кровоток в этой части системы кровообращения поддерживается также через механику легочных сокращений, движений диафрагмы; движение крови в венах рук и ног стимулируется сократительной деятельностью мышц. Чтобы такие «подкачивающие насосы» работали эффективно, вены имеют систему клапанов, пропускающих кровь только в сторону предсердий.
Следовательно, лежание на диване не является оптимальной жизненной стратегией в деле поддержания работы сердечно-сосудистой системы на должном уровне. Двигательная активность организма предусмотрена природой как необходимое условие четкой работы этой системы.
l Венозные сосуды имеют тонкие стенки и сравнительно слабые мышечные волокна. Тем не менее, в венах возникает и по ним распространяется своя пульсовая волна. Ее предназначение – сгладить колебания давления крови, погасить эти колебания. Возникновение этих пульсаций давления связано с гидравлическим ударом, а точнее –с его предотвращением. Дело в том, что перед каждым очередным срабатыванием сердца вход в предсердие резко закрывается, и кровотоку в сторону предсердий становится некуда девать свою кинетическую энергию. Вместо опасных пиков давления возникают упругие растяжения стенок вен на входе в предсердия, а дальше все идет, как в артериальной пульсовой волне, только в обратном направлении – против тока крови.
Таким образом, в сторону капилляров идут две пульсовые волны, затухая окончательно на подступах к ним: кровеносная система бережно создает «режим наибольшего благоприятствования» в работе своего основного участка.
В соответствии с формулой (8), скорость венозной пульсовой волны меньше, чем артериальной. Она может быть измерена по записям венного пульса. Такие записи называются флебограммами.
Источник
Текст работы размещён без изображений и формул.
Полная версия работы доступна во вкладке “Файлы работы” в формате PDF
Несмотря на совершенствование кардиологической помощи в Российской Федерации, гипертоническая болезнь (ГБ) остается одной из самых значимых и распространенных сердечно-сосудистых патологий среди лиц пожилого возраста, обуславливающих высокий уровень смертности и инвалидизации. Современные знания о патогенезе ГБ связывают развитие и прогрессирование болезни с ранним поражением органов – мишеней, в первую очередь сердца и сосудов.
В кровеносной системе различают артерии, артериолы, гемокапилляры, венулы, вены и артериоловенулярные анастомозы. Взаимосвязь между артериями и венами осуществляется системой сосудов микроциркуляторного русла. Стенка всех артерий состоит из трех оболочек (intima, , adventitia), толщина, тканевый состав и функциональные свойства которых неодинаковы в сосудах разных типов, классификация которых основана на соотношении количества мышечных клеток и эластических волокон в средней оболочке (медии).
Структура волокон находится под контролем матриксных металлопротеиназ (ММП-1, ММП-8, ММП-13, ММП-7), приводящих к деструкции коллагена в определенных условиях. На артериальную жесткость влияют конечные продукты гликозилирования (AGEs), возникающие при неферментативном протеиновом гликолизе стойких поперечных связей между молекулами коллагена. Связанный с AGEs коллаген становится более жестким и менее восприимчивым к гидролитическому процессу [1].
Физиологически увеличение диаметра просвета центральных артерий вместе с утолщением и уплотнением сосудистой стенки носит адаптивный характер [2]. Повышение календарного возраста у больных сопровождается снижением упруго-эластических свойств артерий и артериол из-за изменения диаметра их просвета и скорости прохождения пульсовой волны.
При ГБ ремоделирование сосудов приобретает патологический характер и имеет важное значение в возникновении сердечно-сосудистых осложнений (инфаркта миокарда, инсульта, сердечной недостаточности).
В последние годы значительно возросли возможности медицины в диагностике изменений сосудов артериального русла. Для оценки выраженности жесткости сосудистой стенки (ЖСС), возраста сосудистой системы (ВСС), индекса сосудистого стресса (ИСС), индекса сатурации кислородом и типа пульсовой кривой всё чаще используют не дорогостоящие и малодоступные доплеровские технологии, а отечественные портативные диагностические приборы, например, АнгиоСкан-01П [3]. В его работе участвуют оптические сенсоры, которые в ближней инфракрасной области регистрируют пульсовую волнуобъема – фотоплетизмограмму. Фотодетектор преобразует свет в напряжение (преобразователь свет/напряжение) или в частоту (преобразователь свет/частота). Разработанная технология регистрации и контурный анализ пульсовой волны объема дает возможность получать клинически значимую информацию о состоянии сосудистой стенки по вышеперечисленным показателям.
Прирост давления в систолу за счет наложения отраженных волн оценивается индексом аугментации (AIx) [4]. Данный индекс, характеризуя отраженную систолическую волну, может выступать важным индикатором механической перегрузки, ведущей к артериальной гипертензии, гипертрофии миокарда и сердечно-сосудистым осложнениям [5]. При увеличении жесткости аорты отраженная волна приходится на позднюю систолу и вызывает прирост САД. AIx рассчитывается в процентах к ПАД (пульсовому АД):
AIx (%) = ,
где Р1 – первый пик пульсовой волны в систолу, Р2 – второй пик в систолу за счет отраженной волны. По мнению ряда авторов, являясь маркером сосудистой ригидности, AIx находится в прямой зависимости от возраста и к 75 годам достигает более 30% (O ́Rourke., 1999).
Исследование REASON показало, что чем выше жесткость сосудистой стенки (по показателю скорости пульсовой волны – СПВ), тем выше смертность (J. Blacher, A. Guerin, 1999). Другое исследование – ASCOT-CAFÉ установило влияние антигипертензивной терапии на прогноз у больных АГ при сопоставимом снижении плечевого артериального давления (АД), зависящего от степени уменьшения центрального давления в аорте, которое зависит от эластических свойств крупных артерий. Жесткость артерий увеличивается по мере прогрессирования ГБ и связана с уровнем АД. (Mathiassen O.N., 2007).
Цель исследования – оценка упруго-эластических свойств сосудов артериального русла у женщин пожилого возраста, страдающих гипертонической болезнью.
Материалы и методы исследования.
Для достижения цели отобраны 53 пациентки с ГБ II стадии 2 степени пожилого возраста (средний возраст – 68,7±1,5 года), в группу контроля включены 30 человек аналогичного возраста с нормальным уровнем АД.
Все обследуемые подписали информированное согласие на участие в исследовании. Критерии исключения: пациенты с вторичными формами АГ, гипертонической болезнью I, III стадии, сахарным диабетом, заболеваниями щитовидной железы, внутренних органов в стадии обострения, системными заболеваниями соединительной ткани, анемиями, злокачественными новообразованиями, тяжелыми нарушениями ритма.
Всем пациенткам проведено обследование с использованием фотоплетизмографического метода неинвазивным диагностическим аппаратно-программным комплексом «АнгиоСкан-01П». Определялись и оценивались следующие параметры: ЖСС, ВСС, ИСС, толщина комплекса интима – медиа (КИМ), показатель сатурации кислородом и тип пульсовой кривой. Исследование проводилось утром натощак, после 30-минутного отдыха в положении сидя. Употребление кофе и кофе-содержащих продуктов, алкоголя и других пищевых стимуляторов, тяжелая физическая нагрузка прекращались за сутки до проведения теста. Перед анализом результатов определялся характер их распределения.
Статистический анализ результатов проводился с использованием компьютерных программ istica 6.0, BIO. Различия между группами признавались достоверными при p <0,05. Для оценки силы связей между исследуемыми показателями выполнен корреляционный анализ по Пирсону.
Результаты исследования.
Клиническая характеристика обследованных лиц представлена в таблице 1.
Таблица 1
Клиническая характеристика обследованных лиц
Показатель | Контрольная группа (n=30) | Больные ГБ пожилого возраста (n=53) | Р1-2 |
ИМТ, кг/м2 | 27,2 ± 0,6 | 28,6 ± 0,6 | < 0,017 |
ЧСС, уд/мин | 72,3 ± 0,9 | 77,5 ± 1,4 | > 0,05 |
САД, мм. рт. ст | 121,55 ± 1,36 | 151,9 ± 0,7 | < 0,00002 |
ДАД, мм. рт. ст | 71,55 ± 1,7 | 91,1 ± 0,7 | < 0,00018 |
ПАД, мм. рт. ст | 49,8 ± 1,7 | 61,4 ± 1,4 | < 0,00003 |
Значения основных исследованных показателей представлены в таблице 2.
Таблица 2
Показатели упруго-эластических свойств сосудов по данным ангиосканирования у женщин пожилого возраста
Исследуемые показатели | Контрольная группа (n=30) | Больные ГБ пожилого возраста (n=53) | Р1-2 |
Жесткость сосудистой стенки, % | 11,5 ± 0,5 | 24,1 ± 1,3 | < 0,05 |
Возраст сосудистой стенки, лет | 46,8 ± 0,9 | 73,3 ± 1,9 | < 0,05 |
ИСC, ед. | 123,4 ± 5,9 | 366 ± 19,7 | < 0,001 |
КИМ, мм | 0,7±0,3 | 1,03 ± 0,9 | < 0,05 |
С внедрением в амбулаторную практику ангиосканирования появилась простая и доступная методика регистрации вариабельности сердечного ритма и расчета на его основе нового показателя – индекса сосудистого стресса. Нормой индекса Баевского признано значение от 50 до 150 ед. Его величина резко увеличивалась у больных ГБ пожилого возраста – 366 ± 19,7 ед. (р <0,001), что практически в 3 раза превышало уровень аналогичного показателя у группы сравнения, где ИСС находился в пределах физиологической нормы.
Для характеристики жесткости артерий эластического типа проанализированы также типы пульсовой кривой. Тип кривой С указывал на сохранение эластичности сосудов, тип А – на высокую жесткость аорты, тип В – отражал начальные изменения сосудистой стенки. В группе пациенток с ГБ пожилого возраста преобладал тип А (82,6%), тип В – 13,0% больных, тип С – у 4,4%. В группе сравнения превалировал тип В – 70 % и в 26,7% – тип С, тип А только в 3,3%.
AIx пациентов с ГБ составил 23,6±1,7 %, что достоверно превышало аналогичный показатель контрольной группы 16,1±0,5% (р <0,05). Полученные результаты доказывают, что сосудистая стенка подвержена инволютивным трансформациям в виде снижения эластичности, гибкости и тонуса артерий. Модифицируемые факторы – повышенное давление, избыточный вес ускоряют ремоделирование соединительнотканного матрикса, приводя к патологической жесткости сосудов, сужению их просвета и увеличению скорости распространения пульсовой волны.
Изменение ЖСС отражалось на периферическом газообмене, что индуцировало развитие гипоксических изменений в тканях организма, о чём свидетельствовало снижение уровня сатурации кислородом до 95,5 ± 0,25, по сравнению с аналогичными показателями практически здоровых людей 97,3 ± 0,2 (р <0,05).
Выводы.
1. Таким образом, у пожилых женщин, страдающих гипертонической болезнью на фотоплетизмограмме отмечалось увеличение показателей жесткости и возраста сосудистой стенки, индекса сосудистого стресса, снижение сатурации кислородом и изменение типа пульсовой кривой в сравнении с группой контроля, свидетельствующие о снижении эластичности гибкости сосудов и повышении их жесткости.
2. Комплексное исследование фотоплетизмографических параметров состояния жесткости сосудистой стенки позволяет прогнозировать структурно – морфологические и функциональные нарушения, является маркером поражения органов-мишеней и может быть использовано в амбулаторной практике.
СПИСОК ЛИТЕРАТУРЫ
Терегулов Ю.Э., Изменения эластических свойств артерий и гемодинамические процессы/ Ю.Э. Терегулов, С.Д. Маянская, Е. Т. Терегулова // Практическая медицина. – 2017. – Т.2, № 103. – С. 14-20.
Tosello F. Ascending aortic dilatation, arterial stiffness and cardiac organ damage in essential hypertension / F. Tosello, A. Milan, G. Bruno et al // Artery Re. – 2012. – V. 6. – № 4. – P. 162-162.
Горшунова Н.К., Коробанов Ю.Ю. Изменения упруго-эластических свойств артериального русла у больных артериальной гипертонией разного возраста // Материалы Х Нац. Конгресса терапевтов, М., 14-16 октября 2015. – С. 50-51.
Орлова, Я. А. Жесткость артерий как интегральный показатель сердечно-сосудистого риска: физиология, методы оценки и медикаментозной коррекции / Я. А. Орлова, Ф. Т. Агеев // Сердце. – 2006. – № 2. – С. 65-69.
Особенности сердечно-сосудистого ремоделирования у больных гипертонической болезнью I-IIIстадий/ Л.А. Белова, В.В. Машин, В.И. Рузов, О.Ю. Колотик-Каменева / Медицинский вестник Башкортостана. – 2015. – Т.10. – №4. – С.17-22.
Источник
