Какова плотность газа в этом сосуде
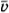
В сосуде содержится гелий под давлением кПа. Концентрацию гелия увеличили в раза, а среднюю кинетическую энергию его молекул уменьшили в раза.
Определите установившееся давление газа.
Ответ дайте в кПа.
Это задание решали 161 раз. С ним справились 34% пользователей.
Газ, который можно считать идеальным, перешел из состояния в состояние
Определите отношение давлений газа в начальном и конечном состояниях
Масса газа постоянна.
Это задание решали 48 раз. С ним справились 27% пользователей.
На рисунке изображен процесс перехода идеального газа постоянной массы из состояния в состояние
Найдите, во сколько раз изменилась абсолютная температура газа в состоянии по сравнению с абсолютной температурой в состоянии
Это задание решали 87 раз. С ним справились 71% пользователей.
Это задание решали 40 раз. С ним справились 57% пользователей.
На рисунке изображена зависимость давления от абсолютной температуры для
постоянной массы идеального газа.
Объем газа в состоянии равен л.
Определите объем газа (в л) в состоянии
Это задание решали 57 раз. С ним справились 70% пользователей.
Это задание решали 55 раз. С ним справились 44% пользователей.
моль идеального газа изохорно нагревают на К, при этом его давление
увеличивается в раза.
Какова первоначальная абсолютная температура газа?
Это задание решали 45 раз. С ним справились 38% пользователей.
Во сколько раз увеличится значение квадрата среднеквадратичной скорости
движения молекул, если для данной массы газа его внутренняя энергия
увеличится в раза?
Это задание решали 50 раз. С ним справились 66% пользователей.
Давление идеального газа в герметичном сосуде объемом л равно кПа.
Каким будет давление (в кПа) этого газа, если объем сосуда изотермически
увеличить в раза?
Это задание решали 58 раз. С ним справились 60% пользователей.
Давление газа на стенки герметичного баллона равно кПа.
Чему будет равно давление этого газа (в кПа) при увеличении квадрата средней скорости движения молекул газа в раза?
Это задание решали 41 раз. С ним справились 76% пользователей.
В ходе эксперимента давление разреженного газа в сосуде увеличилось в раза, а средняя энергия теплового движения его молекул уменьшилась в раза.
Во сколько раз увеличилась концентрация молекул газа в сосуде?
Это задание решали 115 раз. С ним справились 23% пользователей.
В сосуде находится идеальный газ при температуре C. Концентрация молекул этого газа равна м
Определите давление (в кПа), создаваемое
газом на стенки сосуда.
Постоянная Больцмана равна Дж/К.
Это задание решали 73 раза. С ним справились 55% пользователей.
В ходе эксперимента давление разреженного газа в сосуде уменьшилось в
раза.
Во сколько раз уменьшилось среднее значения квадрата скорости
движения молекул этого газа, если его концентрация осталась неизменной?
Это задание решали 22 раза. С ним справились 41% пользователей.
Идеальный газ находится в закрытом сосуде.
Во сколько раз уменьшится давление в этом сосуде, если его наполнить другим идеальным газом, молярная масса которого в два раза больше?
Абсолютная температура и плотность газа в
сосуде не изменились.
Это задание решали 62 раза. С ним справились 77% пользователей.
При проведении опыта в сосуд постоянного объема закачали воздух и одновременно сосуд с воздухом нагрели. В конечном равновесном состоянии воздуха в сосуде абсолютная температура повысилась в раза, а его давление возросло в раза по сравнению с начальными значениями.
Во сколько раз увеличилась масса воздуха в сосуде?
Это задание решали 75 раз. С ним справились 53% пользователей.
Источник
Учебник по физике
10 класс
При решении задач на применение молекулярно-кинетической теории идеального газа используются основное уравнение кинетической теории газов в форме (4.4.9) или (4.4.10) и вытекающие из него выражения для средней кинетической энергии молекул (4.5.5) и средней квадратичной скорости (4.7.2) или (4.7.3). Значительное количество задач удобно решать, используя формулу (4.5.6), связывающую давление газа с концентрацией молекул и абсолютной температурой. Внутренняя энергия идеальных одноатомных газов (например, инертных газов) вычисляется по формуле (4.8.1).
Задача 1
Чему равна масса газа, содержащегося в закрытом цилиндре вместимостью V = 0,5 л, если давление газа р = 5 • 105 Па, а средняя квадратичная скорость молекул 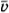 = 500 м/с?
= 500 м/с?
Решение. Согласно основному уравнению молекулярно-кинетической теории
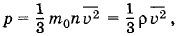
где ρ = m0n — плотность газа. Но ρ = 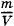 , где m — масса газа, а V — его объем. Поэтому
, где m — масса газа, а V — его объем. Поэтому
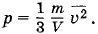
Откуда
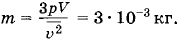
Задача 2
В воздухе при t = 27 °С взвешены пылинки сферической формы. Радиус пылинок r = 10-6 м. Плотность вещества пылинок ρ = 1,3 • 103 кг/м3. Определите средний квадрат скорости пылинок.
Решение. Пылинки принимают участие в броуновском движении. Средний квадрат скорости пылинки
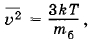
где mб — масса пылинки. Следовательно,
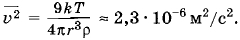
Задача 3
В сосуде находится 1 л воды при температуре 27 °С. Каким стало бы давление внутри сосуда, если бы силы взаимодействия между молекулами внезапно исчезли?
Решение. При исчезновении сил взаимодействия между молекулами вода превратилась бы в идеальный газ. Давление можно найти по уравнению состояния идеального газа:
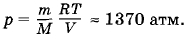
Задача 4
Два сосуда, содержащих различные газы, соединены трубкой с краном. Давление газа в первом сосуде p1, а число молекул N1. Давление газа во втором сосуде р2, число молекул N2. Какое давление установится в сосудах, если открыть кран соединительной трубки? Температуру считать постоянной.
Решение. Согласно формуле (4.5.6)
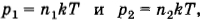
где
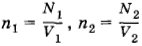
(здесь V1 и V2 — объемы сосудов). Следовательно,
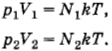
После того как кран будет открыт, давления выравняются и искомое давление согласно той же формуле (4.5.6) определится уравнением
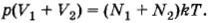
Подставляя сюда выражения для объемов из предыдущих формул, получим
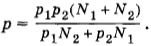
Задача 5
Плотность газа в баллоне газополной электрической лампы ρ = 0,9 кг/м3. При горении лампы давление в ней возросло с р1 = 8 • 104 Па до р2 = 1,1 • 105 Па. На сколько увеличилась при этом средняя квадратичная скорость молекул?
Решение. Плотность газа ρ = m0n, и основное уравнение мо-лекулярно-кинетической теории можно записать в форме
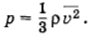
Поэтому
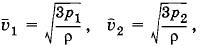
откуда
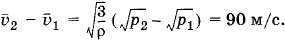
Упражнение З
- При какой температуре молекулы кислорода имеют такую же среднюю квадратичную скорость, что и молекулы азота при температуре 100 °С?
- На стенку площадью S налетает поток молекул со средней скоростью
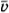 . Число молекул, движущихся по направлению к стенке, в единице объема n0, масса каждой молекулы m0. Найдите действующую на стенку силу и давление, если молекулы движутся перпендикулярно стенке и удары молекул о стенку абсолютно неупругие.
. Число молекул, движущихся по направлению к стенке, в единице объема n0, масса каждой молекулы m0. Найдите действующую на стенку силу и давление, если молекулы движутся перпендикулярно стенке и удары молекул о стенку абсолютно неупругие. - Какое давление на стенки сосуда производит водород, если число молекул в 1 см3 равно 4,1 • 1018, а средняя квадратичная скорость его молекул 2400 м/с?
- Определите число молекул кислорода в 1 м3, если давление равно 77 кПа, а средняя квадратичная скорость его молекул 400 м/с.
- Определите плотность газа, молекулы которого производят на стенки сосуда давление 1,6 • 105 Па. Средняя квадратичная скорость молекул 800 м/с.
- Какова средняя квадратичная скорость молекул газа, который занимает объем 1,3 м3 при давлении 5 • 104 Па? Масса газа 60 г.
- В цилиндре вместимостью 1,2 л содержится газ под давлением 105 Па. Среднее значение кинетической энергии каждой молекулы равно 6 • 10-21 Дж. Сколько молекул газа находится в цилиндре?
- Сколько молекул воздуха выходит из комнаты объемом V0 при повышении температуры от T1 до Т2? Атмосферное давление равно р0.
- Плотность смеси азота и водорода при температуре t = 47 °С и давлении р = 2 атм равна ρ = 0,3 г/л. Найдите концентрации молекул азота и водорода в смеси.
- Ампула объемом V = 1 см3, содержащая воздух при нормальных условиях, оставлена в космосе, где давление можно считать равным нулю. В ампуле проделано отверстие. Через какое время давление в ампуле станет равным нулю, если считать, что через отверстие каждую секунду вылетает 100 млн молекул?
- При повышении температуры идеального газа на 150 К средняя квадратичная скорость его молекул возросла с 400 до 500 м/с. На сколько надо нагреть этот газ, чтобы увеличить среднюю квадратичную скорость его молекул от 500 до 600 м/с?
- Изменится ли внутренняя энергия идеального газа при его изотермическом сжатии?
- Одноатомный газ, находящийся при постоянном давлении р = 2 • 106Па в цилиндре под поршнем площадью S = 160 см2, нагревается так, что поршень перемещается на расстояние Δh = 15 см. Найдите изменение внутренней энергии газа.
Источник
В данной работе предлагается определенный подход к классификации и способам решения задач на газовые законы. Такой подход позволит быстро сориентироваться в большом количестве задач на свойства газов и применить к ним те или иные приемы решения.
Основные теоретические сведения
Состояние газа характеризуется совокупностью трех физических величин или термодинамических параметров:объемом газа V, давлением Р и температурой Т. Состояние газа, при котором эти параметры остаются постоянными считают равновесным состоянием.В этом состоянии параметры газа связаны между собой уравнением состояния. Самый простой вид уравнение состояния имеет для идеального газа. Идеальным газом называют газ, молекулы которого не имеют размеров (материальные точки) и взаимодействуют друг с другом лишь при абсолютно упругих соударениях (отсутствует межмолекулярное притяжение и отталкивание). Реальные газы тем точнее подчиняются законам идеальных газов, чем меньше размеры их молекул (т.е. газ одноатомный), и чем больше он разряжен.
Уравнение состояния идеального газа или уравнение Менделеева-Клапейрона имеет вид:
– универсальная газовая постоянная
Из этого закона вытекает, что для двух произвольных состояний газа справедливо равенство, называемое уравнением Клапейрона:
Так же для идеальных газов имеют место следующие экспериментальные законы:
Закон Бойля — Мариотта:
Закон Гей-Люссака:
Закон Шарля:
Если в сосуде находится смесь нескольких газов, не вступающих друг с другом в химические реакции, то результирующее давление определяется по закону Дальтона: давление смеси равно сумме давлений, производимых каждым газом в отдельности, как если бы он один занимал весь сосуд.
Р = Р1 + Р2 +… + РN
Задачи, решение которых основывается на данных уравнениях, можно разделить на две группы:
§ задачи на применение уравнения Менделеева-Клапейрона.
- задачи на газовые законы.
ЗАДАЧИ НА ПРИМЕНЕНИЕ УРАВНЕНИЯ МЕНДЕЛЕЕВА-КЛАПЕЙРОНА.
Уравнение Менделеева-Клапейрона применяют тогда, когда
I. дано только одно состояние газа изадана масса газа (или вместо массы используют количество вещества или плотность газа).
II. масса газа не задана, но она меняется, то есть утечка газа или накачка.
При решении задач на применение равнения состояния идеального газа надо помнить:
1.если дана смесь газов, то уравнение Менделеева-Клапейрона записывают для каждого компонента в отдельности.Связь между парциальными давлениями газов, входящих в смесь и результирующим давлением смеси, устанавливается законом Дальтона.
2.если газ меняет свои термодинамические параметры или массу, уравнение Менделеева-Клапейрона записывают для каждого состояния газа в отдельности и полученную систему уравнений решают относительно искомой величины.
P.S.
§ Необходимо пользоваться только абсолютной температурой и сразу же переводить значения температуры по шкале Цельсия в значения по шкале Кельвина.
§ В задачах, где рассматривается движение сосуда с газом (пузырька воздуха, воздушного шара) к уравнению газового состояния добавляют уравнения механики.
§ если между газами происходит реакция, то надо составить уравнение реакции и определить продукты реакции
ПЕРВЫЙ ТИП ЗАДАЧ: НЕТ ИЗМЕНЕНИЯ МАССЫ
Определить давление кислорода в баллоне объемом V = 1 м3 при температуре t=27 °С. Масса кислорода m = 0,2 кг.
| V = 1 м3 μ = 0,032кг/моль m = 0,2 кг t=27 °С | Т=300К | Записываем уравнение Менделеева-Клапейрона и находим из него давление, производимое газом: |
| Р-? |
Баллон емкостью V= 12 л содержит углекислый газ. Давление газа Р = 1 МПа, температура Т = 300 К. Определить массу газа.
| V = 12 л μ =0,044кг/моль Т=300К Р =1 МПа | 0,012м3 1∙106Па | Записываем уравнение Менделеева-Клапейрона и находим массу газа |
| m -? |
При температуре Т = 309 К и давлении Р = 0,7 МПа плотность газа ρ = 12 кг/м3. Определить молярную массу газа.
| V = 12 л Т=309К Р =0,7 МПа ρ = 12 кг/м3 | 0,012м3 0,7∙106Па | Записываем уравнение Менделеева-Клапейрона Так как масса газа может быть определена через плотность газа и его объем имеем: |
| μ -? | ||
Отсюда находим молярную массу газа: | ||
Какова плотность водорода при нормальном атмосферном давлении и температуре 20°С.
| V = 12 л t=20°C Р =105 Па μ =0,002кг/моль | 0,012м3 T=293К | Нормальное атмосферное давление – это давление, равное 105 Па. И эту информацию запишем как данные задачи. Записываем уравнение Менделеева-Клапейрона |
| ρ -? | ||
Так как масса газа может быть определена через плотность газа и его объем имеем: Отсюда находим плотность газа: | ||
До какой температуры Т1 надо нагреть кислород, чтобы его плотность стала равна плотности водорода при том же давлении ,но при температуре Т2 = 200 К?
| Т2=200К ρ1 = ρ2 μ1 =0,032кг/моль μ2 =0,002кг/моль | Записываем уравнение Менделеева-Клапейрона для кислорода и для водорода через плотности газов: Так как по условию давление у двух газов одинаковое, то можно приравнять правые части данных уравнений: Сократим на R и на плотность ρ (по условию плотности газов равны) и найдем Т1 |
| Т1 -? | |
В сосуде объемом 4·10-3 м3 находится 0,012 кг газа при температуре 177°С. При какой температуре плотность этого газа будет равна 6·10-6 кг /см3, если давление газа остается неизменным.
Смесь газов
В баллоне объемом 25 литров находится 20г азота и 2 г гелия при 301К. Найдите давление в баллоне.
Определить плотность смеси, состоящей из 4 граммов водорода и 32 граммов кислорода при давлении 7°С и давлении 93кПа?
Сосуд емкостью 2V разделен пополам полупроницаемой перегородкой. В одной половине находится водород массой mВ и азот массой mА. В другой половине вакуум. Во время процесса поддерживается постоянная температура Т. Через перегородку может диффундировать только водород. Какое давление установиться в обеих частях сосуда?
| μа m1 = m2 = m3 = m μв μк Т | отсек №1 отсек №2 отсек №3 Диффундирует только водород. Следовательно, после завершения установочных процессов, в отсеке I будет водород, массой на |
| РI-? РII-? | |
половину меньшей, чем была, и весь азот. А во втором отсеке только половина массы водорода. Тогда для первого отсека установившееся давление равно: Для отсека II можно так же определить установившееся давление: | |
Вакуумированный сосуд разделен перегородками на три равных отсека, каждый объемом V. В средний отсек ввели одинаковые массы кислорода, азота и водорода. В результате чего давление в этом отсеке стало равно Р. Перегородка I проницаема только для молекул водорода, перегородка II проницаема для молекул всех газов. Найти давления Р1 Р2 и Р3, установившиеся в каждом отсеке, если температура газа поддерживается постоянной и равной Т.
| μа m1 = m2 = m3 = m μв μк Р | отсек №1 отсек №2 отсек №3 После диффундирования газов через перегородки в первом отсеке окажется треть массы водорода. Во втором и в третьем отсеках будет треть водорода, половина массы кислорода и половина всей массы азота. Тогда для первого отсека установившееся давление равно: |
| Р1-? Р2-? Р3-? | |
Если до диффундирования первоначальное давление во втором отсеке было Р, то можно записать: Отсюда можно найти Находим выражение для давления во втором и в третьем отсеках | |
И тогда давление в первом отсеке равно: | |
С химическими реакциями
В сосуде находится смесь азота и водорода. При температуре Т, когда азот полностью диссоциирован на атомы, давление равно Р (диссоциацией водорода можно пренебречь). При температуре 2Т, когда оба газа полностью диссоциированы, давление в сосуде 3Р. Каково отношение масс азота и водорода в смеси?
| μа μв Т1 =Т Т2 =2Т Р1=Р Р2=3Р | mв μвmа При температуре Т параметры газов в сосуде следующие: И результирующее давление в сосуде по закону Дальтона равно: |
2Т 2Т При температуре 2Т параметры газов в сосуде следующие: И результирующее давление в сосуде по закону Дальтона равно: | |
В герметично закрытом сосуде находится 1 моль неона и 2 моля водорода. При температуре Т1=300К, когда весь водород молекулярный, атмосферное давление в сосуде Р1=105 Па. При температуре Т2=3000К давление возросло до Р2=1,5∙105 Па. Какая часть молекул водорода диссоциировала на атомы?
| ν1=1 моль ν2=2 моль Т1 =300К Т2 =3000К Р1=105 Па Р2=1,5∙105 Па | При температуре Т1 давление газа в сосуде складывается из парциальных давлений двух газов и равно: При температуре Т2 давление газа равно: |
Из уравнения (1): Из первого находим объем V: | |
В закрытом баллоне находится смесь из m1= 0,50 г водорода и m2 = 8,0 г кислорода при давлении Р1= 2,35∙105 Па. Между газами происходит реакция с образованием водяного пара. Какое давление Р установится в баллоне после охлаждения до первоначальной температуры? Конденсации пара не происходит.
| V = 25 л μ1 = 2г/моль m1 = 0,5 г μ2 = 32г/моль m2 = 8 г | В сосуде будет происходить реакция водорода с кислородом с образованием воды:
|
| Р-? | Из уравнения реакции видно, что если в реакцию вступит весь водород, то кислорода только половина |
В результате образуется ν3=0,25 молей водяного пара и останется ν4= 0,125молей кислорода. По закону Дальтона результирующее давление в сосуде равно сумме парциальных давлений Так как известно, что до реакции давление в сосуде было Р1, то для этого момента можно так же применить закон Дальтона: Решаем полученные уравнение в системе относительно неизвестного: Дата добавления: 2018-04-04; просмотров: 2493; | |
Источник

ТОП 10:
| А 1 | Молярная масса газа 0,044 кг/моль. Какова плотность этого газа при температуре 300 К и давлении 105 Па? 1) 0,5 кг/м3 2) 1,77 кг/м3 3) 3,53 кг/м3 4) 8,31 кг/м3 |
| А 2 | При температуре 300 К и давлении 100 кПа плотность газа 1,77 кг/м3. Молярная масса этого газа равна 1) 2) 3) 4) |
| А 3 | При температуре 200 К и давлении 166 кПа плотность газа 2,4 кг/м3. Молярная масса этого газа равна 1) 2) 3) 4) |
| А 4 | При температуре 240 К и давлении 166 кПа плотность газа 2 кг/м3. Молярная масса этого газа равна 1) 2) 3) 4) |
| А 5 | При температуре 100 К и давлении 100 кПа плотность газа равна 3,85 кг/м3. Молярная масса этого газа равна 1) 2) 3) 4) |
| А 6 | При температуре 10 оС и давлении 100 кПа плотность газа равна 2,5 кг/м3. Молярная масса этого газа равна 1) 59 г/моль 2) 69 г/моль 3) кг/моль 4) кг/моль |
| А 7 | Газ при температуре 200 К и давлении 200 кПа имеет плотность 3,85 кг/ м3. Что это за газ? 1) водород 2) неон 3) кислород 4) азот |
| А 8 | Плотность идеального газа меняется с течением времени так, как показано на рисунке. Температура газа при этом постоянна. Во сколько раз давление газа при максимальной плотности больше, чем при минимальной? |
| 1) 0,3 2) 1,5 3) 3 4) 9 | |
| Атмосфера Венеры состоит из двуокиси углерода с молярной массой , имеет температуру (у поверхности) 700 К и давление 90 земных атмосфер. Для атмосферы Земли температура у поверхности близка к 300 К. Каково отношение плотностей атмосфер у поверхностей Венеры и Земли? Ответ округлите до целых. Молярная масса воздуха 0,029 кг/моль. | |
| С 10 | По фотографии При исследовании уравнения состояния газа ученик соединил сосуд (1) объёмом 150 мл с манометром (2) тонкой трубкой и опустил сосуд в горячую воду. Чему равна плотность воздуха в сосуде? Начальное показание манометра равно 0 мм рт. ст. Шкала манометра и нижняя шкала барометра (3) проградуированы в мм рт. ст. Верхняя шкала барометра проградуирована в кПа. Объём измерительного механизма манометра и соединительной трубки значительно меньше 150 мл. Молярная масса воздуха 0,029 кг/моль. (на фотографии видно, что барометр показывает 746 мм рт. ст.; манометр 40 мм рт. ст.; термометр 45 °С.) |
Воздухоплавание
| С 11 | Воздушный шар имеет газонепроницаемую оболочку массой 400 кг и содержит 100 кг гелия. Какой груз он может удерживать в воздухе на высоте, где температура воздуха 17°С и давление 105 Па? Молярная масса воздуха 0,029 кг/моль, а гелия 0,004 кг/моль. Считать, что оболочка шара не оказывает сопротивления изменению объема шара. |
| С 12 | Воздушный шар с газонепроницаемой оболочкой массой 400 кг заполнен гелием. На высоте, где температура воздуха 17°С и давление 105 Па, шар может удерживать груз массой 225 кг. Какова масса гелия в оболочке шара? Молярная масса воздуха 0,029 кг/моль, гелия 0,004 кг/моль. Считать, что оболочка шара не оказывает сопротивления изменению объема шара. |
| С 13 | Сферическую оболочку воздушного шара делают из материала, квадратный метр которого имеет массу 1 кг. Шар наполняют гелием при атмосферном давлении 105 Па. Определите минимальную массу оболочки, при которой шар начнет поднимать сам себя. Температура гелия и окружающего воздуха одинакова и равна 0 оС. (Площадь сферы , объем шара ). Молярная масса гелия 0,004 кг/моль, а воздуха 0,029 кг/моль. |
| С 14 | Сферическую оболочку воздушного шара делают из материала, квадратный метр которого имеет массу 2 кг. Шар наполняют гелием при атмосферном давлении 105 Па. Определите минимальную массу оболочки, при которой шар начнет поднимать сам себя. Температура гелия и окружающего воздуха одинакова и равна 0 оС. (Площадь сферы , объём шара ). Молярная масса гелия 0,004 кг/моль, а воздуха 0,029 кг/моль. |
| С 15 | Сферическую оболочку воздушного шара делают из материала, квадратный метр которого имеет массу 1 кг. Шар наполняют гелием при атмосферном давлении 105 Па. Определите массу гелия, при которой шар поднимет сам себя. Температура гелия и окружающего воздуха одинакова и равна 0 оС. (Площадь сферы , объём шара ). Молярная масса гелия 0,004 кг/моль, а воздуха 0,029 кг/моль. |
| С 16 | Сферическую оболочку воздушного шара делают из материала, квадратный метр которого имеет массу 1 кг. Радиус оболочки шара м. Шар наполняют газом при атмосферном давлении 105 Па. Температура газа и окружающего воздуха одинакова и равна 0 оС. Определите молярную массу газа, если оказалось, что шар может в таких условиях поднять только себя. (Площадь сферы , объем шара ). Молярная масса воздуха 0,029 кг/моль. |
| С 17 | Сферическую оболочку воздушного шара наполняют гелием при атмосферном давлении 100 кПа. Минимальная масса оболочки, при которой шар начинает поднимать сам себя, равна 500 кг. Температура гелия и окружающего воздуха одинакова и равна 0 оС. Чему равна масса одного квадратного метра материала оболочки шара? (Площадь сферы , объём шара ). Молярная масса гелия 0,004 кг/моль, а воздуха 0,029 кг/моль. |
| С 18 | Сферическая оболочка воздушного шара сделана из материала, квадратный метр которого имеет массу 1 кг. Шар наполнен газом при атмосферном давлении 105 Па. Во сколько раз молярная масса воздуха больше молярной массы газа, которым наполнен шар, если шар поднимает сам себя при радиусе 2,7 м? Температура газа и окружающего воздуха одинакова и равна 0 оС. (Площадь сферы , объём шара ). |
Давление газа на глубине
Источник
