Кальцинаты в сосудах мозга

Болезнь Фара – идиопатическая симметричная кальцификация церебральных структур: подкорковых ганглиев, коры полушарий, мозжечка. Может протекать бессимптомно, клинически проявляется экстрапирамидными расстройствами (гиперкинезами, паркинсонизмом), мозжечковыми нарушениями, интеллектуальным снижением. Диагностируется по данным церебральной КТ при исключении вторичного характера кальцинированных очагов по результатам биохимических, ультразвуковых, ПЦР исследований. Лечение симптоматическое с применением средств, улучшающих тканевый обмен, цитопротекторов, препаратов леводопы, антиконвульсантов.
Общие сведения
Болезнь Фара включает случаи первичного идиопатического отложения кальция в мозговых структурах, вторичные формы церебрального кальциноза в рамках данной патологии не рассматриваются. Первые подробные описания заболевания сделаны в 1930 году немецким невропатологом К.Т. Фаром. Болезнь Фара является редкой нозологией, распространённость составляет менее 1 случая на 1 млн. населения. Гендерные различия в заболеваемости выражаются соотношением мужчин и женщин 2:1. Патология проявляется в любом возрастном периоде, чаще в 30-60 лет. Прижизненно выявляется лишь в 1-2% случаев, что объясняется наличием бессимптомных вариантов течения, диагностикой заболевания под видом иных нейродегенеративных процессов (болезни Паркинсона, сенильной хореи).
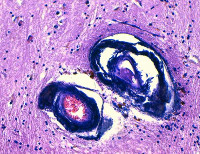
Болезнь Фара
Причины болезни Фара
Приводящие к возникновению заболевания этиологические факторы точно не установлены. Предполагают генетический характер патологии с локализацией нарушений в четырнадцатой (локус 14q13), второй (локус 2q37) хромосомах, хромосомном участке q21.1-q11.23 восьмой хромосомы. При исследовании семейных случаев выявлена генетическая гетерогенность. Установлены варианты, когда болезнь наследовалась аутосомно-доминантным и Х-сцепленным путём. Описаны спорадические случаи, при которых семейный характер патологии не прослеживается. Известно, что клиническая манифестация происходит, когда общий объём кальцификатов достигает критической величины – 3,9 см³.
Патогенез
Формирующие болезнь патогенетические механизмы окончательно не определены. Предполагаются генетически детерминированные сдвиги церебрального метаболизма, становящиеся причиной отложения в мозговых тканях избытков кальция. Выраженная кальцификация подкорковых образований становится причиной дезорганизации лобно-субкортикальной системы, регулирующей произвольные движения и обеспечивающей когнитивные функции (память, мышление, внимание).
Морфологически кальцификаты обнаруживаются симметрично в различных структурах: коре мозга, белом веществе, подкорковых ганглиях, внутренней капсуле, мозжечке, стенках мелких артерий, реже вен. Характерно наличие периваскулярных мелких кальциевых конгломератов. Наиболее массивная кальцификация выявляется в подкорковых отделах. Микроскопически кальцификаты отличаются типичной структурой, представленной нитями толщиной 140-400 мкм. Они зачастую содержат минеральные комплексы с включениями железа, меди, алюминия, фосфора, свинца, цинка, кобальта.
Классификация
В практической неврологии болезнь Фара подразделяется на две клинические формы, отличающиеся возрастом манифестации, типом преобладающей симптоматики:
- Ювенильная форма – дебют заболевания происходит в детском или подростковом периоде. Характерны экстрапирамидные нарушения в виде атетоза, хореи, мышечной дистонии. Патология может сопровождаться олигофренией. По мере взросления отмечается смена гиперкинезов паркинсонической симптоматикой.
- Сенильная форма – манифестирует в пожилом и среднем возрасте. Клиническая картина характеризуется доминированием симптомов паркинсонизма в сочетании с когнитивными расстройствами. Типична прогрессирующая деменция.
Симптомы болезни Фара
В типичных случаях болезнь дебютирует появлением утомляемости, неуклюжести движений, шаткости ходьбы, изменений речи, непроизвольных двигательных актов или ночных мышечных спазмов. Основу клинических проявлений составляют экстрапирамидные нарушения. В молодом возрасте это различные гиперкинезы: атетоз – непроизвольные червеобразные движения в пальцах кистей, хореоатетоз – сочетание атетоза с быстрыми насильственными движениями в конечностях, торсионная дистония – тонические мышечные спазмы, придающие телу неестественные позы. У взрослых наблюдается вторичный паркинсонизм: амимия лица, брадикинезия, замедленные скованные движения, шаркающая походка, постуральный тремор.
Симптоматика паркинсонизма зачастую сочетается с мозжечковой атаксией (дискоординация, несоразмерность движений, нистагм), пирамидной недостаточностью (слабость в конечностях, повышенные сухожильные рефлексы, патологические стопные знаки). Возможна дизартрия, дисфагия, недержание мочи. Эпилептические пароксизмы более характерны для ювенильной формы заболевания, могут отмечаться у взрослых.
Сопровождающие болезнь Фара когнитивные нарушения характеризуются снижением памяти на текущие и прошлые события, замедленным мышлением, неустойчивым вниманием, угасанием способности к аналитической и синтетической интеллектуальной деятельности. Прогрессирование расстройств когнитивной сферы у детей приводит к олигофрении, во взрослом возрасте – к развитию корково-подкорковой деменции с элементами агнозии, апраксии, алексии. Однако часть больных ювенильной формой остаются интеллектуально сохранными.
Диагностика
Основным диагностическим методом, позволяющим неврологу достоверно установить наличие очагов кальциноза в мозговых тканях, является КТ головного мозга. Интенсивность очагов на томограммах отражает уровень концентрации кальция. МРТ головного мозга значительно хуже визуализирует кальцификаты, но позволяет оценить сопутствующие дегенеративные процессы. С целью подтверждения идиопатического характера патологии проводится целый ряд дополнительных обследований:
- Биохимический анализ крови. Производится определение электролитов крови: кальция, фосфора, железа, натрия. Отсутствие существенных отклонений позволяет исключить общие обменные нарушения в организме, приводящие к отложению кальция.
- Определение уровня паратгормона . Нормальные показатели концентрации гормона в крови исключают наличие гипопаратиреоза, псевдогипопаратиреоза, как наиболее распространённых причин кальцификации.
- УЗИ щитовидной и паращитовидных желёз. У пациентов с болезнью Фара эхоскопическая картина остается в пределах нормы, что исключает связанные с поражением этих желёз гормонально-обменные нарушения.
- ТКДГ церебральных сосудов. Необходима для оценки мозговой гемодинамики, выявления хронической церебральной ишемии как первопричины дегенеративных изменений, сопровождающихся кальцификацией.
- ПЦР-исследования. Направлены на выявление токсоплазмы, цитомегаловируса и других инфекционных агентов, способных вызывать воспалительные изменения мозговых тканей с образованием кальцификатов.
Диагноз болезнь Фара правомочен после исключения вторичного характера церебральной кальцификации, наблюдающейся при эндокринных (гипопаратиреоз, псевдогипопаратиреоз, гипотиреоз), сосудистых (атеросклероз, амилоидоз сосудов), инфекционных (краснуха, цистицеркоз, токсоплазмоз, цитомегалия) заболеваниях. Дифференциальная диагностика проводится также с болезнью Галлервордена-Шпатца, туберозным склерозом.
Лечение болезни Фара
Поскольку патогенез заболевания остаётся неясным, терапия имеет преимущественно симптоматический характер. С целью улучшения обменных процессов применяются стимуляторы тканевого метаболизма (ацетилкарнитин, глютаминовая кислота, комплекс L-цитруллин+малат, никотинамид), цитопротекторы (рибофлавин, янтарная кислота, мельдоний). При симптомах паркинсонизма предпочтительно назначение фармпрепаратов леводопы, при гиперкинезах – холинолитиков, бензодиазепинов. Наличие эпилептических приступов служит показанием к лечению современными антиконвульсантами (леветирацетамом). В комплексной терапии применяется лечебная физкультура, водолечение, когнитивные тренинги.
Прогноз и профилактика
Клинически проявленная болезнь Фара рассматривается как хроническое нейродегенеративное заболевание. Прогноз выздоровления неблагоприятный, однако, при должном уровне поддерживающей симптоматической терапии состояние пациентов длительное время остаётся удовлетворительным. Субклинический вариант не сказывается на здоровье и когнитивных способностях больного, может быть случайной находкой при проведении компьютерной томографии. Специфические меры, позволяющие предупредить развитие болезни, не разработаны.
Источник

Кальций – макроэлемент, участвующий в обменных процессах, является строительным материалом для крепких костей и зубов. Избыточное поступление минерала на фоне нарушения усвоения приводит к его отложению в мягких тканях, внутренних органах и кровеносных сосудах. Такой патологический процесс получил название кальциноз. Кальцификация продолжительное время может протекать бессимптомно и привести к необратимым последствиям в организме.
Классификация кальцификации
Кальцификация – патологический процесс, для которого характерно отложение кальция. В зависимости от локализации макроэлемент может накапливаться и поражать:
- сосудистую систему;
- сердечную мышцу;
- головной мозг;
- суставы и сухожилия;
- мягкие ткани и диагностироваться в молочных железах, мышцах и связках, жировых отложениях;
- печень и желчный пузырь;
- органы мочевыделительной системы, чаще почки и мочевой резервуар.
В зависимости от этиологии кальцификация бывает 3 типов:
- дистрофическая – наиболее распространенный вид патологического процесса, который развивается как ответная реакция на любые повреждения мягких тканей и внутренних органов, в том числе после имплантации различных медицинских устройств;
- метастатический вид болезни развивается в результате нарушения баланса кальция, фосфора и магния в организме на фоне почечной недостаточности, дискальциемии и прочих тяжелых патологий;
- опухолевый тип кальциноза связан с формированием шаровидных новообразований вокруг суставов, его этиология до конца не изучена.
Также кальциноз может быть системным, поражая все органы человека или местным, с локализацией в одном органе или системе.
Причины кальцификации
Отложение кальция в мягких тканях, внутренних органах происходит в результате нарушения метаболизма, что приводит к нарушению усвоения важного макроэлемента для человеческого организма. Чаще всего, сбои в обменных процессах вызваны эндокринными патологиями, болезнями почек инфекционного и аутоиммунного характера, нарушением выработки ферментов при печеночных патологиях и заболеваний поджелудочной железы.
К нарушению обмена кальция может привести недостаточное поступление магния и избыток витамина Д, которые принимают непосредственное участие в усвоении организмом макроэлемента.
Кальцификация отдельного органа может развиваться при образовании кист, опухолей доброкачественного и злокачественного характера, дистрофии тканей.
Процесс образования кальциевых конгломератов также затрагивает соединительную и хрящевую ткань, атеросклеротические бляшки, погибшие паразитирующие микроорганизмы, импланты.
Признаки кальцификации
На начальных этапах распознать патологию крайне сложно в связи с ее бессимптомным течением. Однако некоторые виды имеют достаточно выраженную клиническую картину.
При системном виде кальциноза или при поражении кожных покровов, суставов, эпидермис покрывается небольшими пузырьками, изменения структуры и окраса не наблюдается. По мере прогрессирования патологии кальциевые конгломераты разрастаются и становятся более плотными на ощупь, изменяют свой окрас. Возможно образование свищей.
Известковые отложения в ходе плановых осмотров специалистами или при инструментальном исследовании могут обнаруживаться на зубах, костях, сосудах, мышечных и нервных волокнах. Скопление макроэлемента на тканях органов приводит к нарушению их функционирования.
При поражении сердечной мышцы и сосудистой системы, у больного появляется болевой синдром в грудине, руке, шее, спине, который сохраняется продолжительное время. Также происходит нарушение кровотока, что приводит к скачкам артериального давления, появлению чувства холода в конечностях.
При поражении почек нарастают симптомы интоксикации, нарушается диурез, кожные покровы становятся сухими, вялыми. При кальцификации органов пищеварительного тракта, нарушается их работа, что приводит к возникновению тошноты, рвоты, чувства тяжести в абдоминальной области, запоров.
При поражении и скоплении большого количества кальция в головном мозге больной испытывает частые приступы головной боли и головокружения, скачки внутричерепного давления, нарушение координации движения, ухудшение памяти, проблемы со зрением и слухом. По мере прогрессирования болезни возможны обмороки.
Вместе с этим кальциноз приводит к снижению работоспособности, постоянной вялости и усталости, слабости, снижению массы тела.
Диагностика
Для подтверждения диагноза используется рентгенологическая диагностика. Данный метод позволяет определить характер и размер отложений, а также степень поражения органа, в котором локализуется кальциевый конгломерат. В качестве дополнительных методов исследования назначается:
- УЗИ с допплерографией для изучения состояния сосудистой системы;
- ЭКГ для исследования сердечной мышцы;
- КТ с введением контрастирующего вещества;
- МРТ.
Для выявления причины кальцификации тканей назначаются дополнительные исследования, в виде общеклинического и биохимического анализа крови. Последний способ позволяет определить уровень кальция, фосфора и магния в крови. При нарушении функций почек назначается общеклинический и бактериологический анализ мочи для оценки работоспособности почек.
Для исключения злокачественного характера новообразований в пораженном органе назначается биопсия тканей. Данный метод предполагает забор биологического материала и его исследования под микроскопом в лабораторных условиях. Биопсия помогает также дифференцировать доброкачественное и злокачественное новообразование.
Лечение
Для лечения кальциноза назначается терапевтический курс, который поможет справиться с заболеванием-первопричиной. Так, если к избыточному отложению кальция привело воспаление инфекционной природы, назначаются антибактериальные препараты.
При нарушении усвоения кальция назначаются медикаменты, содержащие магний, который является антагонистом кальция. Достаточное поступление магния с продуктами питания и медикаментозными препаратами позволяет растворить конгломераты и вывести избыток кальция из организма. В ходе лечения важно принимать диуретики, которые помогут ускорить процесс выведения макроэлемента.
В процессе усвоения кальция принимает участие витамин Д, избыточное поступление которого также отрицательно сказывается на состоянии организма. Поэтому в ходе лечения необходимо соблюдать специальную диету, которая исключает употребление в большом количестве продуктов питания, богатых кальцием и витамином Д. К таким относят рыбу жирных сортов, листовую зелень, молочные продукты, яичный желток, орехи.
При неэффективности консервативных методов лечения, а также образовании конгломератов больших размеров назначается их оперативное удаление. Выбор метода хирургического вмешательства проводится в зависимости от размеров скоплений кальция, а также их локализации.
Кальциноз в период беременности
Отложение кальция во время вынашивания ребенка чаще всего диагностируется в конце третьего триместра гестационного периода. С медицинской точки зрения такой процесс допустим и связан с видоизменением плаценты.
Если кальцификация диагностируется на более ранних сроках, это может привести к преждевременному созреванию плаценты. Как правило, кальциноз у беременных связан с употреблением большого количества продуктов, богатых кальцием, инфекционными процессами и метаболическими нарушениями.
Избыток макроэлемента в организме беременной женщины также опасен, как и его недостаток. Может стать причиной травм ребенка и матери в период родоразрешения.
Профилактика
Чтобы предупредить кальцификацию мягких тканей и внутренних органов следует особое внимание уделить правильному питанию. Важно обеспечить достаточное поступление всех минералов и витаминов в организм, чтобы предупредить развитие патологий различной этиологии.
Также людям с врожденными и приобретенными заболеваниями сердечно-сосудистой системы, почек, эндокринными патологиями важно регулярно проходить плановые осмотры у специалистов, что поможет своевременно предупредить развитие осложнений.
Лечение различных заболеваний стоит проводить только под контролем специалиста и в соответствии с его рекомендациями. Некоторые группы лекарственных препаратов, в том числе для снижения уровня холестерина в крови, артериального давления, а также антибактериальные и гормональные средства могут привести к повышению уровня кальция в организме и нарушению его обмена.
Для предупреждения кальциноза следует вести активный образ жизни, который помогает восстановить нормальный метаболизм, отказаться от употребления алкогольных напитков и табакокурения.
Кальцификация тканей – патологический процесс, связанный с высокой концентрацией кальция в организме. Поражает сердечно-сосудистую, нервную, опорно-двигательную, пищеварительную и мочевыделительную системы. Для предупреждения болезни необходимо правильно питаться и вести здоровый образ жизни. В качестве терапии назначается курс медикаментозных препаратов для устранения причины патологического процесса и нормализации уровня кальция и магния в крови.
Источник
Неврологические симптомы разного рода, например, экстрапирамидные нарушения (ригидность, тремор, гиперкинезы), эпилептические припадки, деменция, юный возраст, гипопаратиреоз – все это является сигналом для специалистов к постановке диагноза редкого заболевания «болезнь Фара».
Болезнь Фара – это редкое нейродегенеративное заболевание, связанное с неатеросклеротическим обызвествления коры полушарий мозга, базальных ганглиев и зубчатых ядер мозжечка, вследствие отложения солей кальция и железа в стенки мелких артерий и артериол, а также в вещество головного мозга.
Этиология и патогенез. Этиология болезни Фара окончательно не установлена. Главным патогенетическим механизмом является нарушение кальций-фосфорного обмена. Основной причиной, которая может привести к данному нарушению обмена считается первичный (аутоиммунный) или послеоперационный эндокринный аденоматоз щитовидной или паращитовидных желез. Другим возможным механизмом называют хронический респираторный алкалоз, что приводит к электролитных нарушений (в виде гиперкальциемии, гипонатриемии), и как следствие приводит к гипоксии головного мозга. Существует мнение о генетические механизмы нарушения обмена кальция при болезни Фара, ассоциированных с определенным локусом хромосомы 14q. Однако взаимосвязь гипотиреоза с локусом 11-й хромосомы, псевдогипопаратиреоза – 20-й, а синдрома Дауна – 21-й исключает возможность того, что за накопление кальция и других минералов в головном мозге отвечает только один ген.
Спорадические случаи обызвествления мозговых структур обнаруживают у больных гипопаратиреозом, у детей с болезнью Дауна, лейкоэнцефалиты. Также спорадические случаи обызвествления мозговых структур могут наблюдаться после введения в субарахноидальное пространство метотрексата, после облучения черепа, отравления угарным газом, свинцом, при хронической интоксикации витамином D. Случаи кальцификации подкорковых структур описаны у лиц, перенесших краснуху, у больных СПИДом. Кальцификаты в базальных ганглиях нередко оказываются у лиц пожилого возраста, поэтому на практике чаще встречается случайное сочетание болезни Паркинсона и кальцификации базальных ганглиев, чем болезнь Фара. Поскольку целый ряд расстройств сопровождается двусторонним кальцификацией подкорковых структур, лучше использовать термин, отражающий анатомическую локализацию, например «стриопаллидозубчатый», «стриопаллидарный» или «мозжечковой кальциноз».
При болезни Фара кальцификация встречается во всех участках мозга, но преобладает в области базальных ганглиев. Описано, что поражаются обычно артерии среднего и мелкого диаметра и капилляры, но редко встречаются и кальцинированные вены. По ходу сосудов в прилегающей мозговой ткани обнаруживают россыпь мелких обособленных конгломератов кальция. По данным A. Gusеo и соавт., Кальцинаты состоят из тонких нитей размером 140-400 мкм. В образцах тканей обнаруживаются также следы мукополисахаридов, алюминия, мышьяка, кобальта, меди, молибдена, железа, свинца, марганца, магния, фосфора, серебра и цинка.
Клиническая картина заболевания разнообразна и не коррелирует с морфологическими данными. Болезнь Фара часто протекает бессимптомно. По данным ряда авторов, прижизненно эта болезнь проявляется лишь в 1-2% случаев. Так, H. Goldscheider и соавт., Проведя КТ головного мозга в 8000 больных, обнаружили кальцификацию базальных ганглиев в 19 и только в 6 из них были клинические симптомы болезни.
Неврологическими симптомами являются разного рода экстрапирамидные расстройства (ригидность, тремор, гиперкинезы), преходящие или стойкие пирамидные знаки, эпилептические припадки, деменция. К наиболее распространенным проявлений болезни Фара принадлежат двигательные нарушения, половина которых представлена паркинсонизмом, в других случаях наблюдаются гиперкинезы (хорея, тремор, дистония, атетоз, орофациальная дискинезия).
Когнитивные расстройства является вторым по распространенности синдромом, за ним следуют мозжечковые симптомы и нарушения речи. Нередко наблюдается сочетание различных клинических единиц, например гипокинеза, когнитивных нарушений и церебеллярных симптомов.
Другие неврологические микросимптомы включают пирамидные нарушения, психиатрические расстройства, нарушение походки и чувствительности, а также боль. По мнению большинства авторов, неврологические расстройства лишь косвенно связанные с локализацией и размерами ячеек. Нередко отмечаются проявления гиперпаратиреоз или гипопаратиреоз: локальные судороги, тетанические судороги, боли в дистальных отделах конечностей, положительные симптомы Хвостека и Труссо. Заболевание поражает людей любого возраста, но чаще всего лиц молодого и среднего возраста (20-30 лет). Условно выделяют три группы больных: лиц молодого возраста с признаками церебрального кальциноза, пациентов с гипопаратиреозом и пожилых больных с относительно невыраженной кальцификацией.
Диагностика и лечение. Диагноз подтверждается нейровизуализационнымы методиками после исключения нарушений обмена кальция и пороков развития. При проведении рентгенографии черепа, компьютерной томографии у пациентов с болезнью Фара в головном мозге наблюдаются множественные массивные симметричные очаги обызвествления подкорковых ганглиев (чаще бледного шара) и колена внутренней капсулы (рентгенологический синдром Фара).
Несмотря на широкую доступность КТ или МРТ и частые случайные находки отложений кальция в подкорковых ядрах у бессимптомных пациентов, болезнь Фара (двусторонний стриопаллидозубчатый кальциноз) остается редким заболеванием. Если паркинсонизм сочетается с деменцией и мозжечковые симптомами, то КТ головного мозга остается важнейшим диагностическим инструментом, поскольку вышеописанное заболевание часто сопровождается вышеупомянутыми нарушениями. Главной проблемой в дифференциальной диагностике остается гипопаратиреоз. Определение кальция и паратгормона сыворотки помогает отличить гипопаратиреоз от двустороннего стриопаллидозубчатого кальциноза, если при томографии визуализируется двусторонняя кальцификация стриопаллидозубчатых структур.
Дифференциальная диагностика болезни Фара часто проводится с паразитарных поражением нервной системы (токсоплазмоз, эхинококкоз, цистицеркоз). В этих случаях диагностическую ценность представляют эпидемиологический анамнез и специфические серологические реакции крови и спинномозговой жидкости. Реже заболевание дифференцируют с туберозным склерозом Бурневиля, при котором встречаются характерные изменения кожи.
Терапия носит симптоматический характер и, как правило, направлена на улучшение кальций-фосфорного обмена; при наличии симптомов паркинсонизма лучше использовать препараты леводопы (мадопар, синемет, наком), чем дофаминовые агонисты. В качестве патогенетического лечения показано назначение антиоксидантов, мозговых метаболитов, влияние на электролитный состав крови.
Источник
