Кровотечение из сосудов пуповины
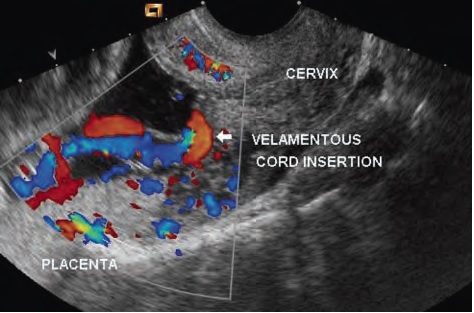
Vasa Previa (Предлежание Сосудов, ПС) может иметь катастрофические последствия для жизни плода и новорожденного. На самом деле существует всего несколько пренатальных ультразвуковых диагнозов, которые имеют настолько выраженное, прямое влияние на исход родов и так значительно повышают выживаемость среди тех, у кого было своевременно диагностировано данное состояние. Исключение ПС с помощью ультразвука занимает менее минуты и обязательно должно входить в стандартные скрининговые ультразвуковые исследования.
«Vasa Previa отняла у нас нашего прекрасного мальчика, нашего первого ребёнка, и мы никогда уже не будем такими, как прежде. Всё о чем мы можем мечтать, это чтобы хоть у кого-то одного из медицинского персонала хватило предусмотрительности сканировать нас на предмет наличия такого состояния.» – Natalie Samat, чей ребёнок Henry Cameron Samat умер врезультате не диагностированного предлежания сосудов в 2005 году.
Что такое Vasa Previa?
Vasa Previa (Предлежание Сосудов) – (от лат. vasa – сосуд, prеvia – находящийся перед, спереди от) – это состояние, характеризующееся наличием сосудов, имеющих связь с плодово-плацентарным кровотоком, проходящих свободно во внеплацентарных плодных оболочках, расположенных между предлежащей частью плода и шейкой матки.
Эти сосуды проходят незащищёнными ни Вартоновым студнем, ни тканью плаценты, вследствие чего легко ранимы и подвержены сдавлению на любом этапе беременности, хотя большинство осложнений происходит в родах.
Vasa Previa является патологическим состоянием, не имеющим клинических проявлений, приводящим в некоторых случаях к развитию плодного кровотечения во время беременности и родов, и как следствие, ведущее к смерти плода/новорожденного.
Различают два типа ПС
1-й тип – наличие над внутренним зевом свободных сосудов пуповины, не защищенных Вартоновым студнем при оболочечном прикреплении пуповины (ОПП) – состояние, при котором пуповина прикрепляется не к ткани плаценты, а к околоплодным оболочкам на некотором расстоянии от края плаценты. ОПП является одной из первых причин ПС, описанных в литературе. Диагностируется анте- или постнатально в среднем от 0,4 до 1,8% случаев всех беременностей, приводя при этом к ПС от 1 до 3% случаев, или в среднем один случай VP на 50 случаев ОПП. При многоплодной беременности частота ОПП намного увеличивается и встречается от 3,6 до 16% в случаях беременностью двойней. У моноамниональных монохориональных двоен ОПП наблюдается в 16%, у диамниональных монохориональных двоен – в 13%, а у дихориональных двоен – в 7% случаев. В случаях беременности тройней ОПП встречается в 28,2% случаев.
2-й тип – наличие над внутренним зевом незащищенных сосудов, соединяющих между собой доли плаценты при двудольной плаценте, или при наличии дополнительных долей, при возможно нормальном прикреплении пуповины к основной доле плаценты.
Из всех случаев ПС тип 1 встречается почти в 90% обнаружения ПС.
Частота встречаемости ПС примерно 1:2500 родов, но есть вероятность того, что на самом деле эта цифра недооценена, так как часть случаев могут проходить без осложнений и не попадать в отчёты. При этом есть работы показывающие, что частота ПС после ЭКО 1:300 беременностей.
В чём опасность?
Учитывая тот факт, что ПС является патологическим состоянием без каких-либо клинических проявлений, данная патология остается одной из опаснейших по развитию осложнений со стороны плода, таких как смерть в результате кровотечения при разрыве ПС либо внутриутробной асфиксии, при пережатии сосудов.
Одними из самых опасных осложнений ПС являются разрыв и возникающее плодное кровотечение. В большинстве случаев повреждение ПС происходит одномоментно с разрывом плодных оболочек, имея при этом «общую точку разрыва». Описаны случаи разрывов сосудов, проходящих свободно в оболочках, расположенных на расстоянии от места первоначального разрыва оболочек. В данных случаях сосуды повреждаются из-за продолжающегося разрыва плодных оболочек во время продвижения плода в процессе родов, что объясняет случаи кровотечения через 12 и более часов после момента разрыва плодных оболочек.
Учитывая тот факт, что объем циркулирующей крови плода к 38 неделям беременности составляет 80-110 мл/кг веса, то начавшееся кровотечение из ПС требует экстренной операции кесарева сечения, так как потеря уже 100 мл плодной крови может привести к развитию геморрагического шока и к смерти плода. Коварной чертой такого кровотечения является то, что состояние матери при этом не меняется, остаётся стабильным.
Перинатальная смертность при не диагностированном ПС составляет 55-75%.
История
Первым ПС при оболочечном прикреплении пуповины описал H. A. Wrisberg в 1773 году, он публиковал свои находки о «свободных сосудах в оболочках, выходящих из плаценты и связывающих ее с пуповиной плода в нижней части матки в месте ее расширения при родах».
В 1778 году E. Sandifort доложил о следующем случае обнаружения «прикрепления пуповины к краю плаценты» и о «свободных сосудах в оболочках, выходящих с противоположной месту прикрепления пуповины стороны плаценты и входящих в сеть сосудов пуповины плода».
В 1801 J.-F. Lobstein первым высказал предположение о «возможном разрыве свободных сосудов, проходящих в оболочках между пуповиной и плацентой, а также между плацентой и ее дополнительными долями, с возможным кровотечением, которое может привести к быстрой смерти плода» .
Но только в 1831 году R. Benckiser в своей «Dissertation inaugurale» сообщил о первом случае смерти новорожденного вследствие кровотечения, связанного с «разрывом венозной ветви, проходящей в 6 см от края плаценты над отверстием матки, во время разрыва амниотических оболочек». Именно после этого случая в европейской, в частности во франкоязычной, литературе за кровотечением, возникающим вследствие разрыва VP, закрепилось название «кровотечение Бенкизера»
Первое ультразвуковое описание ПС было в 1987 году. Gianopoulos и соавторы описали случай УЗ диагностики предлежания сосудов у беременной с добавочной долей плаценты.
В 1990г Nelson впервые сообщил об использовании цветового допплеровского картирования (ЦДК) для диагностики ПС.
И лишь в 1996 году описан первый случай выявления ПС во время скринингового УЗИ во втором триместре, благодаря чему на 35 неделе родился здоровый ребёнок путём операции кесарево сечение.
Но проблема Vasa Previa так и оставалась в разряде «отдельных научных статей, о которых мало кто знал» до очередной трагедии, которая случилась в семье адвокатов Natalie и Daren Samat, когда в 2005 году в результате не диагностированного ПС на 13-м дне жизни скончался их ребёнок Henry. Проблема получила широкую огласку именно благодаря стараниям этих людей, основанному ими благотворительному фонду https://vasaPrevia.co.uk/ и требованию к NHS National Screening Committee Великобритании включить исследование на предмет ПС в скрининг второго триместра.

Natalie и Daren Samat
В 2008 году National Screening Committee ответил, что на данный момент не достаточно доказательств необходимости включения данного обследования в программу скрининга и что есть обеспокоенность о гипердиагностике, которая повлечёт ненужные операции кесарево сечение.
Роль УЗИ в диагностике Предлежания Сосудов
В январе 2014 года в журнале Journal of Ultrasound in Medicine была опубликована статья «Natural History of Vasa Previa Across Geion Using a Screening Protocol», в которой описывается большое исследование, проводившееся с июня 2005 по июнь 2012гг, включившее в себя 27 573 беременных, которым целенаправленно проводилось УЗ исследование на предмет Vasa Previa во время скрининга второго и третьего триместров.
Показаниями для проведения исследования были:
Предлежание плаценты на более ранних сроках, которая «поднялась»
Vasa Previa в прошлые беременности
Оболочечное прикрепление сосудов в области нижнего сегмента матки
Добавочная доля плаценты в области нижнего сегмента матки
Беременность двойней
Диагноз Предлежание Сосудов выставлялся в случае обнаружения оболочечного прикрепления сосудов в пределах 2-х сантиметров от внутреннего зева при трансвагинальном исследовании с использованием серой шкалы, ЦДК и энергетического Доплера.

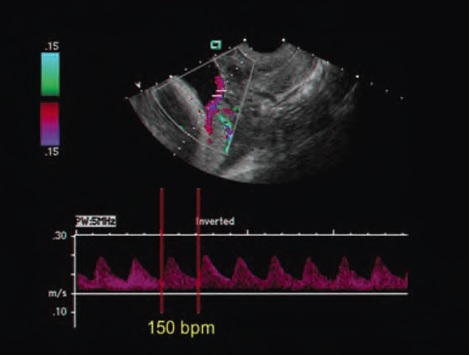
Был выявлен 31 случай ПС, что соответствовало частоте 1.1:1000 беременностей. У авторов нет информации о пропущенных случаях ПС.
В заключении сказано, что использование стандартизированного скрининга ПС является эффективным методом диагностики ПС, благодаря которому достигается 100% выживаемость. Было показано, что примерно в 24% случаев, ПС диагностированное во втором триместре (<26 недель) самостоятельно разрешается благодаря смещению сосудов вверх к третьему триместру, но не было ни одного случая смещения сосудов кверху при диагностике ПС в третьем триместре.
Вероятность ПС минимальна в случаях, когда корень пуповины выходит из ткани плаценты, и при отсутствии добавочной доли плаценты или билобарной плаценты. Учитывая, что описание плаценты уже включено в стандартный протокол УЗИ, необходимо сместить приоритет к исключению оболочечного прикрепления сосудов пуповины, так как такое состояние является предпосылкой для наиболее частого варианта ПС, тип 1. Диагностика нормального прикрепления пуповины к плаценте во время скрининга второго триместра сама по себе имеет большое значение. Помимо ПС существует ещё масса осложнений при оболочечном прикреплении пуповины: повышенный риск отслойки плаценты, задержки роста плода, низкой оценки Апгар при рождении, преждевременных родов. Это не значит, что если Вам поставили диагноз ОПП, то всё это непременно случится, но такая беременность требует повышенного внимания со стороны акушера-гинеколога и более осмотрительного поведения со стороны беременной.
Несколько исследований показали, что определение места прикрепления пуповины к плаценте во время скрининга первого или второго триместра занимает меньше минуты и не требует каких-то особых умений. До 11 недель данное исследование невозможно, так как трофобласт в это время покрывает значительную площадь полости матки.
Определение места прикрепления пуповины к плаценте во время скрининга первого триместра в 11-14 недель предпочтительно, так как на этом сроке это совсем не сложно сделать. При многоплодной беременности, а также при беременности после ЭКО следует рекомендовать трансвагинальное исследование в тех случаях, когда осмотр области внутреннего зева затруднён при трансабдоминальном доступе.
Важно подчеркнуть, что необходимо целенаправленно исключать ОПП, так как если не делать этого специально, то с большой долей вероятности ОПП будет пропущено.
Корень пуповины может располагаться в центре плаценты или эксцентрично, но в ткани плаценты (90%). Либо на краю плаценты (10%) , т.н. краевое прикрепление пуповины к плаценте, в этом случае бывает сложно с помощью УЗ однозначно утверждать, что часть сосудов не расположены оболочечно. И в 1% беременностей определяется оболочечное прикрепление пуповины в стороне от края плаценты. Важно убедиться, что определён именно корень пуповины, а не свободные петли пуповины на поверхности плаценты. В этом может помочь режим ЦДК, показывающий вход сосудов пуповины в хориальную пластину.
В случае, когда отчётливо определено место вхождения пуповины в плаценту, вероятность 1 типа ПС крайне мала и никаких дополнительных исследований не требуется.
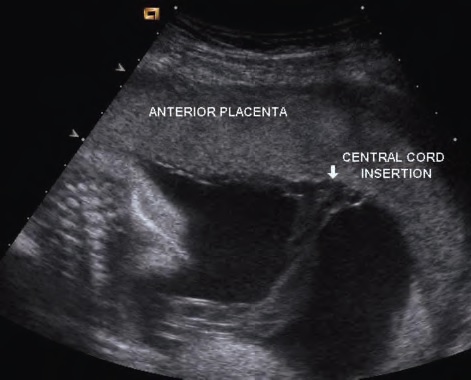
показан корень пуповины входящий в центр плаценты
И, наоборот, в случае, когда не удаётся отчётливо определить место вхождения пуповины, специалисту УЗД необходимо приложить дополнительные усилия, чтобы не пропустить ОПП. Когда не удаётся выявить ОПП в верхнем сегменте матки с помощью трансабдоминального датчика, необходимо провести трансвагинальное исследование с использованием ЦДК.
Кроме того не следует забывать о ПС 2 типа, и осматривать стенки полости матки на предмет добавочных долей плаценты.
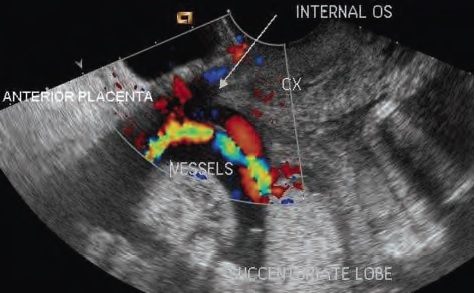
показана плацента по передней стенке матки, добавочная доля плаценты и ПС 2 тип
В случае низкой плацентации во втором триместре беременности, необходимо убедиться, что сосуды не определяются рядом с внутренним зевом, и если это так, то никаких дополнительных действий не требуется.
Низкая плацентация во втором триместре беременности – это состояние, когда край плаценты определяется на расстоянии менее 3-х сантиметров от внутреннего зева, но не перекрывает его. В этом случае не требуется каких-то дополнительных действий или лечения «на всякий» случай. Достаточно повторной оценки расположения плаценты в третьем триместре.
Во время скрининга первого триместра и тем более до 11 недель, не следует ставить диагноз Низкое расположение хориона, так как нижний сегмент матки ещё значительно растянется, и в подавляющем большинстве случаев к 20 неделям уже не будет низкой плацентации.
В настоящее время широко используется трансвагинальное исследование шейки матки с целью исключения истмико-цервикальной недостаточности (ИЦН). Не редко женщины сами, без назначения врача, приходят на цервикометрию просто на всякий случай, потому что им так спокойнее.
Врачу УЗД, проводящему данное исследование следует помнить о Vasa Previa и использовать эту уникальную возможность для того, чтобы, затратив меньше минуты своего времени, лишний раз посмотреть, включить режим ЦДК и, может быть, предотвратить трагедию.
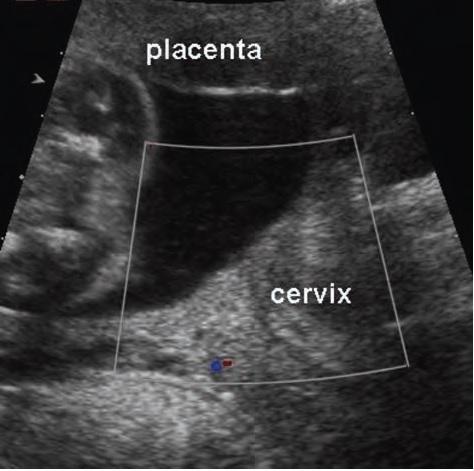
показано отсутствие предлежащих сосудов при трансвагинальном исследовании шейки матки
В заключении хочу предложить диагностический алгоритм для исключения Vasa Previa во время скрининга второго триместра, разработанный командой Philippe Jeanty:
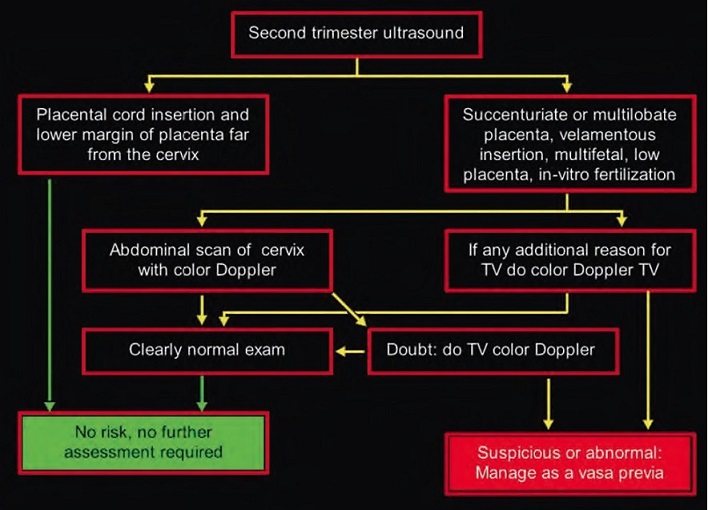
Если Вам поставили диагноз Предлежание Сосудов во втором триместре, не нужно пугаться, но нужно понимать, что к такой беременности нужно относиться с ещё большим трепетом и выполнять все рекомендации наблюдающего Вас врача. Помните, что в 24 % случаев к третьему триместру сосуды могут сместиться кверху, и диагноза ПС уже не будет. Если же и в третьем триместре диагноз подтверждается, то Вам будет показана госпитализация в стационар ближе к 35 неделям беременности, проведение профилактики респираторного дистресс синдрома и родоразрешение путём операции кесарево сечение на сроке 35-36 недель беременности.
Источник
Дата публикации 5 октября 2020Обновлено 22 апреля 2021
Определение болезни. Причины заболевания
Антенатальная гибель плода – это внутриутробная смерть плода, наступившая до начала родов, но после 21 недели беременности. Является причиной 39-42 % мертворождений. У таких детей отсутствует сердцебиение, дыхание, движения и пульсация сосудов пуповины [12].
Согласно первым комплексным оценкам, каждый год на свет появляется более 7200 мертворождённых детей. Даже в высокоразвитых странах Европы и Северной Америки показатель мертворождения не опускается ниже 1,3 % [9]. Уровень мертворождения в России в 2018 году был равен 5,51 %. При этом доля антенатальной гибели плода составила 91,8 %. Однако за последние пять лет показатель перинатальной смертности (гибели ребёнка до и после родов) стал снижаться [13].
Чаще внутриутробная гибель плода наблюдается у девочек-подростков в силу незрелости организма, а также у беременных 35 лет и старше. К этому возрасту у женщины, как правило, возникает ряд хронических заболеваний, снижается овариальный резерв – запас фолликулов в яичниках. Всё это является риском неразвивающейся беременности по причине хромосомной патологии плода.
Также риск антенатальной потери выше у женщин с более чем двумя родами в анамнезе, привычным невынашиванием беременности, искусственными абортами, многоплодными беременностями, наличием послеоперационного рубца на матке и при экстракорпоральном оплодотворении (ЭКО) [23].
Существует множество причин внутриутробной гибели плода. Они могут быть как со стороны самого плода, так и стороны матери [8].
Непосредственной причиной смерти является дистресс-синдром плода. Он подразумевает под собой все нарушения функционального состояния плода, в первую очередь, его движений и сердцебиения.
Опосредованные причины антенатальной гибели плода:
- Врождённые аномалии развития плода – синдром Дауна, синдром Патау, синдром Эдвардса и др.
- Инфицирование плода в утробе матери. Чаще всего это происходит при:
- инвазивной диагностике и лечении беременной – амниоцентезе (во время удаления излишков околоплодных вод, введения лекарств или пункции амниотической оболочки), пунктировании сосудов пуповины и др.;
- нарушении стерильности во время введения препаратов крови внутрь матки через сосуды пуповины (например, при переливании эритроцитарной массы плоду с гемолитической болезнью);
- преждевременном разрыве околоплодных оболочек в случае пролонгированной беременности;
- общих инфекциях беременной – TORCH-инфекциях, сифилисе, туберкулёзе, урогенитальном хламидиозе и ВИЧ-инфекции [13].
- Экстрагенитальные заболевания матери – сахарный диабет, нарушения работы щитовидной железы, почек и надпочечников, травмы, злоупотребление алкоголем и курение, особенно при наличии воспалений урогенитального тракта.
- Особенности течения беременности:
- различные формы позднего токсикоза;
- угроза прерывания беременности;
- истмико-цервикальная и фетоплацентарная недостаточность;
- инфекционные заболевания;
- нарушение кровотока в матке и плаценте;
- тазовое предлежании плода.
- Неустановленные причины.
Инфекция может быть вирусной (цитомегаловирусы, вирусы простого герпеса, краснухи, Коксаки, ВИЧ), бактериальной (хламидии, микоплазмы, уреаплазмы, стрептококки группы В, энтеробактерии, кишечная палочка) и грибковой (кандидоз).
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением – это опасно для вашего здоровья!
Симптомы антенатальной гибели плода
Процесс внутриутробной гибели плода далеко не всегда может сопровождаться изменениями в самочувствии женщины. Иногда беременная отмечает более частые шевеления плода, но позже происходит их полное прекращение. Это говорит об острой гипоксии плода – снижении содержания кислорода в организме [2]. Однако часто гибель малыша наступает незаметно для матери и врача, что приводит к поздней диагностике антенатальной смерти плода [4].
В течение первых трёх дней гибели малыша пациентка может обратить внимание на изменения своего состояния:
- прекращаются шевеления плода;
- уменьшается размер молочных желёз, снижается их напряжение;
- живот перестаёт увеличиваться в объёме;
- возникает слабость, недомогание, тяжесть внизу живота.
Если с момента гибели плода в утробе матери прошло несколько недель, могут присоединяться признаки воспалительной реакции:
- повышение температуры до 38 ℃;
- сильные тянущие боли внизу живота;
- головная боль и головокружение;
- сонливость;
- нарушение сознания [16].
Патогенез антенатальной гибели плода
Несмотря на то, что внутриутробная гибель плода является общемировой проблемой, вопросы её патогенеза остаются нерешёнными [5][14][21][25]. В связи с этим проводится множество исследований, в частности исследования плаценты – предполагается, что её изменения являются основной или одной из главных причин смерти плода. Установить фактическую причину при аутопсии (вскрытии) мертворождённого довольно трудно [3][6][15][22][24].
Суть патогенеза заключается в нарушении функции плаценты, развитии хронической плацентарной недостаточности, нарушении кровоснабжения плода, его росте и развитии. Поражаются внутренние органы плода – развивается внутриутробная пневмония, менингит и др. В какой-то момент происходит нарушение нормального функционирования плаценты, развивается острая плацентарная недостаточность и плод погибает.
Профессором И. В. Бариновой в 2015 году были представлены два типа плодовых потерь при внутриутробной гипоксии. Каждому из них характерно своеобразное сочетание патогенетических факторов, связанных с матерью, плацентой и плодом.
Патогенез первого типа отличается комплексом таких признаков, как ранняя тяжёлая преэклампсия и васкулопатия, т. е. патологическое изменение сосудов базальной пластинки плаценты (неполноценная перестройка спиральных артерий, необходимая для улучшения кровоснабжения плода, острый атероз, тромбоз и кровотечения). Всё это нарушает циркуляцию материнской крови в плаценте [1].
Патогенез второго типа обусловлен нарушением циркуляции в плодовой части плаценты, незрелостью ворсин относительно срока беременности, а также васкулопатией сосудов плода и тромбозом ворсин.
Эти основные звенья патогенеза антенатальной гибели позволяют своевременно профилактировать и назначать патогенетическую терапию фетоплацентарной недостаточности [1].
Классификация и стадии развития антенатальной гибели плода
Пока не существует общепринятой классификации внутриутробной гибели плода. Однако изучение причин перинатальной смертности привело к появлению двух понятий:
- “Необъяснимое” мертворождение – внезапная гибель малыша наступает по неизвестным причинам. Установить их можно только после анатомического вскрытия плода и исследования плаценты. Зачастую выявляются аномалии опорно-двигательной и нервной системы, несовместимые с жизнью, а также поражения сердечно-сосудистой системы, в частности фатальная аритмия – нарушение сердечного ритма.
- Мертворождение, связанное с задержкой роста плода – гибель плода обусловлена нарушениями обмена веществ, поступления кислорода и кровоснабжения плода из-за материнских факторов, а также факторов, связанных с плодом и плацентой [8].
Полноценное гистологическое исследование внутриутробно погибшего плода необходимо для установления причины его смерти. Некоторые матери отказываются от него, но это неправильно. Дело в том, что у многих женщин с гибелью плода в анамнезе повышается риск повторных потерь при следующих беременностях [26]. Поэтому исследование причин мертворождения позволит предотвратить повторение этой трагедии в будущем.
Осложнения антенатальной гибели плода
При своевременном обращении к доктору антенатальная гибель плода не приводит к осложнениям. Если же пациентка обратилась за медицинской помощью спустя больше двух недель после смерти ребёнка, то у неё с большой вероятностью могут развиваться такие осложнения, как:
- Кровотечение во время и после родов.
- Гнойно-септические осложнения:
- хориоамнионит – воспаление стенок плодного пузыря и заражение инфекцией околоплодных вод;
- послеродовой метроэндометрит – воспаление мышечной и слизистой оболочки стенки матки;
- инфекции послеоперационной раны – может возникнуть, если роды проходили путём кесарева сечения, например, при раннем отделении плаценты;
- послеродовой сепсис – заражение крови.
Чтобы избежать их, необходимо тщательно наблюдать за состоянием пациентки и выполнять профилактические мероприятия:
- плановое проведение родов при высоком риске кровотечения;
- профилактика анемии;
- гемостатическая терапия;
- пережатие пуповины ребёнка не раньше первой минуты после рождения;
- строгое соблюдение стерильности при выполнении кесарева сечения и вагинальных исследований во время родов;
- использование индивидуальных комплектов при родоразрешении;
- отказ от катетеризации мочевого пузыря и эпизиотомии (рассечения задней стенки влагалища) без явной необходимости;
- профилактический приём антибиотиков после выполнения инвазивной диагностики или при длительном безводном периоде;
- ранняя выписка из родильного дома (на третьи сутки после родов) [16].
Антенатальная гибель плода является серьёзным состоянием при многоплодной беременности. В случае дихориальной беременности (когда малыши развиваются независимо друг от друга: каждый имеет свои жизненно важные структуры – плодный мешок и плаценту) гибель близнеца не влияет на другого ребёнка. При монохориальной беременности (когда у малышей одна плацента на двоих) риски повреждения второго плода существенно выше:
- в 12 % случаев происходит гибель второго ребёнка;
- в 18 % случаев у него диагностируются неврологические нарушения.
В связи с этим рекомендован контроль показателей эхокардиографии (УЗИ сердца), оценка мозгового кровотока (УЗИ головного мозга) и МРТ выжившего плода [18].
Помимо прочих осложнений у женщины может возникнуть депрессия, тревожное и посттравматическое расстройство на почве пережитой трагедии или чувства вины. У неё может развиться страх перед будущей беременностью, желание избежать её [26]. В этих случаях пациентке требуется психотерапевтическая помощь.
Диагностика антенатальной гибели плода
После того как женщина обращается к врачу с жалобами на недомогание и отсутствие шевеления плода, врач направляет пациентку на диагностическое обследование. Оно позволяет поставить точный диагноз.
Постановка диагноза внутриутробной гибели плода включает следующие этапы обследования:
- Выслушивание сердечных сокращений плода специальным стетоскопом. Обычным медицинским стетоскопом в данном случае услышать сердцебиение невозможно. Для этого существует деревянный акушерский стетоскоп. Он отличается широкой воронкой, которая плотно прикладывается к животу беременной.
- Выслушивание сердечных сокращений фетальным аудиодопплером и/или монитором. Фетальный допплер можно использовать даже в домашних условиях, начиная с 12-ой недели беременности. Для этого женщине нужно лечь на спину и для чёткого сигнала нанести гель на те участки живота, которые будут соприкасаться с датчиком. Сам допплер нужно передвигать медленно, без резких движений. Длительность исследования – 3-7 минут.
- Ультразвуковое исследование плода (УЗИ). Этот метод является одним из самых достоверных для диагностики внутриутробной гибели плода. С его помощью доктор констатирует отсутствие сердцебиения у малыша [16].
Анализы для диагностики внутриутробной гибели плода на позднем сроке беременности не так важны. Отсутствия шевелений плода в течение нескольких дней и сердцебиения по данным УЗИ достаточно для правильной постановки диагноза.
Лечение антенатальной гибели плода
При подтверждённом диагнозе антенатальной гибели плода показана экстренная госпитализация и принятие решения о методе и сроке родоразрешения. Чем меньше интервал между установленным диагнозом и родоразрешением, тем меньше риск возникновения осложнений во время и после родов.
Выбор метода определяется индивидуально, на основании клинических данных и особенностей акушерской ситуации. Оптимальным вариантом родоразрешения при антенатальной гибели плода являются роды через родовые пути. Но иногда выполняется кесарево сечение, например при раннем отделении плаценты от стенок матки, обильном или продолжающемся кровотечении из половых путей.
При родоразрешении беременных с антенатальной гибелью плода, осложнившейся септическим состоянием, показано экстренное оперативное вмешательство. Объём операции решается индивидуально, возможна удаление матки с плодом (экстирпация).
После родов важно тщательно наблюдать за состоянием роженицы, провести профилактику послеродового кровотечения и гнойно-септических осложнений. Необходимо обратить внимание на выделения из половых путей (гнойные или кровянистые), температуру тела, появление озноба, слабости, тянущих болей внизу живота.
Во всех случаях внутриутробной гибели плода показано патологоанатомическое исследование плода и последа (его оболочки). Отказ от исследования по желанию родственников оформляется в соответствии с нормами действующего законодательства [19].
Самым тяжёлым остаётся вопрос о том, когда же произошла гибель плода. Раньше считалось, что в основе определения времени гибели лежит оценка выраженности процессов мацерации – размягчения и разрыхления тканей плода [20]. Однако наличие признаков мацерации не всегда позволяет достоверно судить о давности наступления гибели, т. к. время её развития зависит от причин гибели малыша.
Прогноз. Профилактика
Потеря беременности является показанием к проведению медицинской, психологической и социальной реабилитации пациенток. Необходим полный комплекс диагностических исследований для выяснения причины гибели плода. Выбор алгоритма обследования базируется на данных анамнеза, особенностях течения беременности и результатах патологоанатомического исследования плода и последа.
Женщины с внутриутробной гибелью плода в анамнезе входят в группу риска данного осложнения при последующих беременностях. Поэтому наступление беременности у таких пациенток требует выполнения комплекса мероприятий по подготовке организма женщины к полноценному зачатию, вынашиванию и рождению здорового ребёнка [10]. Оптимальный интервал между беременностями должен составлять не менее 6 месяцев, чтобы минимизировать потенциальные сложности течения последующей беременности [26].
При неустановленной причине гибели плода в анамнезе необходимо учитывать данный факт при выработке тактики родоразрешения последующих беременностей.
Профилактика антенатальной гибели плода предполагает:
- ведение здорового образа жизни;
- диагностику и адекватное лечение соматических и хронических инфекционных заболеваний;
- своевременное выявление генетической патологии;
- лечение высокого артериального давления;
- контроль уровня глюкозы в крови при сахарном диабете [26];
- предупреждение травм живота;
- прекращение контакта с бытовыми токсичными веществами;
- ликвидацию профессиональных вредностей (переход на другую работу);
- адекватное назначение лекарств в период беременности;
- приём фолиевой кислоты до зачатия;
- комплексное антенатальное наблюдение за состоянием плода [7];
- регистрацию шевелений плода на 28 неделе беременности;
- ведение гравидограммы с 24 недели беременности (сводной таблицы данных, регистрирующей динамику течения беременности) – повышает качество диагностики задержки развития плода и снижает риск потери малыша в 1,8 раз [11].
Курение увеличивает риск перинатальной смертности на 27 % [17]. Однако чаще антенатальная гибель плода наблюдается у беременных, употребляющих алкоголь – в 6,25 % случаев [8]. Поэтому отказ от вредных привычек значительно увеличивает шансы родить здорового ребёнка.
Источник
