Магистральные сосуды у детей

Транспозиция магистральных сосудов – тяжелая врожденная патология сердца, характеризующаяся нарушением положения главных сосудов: отхождением аорты от правых отделов сердца, а легочной артерии – от левых. Клинические признаки транспозиции магистральных сосудов включают цианоз, одышку, тахикардию, гипотрофию, сердечную недостаточность. Диагностика транспозиции магистральных сосудов основана на данных ФКГ, ЭКГ, рентгенологического исследования органов грудной клетки, катетеризации полостей сердца, вентрикулографии. Методами оперативной коррекции транспозиции магистральных сосудов служат паллиативные вмешательства (баллонная атриосептостомия) и радикальные операции (Мастарда, Сеннинга, Жатене, Растелли, артериального переключения).
Общие сведения
Транспозиция магистральных сосудов – врожденный порок сердца, анатомическую основу которого составляет неправильное расположение аорты и легочной артерии относительно друг друга и их обратное отхождение от желудочков сердца. Среди различных ВПС транспозиция магистральных сосудов составляет 7–15%; в 3 раза чаще встречается у мальчиков. Транспозиция магистральных сосудов входит в число «большой пятерки» – наиболее часто встречающихся врожденных аномалий сердца, наряду с дефектом межжелудочковой перегородки, коарктацией аорты, открытым артериальным протоком, тетрадой Фалло.
В кардиологии транспозиция магистральных сосудов относится к критическим порокам сердца синего типа, не совместимым с жизнью, поэтому требует хирургического вмешательства в первые недели жизни.
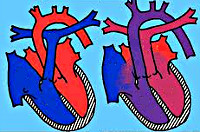
Транспозиция магистральных сосудов
Причины транспозиции магистральных сосудов
Аномалии развития магистральных сосудов формируются в первые 2 месяца эмбриогенеза в результате хромосомных аберраций, неблагоприятной наследственности или отрицательных внешних воздействий. Экзогенными факторами могут выступать вирусные инфекции, перенесенные беременной (ОРВИ, краснуха, ветряная оспа, корь, эпидемический паротит, герпес, сифилис), токсикозы, радиоактивное облучение, лекарственные вещества, алкогольная интоксикация, полигиповитаминоз, заболевания матери (сахарный диабет), возрастные изменения в организме женщины старше 35 лет. Транспозиция магистральных сосудов встречается у детей с синдромом Дауна.
Непосредственные механизмы транспозиции магистральных сосудов до конца не изучены. По одной из версий, порок обусловлен неправильным изгибом аортально-пульмональной перегородки в процессе кардиогенеза. Согласно более современным представлениям, транспозиция магистральных сосудов является результатом неправильного роста субаортального и субпульмонального конуса при разветвлении артериального ствола. При закладке сердце в норме резорбция инфундибулярной перегородки приводит к формированию аортального клапана кзади и книзу от клапана легочной артерии, над левым желудочком. При транспоцизии магистральных сосудов процесс резорбции нарушается, что сопровождается расположением клапана аорты над правым желудочком, а клапана легочной артерии – над левым.
Классификация транспозиции магистральных сосудов
В зависимости от количества сопутствующих коммуникаций, выполняющих компенсирующую роль, и состояния малого круга кровообращения различают следующие варианты транспозиции магистральных сосудов:
1. Транспозиция магистральных сосудов, сопровождающаяся гиперволемией или нормальной величиной легочного кровотока:
- с дефектом межпредсердной перегородки или открытым овальным окном (простая транспозиция)
- с ДМЖП
- с открытым артериальным протоком и наличием дополнительных коммуникаций.
2. Транспозиция магистральных сосудов, сопровождающаяся уменьшением легочного кровотока:
- со стенозом выносного тракта левого желудочка
- с ДМЖП и стенозом выносного тракта левого желудочка (сложная транспозиция)
В 80% случаев транспозиция магистральных сосудов сочетается с одной или несколькими дополнительными коммуникациями; у 85-90% больных порок сопровождается гиперволемией малого круга кровообращения. Для транспозиции магистральных сосудов характерно параллельное расположение аорты относительно легочного ствола, тогда как в нормальном сердце обе артерии перекрещиваются. Чаще всего аорта находится впереди легочного ствола, в редких случаях сосуды располагаются в одной плоскости параллельно, или аорта локализуется кзади от легочного ствола. В 60% наблюдений обнаруживается D-транспозиция – положение аорты справа от легочного ствола, в 40%- L-транспозиция – левостороннее положение аорты.
Особенности гемодинамики при транспозиции магистральных сосудов
С позиций оценки гемодинамики важно различать полную транспозицию магистральных сосудов и корригированную. При корригированной транспозиции аорты и легочной артерии имеет место желудочково-артериальная и предсердно-желудочковая дискордантность. Другими словами, корригированная транспозиция магистральных сосудов сочетается с инверсией желудочков, поэтому внутрисердечная гемодинамика осуществляется в физиологическом направлении: в аорту поступает артериальная кровь, а в легочную артерию венозная. Характер и выраженность гемодинамических нарушений при корригированной транспозиции магистральных сосудов зависят от сопутствующих пороков – ДМЖП, митральной недостаточности и др.
Полная форма сочетает в себе дискордантные желудочково-артериальные взаимоотношения при конкордантном взаимоотношении других отделов сердца. При полной транспозиции магистральных сосудов венозная кровь из правого желудочка поступает в аорту, разносится по большому кругу кровообращения, а затем вновь поступает в правые отделы сердца. Артериальная кровь выбрасывается левым желудочком в легочную артерию, по ней – в малый круг кровообращения и вновь возвращается в левые отделы сердца.
Во внутриутробном периоде транспозиция магистральных сосудов практически не нарушает фетальное кровообращение, поскольку легочный круг у плода не функционирует; циркуляция крови осуществляется по большому кругу через открытое овальное окно или открытый артериальный проток. После рождения жизнь ребенка с полной транспозицией магистральных сосудов зависит от наличия сопутствующих коммуникаций между малым и большим кругом кровообращения (ООО, ДМЖП, ОАП, бронхиальных сосудов), обеспечивающих смешение венозной крови с артериальной. При отсутствии дополнительных пороков дети погибают сразу после рождения.
При транспозиции магистральных сосудов шунтирование крови осуществляется в обоих направлениях: при этом, чем больше размер коммуникации, тем меньше степень гипоксемии. Наиболее благоприятными являются случаи, когда ДМПП или ДМЖП обеспечивают достаточное смешивание артериальной и венозной крови, а наличие умеренного стеноза легочной артерии предотвращает чрезмерную гиперволемию малого круга.
Симптомы транспозиции магистральных сосудов
Дети с транспозицией магистральных сосудов рождаются доношенными, с нормальным или несколько повышенным весом. Сразу после рождения, с началом функционирования отдельного легочного круга кровообращения, нарастает гипоксемия, что клинически проявляется тотальным цианозом, одышкой, тахикардией. При транспозиции магистральных сосудов, сочетающейся с ОАП и коарктацией аорты, выявляется дифференцированный цианоз: синюшность верхней половины тела выражена в большей степени, чем нижней.
Уже в первые месяцы жизни развиваются и прогрессируют признаки сердечной недостаточности: кардиомегалия, увеличение размеров печени, реже – асцит и периферические отеки. При осмотре ребенка с транспозицией магистральных сосудов обращает внимание деформация фаланг пальцев, наличие сердечного горба, гипотрофия, отставание в моторном развитии. При отсутствии стеноза легочной артерии переполнение кровью малого круга кровообращения приводит к частому возникновению повторных пневмоний.
Клиническое течение корригированной транспозиции магистральных сосудов без сопутствующих ВПС длительное время бессимптомное, жалобы отсутствуют, ребенок развивается нормально. При обращении к кардиологу обычно выявляется пароксизмальная тахикардия, атриовентрикулярная блокада, шумы в сердце. При наличии сопутствующих ВПС клиническая картина корригированной транспозиции магистральных сосудов зависит от их характера и степени гемодинамических нарушений.
Диагностика транспозиции магистральных сосудов
Наличие у ребенка транспозиции магистральных сосудов обычно распознается еще в родильном доме. Физикальное обследование выявляет гиперактивность сердца, выраженный сердечный толчок, который смещен медиально, расширенную грудную клетку. Аускультативные данные характеризуются усилением обоих тонов, систолическим шумом и шумом ОАП или ДМЖП.
У детей в возрасте 1-1,5 месяцев по ЭКГ обнаруживаются признаки перегрузки и гипертрофии правых отделов сердца. При оценке рентгенографии грудной клетки высокоспецифичными признаками транспозиции магистральных сосудов являются: кардиомегалия, характерная конфигурация тени сердца яйцеобразной формы, узкий сосудистый пучок в переднезадней проекции и расширенный в боковой проекции, левое положение дуги аорты (в большинстве случаев), обеднение рисунка легких при стенозе легочной артерии или его обогащение при дефектах перегородки.
Эхокардиография показывает аномальное отхождение магистральных сосудов, гипертрофию стенок и дилатацию камер сердца, сопутствующие дефекты, наличие стеноза легочной артерии. С помощью пульсоксиметрии и исследования газового состава крови определяются параметры насыщения крови кислородом и парциальное давление кислорода: при транспозиции магистральных сосудов SО2 менее 30%, PaO2 – менее 20 мм рт.ст. При зондировании полостей сердца обнаруживается повышенное насыщение крови кислородом в правом предсердии и желудочке и пониженное в левых отделах сердца; одинаковое давление в аорте и правом желудочке.
Рентгеноконтрастные методы исследования (вентрикулография, атриография, аортография, коронарография) визуализируют патологическое поступление контраста из левых отделов сердца в легочную артерию, а из правых – в аорту; сопутствующие дефекты, аномалии отхождения венечных артерий. Транспозицию магистральных сосудов следует отличать от тетрады Фалло, атрезии легочной артерии, атрезии трикуспидального клапана, гипоплазии левых отделов сердца.
Лечение транспозиции магистральных сосудов
Всем пациентам с полной формой транспозиции магистральных сосудов показано экстренное оперативное лечение. Противопоказанием служат случаи развития необратимой легочной гипертензии. До операции новорожденным проводится медикаментозная терапия простагландином Е1, помогающим сохранить артериальный проток незаращенным и обеспечить адекватный кровоток.
Паллиативные вмешательства при транспозиции магистральных сосудов необходимы в первые дни жизни для увеличения размера естественного или создания искусственного дефекта между малым и большим кругами кровообращения. К такого рода операциям относятся эндоваскулярная баллонная атриосептостомия (операция Парка–Рашкинда) и открытая атриосептэктомия (резекция межпредсердной перегородки по Блелоку–Хенлону).
К числу гемокорригирующих вмешательств, выполняемых при транспозиции магистральных сосудов, относятся операции Мастарда и Сеннинга – внутрипредсердное переключение потоков артериальной и венозной крови с помощью синтетической заплаты. При этом топография магистральных артерий остается прежней, по внутрипредсердному туннелю из легочных вен кровь поступает в правое предсердие, а из полых вен – в левое.
Варианты анатомической коррекции транспозиции магистральных сосудов включают различные способы артериального переключения: операцию Жатене (пересечение и ортотопическую реплантацию магистральных сосудов, перевязку ОАП), операцию Растелли (пластику ДМЖП и устранение стеноза легочной артерии), артериальное переключение с пластикой МЖП. Специфическими послеоперационными осложнениями, сопровождающими коррекцию транспозиции магистральных сосудов, могут служить СССУ, стеноз устьев легочных и полых вен, стеноз выносящих трактов желудочков.
Прогноз транспозиции магистральных сосудов
Полная транспозиция магистральных сосудов – критический, несовместимый с жизнью порок сердца. При отсутствии специализированной кардиохирургической помощи половина новорожденных погибает в первый месяц жизни, более 2/3 детей – к 1 году от тяжелой гипоксии, недостаточности кровообращения и нарастания ацидоза.
Хирургическая коррекция простой транспозиции магистральных сосудов позволяет достичь хороших отдаленных результатов в 85–90% случаев; при сложной форме порока – в 67% случаев. После операций пациенты нуждаются в наблюдении кардиохирурга, ограничении физических нагрузок, профилактике инфекционного эндокардита. Важное значение имеет пренатальное выявление транспозиции магистральных сосудов с помощью фетальной ЭхоКГ, соответствующее ведение беременности и подготовка к родам.
Источник
Полная транспозиция магистральных сосудов представляет собой тяжелый цианотический врожденный порок сердца, при котором аорта отходит от правого желудочка и располагается спереди по отношению к расположенному сзади стволу легочной артерии; последний отходит от левого желудочка и несет оксигенированную кровь; имеются правильно сформированные атрио-вентрикулярные клапаны и желудочки сердца. Такое определение исключает наличие единственного желудочка сердца, при котором тип расположения магистральных сосудов не имеет существенного значения, и атрезию одного из атрио-вентрикулярных клапанов, которая играет определяющую роль в возникающих расстройствах гемодинамики.
По данным отделений врожденных пороков сердца у детей раннего и старшего возраста ИССХ имени А. Н. Бакулева АМН СССР, частота полной транспозиции магистральных сосудов у больных в возрасте до 1 мес составила 27%, 1-3 мес — 16,7%, 36 мес — 9,4%, 6—12 мес —4%, 1—2 лет—1,2%, старше 2 лет— 0,5%. Разница между клиническими и анатомическими данными, а также разница в данных, полученных в зависимости от возраста, обусловлены большой смертностью больных с этим пороком сердца в раннем детском возрасте, что ведет к уменьшению числа этих больных- в более старшем возрасте.
Это подтверждается данными Liebman с соавторами (1969), согласно которым 28,7% младенцев, родившихся с полной транспозицией магистральных сосудов, умирают в течение 1-й недели жизни, 51,6%—в течение 1-го месяца и 89,3%—к концу 1-го года жизни. Средняя длительность жизни, по данным этих же авторов, зависела от компенсирующих и сопутствующих пороков и составляла при небольших межпредсердных и межжелудочковых сообщениях 0,11—0,28 года, при больших межпредсердных дефектах — 0,81 года, при. больших дефектах межжелудочковой перегородки и со структурными изменениями легочных сосудов — 2 года, при дефектах межжелудочковой перегородки со стенозом легочной артерии — 4,85 года.
Анатомия
При полной транспозиции магистральных сосудов полые и легочные вены несут кровь в правое и левое предсердия, которые при помощи трикуспидального и митрального клапанов сообщаются с соответствующими желудочками. Однако в противоположность нормальной картине аорта отходит от правого желудочка, а ствол легочной артерии — от левого желудочка. Восходящая аорта всегда располагается спереди и чаще справа по отношению к расположенному сзади и слева стволу легочной артерии. В редких случаях аорта лежит по средней линии тела, прямо перед легочным стволом, и еще реже аорта находится слева от ствола легочной артерии. Ход обоих магистральных сосудов параллельный, причем легочная артерия всегда прикрыта аортой на 1/2-1/3, реже — полностью.

Схематическое изображение полной транспозиции магистральных сосудов (аорта отходит от правого желудочка, легочная артерия — от левого желудочка)
Как правило, наблюдается аномальное расположение коронарных артерий. При наиболее частом варианте левая коронарная артерия начинается от аортального синуса Вальсальвы. Ствол ее в противоположность нормальному ходу идет кпереди от ствола легочной артерии и дает начало передней нисходящей и левой огибающей ветвям. Правая коронарная артерия отходит от заднего аортального синуса и идет в правую предсердно-желудочковую борозду. Таким образом, правый аортальный синус при данном пороке — некоронарный (Shaher, Puddu, 1966).
В связи с тем что правый желудочек, нагнетая кровь в аорту, работает в условиях гиперфункции, направленной на преодоление высокого сопротивления выбросу, наблюдается резкая гипертрофия его миокарда. Менее резко выраженная гипертрофия левого желудочка обусловлена тем, что он функционирует в условиях нагрузки увеличенным объемом крови. Лишь наличие стеноза легочной артерии или необратимых морфологических изменений со стороны сосудов легких может привести к его резкой гипертрофии.
Жизнь при полной транспозиции магистральных сосудов невозможна без компенсирующих дефектов. Открытое овальное окно встречается у 33% больных, дефект межжелудочковой перегородки — у 61%, открытый артериальный проток — у 8,5 % и дефект межпредсердной перегородки— у 5,7% больных. Из сопутствующих пороков чаще всего наблюдается стеноз легочной артерии (23%), причем он сочетается с дефектом межжелудочковой перегородки.
Гемодинамика
Кровоток осуществляется по двум разобщенным кругам кровообращения. По первому кругу кровь поступает из правого желудочка в аорту и, пройдя большой круг кровообращения, возвращается через полые вены и правое предсердие вновь в правый желудочек. Следовательно, ткани и органы тела снабжаются кровью с низким содержанием кислорода. По второму кругу кровь поступает из левого желудочка в легочную артерию и, пройдя малый круг кровообращения, возвращается вновь через легочные вены и левое предсердие в левый желудочек. Следовательно, в легких циркулирует кровь с высоким содержанием кислорода, которая не служит полезной цели.
Если в течение внутриутробной жизни наличие порока существенно не влияет на развитие плода, то сразу после рождения ребенок погибает. Это обусловлено разобщенностью кругов кровообращения и невозможностью вследствие этого осуществления нормального газообмена. Лишь наличие внутрисердечных сообщений, по которым происходит обмен крови между кругами кровообращения, делает этих больных жизнеспособными. Сброс крови осуществляется в двух направлениях, так как односторонний его характер мог бы привести к полному опорожнению одного из кругов. Величина этого сброса справа налево и представляет собой эффективный легочный кровоток, поскольку именно в этом объеме (смешанная кровь достигает легочных капилляров (Campbell, Bing, 1949; Shaher, 1964).
Механика сброса осуществляется следующим образом. У новорожденных с началом дыхания происходит расширение сосудистого русла легких и падение легочно-сосудистого сопротивления ниже уровня системного. Это приводит к сбросу крови из аорты в легочную артерию через открытый артериальный проток или бронхиальные артерии. Реже сброс крови справа налево происходит на уровне предсердий. Вследствие этого увеличивается объем крови, циркулирующей в малом круге кровообращения и поступающей в левое предсердие. Среднее давление в левом предсердии увеличивается, превышая его уровень в правом предсердии, и это приводит к сбросу крови слева направо через межпредсердное сообщение.
При наличии дефекта межжелудочковой перегородки с низким или умеренно повышенным легочно-сосудистым сопротивлением сброс крови справа налево, происходящий во время систолы желудочков, приводит к гииерволемии малого круга кровообращения. Увеличивающийся приток крови в левый желудочек сопровождается повышением диастолического давления, которое превышает его уровень в правом желудочке и следовательно, сброс крови слева направо происходит во время диастолы желудочков (Shaher, 1964).
При наличии дефекта межжелудочковой перегородки с высоким легочно-сосудистым сопротивлением или тяжелым стенозом легочной артерии увеличенный системный кровоток приводит к повышению давления в правом предсердии и диастолического давления в правом желудочке. Следовательно, сброс крови справа налево через дефект межжелудочковой перегородки осуществляется во время диастолы, а сброс крови слева направо происходит во время систолы. Таким образом, на направление и величину сброса крови при полной транспозиции магистральных сосудов оказывают влияние соотношение сопротивлений большого и малого кругов кровообращения, объем легочного кровотока, тип и величина компенсирующего сообщения.
Клиника
Порок сердца встречается в 2,5 раза чаще у мальчиков. Сразу после рождения у больных отмечают цианоз, который имеет тенденцию к усилению с увеличением возраста. Если при рождении вес ребенка часто нормальный, то в возрасте 1—3 мес, как правило, можно отметить гипотрофию, рахит. Это обычно связано с трудностями в кормлении, которые усугубляются сердечной недостаточностью. Отставание в физическом развитии приводит к тому, что дети позже начинают сидеть, ходить. Нередко наблюдается отставание в умственном развитии.
Клиническая картина порока во многом определяется наличием или отсутствием стеноза легочной артерии. Больных без сопутствующего стеноза легочной артерии беспокоит одышка в покое, которая связана с увеличением легочного кровотока и гипоксемией. Часто регистрируются респираторные заболевания. В возрасте 1 года у больных можно часто отметить «сердечный горб» и, как правило, положительный симптом «барабанных палочек» на пальцах рук и ног. У всех пациентов с рождения отмечается полицитемия, увеличивающаяся с возрастом. Величина гемоглобина может достигать 23—25, число эритроцитов — 6 000 000—8 000 000, гематокрит — 80%. Перкуссия обнаруживает резкое увеличение сердца в размерах.
При выслушивании сердца определяется акцент II тона, связанный с громким тоном закрытия аортальных клапанов, которые располагаются близко к передней грудной стенке. Наличие легочной гипертензии также приводит к акценту II тона, но он обычно плохо проводится из-за заднего расположения легочных клапанов. У боль-пых с открытым овальным окном шумы обычно отсутствуют, реже во втором — третьем межреберье у левого края грудины можно выслушивать слабый систолический шум. Шумы могут не прослушиваться и при большом дефекте межжелудочковой перегородки, сопровождающемся высокой легочной гипертензией (Wells, 1963). При дефектах межжелудочковой перегородки небольших размеров систолический шум имеет более громкий и грубый тембр и локализуется в третьем — четвертом межреберье у левого края грудины.
Начиная со 2—4-й недели жизни у больных появляются признаки сердечной недостаточности, проявляющиеся в виде кардиомегалии застойными хрипами в легких.
Электрокардиографическая картина характеризуется отклонением электрической оси сердца вправо, гипертрофией правого желудочка и правого предсердия. У больных с большим дефектом межжелудочковой перегородки или открытым артериальным протоком и значительно увеличенным легочным кровотоком можно наблюдать нормальную электрическую ось сердца и признаки гипертрофии обоих желудочков.
Рентгенологическое исследование в прямой проекции выявляет прогрессирующую кардиомегалию. При этом форма сердца напоминает яйцо, наклоненное так, что его длинная продольная ось лежит в косом направлении.
Рентгенограммы ребенка 5 дней с полной транспозицией магистральных сосудов и открытым овальным «окном». Сердце имеет овальную конфигурацию, сосудистый пучок в передне-задней проекции (а) шире, чем в боковой проекции (б)
Полюс с наименьшей выпуклостью обращен вверх и вправо, а с наибольшей выпуклостью — вниз и влево (Carey, Elliott, 1964). Сердце увеличено за счет левых отделов, подвергающихся нагрузке увеличенным объемом крови, и за счет правого желудочка, нагнетающего кровь в большой круг кровообращения. У больных с легочной гипертензией и равным системным и легочно-сосудистым сопротивлением размеры сердца увеличены в меньшей степени, так как отсутствует объемная перегрузка левых отделов.
Характерным рентгенологическим признаком для данного порока Taussig считает увеличение ширины сосудистого пучка в левой передней косой проекции в противоположность ее узости в прямой проекции. Следует отметить, что у младенцев в возрасте 1—2 нед легочный рисунок нормальный или незначительно усилен. В более старшем возрасте легочный рисунок, как правило, усилен, причем степень усиления коррелирует со степенью увеличения размеров сердца.
У больных с сопутствующим стенозом легочной артерии одышка выражена несколько в меньшей степени, чем у больных с увеличенным легочным кровотоком, а полицитемия — в большей степени. На основании сердца выслушивается грубый систолический шум. Признаки сердечной недостаточности умеренно выражены или отсутствуют. На электрокардиограмме отмечаются отклонение электрической оси сердца вправо, признаки гипертрофии правого желудочка и правого предсердия. Лишь в редких случаях можно наблюдать отклонение электрической оси сердца влево (А. А. Вишневский, Н. К. Галанкин, 1962; И. В. Матвеева, Б. А. Константинов, 1965).
Рентгенологически выраженность легочного рисунка зависит от тяжести стеноза легочной артерии; тень сердца умеренно увеличена в размерах, но в меньшей степени, чем у больных предыдущей подгруппы, и в большей степени, чем у больных с тетрадой Фалло. Это является важным дифференциальным признаком с последним пороком.
Катетеризация сердца обнаруживает низкие цифры насыщения крови кислородом в правых полостях сердца и в системной артерии, достигающие иногда 30%. В правом желудочке всегда регистрируется высокое давление, равное системному, и из его полости нередко удается провести катетер в восходящую аорту. Абсолютную диагностическую ценность имеет катетеризация сердца, когда измеряют давление и берут пробы крови из всех полостей и магистральных сосудов. Исключительную важность приобретает катетеризация легочной артерии. В таких случаях можно отметить более высокое насыщение крови кислородом в этом сосуде по сравнению с аортой, определить степень легочной гипертензии, что является важным при планировании хирургического вмешательства. Однако такие сведения получить удается редко, так как провести катетер в легочную артерию обычными приемами не удается.
Селективная ангиокардиография, выполненная в двух проекциях, является методом выбора и решающим исследованием, позволяющим установить не только наличие транспозиции аорты и легочной артерии, но также компенсирующие и сопутствующие пороки. При введении контрастного вещества в полость правого желудочка наблюдается его преимущественное поступление в аорту, при левой вентрикулографии — в легочную артерию. На ангиокардиограммах выявляется переднее расположение восходящей аорты и заднее — ствола легочной артерии, которые имеют параллельный ход.
Ангиокардиограммы больного с полной транспозицией магистральных сосудов и открытым овальным окном:
а, б — контрастное вещество на левого желудочка поступает в расположенную сзади легочную артерию; в, г — контрастное вещество заполняет полость правого желудочка и аорту, занимающую переднее положение
В отличие от нормальной картины выходной отдел правого желудочка чаще направлен вправо, как это прослеживается в прямой проекции, а выходной отдел левого желудочка направлен кзади, как это видно в боковой проекции. Аортальные клапаны расположены выше уровня легочных.
Наибольшую диагностическую ценность в выявлении сопутствующих пороков имеет введение контрастного вещества в правый желудочек. В таких случаях прослеживается межжелудочковая перегородка. Отсутствие поступления контрастированной крови в левый желудочек будет косвенно свидетельствовать о межпредсердном сообщении. При наличии дефекта межжелудочковой перегородки иногда можно определить его размеры при прохождении через него струи контрастированной крови.
Ангиокардиограммы больного с полной транспозицией магистральных сосудов, дефектом межжелудочковой перегородки и стенозом легочной артерии. Контрактное вещество из правого желудочка поступает в аорту, а также через дефект межжелудочковой перегородки — в левый желудочек и далее — в расположенную сзади легочную артерию:
а — прямая проекция: б — боковая проекция
При поступлении контрастированного вещества из аорты в легочную артерию устанавливают наличие открытого артериального протока. Для точного определения локализации PI тяжести стеноза легочной артерии контрастное вещество целесообразнее вводить из левого желудочка (Ю. Д. Волынский и др., 1966; И. X. Рабкин и др., 1966). В тех случаях, когда полная транспозиция магистральных сосудов сопровождается легочной гипертензией, диаметр ствола легочной артерии, выявляемый при ангиокардиографии, всегда шире диаметра восходящей аорты, а при стенозе легочной артерии, за исключением клапанного, соотношения обратные.
В. Я. Бухарин, В. П. Подзолков
Опубликовал Константин Моканов
Источник
