Мальформация сосудов головного мозга рекомендации

Алгоритм лечения артерио-венозной мальформации головного мозга – Европейские рекомендации
I. Хирургическое лечение артерио-венозной мальформации (АВМ) головного мозга. Хотя существуют различные виды современной терапии при церебральных артерио-венозных мальформаций (АВМ), хирургическое лечение является наиболее известным вариантом и относится к первому выбору при наличии такой возможности. С развитием микрохирургических методов показатели эффективности полного удаления заметно улучшились.
Принятие решений при церебральных артерио-венозных мальформаций (АВМ) является одним из наиболее сложных аспектов нейрохирургической практики. Решение, следует ли рекомендовать операцию, должно быть основано на объективном сравнении долгосрочных рисков неоперированной артерио-венозной мальформации (АВМ) с риском оперативного лечения.
У молодых пациентов, особенно при наличии неврологических симптомов, попытки хирургического удаления связаны с хирургическим риском, хотя и высоким, но по-прежнему меньшим, чем при естественном течении. У пациентов средних лет и пожилых пациентов с минимальной симптоматикой консервативный подход кажется более разумным, так как риск лечения может быть не меньше, чем при естественном течении.
Наиболее популярная система для оценки риска операции — пятибалльная шкала, разработанная Spetzler и Martin. Она включает в себя три переменные:
• Размер артерио-венозной мальформации (АВМ)
• Характер венозного оттока
• Локализацию артерио-венозной мальформации (АВМ) (функционально значимая зона или нет).
Тип I — малые размеры, поверхностные и расположенные в функционально незначимой зоне мозга, в то время как тип поражения V — это большие, глубокие АВМ в функционально значимой зоне мозга. Размер и структуру венозного оттока из АВМ как хирургические факторы риска оценить довольно несложно, но гораздо сложнее определиться в отношении функционально значимых зон мозга. Повреждение извилин и перемещение функций в связи с реорганизацией коры у пациентов с АВМ может затруднять выявление функционально значимых зон.
Перед операцией полезно проведение функциональной МРТ или ПЭТ для определения функциональных областей мозга и для получения информации о местонахождении зон речи, сенсорной и зрительной коры. Во время операции, выявлению и сохранению важных областей мозговой ткани могут способствовать электрофизиологический мониторинг, системы картирования и корковой нейронавигации.
При хирургическом вмешательстве в принципе допустимы мелкие и средние повреждения конвекситальной поверхности мозга вне критических областей. По сравнению с радиохирургией или наблюдением только хирургическое иссечение является рентабельным и очень эффективным способом улучшения качества и продлении жизни.
По нашему опыту, примерно треть пациентов с АВМ может быть направлена только на хирургическое лечение, а в остальных случаях необходимы эмболизация и/или радиохирургия до, после или вместо хирургического вмешательства.
Лечение при больших АВМ, расположенных в критически важных областях с подкорковыми клинообразными расширениями, достигающими стенок бокового желудочка, представляет собой сложную задачу. Глубокая их часть обычно снабжается из хориоидальных артерий или мелких сосудов, обычно питающих базальные ганглии, внутреннюю капсулу и таламус. Кровотечение из этих сосудов во время операции может привести к гематоцефалии.
Кроме того, трудности контроля глубоких сосудов, таких как лентикулостриарные артерии, при использовании транскортикального или трансвентрикулярного подхода увеличивают риск хирургических осложнений. В этих случаях полезно проведение эндоваскулярной эмболизации до операции.
При больших высокопотоковых артерио-венозных мальформаций (АВМ) обычно требуется предоперационная эмболизация, а некоторые авторы рекомендуют несколько этапов резекции. Поэтапное лечение при больших АВМ может свести к минимуму риски синдрома гиперперфузии и кровоизлияния в мозг после хирургического лечения.
II. Эндоваскулярное лечение артерио-венозной мальформации (АВМ). Альтернативой хирургической резекции артерио-венозной мальформации (АВМ) является эндоваскулярная эмболизация. Принцип эмболизации заключается в окклюзии тела АВМ либо частицами, либо жидким веществом, которое быстро затвердевает при попадании в кровеносный сосуд. Так как частицы не приводят к достаточно надежной окклюзии, в настоящее время используют эмболизаты на основе NBCA (N-бутил-цианакрилат) и ONYX®. Оба агента в настоящее время достаточно изучены для оценки результатов после долгосрочного наблюдения.
Эмболизация обычно проводится под общим наркозом. После пункции бедренной артерии, катетер проводится в сонную артерию по методике Сельдингера. С помощью микрокатетера выполняется суперселективная катетеризация питающих сосудов АВМ, что позволяет получить точное изображение тела АВМ и выявить возможные факторы риска, такие как интранидальные аневризмы. Так как большинство артериальных афферентов не только питают очаг, но и снабжают нормальные ткани мозга (так называемые «транзитные» артерии), устанавливают кончик микрокатетера в положении, из которого снабжается только тело АВМ. В этом положении эмболизационный агент высвобождается и продвигается в тело.
Как правило, для достижения благоприятного результата необходимо проведение нескольких этапов эмболизации.
Хотя метод эндоваскулярной эмболизации достаточно изящен и привлекателен для пациента отказом от краниотомии, к его недостаткам относится возможность излечения лишь в 15% случаев, а неоднократная эмболизация ведет к кумуляции осложнений. Поэтому, эмболизация обычно применяется в составе комбинированной терапии вместе с хирургией или радиохирургией при АВМ степени 3 или выше по Spetzler. Эмболизация служит, например для того, чтобы уменьшить размеры патологического очага и, следовательно, улучшить результаты радиохирургического лечения, или эмболизировать глубокие сосуды, которые трудно контролировать при хирургической резекции АВМ.
В качестве заключения следует сказать, что, эндоваскулярная эмболизация является устоявшимся методом в лечении АВМ. Возможные риски следует соотнести с потенциальным эффектом в каждом конкретном случае. Таким образом, она заняла свое место, в основном, в комбинированном лечении.
III. Стереотаксическая радиохирургия в лечении артерио-венозной мальформации (АВМ):
а) Определение. Однофракционное высокофокусированное стереотаксически направленное излучение малого объема, применяемое для облучения внутричерепных объектов.
б) Синонимы. Радиохирургия, SRS, STRS, хирургия гамма-ножом.
в) История развития:
– 1951 г.: понятие введено Lars Leksell (1907-1986)
– Первое лечение было проведено в 1950 г. с применением рентгеновской трубки и стереотаксической дуги
– 1954 г.: в лаборатории Lawrence и Berkeley разработан перекрестный пучок протонов
– 1968 г.: проведено лечение гамма-ножом
– 1985 г.: Colombo разработал модифицированный линейный ускоритель
– 2000 г.: для гамма-ножа была разработана автоматическая система позиционирования (APS).

г) Принципы радиохирургии. Лечение обычно проводится под местной анестезией, у всех пациентов, кроме детей и лиц, страдающих клаустрофобией. Принцип действий:
• Формирование контуров патологического очага
• Планирование дозы
• Доставка дозы.
1. Формирование контуров патологического очага. Прежде всего, вокруг головы с помощью стереотаксической рамы устанавливается набор стандартных ориентиров или «нормирующих систем».
Контуры патологического очага формируются при помощи цифровой субтракционной ангиографии (DSA), дополненной МРТ и/или КТ в аксиальной проекции. В редких случаях, аксиальных изображений может быть достаточно. Затем вычерчивают контур мишени.
2. Планирование дозы. Цель заключается в максимально точном соответствии дозы лучистой энергии контурам очага поражения. Включение смежных нормальных тканей может привести к побочным эффектам и осложнениям, в то время как эффективность облучения патологического очага снижается. Помимо соответствия форме, внимание уделяется тому, чтобы избежать прохождения пучков излучения через важные структуры, прилегающие к очагу поражения или даже на расстоянии (например, хрусталик глаза). Это достигается путем подключения нескольких источников излучения в гамма-нож или выбором лечения при помощи линейного ускорителя.
3. Доставка дозы. Существуют две основные технологии для доставки дозы: гамма-нож и линейный ускоритель. С точки зрения количества пациентов и публикаций, гамма-нож доминирует над ускорителем и, следовательно, считается «золотым стандартом».
– Гамма-нож. Концентрический массив из 201 источника кобальт-60 обеспечивает выход гамма-лучей, сфокусированных на цели. Комбинация стационарных источников и коллиматоров позволяет достичь точности в 0,1 мм.
– Линейный ускоритель. Существует несколько методов лечения с помощью линейного ускорителя (LINAC — «linear accelerator»). Может быть использована модифицированная LINAC лучевая терапия с вторичной системой коллиматоров или выделенная LINAC лучевая терапия. Наиболее часто применяется многоуровневая однофокусная некомпланарная дуга и методы конформного блока. При первой технике источник излучения перемещается вдоль нескольких дуг, а вторая основана на высоковольтном трансформаторе, создающим высокое переменное напряжение, после чего пучок проходит в нужной фазе вблизи максимума электрического поля.
Коллиматор состоит из ряда индивидуально моторизованных листов вольфрама, которые устанавливаются автоматически и создают любую форму пучка. При технике модуляции интенсивности доза радиации различной интенсивности доставляется по периметру всего очага поражения. Коллиматор динамически открывается и закрывается под управлением компьютера для выбора экспозиции или частей мишени. Эта технология пока находится на раннем этапе развития, в стадии клинической оценки.
4. Лечение артерио-венозной мальформации (АВМ). Целью является тело АВМ. Тело определяется как сеть слабо дифференцированных и незрелых сосудов, в которой сходятся питающие артерии и выходят переполненные вены.
Механизмы действия:
– Преобладающий фактор: пролиферация эндотелиальных клеток и гиалинизация стенок сосудов.
– Вторичный фактор: развитие миофибробластов адвентициальной оболочки.
5. Критерии отбора пациентов. Лечение артерио-венозной мальформации (АВМ) является мультидисциплинарным. Критерии отбора представлены в таблице ниже.

6. Подходящие артерио-венозные мальформации (АВМ). Большинство артерио-венозных мальформаций (АВМ) поддается терапии. В идеальном случае АВМ небольших размеров (<3 см), компактная и глубоко расположена в функционально значимой зоне. Особенности непригодной АВМ:
• Фистулезное строение (эндоваскулярное лечение, как правило, достаточно).
• Множественные узлы (часто неизлечимы независимо от метода лечения).
• Расположенные вокруг функционально важной структуры, например, вокруг зрительного нерва при синдроме Wyburn-Mason.
• Большинство дуральных АВМ (большой объем, плоская форма и нет истинного узла).
• Диаметр >4 см.
7. Результаты. Результат зависит от размера очага и дозы. При небольших (<2 см) артерио-венозных мальформациях (АВМ) излечение наступает у 85-95% пациентов.
8. Осложнения лечения артерио-венозной мальформации (АВМ):
– Отек, выявляемый на МРТ. В среднем развивается через 11 месяцев примерно у 2,5% больных
– Очаговый неврологический дефицит (парезы, поле зрения, учащение судорог у 2-8%).
– Факторы риска: функционально значимая зона (например, ствол мозга, таламус), размер > 3,5 см, периферическая доза > 25 Гр.
9. Варианты лечения при крупных артерио-венозных мальформациях (АВМ):
• Выжидательная тактика
• Стереотаксическая радиохирургия:
— Малая доза менее эффективна
— Стадирование (радиохирургия проводится с интервалом в несколько месяцев между процедурами)
• Уменьшение объема:
— Хирургия
— Эмболизация
III. Консервативное лечение артерио-венозной мальформации (АВМ) без операции. Сведения о долгосрочных спонтанных исходах у пациентов с АВМ в значительной степени основаны на данных Ondra et al. Частота массивных повторных кровоизлияний составила 4,0%, а смертность 1,0% в год, 23% пациентов погибли из-за кровоизлияния из АВМ. Совокупная частота тяжелых осложнений и смертность составили 2,7% в год. Эти ежегодные показатели практически не менялись в течение всего периода исследования. Риск лечения АВМ IV-V степени по Spetzler сопоставим с рисками естественного течения в течение 10 лет.
Таким образом, только в случае эпилепсии или головной боли консервативное лечение может быть оправдано с рекомендацией пересмотра в случае кровоизлияния.
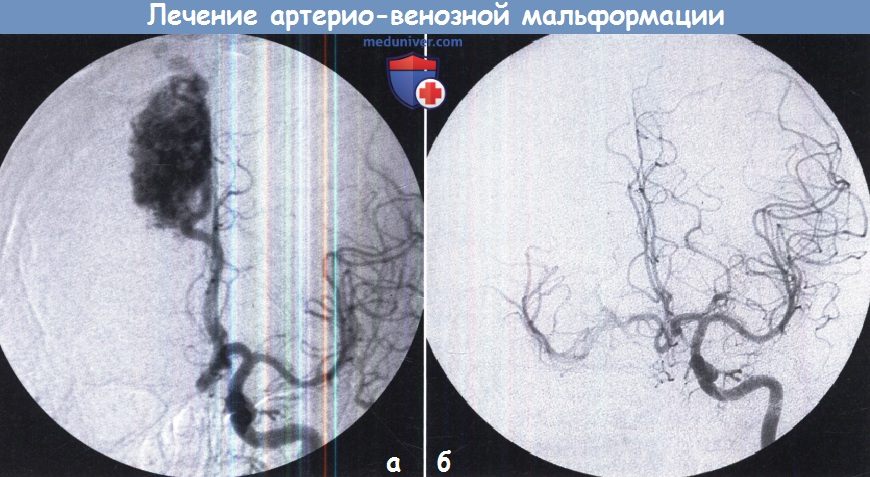
а – Артериовенозная мальформация до радиохирургии.
б – Спустя два года контрольная ангиография показывает полную облитерацию после радиохирургии.
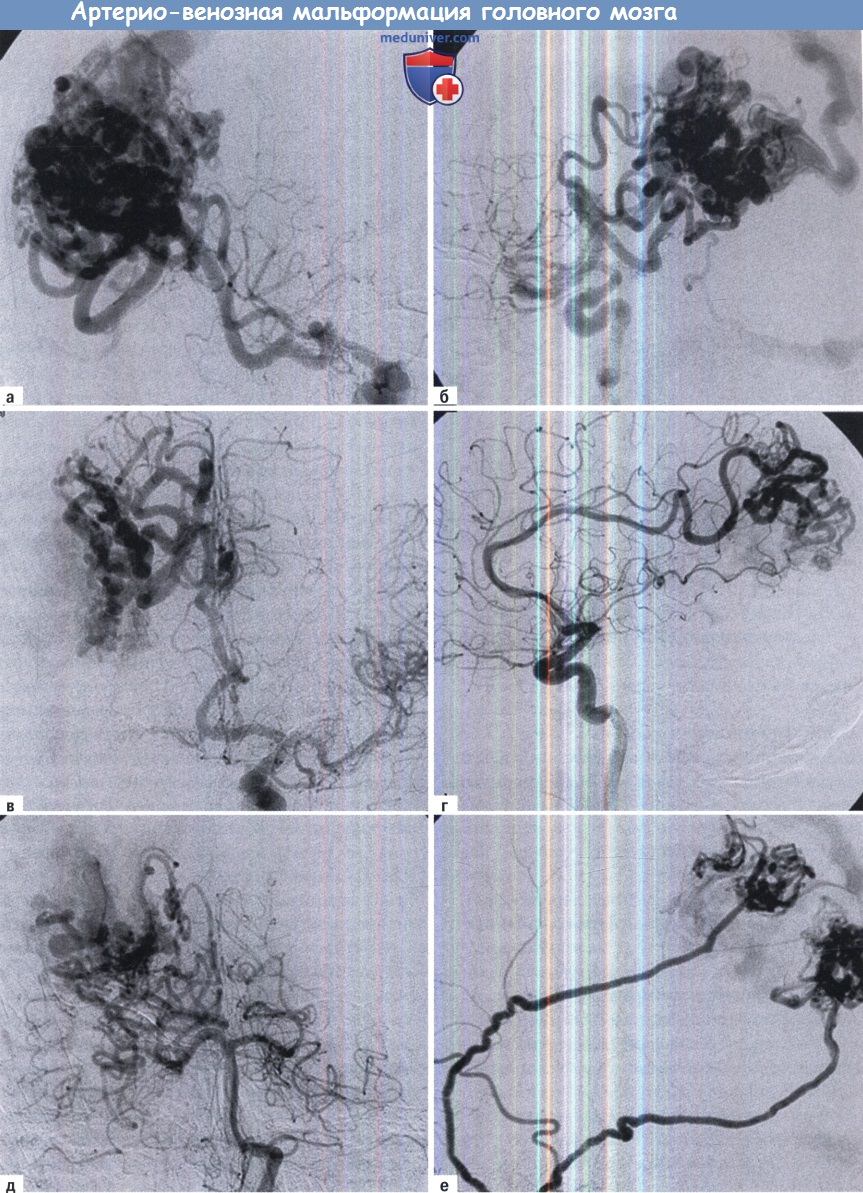
(А, Б) Пример обширной артериовенозной мальформации теменной локализации, питаемой из средней (В, Г) передней и (Д) задней мозговых артерий, а так же из (Е) наружной сонной артерии.
Данный пациент 63 лет поступил с кровоизлиянием. Венозный дренаж осуществляется через верхний сагиттальный синус.
Лечение состояло из совмещения эмболизации и микрохирургии.
– Также рекомендуем “Алгоритм диагностики каверномы головного мозга – Европейские рекомендации”
Оглавление темы “Болезни сосудов головного мозга.”:
- Алгоритм эндоваскулярного лечения аневризмы сосуда головного мозга – Европейские рекомендации
- Алгоритм диагностики артерио-венозных мальформаций головного мозга – Европейские рекомендации
- Алгоритм лечения артерио-венозной мальформации головного мозга – Европейские рекомендации
- Алгоритм диагностики каверномы головного мозга – Европейские рекомендации
- Алгоритм лечения каверномы головного мозга – Европейские рекомендации
- Причины и классификация дуральных артериовенозных фистул (ДАВФ)
- Алгоритм диагностики и лечения дуральной артериовенозной фистулы – Европейские рекомендации
- Алгоритм диагностики сужения сосуда головного мозга и его окклюзии – Европейские рекомендации
- Алгоритм лечения сужения сосуда головного мозга и его окклюзии – Европейские рекомендации
- Алгоритм лечения заболеваний сосудов головного мозга – Европейские рекомендации
Источник
Последствиями патологии являются разрывы сосудистой стенки с кровоизлияниями, ишемия, аневризмы. Лечение только хирургическое, направленное на удаление, эмболизацию или облитерацию мальформации.
Что это такое
В норме вены с артериями соединяются обширной сетью мелких капилляров. Функция последних – перенос питательных веществ из крови в ткани органов. Диффузия возможна за счет однослойного строения стенки капилляров. При мальформации часть капиллярной сети заменяется более крупными извитыми сосудами. Чаще всего этот клубок представляет собой комбинацию вен с артериями – в этом случае речь идет об артериальновенозной мальформации сосудов головного мозга (сокращенно АВМ). Иногда наблюдаются аномалии только одного типа.
Чем опасна данная патология? При небольшом размере конгломерата он может продолжительное время не проявлять себя, однако крупные образования очень опасны. Прежде всего риском разрыва, так как сосудистая стенка мальформации деформированная, истонченная. Вероятность такого исхода составляет до 4% в год, при этом повторное кровоизлияние наступает в 2 раза чаще. Летальный исход в случае разрыва – 1 случай из десяти, а стойкая инвалидизация наступает в половине из них. Если же помимо мальформации имеются аневризмы, смертность повышается.
Еще одно вероятное последствие – ишемия тканей мозга. Сброс крови напрямую из артерий в вены приводит к тому, что участки мозгового вещества, расположенные ниже по направлению тока крови, лишаются кислорода с питательными веществами. Результатом продолжительного «голодания» становятся дисфункция и отмирание тканей по типу ишемического инсульта.
Несмотря на то что заболевание достаточно редкое – 2 случая на 100 000 – из-за негативных последствий и высокой летальности ему уделяется особое внимание в неврологии.
Классификация
Сосудистая мальформация, находящаяся в головном мозге, может состоять только из вен, артерий либо быть комбинированной. Последний вариант – артериальновенозный – встречается чаще всего.
По типу строения церебральные АВМ подразделяются на:
- Рацемозные (составляют ¾ от общего количества) – разветвленный сосудистый конгломерат.
- Фистулезная – представляет собой массивный шунт между крупными сосудами.
- Кавернозная – скопление тонкостенных полостей, внешне напоминающее ягоды шелковицы (диагностируется в 11% случаев АВМ).
- Микромальформация – небольшое по размерам образование.
Среди изолированных выделяют венозную мальформацию, артериальную, телеангиоэктазию. Аномалии различают также по размеру. Диаметр малых не превышает 30 мм, средних – 60 мм, а крупные – это клубки больше 6 см. Для диагностики и лечения имеет значение локализация дефекта: в легких случаях они расположены вне функционально значимых зон, к которым относятся мозговой ствол, височные и затылочные доли, таламус, сенсомоторная кора, речевая область, центр Брока. Важен также характер дренирования, то есть наличие выхода в крупные вены.
Перечисленные параметры классификации важны для определения риска в случае операции. Каждый из них (локализация, тип дренирования, размер) оценивается по трехбалльной шкале, и в зависимости от суммы набранных баллов определяется операционный риск. Низкий – это 1, а пятерка означает повышенную техническую сложность вмешательства, высокую вероятность инвалидизации или летального исхода.
Причины
В большинстве случаев артериовенозная мальформация головного мозга – следствие нарушения формирования церебральной сосудистой сети во внутриутробном периоде. Генетический фактор не доказан, поэтому наследственность роли, предположительно, не играет. Негативное влияние на развитие системы мозгового кровообращения у плода оказывают хронические заболевания будущей матери, внутриутробные инфекции, повышение радиационного фона. Тератогенный эффект дают также прием некоторых препаратов, интоксикации, наличие у беременной вредных привычек (алкоголизм, наркомания, курение).
Частота кровоизлияний у детей с цереброваскулярной патологией данного типа невелика. Обычно заболевание впервые проявляется после достижения 20-летнего возраста. По мере взросления пациента риск разрыва образования возрастает. Приобретенные мальформации встречаются очень редко, манифестируя к 50 годам. Среди причин развития болезни выделяют атеросклеротические, склеротические изменения сосудистой стенки, а также черепно-мозговые травмы.
Симптомы
Симптоматика заболевания зависит от типа его протекания. Первый, геморрагический, наблюдается более чем в половине случаев (по статистике, до 70%). Он характерен для сосудистых мальформаций небольших размеров. Второй вариант клинических проявлений – торпидный – встречается при крупных и средних образованиях.
Геморрагическое течение патологии
Мелкие конгломераты, характерные для этого типа протекания, могут не проявляться годами. Часто первым признаком заболевания становится разрыв дефектной стенки сосуда с последующим кровоизлиянием. Если артериовенозная аномалия дислоцируется в задней черепной ямке и имеет дренирующие вены, появляется такой клинический симптом, как артериальная гипертензия. В случае разрыва развивается симптоматика геморрагического инсульта:
- интенсивная головная боль;
- тошнота с приступами рвоты;
- парестезии, параличи, мышечная слабость;
- спутанность и потеря сознания;
- расстройства мозговой деятельности (координации, зрения, речи).
Перечисленные признаки свойственны субарахноидальному кровоизлиянию (кровотечение происходит между мозговыми оболочками). На его долю приходится почти половина от общего числа случаев. В остальных кровь изливается непосредственно в мозг с образованием гематом различной локализации. Наиболее опасны из них внутрижелудочковые. К общей симптоматике при внутримозговом кровоизлиянии присоединяются специфические симптомы, по которым можно определить пораженную область мозга.
Торпидное течение патологии
В отличие от геморрагического, о наличии сосудистой мальформации можно судить еще до ее разрыва. Крупные и средние по размеру аномалии проявляются регулярными кластерными головными болями. Приступы могут длиться на протяжении 3 часов, на их фоне нередко развивается судорожный синдром. Еще одним характерным признаком может стать неврологический дефицит, свойственный для опухолей мозга.
В этом случае развиваются общемозговые симптомы: диффузные головные боли распирающего характера, расстройства психики и зрения, рвота, эпиприступы. По характеру эпилептических припадков и предшествующей им ауры можно достаточно достоверно установить местоположение мальформации. Когда она оказывает давление на близлежащие ткани и отдаленные структуры, к общемозговой симптоматике присоединяется очаговая. В зависимости от локализации могут наблюдаться нарушения когнитивных функций, парезы лицевых нервов, параличи конечностей и другие неврологические расстройства.
АВМ вены Галена
Отдельный вид врожденной цереброваскулярной патологии у детей, характеризующийся комплексом дефектов развития большой мозговой вены, включая шунтирование. Встречается достаточно редко, однако в большинстве случаев приводит к летальному исходу.
Единственный вид лечения – нейрохирургическая операция в первый год жизни. Основные симптомы определяются сразу после рождения у половины младенцев с данным типом АВМ: сердечная недостаточность, гидроцефалия. В последующем наблюдается отставание в психическом и физическом развитии.
Диагностика
До разрыва сосудистая мальформация геморрагического типа часто никак не проявляется и может быть обнаружена случайным образом. При торпидном течении заболевания поводом для обращения к неврологу служат головные боли, появление судорожного синдрома, очаговых признаков. На основании жалоб врач назначает консультацию нейрохирурга, который проводит комплексное обследование:
- электроэнцефалографию;
- эхоэнцефалографию;
- реоэнцефалографию;
- КТ и МРТ;
- церебральную ангиографию.
Компьютерная и магнитно-резонансная томография в случае патологии торпидного типа может оказаться неинформативной. Для подтверждения диагноза предпочтительна ангиография с использованием контрастного вещества. При разрыве весь комплекс диагностических мероприятий проводится экстренно, наибольшей информативностью при этом обладает МРТ.
Как лечится мальформация
Лечение аномалии до ее разрыва сводится к исключению конгломерата из кровотока. Выполняется эта задача одним из трех методов: эмболизацией АВМ головного мозга, транскраниальным или радиохирургическим удалением. Методика подбирается с учетом всех операционных рисков, величины и локализации образования.
Операция проводится по показаниям также после разрыва, когда состояние пациента стабилизируется. На остром этапе возможно только удаление гематомы. Комбинированное вмешательство (экстракция сгустка и иссечение АВМ) показано при небольших размерах образования.
Хирургическое удаление
Выполняется транскраниально после трепанации черепа, если объем сосудистой мальформации не превышает 100 мл. Применяется при неглубоком залегании конгломерата вне функционально значимых областей мозга. В ходе операции приводящие сосуды перекрываются методом коагуляции, конгломерат выделяется, отводящие вены перевязываются, АВМ иссекается полностью.
Классическое удаление в большинстве случаев гарантирует полное выздоровление, однако требуется прием ноотропов с ангиопротекторами в восстановительном периоде. Обязательно систематическое наблюдение у врача, поскольку вероятны осложнения – инсульты.
Эмболизация АВМ
Менее травматичная методика лечения, направленная не на удаление, а на окклюзию цереброваскулярной аномалии. С помощью микрокатетера, введенного в разрез бедренной артерии, в мальформацию вводят специальный сополимер, склеивающий сосуды. Данный способ используется только в том случае, когда имеются приводящие сосуды, доступные для катетеризации.
Кроме того, эмболизация проводится в несколько этапов, а полной окклюзии удается добиться только у трети пациентов. Поэтому часто эта манипуляция проводится в качестве подготовительной перед хирургическим иссечением. Предварительное склеивание части сосудов уменьшает риск операционных кровотечений и осложнений в послеоперационном периоде.
Радиохирургический метод
Как и классическая хирургическая операция, позволяет полностью удалить аномалию (однако размер ее не должен превышать 3 см). Этот способ используется, когда транскраниальный доступ к сосудистой мальформации мозга затруднен, а также нет возможности провести эмболизацию. Операция представляет собой часовое облучение пораженной зоны узконаправленным излучением. После этого происходит постепенное склерозирование АВМ в течение нескольких лет.
Недостатком радиохирургического лечения является долго ожидание полного закрытия сосудов, поскольку сохраняется вероятность разрыва. Поэтому современные методики чаще всего состоят из разных типов операций. Например, сначала делается частичная эмболизация, а затем АВМ удаляется хирургически.
Последствия и прогнозы
Наиболее вероятный исход мальформации – это ее разрыв со всеми специфическими симптомами и последствиями геморрагического инсульта. Степень инвалидизации, вероятность летального исхода зависят от объема и локализации кровоизлияния. Повторные разрывы повышают процент смертности. Однако есть возможность дожить до преклонных лет без хирургического вмешательства, что наблюдается примерно в половине случаев АВМ.
Если появляются характерные мозговые симптомы в виде головных болей, эпиприступов, обращение к неврологу и начало лечения помогут избежать осложнений. Каков процент выздоровления после операции? Радиохирургическое и классическое удаление – 85%, эмболизация – около 30%. В комбинации эти методики более эффективны и дают почти стопроцентный результат. Из послеоперационных осложнений наиболее вероятным является инсульт.
Источник
