Механическое сопротивление кровеносных сосудов выше
Vascular resistance is the resistance that must be overcome to push blood through the circulatory system and create flow.The resistance offered by the systemic circulation is known as the systemic vascular resistance (SVR) or may somes be called by the older term total peripheral resistance (TPR), while the resistance offered by the pulmonary circulation is known as the pulmonary vascular resistance (PVR). Systemic vascular resistance is used in calculations of blood pressure, blood flow, and cardiac . Vasoconstriction (i.e., decrease in blood vessel diameter) increases SVR, whereas vasodilation (increase in diameter) decreases SVR.
Units for measuring vascular resistance are dyn·s·cm−5, pascal seconds per cubic metre (Pa·s/m3) or, for ease of deriving it by pressure (measured in mmHg) and cardiac output (measured in L/min), it can be given in mmHg·min/L. This is numerically equivalent to hybrid resistance units (HRU), also known as Wood units (in honor of Paul Wood, an early pioneer in the field), frequently used by pediatric cardiologists. The conversion between these units is:[1]
| Measurement | Reference range | ||
|---|---|---|---|
| dyn·s/cm5 | MPa·s/m3 | mmHg·min/l or HRU/Wood units | |
| Systemic vascular resistance | 700-1600[2] | 70-160[3] | 9-20[3] |
| Pulmonary vascular resistance | 20-130[2] | 2-13[3] | 0.25-1.6[3] |
Calculation[edit]
The basic tenet of calculating resistance is that flow is equal to driving pressure divided by flow rate.[citation needed]
where
- R is Resistance
- ΔP is the change in pressure across the circulation loop (systemic / pulmonary) from its beginning (imtely after exiting the left ventricle / right ventricle) to its end (entering the right atrium / left atrium)
- Q is the flow through the vasculature (when ing SVR this is equal to cardiac output)
- This is the hydraulic version of Ohm’s law, V=IR (which can be reed as R=V/I), in which the pressure differential is analogous to the electrical voltage drop, flow is analogous to electric current, and vascular resistance is analogous to electrical resistance.
Systemic calculations[edit]
The systemic vascular resistance can therefore be calculated in units of dyn·s·cm−5 as
where mean arterial pressure is 2/3 of diastolic blood pressure plus 1/3 of systolic blood pressure [or Diastolic + 1/3(Systolic-Diastolic)].
In other words:
Systemic Vascular Resistance = 80x(Mean Arterial Pressure – Mean Venous Pressure or CVP) / Cardiac Output
Mean arterial pressure is most commonly measured using a sphygmomanometer, and calculating a specialized average between systolic and diastolic blood pressures. Venous pressure, also known as central venous pressure, is measured at the right atrium and is usually very low (normally around 4 mm Hg). As a result, it is somes disregarded.
Pulmonary calculations[edit]
The pulmonary vascular resistance can be calculated in units of dyn·s·cm−5 as[citation needed]
where the pressures are measured in units of millimetres of mercury (mmHg) and the cardiac output is measured in units of litres per minute (L/min). The pulmonary artery wedge pressure (also called pulmonary artery occlusion pressure or PAOP) is a measurement in which one of the pulmonary arteries is occluded, and the pressure downstream from the occlusion is measured in order to approximately sample the left atrial pressure.[4] Therefore, the numerator of the above equation is the pressure difference between the input to the pulmonary blood circuit (where the heart’s right ventricle connects to the pulmonary trunk) and the output of the circuit (which is the input to the left atrium of the heart). The above equation contains a numerical constant to compensate for the units used, but is conceptually equivalent to the following:[citation needed]
where R is the pulmonary vascular resistance (fluid resistance), ΔP is the pressure difference across the pulmonary circuit, and Q is the rate of blood flow through it.
As an example: If Systolic pressure: 120 mmHg, Diastolic pressure: 80 mmHg, Right atrial mean pressure: 3 mmHg, Cardiac output: 5 l/min, Then Mean Arterial Pressure would be: (2 Diastolic pressure + Systolic pressure)/3 = 93.3 mmHg, and Systemic vascular resistance: (93 – 3) / 5 = 18 Wood Units. Or Systemic vascular resistance: 18 x 80 = 1440 dyn·s/cm5. These values are in the normal limits.[citation needed]
Regulation[edit]
There are many factors that alter the vascular resistance. Vascular compliance is determined by the muscle tone in the smooth muscle tissue of the tunica and the elasticity of the elastic fibers there, but the muscle tone is subject to continual homeoic changes by hormones and cell aling molecules that induce vasodilation and vasoconstriction to keep blood pressure and blood flow within reference ranges.[citation needed]
In a first approach, based on fluids dynamics (where the flowing material is continuous and made of continuous atomic or molecular bonds, the internal friction happen between continuous parallel layers of different velocities) factors that influence vascular resistance are represented in an adapted form of the Hagen-Poiseuille equation:[citation needed]
where
- R = resistance to blood flow
- L = length of the vessel
- η = viscosity of blood
- r = radius of the blood vessel
Vessel length is generally not subject to change in the body.
In Hagen-Poiseuille equation, the flow layers start from the wall and, by viscosity, reach each other in the central line of the vessel following a parabolic velocity profile.[citation needed]
In a second approach, more realistic and coming from experimental observations on blood flows, according to Thurston,[5] there is a plasma release-cell layering at the walls surrounding a plugged flow. It is a fluid layer in which at a distance δ, viscosity η is a of δ written as η(δ), and these surrounding layers do not meet at the vessel centre in real blood flow. Instead, there is the plugged flow which is hyperviscous because holding high concentration of RBCs. Thurston assembled this layer to the flow resistance to describe blood flow by means of a viscosity η(δ) and thickness δ from the wall layer.[citation needed]
The blood resistance law appears as R adapted to blood flow profile :
[5]
where
- R = resistance to blood flow
- c = constant coefficient of flow
- L = length of the vessel
- η(δ) = viscosity of blood in the wall plasma release-cell layering
- r = radius of the blood vessel
- δ = distance in the plasma release-cell layer
Blood resistance varies depending on blood viscosity and its plugged flow (or sheath flow since they are complementary across the vessel section) size as well, and on the size of the vessels.
Blood viscosity increases as blood is more hemoconcentrated, and decreases as blood is more dilute. The greater the viscosity of blood, the larger the resistance will be. In the body, blood viscosity increases as red blood cell concentration increases, thus more hemodilute blood will flow more readily, while more hemoconcentrated blood will flow more slowly.[citation needed]
Counteracting this effect, decreased viscosity in a liquid results in the potential for increased turbulence. Turbulance can be viewed from outside of the closed vascular system as increased resistance, thereby countering the ease of flow of more hemodilute blood. Turbulence, particularly in large vessels, may account for some pressure change across the vascular bed.
The major regulator of vascular resistance in the body is regulation of vessel radius. In humans, there is very little pressure change as blood flows from the aorta to the large arteries, but the small arteries and arterioles are the site of 70% of the pressure drop, and are the main regulators of SVR. When environmental changes occur (e.g. exercise, immersion in water), neuronal and hormonal als, including binding of norepinephrine and epinephrine to the α1 receptor on vascular smooth muscles, cause either vasoconstriction or vasodilation. Because resistance is inversely proportional to the fourth power of vessel radius, changes to arteriole diameter can result in large increases or decreases in vascular resistance.[6]
If the resistance is inversely proportional to the fourth power of vessel radius, the resulting force exerted on the wall vessels, the parietal drag force, is inversely proportional to the second power of the radius. The force exerted by the blood flow on the vessel walls is, according to the Poiseuille equation, the wall shear stress. This wall shear stress is proportional to the pressure drop. The pressure drop is applied on the section surface of the vessel, and the wall shear stress is applied on the sides of the vessel. So the total force on the wall is proportional to the pressure drop and the second power of the radius. Thus the force exerted on the wall vessels is inversely proportional to the second power of the radius.
The blood flow resistance in a vessel is mainly regulated by the vessel radius and viscosity when blood viscosity too varies with the vessel radius. According to very recent results showing the sheath flow surrounding the plug flow in a vessel,[7] the sheath flow size is not neglectible in the real blood flow velocity profile in a vessel. The velocity profile is directly ed to flow resistance in a vessel. The viscosity variations, according to Thurston,[5] are also balanced by the sheath flow size around the plug flow. The secondary regulators of vascular resistance, after vessel radius, is the sheath flow size and its viscosity.
Thurston,[5] as well, shows that the resistance R is constant, where, for a defined vessel radius, the value η(δ)/δ is constant in the sheath flow.
Vascular resistance depends on blood flow which is divided into 2 adjacent parts : a plug flow, highly concentrated in RBCs, and a sheath flow, more fluid plasma release-cell layering. Both coexist and have different viscosities, sizes and velocity profiles in the vascular system.[citation needed]
Combining Thurston’s work with the Hagen-Poiseuille equation shows that blood flow exerts a force on vessel walls which is inversely proportional to the radius and the sheath flow thickness. It is proportional to the mass flow rate and blood viscosity.
[5]
where
- F = Force exerted by blood flow on vessel walls
- Q = Volumetric flow rate
- c = constant coefficient of flow
- L = length of the vessel
- η(δ) = dynamic viscosity of blood in the wall plasma release-cell layering
- r = radius of the blood vessel
- δ = distance in the plasma release-cell layer or sheath flow thickness
Other factors[edit]
Many of the platelet-derived substances, including serotonin, are vasodilatory when the endothelium is intact and are vasoconstrictive when the endothelium is damaged.[citation needed]
Cholinergic stimulation causes release of endothelium-derived relaxing factor (EDRF) (later it was discovered that EDRF was nitric oxide) from intact endothelium, causing vasodilation. If the endothelium is damaged, cholinergic stimulation causes vasoconstriction.[citation needed]
Adenosine most likely does not play a role in maintaining the vascular resistance in the resting e. However, it causes vasodilation and decreased vascular resistance during hypoxia. Adenosine is formed in the myocardial cells during hypoxia, ischemia, or vigorous work, due to the breakdown of high-energy phosphate compounds (e.g., adenosine monophosphate, AMP). Most of the adenosine that is produced leaves the cell and acts as a direct vasodilator on the vascular wall. Because adenosine acts as a direct vasodilator, it is not dependent on an intact endothelium to cause vasodilation.[citation needed]
Adenosine causes vasodilation in the small and medium-sized resistance arterioles (less than 100 μm in diameter). When adenosine is administered it can cause a coronary steal phenomenon,[8] where the vessels in healthy tissue dilate as much as the ischemic tissue and more blood is shunted away from the ischemic tissue that needs it most. This is the principle behind adenosine stress testing. Adenosine is quickly broken down by adenosine deaminase, which is present in red cells and the vessel wall.[citation needed]
Systemic[edit]
Effects of systemic on the body[edit]
A decrease in SVR (e.g., during exercising) will result in an increased flow to tissues and an increased venous flow back to the heart. An increased SVR will decrease flow to tissues and decrease venous flow back to the heart.[citation needed]
Pulmonary[edit]
The major determinant of vascular resistance is small arteriolar (known as resistance arterioles) tone. These vessels are from 450 μm down to 100 μm in diameter. (As a comparison, the diameter of a capillary is 5 to 10 μm.)[citation needed]
Another determinant of vascular resistance is the pre-capillary arterioles. These arterioles are less than 100 μm in diameter. They are somes known as autoregulatory vessels since they can dynamically change in diameter to increase or reduce blood flow.[citation needed]
Any change in the viscosity of blood (such as due to a change in hematocrit) would also affect the measured vascular resistance.[citation needed]
Pulmonary vascular resistance (PVR) also depends on the lung volume, and PVR is lowest at the al residual capacity (FRC). The highly compliant nature of the pulmonary circulation means that the degree of lung distention has a large effect on PVR. This results primarily due to effects on the alveolar and -alveolar vessels. During inspiration, increased lung volumes cause alveolar expansion and lengthwise stretching of the interstitial alveolar vessels. This increases their length and reduces their diameter, thus increasing alveolar vessel resistance. On the other hand, decreased lung volumes during expiration cause the -alveolar arteries and veins to become narrower due to decreased radial traction from adjacent tissues. This leads to an increase in -alveolar vessel resistance. PVR is calculated as a sum of the alveolar and -alveolar resistances as these vessels lie in series with each other. Because the alveolar and -alveolar resistances are increased at high and low lung volumes respectively, the total PVR takes the shape of a U curve. The point at which PVR is the lowest is near the FRC.[citation needed]
Coronary[edit]
The regulation of tone in the coronary arteries is a complex subject. There are a number of mechanisms for regulating coronary vascular tone, including bolic demands (i.e. hypoxia), neurologic control, and endothelial factors (i.e. EDRF, endothelin).[citation needed]
Local bolic control (based on bolic demand) is the most important mechanism of control of coronary flow. Decreased tissue oxygen content and increased tissue CO2 content act as vasodilators. Acidosis acts as a direct coronary vasodilator and also potentiates the actions of adenosine on the coronary vasculature.[citation needed]
See also[edit]
- Arterial resistivity index
- Hemodynamics
- Blood pressure
- Adenosine
- Perfusion
- Cardiac output
- Vasoconstriction
- Vasodilation
References[edit]
- ^ Fuster, V.; Alexander, R.W.; O’Rourke, R.A. (2004) Hurst’s the heart, book 1. 11th Edition, McGraw-Hill Professional, Medical Pub. Division. Page 513. ISBN 978-0-07-143224-5.
- ^ a b Table 30-1 in: Trudie A Goers; Washington University School of Medicine Department of Surgery; Klingensmith, Mary E; Li Ern Chen; Sean C Glasgow (2008). The Washington manual of surgery. Philadelphia: Wolters Kluwer Health/Lippincott Williams & Wilkins. ISBN 978-0-7817-7447-5 .CS1 maint: multiple names: s list ()
- ^ a b c d Derived from values in dyn·s/cm5
- ^ University of Virginia Health System.”The Physiology: Pulmonary Artery Catheters”
- ^ a b c d e GB Thurston, Viscosity and viscoelasticity of blood in small diameter tubes, Microvasular Re 11, 133 146, 1976
- ^ “Cardiac Output and Blood Pressure”. biosbcc. Retrieved 7 April 2011.
- ^ Measurement of real pulsatile blood flow using X-ray PIV technique with CO2 microbubbles, Hanwook Park, Eunseop Yeom, Seung-Jun Seo, Jae-Hong Lim & Sang-Joon Lee, NATURE, Scientific Reports 5, Article number: 8840 (2015), doi:10.1038/srep08840.
- ^ Masugata H, Peters B, Lafitte S, et al. (2003). “Assessment of adenosine-induced coronary steal in the setting of coronary occlusion based on the extent of opacification defects by myocardial contrast echocardiography”. Angiology. 54 (4): 443-8. doi:10.1177/000331970305400408. PMID 12934764.
Table 30-1 describing normal values of hemodynamic parameters is found in the Fifth Edition of the Washington Manual of Surgery.
Further reading[edit]
- Grossman W, Baim D. Grossman’s Cardiac Catheterization, Angiography, and Intervention, Sixth Edition. Page 172, Tabe 8.1 ISBN 0-683-30741-X
- Heart rmation: Systemic vascular resistance
Источник
Сопротивляемость сосудов. Проводимость сосудов
Сопротивление представляет собой препятствие кровотоку, которое возникает в кровеносных сосудах. Сопротивление не может быть измерено никаким прямым методом. Оно может быть рассчитано с использованием данных о величине кровотока и разницы давления на обоих концах кровеносного сосуда. Если разница давления равна 1 мм рт. ст., а объемный кровоток равен 1 мл/сек, сопротивление составляет 1 единицу периферического сопротивления (ЕПС).
Сопротивление, выраженное в единицах системы СГС. Иногда для выражения единиц периферического сопротивления используют единицы системы СГС (сантиметры, граммы, секунды). В этом случае единицей сопротивления будет дина сек/см5. Сопротивление в этих единицах может быть рассчитано по следующей формуле:
R(дина*сек/см5) = (1333 * мм.рт.ст.) / мл/сек.
Общее периферическое сосудистое сопротивление и общее легочное сосудистое сопротивление. Объемная скорость кровотока в системе кровообращения соответствует сердечному выбросу, т.е. тому объему крови, которое сердце перекачивает за единицу времени. У взрослого человека это составляет примерно 100 мл/сек. Разница давления между системными артериями и системными венами равна примерно 100 мм рт. ст. Следовательно, сопротивление всего системного (большого) круга кровообращения или, иными словами, общее периферическое сопротивление соответствует 100/100 или 1 ЕПС.
В условиях, когда все кровеносные сосуды организма резко сужены, общее периферическое сопротивление может возрасти до 4 ЕПС. И наоборот, если все сосуды окажутся расширенными, сопротивление может упасть до 0,2 ЕПС.
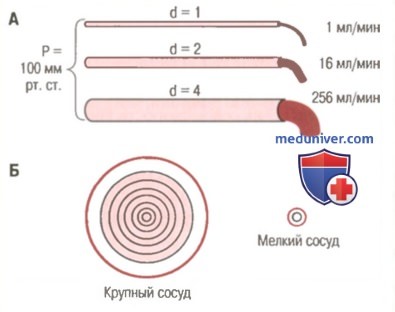
 А. Влияние диаметра сосуда на объемный кровоток.
А. Влияние диаметра сосуда на объемный кровоток.
Б. Концентрические слои крови, текущие вдоль сосуда с разной скоростью; поток тем быстрее, чем дальше от стенки сосуда
В сосудистой системе легких артериальное давление в среднем равно 16 мм рт. ст., а среднее давление в левом предсердии – 2 мм рт. ст. Следовательно, общее легочное сосудистое сопротивление составит 0,14 ЕПС (примерно 1/7 общего периферического сопротивления) при обычном сердечном выбросе, равном 100 мл/сек.
Проводимость сосудистой системы для крови и ее взаимосвязь с сопротивлением. Проводимость определяется объемом крови, протекающим по сосудам, за счет данной разницы давления. Проводимость выражается в миллилитрах за секунду на миллиметр ртутного столба, но может быть выражена также в литрах за секунду на миллиметр ртутного столба или в каких-либо других единицах объемного кровотока и давления.
Очевидно, что проводимость – это величина, обратная сопротивлению: проводимость = 1/сопротивление.
Незначительные изменения диаметра сосудов могут привести к существенным изменениям их проводимоаи. В условиях ламинарного течения крови незначительные изменения диаметра сосудов могут резко изменить величину объемного кровотока (или проводимость кровеносных сосудов). На рисунке показаны три сосуда, диаметры которых соотносятся как 1, 2 и 4, а разница давления между концами каждого сосуда одинакова – 100 мм рт. ст. Скорость объемного кровотока в сосудах равна 1, 16 и 256 мл/мин, соответственно.
Обратите внимание, что при увеличении диаметра сосуда только в 4 раза объемный кровоток увеличился в нем в 256 раз. Таким образом, проводимость сосуда увеличивается пропорционально четвертой степени диаметра в соответствии с формулой: Проводимость ~ Диаметр4.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
– Также рекомендуем “Закон Пуазейля. Диаметр артериол и их сопротивление”
Оглавление темы “Сосудистая система”:
1. Электрокардиограмма при фибрилляции желудочков. Электрошоковая дефибрилляция желудочков
2. Ручной массаж сердца в помощь дефибрилляции. Фибрилляция предсердий
3. Трепетание предсердий. Остановка сердца
4. Функциональные участки системы кровообращения. Объемы крови в различных отделах сосудистой системы
5. Давление крови в различных участках сосудистой системы. Теоретические основы кровообращения
6. Регуляция объема кровотока и периферического сопротивления. Объемный кровоток
7. Ультразвуковой флоуметр. Ламинарное течение крови в сосудах
8. Турбулентное течение крови. Давление крови
9. Сопротивляемость сосудов. Проводимость сосудов
10. Закон Пуазейля. Диаметр артериол и их сопротивление
Источник
8)классификация кровеносных сосудов.
Кровено́сные сосу́ды – эластичные трубчатые образования в теле животных и человека, по которым силой ритмически сокращающегося сердца или пульсирующего сосуда осуществляется перемещение крови по организму: к органам и тканям по артериям, артериолам, артериальным капиллярам, и от них к сердцу – по венозным капиллярам, венулам и венам.
Среди сосудов кровеносной системы различают артерии, артериолы, капилляры, венулы, вены и артериоло-венозные анастомозы; сосуды системы микроциркуляторного русла осуществляют взаимосвязь между артериями и венами. Сосуды разных типов отличаются не только по своей толщине, но и по тканевому составу и функциональным особенностям.
Артерии – сосуды, по которым кровь движется от сердца. Артерии имеют толстые стенки, в которых содержатся мышечные волокна, а также коллагеновые и эластические волокна. Они очень эластичные и могут сужаться или расширяться, в зависимости от количества перекачиваемой сердцем крови.
Артериолы – мелкие артерии, по току крови непосредственно предшествующие капиллярам. В их сосудистой стенке преобладают гладкие мышечные волокна, благодаря которым артериолы могут менять величину своего просвета и, таким образом, сопротивление.
Капилляры – это мельчайшие кровеносные сосуды, настолько тонкие, что вещества могут свободно проникать через их стенку. Через стенку капилляров осуществляется отдача питательных веществ икислорода из крови в клетки и переход углекислого газа и других продуктов жизнедеятельности из клеток в кровь.
Венулы – мелкие кровеносные сосуды, обеспечивающие в большом круге отток обедненной кислородом и насыщенной продуктами жизнедеятельности крови из капилляров в вены.
Вены – это сосуды, по которым кровь движется к сердцу. Стенки вен менее толстые, чем стенки артерий и содержат соответственно меньше мышечных волокон и эластических элементов.
9)Объемная скорость кровотока
Объемная скорость потока крови (кровотока) сердца – это динамический показатель деятельности сердца. Соответствующая этому показателю переменная физическая величина характеризует объёмное количество крови, проходящее через поперечное сечение потока (в сердце) за единицу времени. Объемную скорость кровотока сердца оценивают по формуле:
CO = HR · SV / 1000,
где: HR – частота сокращений сердца (1 / мин), SV – систолический объём кровотока (мл, л). Система кровообращения, или сердечно-сосудистая система представляет собой замкнутую систему (см. схему 1, схему 2, схему 3). Она состоит из двух насосов (правое сердце и левое сердце), соединенных между собой последовательнокровеносными сосудами большого круга кровообращения и кровеносными сосудами малого круга кровообращения(сосудами лёгких). В любом совокупном сечении этой системы протекает одно и то же количество крови. В частности, при одних и тех же условиях поток крови, протекающий через правое сердце, равен потоку крови, протекающей через левое сердце. У человека в состоянии покоя объёмная скорость кровотока (как правого, так и левого) сердца составляет ~4,5 ÷ 5,0 л / мин. Целью системы кровообращения является обеспечение непрерывного кровотока во всех органах и тканях в соответствии с потребностями организма. Сердце является насосом, перекачивающим кровь по системе кровообращения. Вместе с кровеносными сосудами сердце актуализирует цель системы кровообращения. Отсюда, объёмная скорость кровотока сердца является переменной, характеризующей эффективность работы сердца. Кровоток сердца управляется сердечно-сосудистым центром и зависит от ряда переменных. Главными из них являются:объёмная скорость потока венозной крови к сердцу (л / мин), конечно-диастолический объём кровотока (мл), систолический объём кровотока (мл), конечно-систолический объём кровотока (мл), частота сокращений сердца (1 / мин).
10) Линейная скорость потока крови (кровотока) – это физическая величина, являющаяся мерой движения частиц крови, составляющих поток. Теоретически она равна расстоянию, проходимому частицей вещества, составляющего поток, в единицувремени: v = L / t. Здесь L – путь (м), t – время (c). Кроме линейной скорости кровотока различают объёмную скорость потока крови, или объёмную скорость кровотока. Средняя линейная скорость ламинарного кровотока (v) оценивается интегрированием линейных скоростей всех цилиндрических слоев потока:
v = ( dP · r4 ) / ( 8η · l ),
где: dP – разница давления крови в начале и в конце участка кровеносного сосуда, r – радиус сосуда, η – вязкость крови, l – длина участка сосуда, коэффициент 8 – это результат интегрирования скоростей, движущихся в сосуде слоев крови. Объемная скорости кровотока (Q) и линейная скорости кровотока связаныотношением :
Q = v · π · r2 .
Подставив в это отношение выражение для v получим уравнение («закон») Хагена-Пуазейля для объёмной скорости кровтотка:
Q = dP · ( π · r4 / 8η · l ) (1).
Исходя из простой логики, можно утверждать, что объёмная скорость любого потока прямо пропорциональна движущейсиле и обратно пропорциональна сопротивлению потоку. Аналогично, объёмная скорость кровотока ( Q ) прямо пропорциональна движущей силе (градиентдавления, dP ), обеспечивающей кровоток, и обратно пропорциональна сопротивлению кровотоку ( R ): Q = dP / R . Отсюда R = dP / Q . Подставляя в это отношение выражение (1) для Q , получим формулу для оценки сопротивления кровотоку:
R = ( 8η · l ) / ( π · r4 ).
Из всех этих формул видно, что самой значимой переменной, определяющей линейную и объёмную скорости кровотока, является просвет (радиус) сосуда. Эта переменная является главной переменной в управлении кровотоком.
11)
Гидродинамическое сопротивление прямо пропорционально длине сосуда и вязкости крови и обратно пропорционально радиусу сосуда в 4-й степени, то есть больше всего зависит от просвета сосуда. Так как наибольшим сопротивлением обладают артериолы , ОПСС зависит главным образом от их тонуса.
Различают центральные механизмы регуляции тонуса артериол и местные механизмы регуляции тонуса артериол.
К первым относятся нервные и гормональные влияния , ко вторым – миогенная , метаболическаяи эндотелиальная регуляция .
На артериолы оказывают постоянный тонический сосудосуживающий эффект симпатические нервы . Величина этого симпатического тонуса зависит от импульсации, поступающей отбарорецепторов каротидного синуса , дуги аорты и легочных артерий .
Основные гормоны, в норме участвующие в регуляции тонуса артериол, – это адреналин инорадреналин , вырабатываемые мозговым веществом надпочечников .
Миогенная регуляция сводится к сокращению или расслаблению гладких мышц сосудов в ответ на изменения трансмурального давления; при этом напряжение в их стенке остается постоянным. Тем самым обеспечивается ауторегуляция местного кровотока – постоянство кровотока при меняющемся перфузионном давлении.
Метаболическая регуляция обеспечивает расширение сосудов при повышении основного обмена(за счет выброса аденозина и простагландинов ) и гипоксии (также за счет выделения простагландинов).
Наконец, эндотелиальные клетки выделяют ряд вазоактивных веществ – окись азота ,эйкозаноиды ( производные арахидоновой кислоты ), сосудосуживающие пептиды ( эндотелин-1, ангиотензин II ) и свободные радикалы кислорода .
12)давление крови в разных отделах сосудистого русла
Давление крови в различных участках сосудистой системы. Среднее давление в аорте поддерживается на высоком уровне (примерно 100 мм рт. ст.), поскольку сердце непрестанно перекачивает кровь в аорту. С другой стороны, артериальное давление меняется от систолического уровня 120 мм рт. ст. до диастолического уровня 80 мм рт. ст., поскольку сердце перекачивает кровь в аорту периодически, только во время систолы. По мере продвижения крови в большом круге кровообращения среднее давление неуклонно снижается, и в месте впадения полых вен в правое предсердие оно составляет 0 мм рт. ст. Давление в капиллярах большого круга кровообращения снижается от 35 мм рт. ст. в артериальном конце капилляра до 10 мм рт. ст. в венозном конце капилляра. В среднем «функциональное» давление в большинстве капиллярных сетей составляет 17 мм рт. ст. Этого давления достаточно для перехода небольшого количества плазмы через мелкие поры в капиллярной стенке, в то время как питательные вещества легко диффундируют через эти поры к клеткам близлежащих тканей. В правой части рисунке показано изменение давления в различных участках малого (легочного) круга кровообращения. В легочных артериях видны пульсовые изменения давления, как и в аорте, однако уровень давления значительно ниже: систолическое давление в легочной артерии – в среднем 25 мм рт. ст., а диастоли-ческое – 8 мм рт. ст. Таким образом, среднее давление в легочной артерии составляет всего 16 мм рт. ст., а среднее давление в легочных капиллярах равно примерно 7 мм рт. ст. В то же время общий объем крови, проходящий через легкие за минуту, – такой же, как и в большом круге кровообращения. Низкое давление в системе легочных капилляров необходимо для выполнения газообменной функции легких.
Источник: https://meduniver.com/Medical/Physiology/581.html MedUniver
13)артериальное давление
Артериальное давление – один из важнейших параметров, характеризующих работу кровеносной системы. Давление крови определяется объёмом крови, перекачиваемым в единицу времени сердцем и сопротивлением сосудистого русла. Поскольку кровь движется под влиянием градиента давления в сосудах, создаваемого сердцем, то наибольшее давление крови будет на выходе крови из сердца (в левом желудочке), несколько меньшее давление будет в артериях, ещё более низкое в капиллярах, а самое низкое в венах и на входе сердца (в правом предсердии). Давление на выходе из сердца, в аорте и в крупных артериях отличается незначительно (на 5-10 мм рт. ст.), поскольку из-за большого диаметра этих сосудов их гидродинамическое сопротивление невелико. Точно так же незначительно отличается давление в крупных венах и в правом предсердии. Наибольшее падение давления крови происходит в мелких сосудах: артериолах, капиллярах и венулах.
Верхнее число – систолическое артериальное давление, показывает давление в артериях в момент, когда сердце сжимается и выталкивает кровь в артерии, оно зависит от силы сокращения сердца, сопротивления, которое оказывают стенки кровеносных сосудов, и числа сокращений в единицу времени.
Нижнее число – диастолическое артериальное давление, показывает давление в артериях в момент расслабления сердечной мышцы. Это минимальное давление в артериях, оно отражает сопротивление периферических сосудов. По мере продвижения крови по сосудистому руслу амплитуда колебаний давления крови спадает, венозное и капиллярное давление мало зависят от фазы сердечного цикла.
Типичное значение артериального кровяного давления здорового человека (систолическое/диастолическое) = 120 и 80 мм рт. ст., давление в крупных венах на несколько мм. рт. ст. ниже нуля (ниже атмосферного). Разница между систолическим артериальным давлением и диастолическим (пульсовое давление) в норме составляет 30-40 мм рт. ст.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
