Механизм гемостаза в мелких сосудах

Система гемостаза
– это биологическая система, обеспечивающая
сохранение жидкого состояния крови, с
одной стороны, предупреждение и остановка
кровотечений – с другой, путем поддержания
структурной целостности стенок
кровеносных сосудов и достаточно
быстрого тромбирования последних при
повреждениях.
Реализуется
гемостаз в основном тремя, взаимодействующими
между собой функционально-структурными
компонентами: стенками кровеносных
сосудов, клетками крови и плазменными
ферментными системами – свертывающей,
фибринолитической, каликреин-кининовой
и другими. Система подчинена сложной
нейрогуморальной регуляции, в ней четко
функционируют механизмы положительной
и отрицательной обратной связи, вследствие
чего клеточный гемостаз и свертывание
крови вначале подвергаются самоактивации,
а затем нарастает антитромботический
потенциал крови.
Стенки сосудов,
интима которых обладает высокой
тромборезистентностью, прежде всего
поддерживают жидкое состояние крови.
Это свойство эндотелия связано со
следующими его особенностями (Баркаган
З.С., 1980):
– способностью
эндотелия синтезировать и выделять
мощный ингибитор агрегации тромбоцитов
– простациклин;
– продукцией
тканевого активатора фибринолиза;
– созданием
антикоагулянтного потенциала на границе
кровь/ткань, путем синтеза антитромбина
III и фиксации на эндотелии комплекса
гепарин – антитромбин III;
– неспособностью
к контактной активации системы свертывания
крови;
– способностью
удалять из кровотока активированные
факторы свертывания крови.
С другой стороны,
эндотелий синтезирует и вещества,
реализующие гемостатические реакции
следующими путями:
– выделением в
кровь тканевого тромбопластина (фактора
III), а также стимуляторов тромбоцитов –
адреналин, норадреналин, АДФ и др.;
– контактной
активацией коллагеном и другими
компонентами субэндотелия как тромбоцитов
(адгезия), так и свертывания крови
(активация фактора XII);
– продукцией
плазменных кофакторов адгезии и агрегации
тромбоцитов – фактор Виллебранда.
Коллаген запускает и фибринолитическую
систему (З.С. Баркаган, 1980, 1985).
Участие тромбоцитов
в гемостазе обусловлено следующими их
функциями:
– ангиотрофической
– способностью поддерживать нормальную
структуру, резистентность и непроницаемость
для эритроцитов стенок микрососудов.
Клетки эндотелия не способны самостоятельно
впитывать нужные им вещества, однако
эти клетки активно поглощают тромбоциты
со всем, что те успели накопить.
Эндотелиальные клетки, лишенные
тромбоцитарной подкормки, быстро
дистрофируются, становясь повышенно
ломкими, и начинают пропускать через
свою цитоплазму эритроциты;
– адгезивно-агрегационной
функцией – тромбоциты способны прилипать
к поврежденной стенке сосуда и друг к
другу, образовывать тромбоцитарную
пробку, а также транспортировать к месту
повреждения собственные и адсорбированные
факторы гемостаза.
Агрегация тромбоцитов
реализуется рядом стимуляторов:
коллагеном, АДФ, арахидоновой кислотой
и ее производными (тромбоксан), адреналином,
тромбином. Наиболее важным плазменным
кофактором адгезии тромбоцитов к
коллагену является циркулирующий в
крови гликопротеин – фактор Виллебранда.
Тромбоциты накапливают его и выделяют
при “реакции освобождения” (3. С.
Баркаган, 1985);
– способностью
поддерживать спазм поврежденных сосудов
путем секреции вазоактивных веществ –
норадреналина, адреналина, серотонина
и др.;
– участие в
свертывании крови – тромбоциты, являясь
своеобразной губкой, адсорбирующей
многие плазменные компоненты свертывания
крови, активируют свертывание при
освобождении этих компонентов. Однако
есть собственные тромбоцитарные факторы,
участвующие в свертывании крови. Это
третий пластиночный фактор (3 пф),
ускоряющий взаимодействие плазменных
факторов свертывания; антигепариновый
фактор (4 пф), обладающий высокой
антигепариновой активностью, способный
потенцировать агрегацию тромбоцитов
и эритроцитов. Весьма выражено активирующее
влияние тромбоцитов на фибринолиз.
Механизмы
гемостаза.В зависимости от размеров
поврежденного сосуда различают два
механизма гемостаза: сосудисто-тромбоцитарный,
или первичный, и коагуляционный, или
вторичный. В первом случае ведущее
значение в остановке кровотечения
принадлежит сосудистой стенке и
тромбоцитам, во втором – системе
свертывания крови. В процессе остановки
кровотечения оба механизма взаимосвязаны.
Сосудисто-тромбоцитарный
гемостазосуществляется непосредственно
после травмы мелких сосудов: вначале
происходит спазм концевых сосудов в
месте травмы, обусловленный нейрососудистым
рефлексом, дальнейшее сужение сосудов
обеспечивается адреналином, который
рефлекторно выбрасывается в кровь (рис.
4).
Схема тромбоцитарного
гемостаза
Повреждение | |||||||||||||||||
Плазменные | Гемолиз | ||||||||||||||||
Соединительная | Образование | ||||||||||||||||
АДФ | |||||||||||||||||
| | ||||||||||||||||
Фактор Виллебранда | Адгезия | Начальная агрегация | |||||||||||||||
Реакция освобождения | Пластиночные факторы + Плазменные факторы | ||||||||||||||||
АДФ, серотонин | |||||||||||||||||
Са++, | |||||||||||||||||
Агрегация обратимая Агрегация необратимая | |||||||||||||||||
Реакция освобождения | Тромбин (малые | ||||||||||||||||
Нарастание | |||||||||||||||||
Консолидация Армирование | |||||||||||||||||
Рис. 4. Схема
тромбоцитарного гемостаза
В
течение 1-3 с после травмы начинает
формироваться гемостатический
тромбоцитарный тромб: в месте повреждения
сосуда происходит адгезия и агрегация
тромбоцитов, они прилипают к поврежденным
эндотелиальным клеткам, коллагену.
Ведущая роль в первичном запуске
агрегации принадлежит АДФ, поступающему
из поврежденных сосудистой стенки и
эритроцитов (3.С. Баркаган, 1985). Поврежденная
стенка сосуда активирует высвобождение
из тромбоцитов эндогенных факторов
агрегации (АДФ, адреналин, серотонин,
тромбоксан).
Микродозы тромбина
завершают “реакцию освобождения”
внутрипластиночных факторов, консолидацию
и армирование тромба фибрином. Увеличение
времени кровотечения (проба Дьюка)
подтверждает, что первичный гемостаз
осуществляется в основном тромбоцитами,
а не свертыванием крови.
Тромбоцитарный
тромб останавливает кровотечение лишь
в микрососудах с низким артериальным
давлением. В сосудах же более крупных,
с более высоким давлением крови
тромбоцитарный тромб уже не в состоянии
обеспечить надежный гемостаз. В таких
случаях ведущая роль принадлежит
свертывающей системе крови, коагуляционному
гемостазу.
Свертывание
крови –многоэтапный каскадный
ферментный процесс, в котором
последовательно активируются проферменты
и действуют силы аутокатализа,
функционирующие как сверху вниз, так и
по механизму обратной связи (3.С. Баркаган,
1985).
Факторы свертывания:
I- фибриноген; II – протромбин;
III – тромбопластин; IV – ионы кальция; V –
проакцелерин; VI – акцелерин; VII-проконвертин;
VIII – антигемофильный глобулин;IX- компонент тромбопластина плазмы; Х –
фактор Проуэра-Стюарта;XI- предшественник тромбопластина плазмы;
ХII – фактор контакта (фактор Хагемана);
ХIII – фибринстабилизирующий фактор.
В свертывающей
системе различают внутренний и внешний
механизмы, активирующие запуск гемостаза.
Для первого из них (внутреннего) необходим
контакт белков плазмы с коллагеном и
другими субэндотелиальными структурами,
при этом активируется контактный фактор
(фактор XII) с последующим
запуском свертывания крови по внутреннему
механизму. Для второго (внешнего)
необходимо поступление из стенки сосуда
и тканей в кровь тканевого тромбопластина
(факторIII), который в
комплексе с факторомVIIобразует активаторX. Оба
механизма необходимы для нормального
гемостаза.
В коагуляционном
гемостазевыделяют четыре последовательные
фазы:I- формирование
активной протромбиназы;II-образование
тромбина;III- образование
фибрина иIV- послефаза,
представленная процессами ретракции
и фибринолиза (рис. 5).
Взаимодействие
между ферментными и неферментными
факторами происходит в сложных
белково-липидных комплексах, которые
образуются на разных ступенях
коагуляционного каскада. В активации
начальных этапов свертывания крови
участвует калликреин-кининовая система.
При внутреннем
механизме активации протромбиназы в
контакте с коллагеном или какой-либо
другой чужеродной поверхностью
активируется фактор XII,
который через калликреин-кининовую
систему вступает во взаимодействие сXIфактором и превращает
его в активную форму. Эта начальная
“контактная” фаза ускоряется
фосфолипидным фактором тромбоцитов (3
пф) и не требует ионов кальция (факторIV). Все последующие фазы
коагуляционного каскада начиная с
активации фактораIXнуждаются в ионизированном кальции.
В первом комплексе
факторов внутреннего механизма “Xlla+XI+
3 пф” активируется факторIX;
в комплексе “факторIXa+VIIICa+++
З пф”- факторX; в комплексе
“фактор Ха+факторV+Ca+++
3 пф”- фактор У, последний комплекс
действует энзиматически на протромбин,
превращая его в тромбин (протромбиновый
комплекс, протромбиназа).
Р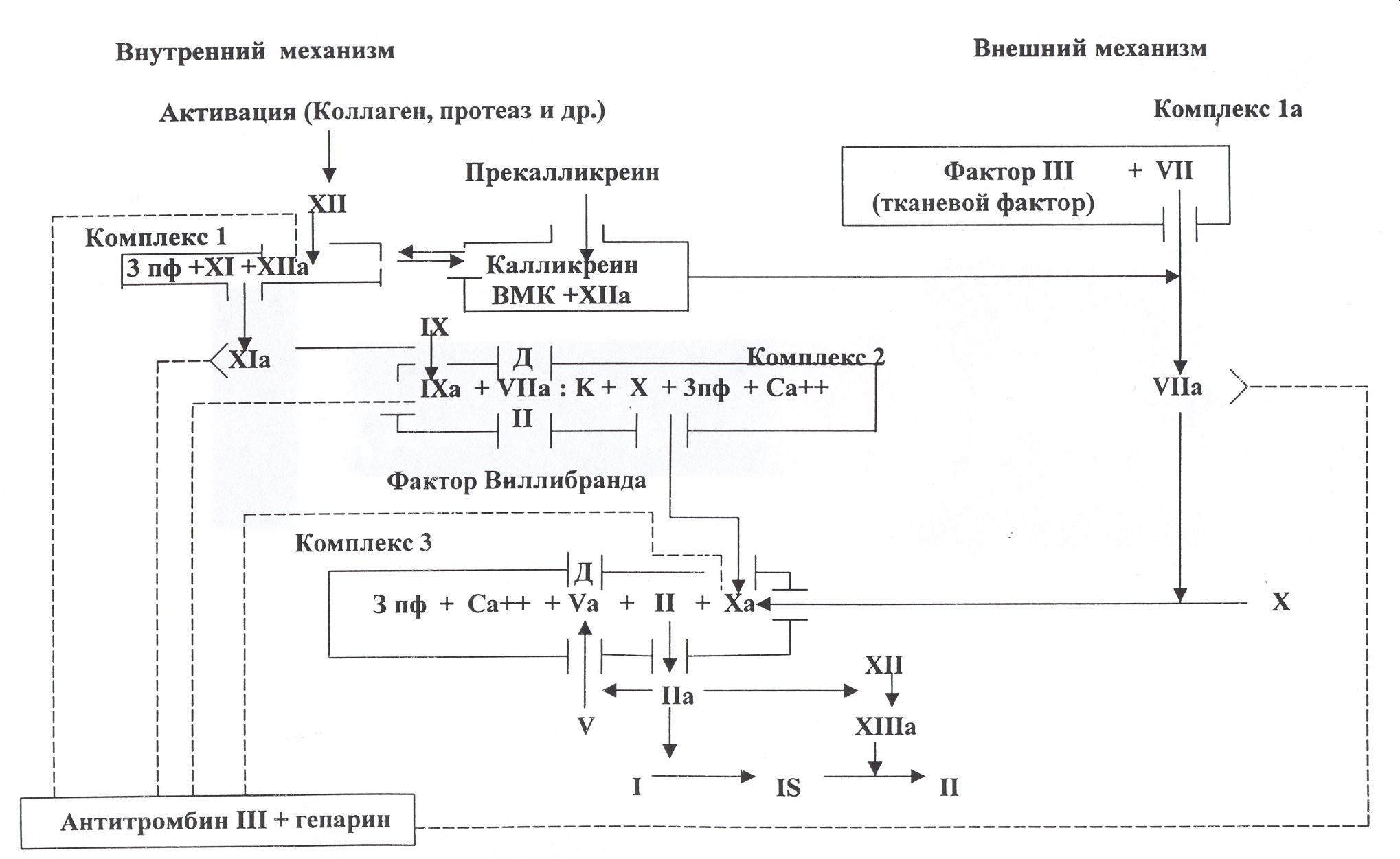 ис.
ис.
5. Каскадно-комплексная (матричная)
схема свертывания.
Во внешнем механизме
формирования протромбиназной активности
образуется комплекс факторов “III+VII+Ca++”,
направленный на активацию фактораX.
Далее процесс свертывания переходит
во вторую фазу – фазу превращения
протромбина в тромбин. В третьей фазе
тромбин отщепляет фибринопептиды А и
В от молекул фибриногена, превращая их
в фибринмономеры, которые спонтанно
полимеризуются в волокна фибрина.
Тромбин активирует факторXIII,
который укрепляет фибрин-полимеры
(фибринстабилизирующий фактор), переводит
растворимый фибринS (solubile)
в нерастворимый фибринJ(insolubile). В сгустке фибрина
задерживаются форменные элементы крови
– эритроциты, лейкоциты, тромбоциты,
последние вызывают уплотнение и ретракцию
сгустка.
Фибринолиз.Свертывающая система крови функционально
взаимосвязана с фибринолитической,
кининовой и системой комплемента.
Фибринолитическая система, обеспечивающая
лизис фибрина в кровяном русле, запускается
теми же факторами, что и свертывание
крови. ФакторXIIа
взаимодействует с прекалликреином и
высокомолекулярным кининогеном плазмы
(ВМК) и активирует плазминоген. Фибринолиз
идет тем быстрее, чем выше локальная
концентрация плазминогена в сгустках.
Кроме ферментной фибринолитической
системы, в организме происходит
неферментативный фибринолиз, осуществляемый
комплексом гепарин-антитромбинIII-адреналин и функционирующий
в физиологических условиях (Б. А. Кудряшов,
1977).
Ингибиторы
свертывания крови.Существенная
сторона гемостаза – ингибирование
процесса свертывания крови. Ингибиторы
сохраняют жидкое состояние крови в
циркуляции, препятствуют переходу
локального тромбообразования в
распространенное (В.А. Кудряшов, 1975).
Известны две группы
естественных ингибиторов свертывания
крови:
– первичные,
предшествующие свертыванию крови
(антитромбин III, протеин С, 2-макроглобулин);
– вторичные,
образующиеся в процессе свертывания
крови, группа протеолиза (3.С. Баркаган,
К.М. Бишевский, 1978).
Антитромбин IIIявляется наиболее мощным ингибитором
свертывания, действующим не только как
антитромбин, но и как инактиватор
факторов Ха, 1Ха, ХIа, ХIIа,VIIa,V. На
антитромбинIIIи его
кофактор – гепарин приходится 4/5
физиологической антикоагулянтной
активности.
Протеин С –
синтезируемый гепатоцитами,
К-витаминзависимый профермент,
активирующийся тромбином и фактором
Ха, расщепляет и инактивирует основные
неферментные факторы VIIIиV.
2-макроглобулин
– белок, обладающий способностью связывать
активированные компоненты свертывающей
системы крови и фибринолиза, выключать
их из взаимодействия с другими факторами.
Типы и тяжесть
кровоточивости, установленные
во время обследования, облегчают
диагностический поиск. Различают 5
основных типов кровоточивости:
I.
Гематомный с
болезненными, напряженными кровоизлияниями
как в мягкие ткани, так и в суставы,
выраженной патологией опорно-двигательного
аппарата. Типично для гемофилии А и Б.
2.
Петехиально-пятнистый
(синячковый) характерен
для тромбоцитопений, тромбоцитопатий,
редко встречающихся наследственных
дефицитов факторов Х и П, иногда УП.
3.
Смешанный
синячково-гематомный
характеризуется сочетанием
петехиально-пятнистой кровоточивости
с появлением отдельных больших гематом
(забрюшинных, в стенку кишечника и т.д.)
при отсутствии поражений суставов и
костей, либо с единичными геморрагиями
в суставы: синяки могут быть обширными
и болезненными. Такой тип кровоточивости
наблюдается при тяжелом дефиците
факторов протромбинового комплекса и
фактора УШ, болезни Виллебранда,
ДВС-синдрома, передозировке антикоагулянтов
и тромболитиков, при появлении в крови
иммунных ингибиторов факторов VIII и IX.
4.
Васкулитно-пурпурный
тип характеризуется геморрагиями в
виде сыпи или эритемы (на воспалительной
основе), возможно присоединение нефрита
и кишечных кровотечений; наблюдается
при инфекционных и иммунных васкулитах,
легко трансформируется в ДВС-синдром.
5.
Ангиоматозный тип наблюдается при
телеангиоэктазиях, ангиомах,
артерио-венозных шунтах, характеризуется
упорными, строго локализованными и
привязанными к локальной сосудистой
патологии геморрагиями.
При
распознавании геморрагий важно учитывать,
что одни виды патологии часты, другие
редки, а третьи крайне редки. Из
наследственных нарушений гемостаза
наиболее часты тромбоцитопатии (в
совокупности), гемофилия А, а из сосудистых
форм телеангиоэктазия. На долю этих
заболеваний приходитсяболее
99% всех генетически обусловленных форм
кровоточивости. Петехиально-пятнистый
тип встречается чаще всего. Он наблюдается
при тромбоцитопениях, тромбоцитопатиях,
а также при некоторых редких наследственных
нарушениях внешнего механизма свертывания
(дефицит X,
VII, II факторов).
Определение
типа кровоточивости дает направленность
лабораторных исследований.
Тесты
для характеристики сосудисто-тромбоцитарного
звена гемостаза:
– резистентность
сосудистой стенки;
– число тромбоцитов
150 000-400 000 /мкл;
– длительность
кровотечения (по Дюке 2-4 мин, Айви 8 мин);
– адгезивно-агрегационные
тесты.
Тесты
для характеристики плазменно-коагуляционного
звена гемостаза:
– время свертывания
венозной крови по Ли-Уайту 5-8 мин;
– время рекальцификации
плазмы 60-120 сек;
– протромбиновое
время (протромбиновый индекс) 11-15 сек;
– тромбиновое время
15-20 сек;
– уровень фибриногена
2-4 г/л;
– тест
растворимости фибринового сгустка в
мочевине (активность фактора XIII) 45 сек.
Таким
образом, исследование системы гемостаза
необходимо для установления причин
кровоточивости и дифференциации
различных форм врожденных и приобретенных
коагулопатий, тромбоцитопений и
тромбоцитопатий.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
Гемостаз (haemostasis; греч. haima кровь + stasis стояние) — эволюционно сложившаяся защитная реакция организма, выражающаяся в остановке кровотечения при повреждении стенки сосуда.
Гемостаз в патологии — прекращение движения крови в кровеносном сосуде (см. Стаз, Тромбоз). В хирургии термин «гемостаз» часто употребляется в смысле остановки кровотечения (см.). Система Гемостаза как нормальной защитной реакции организма — совокупность кровяных (плазменных и клеточных) и сосудистых компонентов, обеспечивающих быструю остановку кровотечения при повреждении сосудов.
Первое описание Гемостаза дал Цан (F. W. Zahn, 1882), который наблюдал формирование тромба на раневой поверхности мезентериальных сосудов лягушки. Установлено, что образование тромба обусловлено адгезией (прилипанием) тромбоцитов к травмированному участку сосуда. Комплекс морфологических изменений тромбоцитов в процессе Г., обозначенный термином «вязкий метаморфоз», описали Эберт (G. G. Eberth) и К. Шиммельбуш. С введением метода определения времени кровотечения (см.) стало возможным изучение Г. не только в эксперименте, но и в клинике. Гипотеза Роскама (J. Roskam) о сосудисто-кровяном патогенезе нарушения Г. при ряде патол, состояний организма стимулировала исследования по выяснению роли сосудистой стенки в механизме Г. [Магнус, Бернут (G. Magnus, F. Bernuth) и др. ]. Фундаментальным вкладом в учение о Г. явились работы А. А. Шмидта — основоположника ферментативной теории процесса свертывания крови. В дальнейшем эта теория была развита в трудах Е. С. Иваницкого-Василенко, Б. А. Кудряшова, А. А. Маркосяна.
Методом электронной микроскопии установлено, что сразу после повреждения сосуда к внутренней поверхности травмированного участка прикрепляются тромбоциты, часть из них образует агрегаты. Почти все тромбоциты приобретают сфероидную форму с 1—6 псевдоподиями. Через 30 сек. большинство тромбоцитов, фиксированных у раневой поверхности, находится в состоянии агрегации (прилипание друг к другу), в них преобладают электронноплотные гранулы. Отчетливо идентифицируются мембраны тромбоцитов; обнаруживаются дегранулированные тромбоциты. Наряду с изменившимися встречаются интактные тромбоциты с сохранившимися митохондриями. В участках тромбоцитарного агрегата видны фибриновые волокна. Через 1 мин. после травмы агрегаты тромбоцитов на раневой поверхности сосуда представляют или хаотически склеившуюся массу дегранулированных и гранулсодержащих тромбоцитов, или имеют форму розетки: центрально расположенные гранулсодержащие тромбоциты окружены дегранулированными тромбоцитами. По периферии тромбоцитарной розетки расположены эритроциты; между эритроцитами — фибриновые волокна. Через 7 мин. дегранулированные пластинки в агрегате увеличены в размерах, их форма многообразна. В местах соприкосновения тромбоцитов мембраны их не различаются. Фибриновые волокна, утолщенные и удлиненные, расположены между тромбоцитами.
В сети фибрина расположены эритроциты. Спустя 15 мин. у места повреждения сосуда обнаруживают фибриновые волокна, переплетающиеся с «обломками» тромбоцитов.
В некоторых случаях в гемостатическом тромбе видны только фибриновые волокна.
Физиология
В процессе Гемостаза принимают участие экстраваскулярная ткань, стенка сосуда, плазменные факторы свертывания крови, тромбоциты и другие форменные элементы крови. Важная роль в Г. принадлежит физиологически активным веществам (адреналин, норадреналин, серотонин и др.), местным изменениям ионных отношений, pH крови, дзета-потенциалу (разности потенциалов между дисперсной фазой и дисперсной средой, тромбоцитами и сосудистой стенкой).
Различные ткани, окружающие травмированный сосуд, имеют неодинаковую тромбопластическую активность; биол, значение этих различий для местного Г. еще не ясно. В результате взаимодействия тканевых и плазменных факторов свертывающей системы крови у места повреждения стенки сосуда образуется активный тканевой тромбопластин, включающийся в цепь последующих реакций, конечным продуктом которых является фибрин. Однако тканевой тромбопластин (менее активный, чем кровяной) имеет, вероятно, меньшее значение в Г. при ранении крупных сосудов. Окружающие сосуд ткани оказывают также и механическое сопротивление выходу крови из поврежденного сосуда, влияя, т. о., на величину кровопотери.
Роль стенки сосуда в Г. обусловлена наличием в ней ряда факторов, оказывающих влияние на процесс свертывания крови, адгезию и агрегацию тромбоцитов; при травме стенка сосуда сокращается и приток крови к раневому участку уменьшается. Стенка сосуда является эфферентным регулятором скорости свертывания крови и фибринолиза (см.). Интима сосудов заряжена отрицательно по отношению к адвентиции. При повреждении сосудов происходит реверсия потенциала и интима становится положительно заряженной, изменяется дзета-потенциал, что имеет значение для взаимодействия тромбоцитов с раневой поверхностью.
Плазменные факторы свертывания крови в организме здорового человека находятся в неактивном состоянии. Международный комитет по факторам свертывания крови ввел обозначение плазменных прокоагулянтов римскими цифрами; количество их тринадцать (с I по XIII).
Плазменные факторы свертывания крови
Фактор I — фибриноген
Фактор II — протромбин
Фактор III — тромбопластин
Фактор IV — кальций
Фактор V — ускоритель (акцелератор) превращения протромбина (Ас-глобулин)
Фактор VI — изъят из классификации Фактор VII — проконвертин Фактор VIII — антигемофильный глобулин
Фактор IX — плазменный компонент тромбопластина (Кристмас-фактор)
Фактор X — фактор Стюарта — Прауер
Фактор XI — плазменный предшественник тромбопластина Фактор XII — фактор контакта (Хагемана)
Фактор XIII — фибринстабилизирующий фактор, фибриназа
Активация системы свертывания крови происходит при соприкосновении с чужеродной поверхностью, что является пусковым механизмом внутренней системы Гемостаза (активные факторы свертывания крови обозначают добавлением к соответствующей римской цифре буквы «а»). Завершается Г. образованием тромба у места повреждения стенки сосуда.
Участие тромбоцитов в Г. обусловлено такими их свойствами, как адгезия и агрегация, содержанием в них собственных и адсорбированных факторов свертывания крови, а также физиологически активных веществ.
Роль эритроцитов и лейкоцитов в Г. обусловлена содержанием в них большинства факторов свертывания крови. При повреждении стенки сосудов эти факторы включаются в реакцию фибринообразования. В процессе Г. эритроциты задерживаются в фибриновой сети, способствуя образованию кровяного сгустка и увеличению его массы.
Процесс Гемостаза имеет нейрогуморальную регуляцию: экстремальные факторы, вызывая повышение тонуса симпатического отдела в. н. с., увеличивают поступление в кровь адреналина и норадреналина, что ускоряет адгезию и агрегацию тромбоцитов и активирует процесс свертывания крови в целом. Распространение процесса тромбообразования по сосудистому руслу предотвращается циркулирующими в крови антикоагулянта-ми, фибринолитическими агентами и ингибиторами адгезии и агрегации тромбоцитов — аденозином и аденозинмонофосфатом, которые образуются при распаде АДФ.
В зависимости от размеров поврежденного сосуда и роли отдельных факторов в ограничении кровопотери различают два основных механизма Г.: сосудисто-тромбоцитарный (или микроциркуляторный) и коагуляционный. В первом ведущую роль в остановке кровотечения отводят сосудистой стенке и тромбоцитам (см.), во втором — системе свертывания крови (см. Свертывающая система крови). Помимо этого, может возникнуть ДВС-синдром (диссеминированное внутрисосудистое свертывание крови).
Схема 1. Сосудисто-тромбоцитарный механизм гемостаза.
Сосудисто-тромбоцитарный механизм (схема 1) имеет место при остановке кровотечения из мелких сосудов: артериол, прекапилляров, капилляров и венул. Он складывается из следующих этапов: 1) кратковременный спазм сосудов, 2) адгезия тромбоцитов к раневой поверхности, 3) аккумуляция и агрегация тромбоцитов у места повреждения, 4) вязкий метаморфоз и реакция освобождения тромбоцитов, 5) вторичный спазм сосудов, 6) образование фибрина и физиол, гемостатического тромба (см.).
Под влиянием травмы повышается тонус симпатического отдела в. н. с. и происходит местный спазм сосудов, уменьшающий приток крови. Сужению сосудов способствует также и рефлекторное выбрасывание в кровоток адреналина и освобождение холинэстеразы, блокирующей ацетилхолин. Тромбоциты прилипают к поврежденным эндотелиальным клеткам и тканевым волокнам сосудистой стенки на раневой поверхности: начинается формирование гемостатического тромбоцитарного тромба.
Основными структурами сосудистой стенки, с к-рыми взаимодействуют тромбоциты, являются коллагеновые волокна, микрофибриллы и базальная мембрана. Адгезия тромбоцитов к коллагеновым волокнам не связана, по-видимому, с процессом свертывания крови, т. к. при полной несвертываемости крови (напр., в результате гепаринизации) она не нарушается. Тромбин не вызывает адгезии тромбоцитов, а усиливает ее, способствуя выделению из тромбоцитов АДФ. В механизме взаимодействия тромбоцитов с поврежденной стенкой сосуда в процессе Г. имеют, вероятно, значение электростатические силы, усиливающие прилипание тромбоцитов к раневой поверхности. Замедление кровотока и движение крови способствуют взаимодействию тромбоцитов с поврежденной стенкой сосудов.
Вслед за адгезией наступает агрегация тромбоцитов у места ранения стенки сосуда. Из поврежденных эндотелиальных клеток, а также из эритроцитов и тромбоцитов выделяется АТФ, к-рая под действием клеточной аденозинтрифосфатазы превращается в АДФ. Под влиянием последней происходит агрегация тромбоцитов (обратимая); действие АДФ на тромбоциты проявляется при наличии в среде ионов кальция и плазменного кофактора — фактора Виллебранда, фактора XIII (фибринстабилизирующего фактора) или фактора I (фибриногена). Для объяснения механизма агрегации тромбоцитов предложен ряд гипотез; наибольшее признание получила гипотеза Гаардера и Лаланда (A. Gaarder, J. Laland), которые считают, что тромбоцитагрегирующая активность АДФ обусловлена тремя свободными отрицательными валентностями: две валентности связывают один ион кальция, а третья — вместе с такой же валентностью соседней молекулы АДФ — присоединяет еще один ион кальция; агрегация тромбоцитов происходит в результате образования кальциевых «мостиков» между тромбоцитарно-нуклеотидными комплексами.
Тромбоциты, агрегирующие у раневой поверхности, подвергаются вязкому метаморфозу под влиянием тромбина. В процессе вязкого метаморфоза из тромбоцитов освобождаются факторы свертывания крови, серотонин, гистамин, адреналин, кинины, нуклеотиды, энзимы; агрегация тромбоцитов Становится необратимой. Выделение из тромбоцитов указанных факторов способствует вторичному сужению поврежденного сосуда. Параллельно идет реакция фибринообразования. Фибриновые волокна и последующая ретракция кровяного сгустка уплотняют гемостатический тромб, что приводит к окончательной остановке кровотечения.

Схема 2. Коагуляционный механизм гемостаза.
Коагуляционный механизм (схема 2) имеет место при травме крупных артерий и вен вслед за ограничением кровопотери в результате спазма сосудов, в особенности мышечного типа. Однако и в этом случае к месту повреждения стенки сосуда в первую очередь прикрепляются тромбоциты. Одновременно активируется система свертывания крови в результате сложного взаимодействия плазменных и клеточных прокоагулянтов, протекающего по типу проферментно-ферментного каскадного преобразования, и образуется фибрин. В фибриновую сеть вовлекаются форменные элементы крови, формируется кровяной сгусток, который уменьшает или полностью предотвращает кровопотери). Конечным этапом является ретракция кровяного сгустка, к-рая длится несколько часов. В результате ретракции гемостатический тромб становится более надежным. При этом из сгустка выделяется сыворотка, богатая тромбином.
Диссеминированное внутрисосудистоe свертывание крови (ДВС) — синдром, который может возникнуть при различных патологических состояниях (остром гемолизе, инфекционных процессах, интоксикациях, реакции антиген — антитело и др.). В его развитии принимают участие как сосудисто-тромбоцитарный, так и коагуляционный факторы.
Нарушение гемостаза в связи с дефектностью отдельных компонентов его системы — см. табл.
Методы исследования
Состояние Г. выявляют по показателям коагулограммы (см.), а также на основании тестов, определяющих: состояние резистентности стенки сосудов, время кровотечения (см.), как первичного, так и вторичного, объем теряемой крови, толерантность к аспирину, прочность ранней фиксации тромбоцитарных пробок в сосудах, количество Тромбоцитов, их функциональную активность (способность к адгезии in vitro и in vivo, АДФ-, коллаген- и тромбин-агрегации).
Принцип восстановления гемостаза состоит в укреплении стенки сосуда, повышении адгезивной и агрегационной способности тромбоцитов, восстановлении утраченной или сниженной способности крови к свертыванию.
Основным принципом медикаментозного способа остановки кровотечения является дифференцированное применение гемостатических средств с учетом механизма развития кровоточивости. Поэтому, прежде чем начинать антигеморрагическую терапию, необходимо провести тщательное лабораторное исследование функционального состояния свертывающей системы крови с целью выявления основной причины нарушения гемостаза.
КЛАССИФИКАЦИЯ НАРУШЕНИЙ ГЕМОСТАЗА
Механизм гемостаза | Локализация травмы | Нарушения гемостаза | Механизмы нарушения гемостаза |
Сосудисто-тромбоцитарный | Артериолы, капилляры, венулы | Нарушение образования тромбоцитарного тромба | 1. Сосудистый (изменение основного 2. Тромбоцитарный (уменьшение 3. Сосудистый и тромбоцитарный |
Коагуляционный | Крупные вены и артерии | Нарушение процесса формирования гемостатического | Система гемостаза функционирует нормально, но у места |
Нарушение процесса фибринообразования | Кровяной (снижение содержания одного или нескольких прокоагулянтов, | ||
Лизис тромба | Кровяной (в сосудистое русло поступает большое количество | ||
Диссеминированное внутрисосудистое свертывание крови | Сосуды малого и большого круга кровообращения | Первичное локальное внутрисосудистое свертывание крови, | Кровяной, тромбоцитарный и сосудистый (активация |
Агрегация тромбоцитов, стаз крови, вторичное поражение | Тромбоцитарный, кровяной и сосудистый (индуцирование | ||
Первичное тотальное внутрисосудистое свертывание | 1. Кровяной (потребление факторов 2. Тромбоцитарный (уменьшение |
Библиография: Балуда В. П. и Сушкевич Г. Н. Роль тромбоцитов в гемостазе и поддержании резистентности стенки сосудов в норме и при патологий, Пробл, гематол. и перелив, крови, т. 16,. № 5, с. 28, 1971, библиогр.; Гусейнов Ч. С. Физиология и патология тромбоцитов, М., 1971, библиогр.; Коблов Л. Ф. Методы и приборы для исследования гемостаза, М., 1975, библиогр.; Кудряшов Б. И. Биологические проблемы регуляции жидкого состояния крови и ее свертывания, М., 1975, библиогр.; Кузник Б.И. и Скипетров В. П. Форменные элементы крови, сосудистая стенка, гемостаз и тромбоз, М., 1974, библиогр.; Маркосян А. А. Физиология тромбоцитов, Л., 1970, библиогр.; Воrn G. Y. Aggregation of blood platelets by adenosine diphosphate and its reversal, Nature (Lond.), v. 194, p. 927, 1962; Gaarder A. a. Laland S. Hypothesis for the aggregation of platelets by nucleotides, ibid., v. 202, p. 909, 1964; H&mostaseologische Untersuchungen, hrsg. v. J. Rex u. G. Bach, B., 1974; HellemA. a. OwrenP. A. The mechanism of hemostatic function of blood platelets, Acta haemat. (Basel), v. 31, p. 230, 1964; Human blood coagulation, haemostasis and thrombosis, ed. by R. Biggs, Oxford, 1972; Johnson S. A. a. o. The function of platelets, Transfusion (Philad.), v. 6, p. 3, 1966, bibliogr.; Liischer E. F. Platelets in haemostasis and thrombosis, Brit. J. Haemat., v. 13, p. 1, 1967; Ratnoff O. D. Some recent advances in the study of hemostasis, Circulat. Res., v. 35, p. 1, 1974, bibliogr.; Willis A. L. a. o. An endoperoxide aggregator (LASS) formed in platelets in response to thrombotic stimuli, Prostaglandins, v. 8, p. 453, 1974.
В. П. Балуда, Г. H. Сушкевич.
Источник
