Найти объем сосуда в котором находится газ
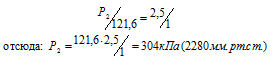
19 ноября 2011
Автор
КакПросто!
Газ, как и вещества, находящиеся в других агрегатных состояниях, имеет ряд параметров, в число которых входит и объем. Объем газа находится на основании других его характеристик, которые приведены в условии задачи. Любой газ, независимо от вида и состава, имеет объем, который и требуется найти во многих задачах.
Инструкция
Газ, независимо от его состава, имеет три основных параметра: массу, объем и плотность. В большинстве задач оперируют так называемым идеальным газом, поэтому опираться в них необходимо лишь на приведенные в условии значения массы, давления, температуры. Например, в условии задачи может быть указан газ азот N2 с температурой в 60 градусов, давлением в 30 кПа и массой в 0,05 г. Зная эти три параметра и состав газа, по уравнению Менделеева-Клапейрона можно найти его объем. Для этого необходимо переделать данное уравнение следующим образом:
pV=mRT/M.
Осуществив дальнейшее преобразование формулы, найдите объем азота:
V =mRT/pM.
При этом молярную массу M можно найти по таблице Д.И. Менделеева. У азота она равна 12 г/моль. Тогда:
V=0,05*12*8,31*333/30*12≈4,61.
Если известны объем при нормальных условиях, а объем при других условиях является искомым, примените законы Бойля-Мариотта и Гей-Люссака:
pV/T=pнVн/Tн.
В таком случае преобразуйте формулу следующим образом:
pV*Tн=pнVн*T.
Отсюда объем V равен:
V=pнVн*T/p*Tн.
Индекс н означает величину того или иного параметра при нормальных условиях.
Если рассматривать объем газа с точки зрения термодинамики, можно заметить, что на газы могут действовать силы, за счет которых меняется объем. При этом давление газа постоянно, что характерно для изобарных процессов. В ходе таких процессов объем изменяется с одной величины на другую. Их можно обозначить как V1 и V2. В условиях ряда задач описывается некоторый газ, находящийся под поршнем в сосуде. При расширении этого газа поршень передвигается на некоторое расстояние dl, в результате чего осуществляется работа:
A=pdV=p(V2 -V1).
Эта формула связывает изменение объема газа и работу. Как известно, если дан конечный объем V2, то можно найти начальный объем V1:
V1=pV2-A/p.
Наконец, наиболее просто найти объем газа, исходя из двух других физических параметров – массы и плотности. Если в условиях задан газ с некоторой плотностью и массой, то его объем следует вычислять по формуле:
V=m/ρ.
У каждого газа имеется определенная плотность, как и у любого твердого или жидкого вещества. Поэтому, находя объем газа, в первую очередь необходимо учитывать именно этот параметр.
Войти на сайт
или
Забыли пароль?
Еще не зарегистрированы?
This site is protected by reCAPTCHA and the Google
Privacy Policy and
Terms of Service apply.
Источник
Алеkсей 8 лет назад тэги: газ, объем, химия категория: наука и техника ответить комментировать в избранное бонус 2 ответа: старые выше новые выше по рейтингу 1 alexm12 8 лет назад Очень просто! Измеряем объем сосуда, в который хотим поместить газ. Закачиваем туда газ. Вуаля! Теперь мы знаем объем газа, ибо, по определению, газ всегда занимает весь объем сосуда в который оный газ помещен. комментировать в избранное ссылка отблагодарить Katar 8 лет назад Объём газа, заключённого в сосуд, определяют произведением объёма сосуда на давление в нём (в атмосферах), измеренное манометром. комментировать в избранное ссылка отблагодарить Знаете ответ? 0 | Смотрите также: Может ли давление газа в цилиндре при его сжатии в пять раз не измениться? Можно ли сказать объем газа в сосуде равен сумме объемов его молекул? Газ изобарно расширился. Насколько увеличился объем газа? Как вычислить массу соли и объем газа в результате реакции Al (см)? Как рассчитать объем аквариума? Как уменьшить бёдра? Как измерить объём слона? Купила флешку на 8 Гб, почему реальный объем оказался меньше? Как при помощи макияжа визуально увеличить губы? Почему бензин продают в литрах? |
Источник
Задача 28.
При 17°С некоторое количество газа занимает объем 580 мл. Какой объем займет это же количество газа при 100°С, если давление его останется неизменным?
Решение:
По закону Гей – Люссака при постоянном давлении объём газа изменяется прямо пропорционально абсолютной температуре (Т):
V2 – искомый объём газа;
T2 – соответствующая V2 температура;
V1 – начальный объём газа при соответствующей температуре Т1.
По условию задачи V1 = 580мл; Т1 = 290К (273 + 17 = 290) и Т2 = 373К (273 + 100 = 373). Подставляя эти значения в выражение закона Гей – Люссака, получим:
Ответ: V2 = 746мл.
Задача 29.
Давление газа, занимающего объем 2,5л, равно 121,6 кПа (912мм рт. ст.). Чему будет равно давление, если, не изменяя температуры, сжать газ до объема в 1л?
Решение:
Согласно закону Бойля – Мариотта, при постоянной температуре давление, производимое данной массой газа, обратно пропорционально объёму газа:
Обозначив искомое давление газа через Р2, можно записать:
Ответ: Р2 = 304кПа (2280мм.рт.ст.).
Задача 30. На сколько градусов надо нагреть газ, находящийся в закрытом сосуде при 0 °С, чтобы давление его увеличилось вдвое?
Решение:
При постоянном объёме давление газа изменяется прямо пропорционально температуре:
По условию задачи Т1 = 0 °С + 273 = 273К; давление возросло в два раза: Р2 = 2Р1.
Подставляя эти значения в уравнение, находим:
Ответ: Газ нужно нагреть на 2730С.
Задача 31.
При 27°С и давлении 720 мм.рт. ст. объем газа равен 5л. Кой объем займет это же количество газа при 39°С и давлении 104кПа?
Решение:
Зависимость между объёмом газа, давлением и температурой выражается общим уравнением, объединяющим законы Гей-Люссака и Бойля-Мариотта:
где Р и V – давление и объём газа при температуре Т; Р0 и V0 – давление и объём газа при нормальных условиях. Данные задачи: V = 5л; Т = 298К (273 + 25 = 298); Р = 720 мм.рт.ст. (5,99 кПа); Р0 = 104 кПа; Т = 312К (273 + 39 = 312); Т = 273К. Подставляя данные задачи в уравнение, получим:
Ответ: V0 = 4,8л
Задача 32.
При 7°С давление газа в закрытом сосуде равно 96,0 кПа. Каким станет давление, если охладить сосуд до —33 °С?
Решение:
При постоянном объёме давление газа изменяется прямо пропорционально абсолютной температуре:
Обозначим искомое давление через Р2, а соответствующую ему температуру через Т2. По условию задачи Р1 = 96,0 кПа; Т1 = 280К (273 + 7 = 280); Т2 = 240К (273 – 33 = 240). Подставляя эти значения в уравнение, получим:
Ответ: Р2 = 82,3кПа.
Задача 33.
При нормальных условиях 1г воздуха занимает объем 773 мл. Какой объем займет та же масса воздуха при 0 °С и )и давлении, равном 93,3 кПа (700мм. рт. ст.)?
Решение:
Зависимость между объёмом газа, давлением и температурой выражается общим уравнением, объединяющим законы Гей-Люссака и Бойля-Мариотта:
где Р и V – давление и объём газа при температуре Т; Р0 и V0 – давление и объём газа при нормальных условиях. Данные задачи: Р0 = 101,325кПа; V0 = 773мл; Т0 = 298К (273 + 25 = 298); Т = 273К; Р = 93,3кПа. Подставляя данные задачи и преобразуя уравнение, получим:
Ответ: V = 769, 07 мл.
Задача 34.
Давление газа в закрытом сосуде при 12°С равно 100 кПа (750мм рт. ст.). Каким станет давление газа, если нагреть сосуд до 30°С?
Решение:
При постоянном объёме давление газа изменяется прямо пропорционально абсолютной температуре:
Обозначим искомое давление через Р2, а соответствующую ему температуру через Т2. По условию задачи Р1 = 100 кПа; Т1 = 285К (273 + 12 = 285); Т2 = 303К (273 + 30 = 303). Подставляя эти значения в уравнение, получим:
Ответ: Р2 = 106,3кПа.
Задача 35.
В стальном баллоне вместимостью 12л находится при 0°С кислород под давлением 15,2 МПа. Какой объем кислорода, находящегося при нормальных условиях можно получить из такого баллона?
Решение:
Зависимость между объёмом газа, давлением и температурой выражается общим уравнением, объединяющим законы Гей-Люссака и Бойля-Мариотта:
где Р и V – давление и объём газа при температуре Т; Р0 и V0 – давление и объём газа при нормальных условиях. Данные задачи: V = 12л; Т = 273К (273 + 0 = 2273); Р =15,2МПа); Р0 = 101,325кПа; Т0 = 298К (273 + 25 = 298). Подставляя данные задачи в уравнение, получим:
Ответ: V0 = 1,97м3.
Задача 36.
Температура азота, находящегося в стальном баллоне под давлением 12,5 МПа, равна 17°С. Предельное давление для баллона 20,3МПа. При какой температуре давление азота достигнет предельного значения?
Решение:
При постоянном объёме давление газа изменяется прямо пропорционально абсолютной температуре:
Обозначим искомое давление через Р2, а соответствующую ему температуру через Т2. По условию задачи Р1 = 12,5МПа; Т1 = 290К (273 + 17 = 290); Р2 = 20,3МПа. Подставляя эти значения в уравнение, получим:
Ответ: Т2 = 1980С.
Задача 37.
При давлении 98,7кПа и температуре 91°С некоторое количество газа занимает объем 680 мл. Найти объем газа при нормальных условиях.
Решение:
Зависимость между объёмом газа, давлением и температурой выражается общим уравнением, объединяющим законы Гей-Люссака и Бойля-Мариотта:
где Р и V – давление и объём газа при температуре Т; Р0 и V0 – давление и объём газа при нормальных условиях. Данные задачи: Р0 = 101,325кПа; V = 680мл; Т0 = 298К (273 + 25 = 298); Т = 364К (273 + 91 = 364); Р = 98,7кПа. Подставляя данные задачи и преобразуя уравнение, получим:
<
Ответ: V0 = 542,3мл.
Задача 38.
При взаимодействии 1,28г металла с водой выделилось 380 мл водорода, измеренного при 21°С и давлении 104,5кПа (784мм рт. ст.). Найти эквивалентную массу металла.
Решение:
Находим объём выделившегося водорода при нормальных условиях, используя уравнение:
где Р и V – давление и объём газа при температуре Т = 294К (273 +21 = 294); Р0 = 101,325кПа; Т0 = 273К; Р = 104,5кПа. Подставляя данные задачи в уравнение,
получим:
Согласно закону эквивалентов, массы (объёмы) реагирующих друг с другом веществ m1 и m2 пропорциональны их эквивалентным массам (объёмам):
Мольный объём любого газа при н.у. равен 22,4л. Отсюда эквивалентный объём водорода равен 22,4 : 2 = 11,2л или 11200 мл. Тогда, используя формулу закона эквивалентов, рассчитаем эквивалентную массу металла:
Ответ: mЭ(Ме) = 39,4г/моль.
Задача 39.
Как следует изменить условия, чтобы увеличение массы данного газа не привело к возрастанию его объема: а) понизить температуру; б) увеличить давление; в) нельзя подобрать условий?
Решение:
Для характеристики газа количеством вещества (n, моль) применяется уравнение РV = nRT, или – это уравнение Клапейрона-Менделеева. Оно связывает массу (m, кг); температуру (Т, К); давление (Р, Па) и объём (V, м3) газа с молярной массой (М, кг/моль).
Тогда из уравнения Клапейрона-Менделеева объём газа можно рассчитать по выражению:
Отсюда следует, что V = const, если при увеличении массы (m) газа на некоторую величину будет соответственно уменьшена температура (T) системы на некоторое необходимое значение. Объём системы также не изменится при постоянной температуре, если при увеличении массы (m) газа на некоторую величину будет соответственно увеличено давление (P) системы на необходимую величину.
Таким образом, при увеличении массы газа объём системы не изменится, если понизить температуру системы или же увеличить давление в ней на некоторую величину.
Ответ: а); б).
Задача 40.
Какие значения температуры и давления соответствуют нормальным условиям для газов: а) t = 25 °С, Р = 760 мм. рт. ст.; б) t = 0 °С, Р = 1,013 • 105Па; в) t = 0°С, Р = 760 мм. рт. ст.?
Решение:
Состояние газа характеризуется температурой, давлением и объёмом. Если температура газа равна 0 °С (273К), а давление составляет 101325 Па (1,013 • 105) или 760 мм. рт. ст., то условия, при которых находится газ, принято считать нормальными.
Ответ: б); в).
Источник
Как вычислить объем газа
Газ, независимо от его состава, имеет три основных параметра: массу, объем и плотность. В большинстве задач оперируют так называемым идеальным газом, поэтому опираться в них необходимо лишь на приведенные в условии значения массы, давления, температуры. Например, в условии задачи может быть указан газ азот N2 с температурой в 60 градусов, давлением в 30 кПа и массой в 0,05 г. Зная эти три параметра и состав газа, по уравнению Менделеева-Клапейрона можно найти его объем. Для этого необходимо переделать данное уравнение следующим образом:
Осуществив дальнейшее преобразование формулы, найдите объем азота:
При этом молярную массу M можно найти по таблице Д.И. Менделеева. У азота она равна 12 г/моль. Тогда:
Если известны объем при нормальных условиях, а объем при других условиях является искомым, примените законы Бойля-Мариотта и Гей-Люссака:
В таком случае преобразуйте формулу следующим образом:
Отсюда объем V равен:
Индекс н означает величину того или иного параметра при нормальных условиях.
Если рассматривать объем газа с точки зрения термодинамики, можно заметить, что на газы могут действовать силы, за счет которых меняется объем. При этом давление газа постоянно, что характерно для изобарных процессов. В ходе таких процессов объем изменяется с одной величины на другую. Их можно обозначить как V1 и V2. В условиях ряда задач описывается некоторый газ, находящийся под поршнем в сосуде. При расширении этого газа поршень передвигается на некоторое расстояние dl, в результате чего осуществляется работа:
Эта формула связывает изменение объема газа и работу. Как известно, если дан конечный объем V2, то можно найти начальный объем V1:
Наконец, наиболее просто найти объем газа, исходя из двух других физических параметров — массы и плотности. Если в условиях задан газ с некоторой плотностью и массой, то его объем следует вычислять по формуле:
У каждого газа имеется определенная плотность, как и у любого твердого или жидкого вещества. Поэтому, находя объем газа, в первую очередь необходимо учитывать именно этот параметр.
Источник
Как_объем_зависит_от_давления
Основные понятия гидропневмоавтоматики
Схема гидравлического привода с дроссельным регулированием
Основные свойства рабочих жидкостей и газов
Плотность – количество массы в единице объема:
Вязкость
Свойство жидкости сопротивляться сдвигу или скольжению ее слоев.
,
где:
— напряжение сдвига;
— динамический коэффициент вязкости;
— скорость течения жидкости;
— расстояние между слоями жидкости.
— кинематический коэффициент вязкости
Сжимаемость
Свойство жидкости изменять свой объем под действием давления.
,
где:
— адиабатический модуль объемной упругости жидкости;
— объем рабочей жидкости;
— давление рабочей жидкости.
Для газов:
или — закон Бойля-Мариотта.
Облитерация
Свойство жидкости заращивать (засорять) узкие каналы и капиллярные щели при ее течении под действием перепада давления.
Кавитация
Разрыв рабочей жидкости под действием высокого давления при наличии большого количества растворенного воздуха.
Для идеального газа
Зависимость давления и объема
Изотермный процесс – процесс, проходящий при постоянной температуре
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: На стипендию можно купить что-нибудь, но не больше. 9423 —
| 7465 — или читать все.
Связь между давлением, температурой, объемом и количеством молей газа («массой» газа). Универсальная (молярная) газовая постоянная R. Уравнение Клайперона-Менделеева = уравнение состояния идеального газа.
Ограничения практической применимости:
- температуры ниже -100°C и выше температуры диссоциации / разложения
- давления выше 90 бар
- вакуум глубже чем 99%
Внутри диапазона точность уравнения превосходит точность обычных современных инженерных средств измерения. Для инженера важно понимать, что для всех газов возможна существенная диссоциация или разложение при повышении температуры.
- в СИ R= 8,3144 Дж/(моль*К) — это основная (но не единственная) инженерная система измерений в РФ и большинстве стран Европы
- в СГС R= 8,3144*10 7 эрг/(моль*К) — это основная (но не единственная) научная система измерений в мире
- m-масса газа в (кг)
- M-молярная масса газа кг/моль (таким образом (m/M) — число молей газа)
- P-давление газа в (Па)
- Т-температура газа в ( °K)
- V-объем газа в м 3
Давайте решим парочку задач относительно газовых объемных и массовых расходов в предположении, что состав газа не изменяется (газ не диссоциирует) — что верно для большинства газов в указанных выше пределах применимости.
1) Доставка объемов газа одинаковой массы при одинаковом давлении но различных температурах.
Данная задача актуальна в основном, но не только, для применений и устройств, в которых напрямую измеряется объем газа.
Пусть счетчик (расходомер) в точке доставки дает объемные накопленные расходы V1 и V2, при температурах, соответственно, T1 и T2 и, пусть T1 V2 для одинаковых количеств газа при данных условиях. Попробуем сформулировать несколько важных на практике выводов для данного случая:
- показатели объемного счетчика газа тем «весомее», чем выше давление
- выгодно поставлять газ низкого давления
- выгодно покупать газ высокого давления
Как с этим бороться? Необходима хотя бы простая компенсация по давлению, т.е в считающее устройство должна подаваться информация с дополнительного датчика давления.
Состояние идеального газа полностью описывается измеряемыми величинами: давлением, температурой, объемом. Отношение между этими тремя величинами определяется основным газовым законом:
,
где р – давление; V- объем; Т – температура;- количество идеального газа в молях;R- универсальная газовая постоянная (8,31 Дж/(Кмоль).
Если одна из величин давление, объем или температура остается постоянной, то другие две величины не могут быть изменены независимо друг от друга. Например, при постоянной температуре выполняется закон Бойля-Мариотта в виде:
Проверка закона Бойля-Мариотта.
Измерение давления воздуха в шприце при изменении объема учитывая, что температура газа постояна.
Ручной вакуумный насос
Рис 1. Общий вид установки по изучению закона Бойля – Мариотта. (1) шприц, (2) манометр (отсчет производить по черной шкале), (3) ручной вакуумный насос
В данном эксперименте закон Бойля – Мариотта подтверждается с помощью установки показанной на рисунке 1. Объем воздуха в шприце определяется следующим образом:
где rрадиус шприца, аh– расстояние от носика до поршня шприца.
Давление в системе нужно находить как:
где p атмосферное давление, аp– давление, измеренное при помощи манометра.
Порядок выполнения работы
Установите поршень шприца на отметке 50 мл.
Плотно надеть свободный конец соединительного шланга ручного вакуумного насоса на выходной патрубок шприца.
Выдвигая поршень, увеличивайте объем с шагом 5 мл, фиксируйте показания маномета по черной шкале.
Чтобы определить давление под поршнем, надо из атмосферного давления вычесть показания монометра, выраженного в паскалях. Атмосферное давление равно приблизительно 1 бар, что соответствует 100 000 Па.
Для обработки результатов измерений следует учитывать наличие воздуха в соединительном шланге. Для этого измерьте расчитайте объем соединительного шланга, измерив длину шланга рулеткой, а диаметр шланга штангенциркулем, учитывая, что толщина стенок составляет 1,5 мм.
Постройте график измеренной зависимости объема воздуха от давления.
Рассчитайте зависимость объема от давления при постоянной температуре по закону Бойля-Мариотта и постройте график.
Сравните теоретические и экспериментальные зависимости.
2133. Зависимость давления газа от температуры при постоянном объеме (закон шарля)
Рассмотрим зависимость давления газа от температуры при условии неизменного объема определенной массы газа. Эти исследования были впервые произведены в 1787 г. Жаком Александром Сезаром Шарлем (1746—1823). Газ нагревался в большой колбе, соединенной с ртутным манометром в виде узкой изогнутой трубки. Пренебрегая ничтожным увеличением объема колбы при нагревании и незначительным изменением объема при смещении ртути в узкой манометрической трубке. Таким образом, можно считать объем газа неизменным. Подогревая воду в сосуде, окружающем колбу, измеряли температуру газа по термометру Т, а соответствующее давлениер— по манометру. Наполнив сосуд тающим льдом, определяли давлениеро, и соответствующую температуруТо. Было установлено, что если при 0 С давлениеро, то при нагревании на 1 С приращение давления будет вро. Величинаимеет одно и то же значение (точнее, почти одно и тоже) для всех газов, а именно 1/273 C -1 . Величинуназывают температурным коэффициентом давления.
Закон Шарля позволяет рассчитать давление газа при любой температуре, если известно его давление при температуре 0 C. Пусть давление данной массы газа при 0 Cв данном объемеpo, а давление того же газа при температуреtp. Температура меняется наt, а давления изменяется нароt, тогда давлениерравно:
При очень низких температурах, когда газ приближается к состоянию сжижения, а также в случае сильно сжатых газов закон Шарля неприменим. Совпадение коэффициентов и, входящих в закон Шарля и закон Гей-Люссака, не случайно. Так как газы подчиняются закону Бойля — Мариотта при постоянной температуре, тоидолжны быть равны между собой.
Подставим значение температурного коэффициента давления в формулу температурной зависимости давления:
Величину (273+t) можно рассматривать как значение температуры, отсчитанное по новой температурной шкале, единица которой такая же, как и у шкалы Цельсия, а за нуль принята точка, лежащая на 273 ниже точки, принятой за нуль шкалы Цельсия, т. е. точки таяния льда. Нуль этой новой шкалы называют абсолютным нулем. Эту новую шкалу называют термодинамической шкалой температур, гдеTt+273 .
Тогда, при постоянном объеме справедлив закон Шарля:
Проверка закона Шарля
Определение зависимости давления газа от температуры при постоянном объеме
Определение абсолютной шкалы температур путем экстраполяции в сторону низких температур
Внимание: в работе используется стекло.
Будьте предельно аккуратны при работе с газовым термометром; стеклянным сосудом и мерным стаканом.
Будьте предельно внимательны при работе с горячей водой.
Мобильный CASSY Lab
Электрическая нагревательная плитка
Стеклянный мерный стакан
Ручной вакуумный насос
При откачке воздуха при комнатной температуре с помощью ручного насоса, создается давление на столб воздуха р0+р, где р – внешние давление. Капля ртути также оказывает давление на столб воздуха:
где Hg=13,6 г/см 3 – плотность ртути;g=9,81 м/c 2 – ускорение свободного падения; hHg – высота капли ртути.
Общее давление на столб воздухав газовом термометре определяется выражением:
В данном эксперименте этот закон подтверждается с помощью газового термометра. Термометр помещают в воду с температурой около 90°С и эта система постепенно охлаждается. Откачивая воздух из газового термометра с помощью ручного вакуумного насоса, поддерживают постоянный объём воздуха во время охлаждения.
Порядок выполнения работы
Откройте заглушку газового термометра, подключите к термометру ручной вакуумный насос.
Поверните осторожно термометр как показано слева на рис. 2 и откачайте воздух из него с помощью насоса так, чтобы капелька ртути оказалась в точке a) (см. рис.2).
После того как капелька ртути собралась в точке a)поверните термометр отверстием наверх и спустите нагнетенный воздух ручкойb) на насосе (см. рис.2) осторожно, чтобы ртуть не разделилась на несколько капелек.
Нагреть воду в стеклянном сосуде на плитке до 90°С.
Налить горячую воду в стеклянный сосуд.
Поместить в сосуд газовый термометр, закрепив его на штативе.
Поместить термопару в воду, постепенно эта система охлаждается. Откачивая воздух из газового термометра с помощью ручного вакуумного наноса, поддерживаете постоянный объём столба воздуха в течении всего процесса охлаждения.
Фиксируйте показание манометра ри температуруТ.
Постройте зависимость полного давления газаp +p+pHgот температуры в о С.
Продолжите график до пересечения с осью абсцисс. Определите температуру пересечения, объясните полученные результаты.
По тангенсу угла наклона определите температурный коэффициент давления.
Рассчитайте зависимость давления от температуры при постоянном объеме по закону Шарля и постройте график. Сравните теоретические и экспериментальные зависимости.
Источник
Источник
