Натяжение воды в сосудах
Главная Онлайн учебники База репетиторов России Тренажеры по физике Подготовка к ЕГЭ 2017 онлайн
Глава 3. Молекулярная физика и термодинамика
Молекулярно-кинетическая теория
3.5. Свойства жидкостей. Поверхностное натяжение
Молекулы вещества в жидком состоянии расположены почти вплотную друг к другу. В отличие от твердых кристаллических тел, в которых молекулы образуют упорядоченные структуры во всем объеме кристалла и могут совершать тепловые колебания около фиксированных центров, молекулы жидкости обладают большей свободой. Каждая молекула жидкости, также как и в твердом теле, «зажата» со всех сторон соседними молекулами и совершает тепловые колебания около некоторого положения равновесия. Однако, время от времени любая молекула может переместиться в соседнее вакантное место. Такие перескоки в жидкостях происходят довольно часто; поэтому молекулы не привязаны к определенным центрам, как в кристаллах (см. §3.6), и могут перемещаться по всему объему жидкости. Этим объясняется текучесть жидкостей. Из-за сильного взаимодействия между близко расположенными молекулами они могут образовывать локальные (неустойчивые) упорядоченные группы, содержащие несколько молекул. Это явление называется ближним порядком (рис. 3.5.1).
| Рисунок 3.5.1. Пример ближнего порядка молекул жидкости и дальнего порядка молекул кристаллического вещества: 1 – вода; 2 – лед |
Рис. 3.5.2 иллюстрирует отличие газообразного вещества от жидкости на примере воды. Молекула воды H2O состоит из одного атома кислорода и двух атомов водорода, расположенных под углом 104°. Среднее расстояние между молекулами пара в десятки раз превышает среднее расстояние между молекулами воды. В отличие от рис. 3.5.1, где молекулы воды изображены в виде шариков, рис. 3.5.2 дает представление о структуре молекулы воды.
| Рисунок 3.5.2. Водяной пар (1) и вода (2). Молекулы воды увеличены примерно в 5·107 раз |
Вследствие плотной упаковки молекул сжимаемость жидкостей, т. е. изменение объема при изменении давления, очень мала; она в десятки и сотни тысяч раз меньше, чем в газах. Например, для изменения объема воды на 1 % нужно увеличить давление приблизительно в 200 раз. Такое увеличение давления по сравнению с атмосферным достигается на глубине около 2 км.
Жидкости, как и твердые тела, изменяют свой объем при изменении температуры. Для не очень больших интервалов температур относительное изменение объема ΔV / V0 пропорционально изменению температуры ΔT:
Коэффициент β называют температурным коэффициентом объемного расширения. Этот коэффициент у жидкостей в десятки раз больше, чем у твердых тел. У воды, например, при температуре 20 °С βв ≈ 2·10-4 К-1, у стали βст ≈ 3,6·10-5 К-1, у кварцевого стекла βкв ≈ 9·10-6 К-1.
Тепловое расширение воды имеет интересную и важную для жизни на Земле аномалию. При температуре ниже 4 °С вода расширяется при понижении температуры (β < 0). Максимум плотности ρв = 103 кг/м3 вода имеет при температуре 4 °С.
При замерзании вода расширяется, поэтому лед остается плавать на поверхности замерзающего водоема. Температура замерзающей воды подо льдом равна 0 °С. В более плотных слоях воды у дна водоема температура оказывается порядка 4 °С. Благодаря этому жизнь может существовать в воде замерзающих водоемов.
Наиболее интересной особенностью жидкостей является наличие свободной поверхности. Жидкость, в отличие от газов, не заполняет весь объем сосуда, в который она налита. Между жидкостью и газом (или паром) образуется граница раздела, которая находится в особых условиях по сравнению с остальной массой жидкости. Молекулы в пограничном слое жидкости, в отличие от молекул в ее глубине, окружены другими молекулами той же жидкости не со всех сторон. Силы межмолекулярного взаимодействия, действующие на одну из молекул внутри жидкости со стороны соседних молекул, в среднем взаимно скомпенсированы. Любая молекула в пограничном слое притягивается молекулами, находящимися внутри жидкости (силами, действующими на данную молекулу жидкости со стороны молекул газа (или пара) можно пренебречь). В результате появляется некоторая равнодействующая сила, направленная вглубь жидкости. Поверхностные молекулы силами межмолекулярного притяжения втягиваются внутрь жидкости. Но все молекулы, в том числе и молекулы пограничного слоя, должны находиться в состоянии равновесия. Это равновесие достигается за счет некоторого уменьшения расстояния между молекулами поверхностного слоя и их ближайшими соседями внутри жидкости. Как видно из рис. 3.1.2, при уменьшении расстояния между молекулами возникают силы отталкивания. Если среднее расстояние между молекулами внутри жидкости равно r0, то молекулы поверхностного слоя упакованы несколько более плотно, а поэтому они обладают дополнительным запасом потенциальной энергии по сравнению с внутренними молекулами (см. рис. 3.1.2). Следует иметь ввиду, что вследствие крайне низкой сжимаемости наличие более плотно упакованного поверхностного слоя не приводит к сколь-нибудь заметному изменению объема жидкости. Если молекула переместится с поверхности внутрь жидкости, силы межмолекулярного взаимодействия совершат положительную работу. Наоборот, чтобы вытащить некоторое количество молекул из глубины жидкости на поверхность (т. е. увеличить площадь поверхности жидкости), внешние силы должны совершить положительную работу ΔAвнеш, пропорциональную изменению ΔS площади поверхности:
Коэффициент σ называется коэффициентом поверхностного натяжения (σ > 0). Таким образом, коэффициент поверхностного натяжения равен работе, необходимой для увеличения площади поверхности жидкости при постоянной температуре на единицу.
В СИ коэффициент поверхностного натяжения измеряется в джоулях на метр квадратный (Дж/м2) или в ньютонах на метр (1 Н/м = 1 Дж/м2).
Следовательно, молекулы поверхностного слоя жидкости обладают избыточной по сравнению с молекулами внутри жидкости потенциальной энергией. Потенциальная энергия Eр поверхности жидкости пропорциональна ее площади:
Из механики известно, что равновесным состояниям системы соответствует минимальное значение ее потенциальной энергии. Отсюда следует, что свободная поверхность жидкости стремится сократить свою площадь. По этой причине свободная капля жидкости принимает шарообразную форму. Жидкость ведет себя так, как будто по касательной к ее поверхности действуют силы, сокращающие (стягивающие) эту поверхность. Эти силы называются силами поверхностного натяжения.
Наличие сил поверхностного натяжения делает поверхность жидкости похожей на упругую растянутую пленку, с той только разницей, что упругие силы в пленке зависят от площади ее поверхности (т. е. от того, как пленка деформирована), а силы поверхностного натяжения не зависят от площади поверхности жидкости.
Некоторые жидкости, как, например, мыльная вода, обладают способностью образовывать тонкие пленки. Всем хорошо известные мыльные пузыри имеют правильную сферическую форму – в этом тоже проявляется действие сил поверхностного натяжения. Если в мыльный раствор опустить проволочную рамку, одна из сторон которой подвижна, то вся она затянется пленкой жидкости (рис. 3.5.3).
Силы поверхностного натяжения стремятся сократить поверхность пленки. Для равновесия подвижной стороны рамки к ней нужно приложить внешнюю силу Если под действием силы перекладина переместится на Δx, то будет произведена работа ΔAвн = FвнΔx = ΔEp = σΔS, где ΔS = 2LΔx – приращение площади поверхности обеих сторон мыльной пленки. Так как модули сил и одинаковы, можно записать:
Таким образом, коэффициент поверхностного натяжения σ может быть определен как модуль силы поверхностного натяжения, действующей на единицу длины линии, ограничивающей поверхность.
Из-за действия сил поверхностного натяжения в каплях жидкости и внутри мыльных пузырей возникает избыточное давление Δp. Если мысленно разрезать сферическую каплю радиуса R на две половинки, то каждая из них должна находиться в равновесии под действием сил поверхностного натяжения, приложенных к границе разреза длиной 2πR и сил избыточного давления, действующих на площадь πR2 сечения (рис. 3.5.4). Условие равновесия записывается в виде
Отсюда избыточное давление внутри капли равно
(капля жидкости).
| Рисунок 3.5.4. Сечение сферической капли жидкости |
Избыточное давление внутри мыльного пузыря в два раза больше, так как пленка имеет две поверхности:
(мыльный пузырь).
Вблизи границы между жидкостью, твердым телом и газом форма свободной поверхности жидкости зависит от сил взаимодействия молекул жидкости с молекулами твердого тела (взаимодействием с молекулами газа (или пара) можно пренебречь). Если эти силы больше сил взаимодействия между молекулами самой жидкости, то жидкость смачивает поверхность твердого тела. В этом случае жидкость подходит к поверхности твердого тела под некоторым острым углом θ, характерным для данной пары жидкость – твердое тело. Угол θ называется краевым углом. Если силы взаимодействия между молекулами жидкости превосходят силы их взаимодействия с молекулами твердого тела, то краевой угол θ оказывается тупым (рис. 3.5.5). В этом случае говорят, что жидкость не смачивает поверхность твердого тела. При полном смачивании θ = 0, при полном несмачивании θ = 180°.
| Рисунок 3.5.5. Краевые углы смачивающей (1) и несмачивающей (2) жидкостей |
Капиллярными явлениями называют подъем или опускание жидкости в трубках малого диаметра – капиллярах. Смачивающие жидкости поднимаются по капиллярам, несмачивающие – опускаются.
На рис. 3.5.6 изображена капиллярная трубка некоторого радиуса r, опущенная нижним концом в смачивающую жидкость плотности ρ. Верхний конец капилляра открыт. Подъем жидкости в капилляре продолжается до тех пор, пока сила тяжести действующая на столб жидкости в капилляре, не станет равной по модулю результирующей Fн сил поверхностного натяжения, действующих вдоль границы соприкосновения жидкости с поверхностью капилляра: Fт = Fн, где Fт = mg = ρhπr2g, Fн = σ2πr cos θ.
Отсюда следует:
| Рисунок 3.5.6. Подъем смачивающей жидкости в капилляре |
При полном смачивании θ = 0, cos θ = 1. В этом случае
При полном несмачивании θ = 180°, cos θ = -1 и, следовательно, h < 0. Уровень несмачивающей жидкости в капилляре опускается ниже уровня жидкости в сосуде, в которую опущен капилляр.
Вода практически полностью смачивает чистую поверхность стекла. Наоборот, ртуть полностью не смачивает стеклянную поверхность. Поэтому уровень ртути в стеклянном капилляре опускается ниже уровня в сосуде.
Источник
Сегодня поверхностно рассматриваем тему поверхностного натяжения и решаем соответствующие задачи по физике.
Даже если вы не большой любитель жидкости, подписывайтесь на наш телеграм-канал, это интересно и полезно для всех.
Поверхностное натяжение, задачи
Задача №1. Поверхностное натяжение
Условие
Для определения коэффициента поверхностного натяжения воды была использована пипетка с диаметром выходного отверстия d=2 мм. Оказалось, что n=40 капель имеют массу m=1,9 г. Каким по этим данным получится коэффициент поверхностного натяжения «сигма»?
Решение
На каплю действует сила тяжести и сила поверхностного натяжения. Эти силы уравновешивают друг друга. Из условия задачи можно найти массу одной капли m0 и длину ее окружности l:
Далее запишем условие равновесия капли:
Отсюда находим коэффициент поверхностного натяжения:
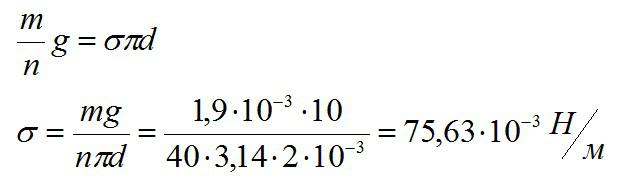
Ответ: 75,63*10^-3 Н/м.
Задача №2. Капиллярные явления
Условие
В капиллярной трубке радиусом 0,5 мм жидкость поднялась на высоту 11 мм. Оценить плотность данной жидкости, если ее коэффициент поверхностного натяжения равен 22 мН/м.
Решение
Для капилляра существует формула:
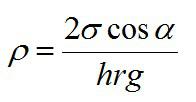
Альфа в этой формуле – угол смачивания стенки капилляра жидкостью. Пример его равным 90 градусов.
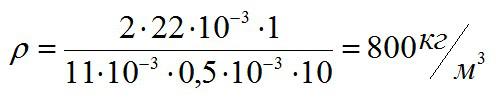
Ответ: 800 килограмм на кубический метр.
Задача №3. Поверхностное натяжение
Условие
В дне сосуда со ртутью имеется круглое отверстие диаметром 70 мкм. При какой максимальной высоте слоя ртути H она не будет вытекать через отверстие?
Решение
Ртуть не будет вытекать до тех пор, пока сила ее давления не превысит силу поверхностного натяжения:
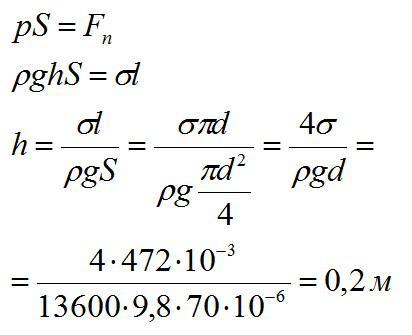
Значения коэффициента поверхностного натяжения разных жидкостей берутся в справочнике.
Ответ: 0,2 м.
Задача №4. Поверхностное натяжение
Условие
Швейная игла имеет длину 3,5 см и массу 0,3 г. Будет ли игла лежать на поверхности воды, если ее положить аккуратно?
Решение
Найдем силу тяжести, которая действует на иглу и сравним ее с силой поверхностного натяжения.
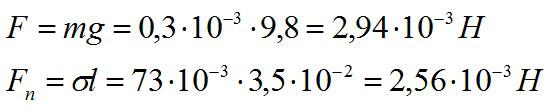
Ответ: Так как сила тяжести больше, игла утонет.
Задача №5. Поверхностное натяжение
Условие
Тонкое алюминиевое кольцо радиусом 7,8 см соприкасается с мыльным раствором. Каким усилием можно оторвать кольцо от раствора? Температуру раствора считать комнатной. Масса кольца 7 г.
Решение
На кольцо действуют силы поверхностного натяжения, сила тяжести и внешняя сила, стремящаяся оторвать кольцо от поверхности. Найдем силу поверхностного натяжения:
Множитель «2» используется в формуле, так как кольцо взаимодействует с жидкостью двумя своими сторонами.
Теперь запишем условие отрыва кольца:
Значение поверхностного натяжения мыльного раствора при комнатной температуре возьмем из таблицы, подставим числа, и получим:
Ответ: 0,11 Н.
Вопросы на тему «Поверхностное натяжение и свойства жидкостей»
Вопрос 1. Что такое жидкость?
Ответ. Жидкость – физическое тело, которое не может самостоятельно сохранять свою форму. Агрегатное состояние вещества между твердым телом и газом.
Вопрос 2. Какие свойства жидкости вы знаете?
Ответ. Среди основных свойств жидкости можно выделить:
- текучесть;
- вязкость;
- сохранение объема;
- поверхностное натяжение.
Вопрос 3. Что такое поверхностное натяжение?
Ответ. Поверхностное натяжение – это явление, при котором жидкость стремиться приобрести форму с наименьшей возможной площадью поверхности.
Примеры поверхностного натяжения в природе:
- Именно благодаря поверхностному натяжению в поле силы тяжести Земли жидкость приобретает форму капли.
- В отсутствие силы тяжести жидкости капля примет шарообразную форму.
- Водомерка удерживается на поверхности воды благодаря силе поверхностного натяжения.
Коэффициент поверхностного натяжения – коэффициент, равный работе, которую необходимо совершить для образования поверхности жидкости площадью S при постоянной температуре.
Вопрос 4. Что такое капиллярные явления?
Ответ. Капиллярные явления – подъем или опускание жидкости в капиллярах (трубках малого диаметра).
Вопрос 5. Что называется смачиванием?
Ответ. Смачивание – это искривление поверхности жидкости вблизи твердого тела. Возникает из-за взаимодействия молекул жидкости с молекулами твердого тела.
Количественная характеристика этого явления – угол смачивания.
Нужна помощь в решении заданий по учебе? Профессиональный студенческий сервис всегда готов ее оказать! Оформляйте заявку в любое время суток и забудьте о наболевших вопросах.
Источник
Вещество, находящееся в жидком состоянии, характеризуется крайне плотным расположением молекул друг относительно друга. Отличаясь от твердых кристаллических тел, чьи молекулы формируют упорядоченные структуры по всему объему кристалла и ограничены в своих тепловых колебаниях фиксированными центрами, молекулы жидкости обладают значительной степенью свободы. Любая конкретная молекула жидкого вещества, как это происходит и в твердых телах, «зажата» соседними молекулами и может совершать тепловые колебания поблизости с некоторым положением равновесия. Несмотря на это, в какой-то момент, любая молекула может переместиться на соседнее вакантное место. Подобные перемещения в жидкостях происходят довольно часто, благодаря чему молекулы не привязаны к конкретным центрам, как в кристаллах, а имеют возможность перемещаться по всему объему жидкости. Именно на этом факте основывается текучесть жидкостей.
Определение 1
По причине сильного взаимодействия между близко расположенными молекулами они могут образовывать локальные, то есть неустойчивые, упорядоченные группы, включающие в себя несколько молекул. Данное явление носит название ближнего порядка (рис. 3 . 5 . 1 ).
Рисунок 3 . 5 . 1 . Пример ближнего порядка молекул жидкости и дальнего порядка молекул кристаллического вещества: 1 – вода; 2 – лед.
Свойства жидкостей
На рисунке 3 . 5 . 2 , на примере воды, проиллюстрировано различие между газообразным веществом и жидкостью. Молекула воды H 2 O включает в свой состав один атом кислорода и два атома водорода, которые расположены под углом 104 ° . В среднем, расстояние между молекулами пара в десятки раз больше, чем между молекулами воды. На рисунке 3 . 5 . 2 , в отличие от рисунка 3 . 5 . 1 , на котором молекулы воды представляют из себя шарики, дается представление о структуре молекулы воды.
Рисунок 3 . 5 . 2 . Водяной пар ( 1 ) и вода ( 2 ) . Молекулы воды увеличены примерно в 5 · 10 7 раз.
Сжимаемость жидкостей, то есть изменение объема вещества при изменении давления, по причине плотности расположения молекул в десятки и сотни тысяч раз меньше, чем сжимаемость газов. К примеру, чтобы изменить объем воды всего на 1 % необходимо повысить значение давления примерно в 200 раз. Подобное увеличение давления по сравнению с атмосферным достигается на глубине близкой к 2 к м .
Подобно твердым телам, жидкости имеют свойство менять свой объем при изменении температуры. В случае не самых больших интервалов температур относительное изменение объема Δ V V 0 пропорционально изменению температуры Δ T , что может быть записано в виде следующего соотношения:
Δ V V 0 = β ∆ T .
В котором коэффициент β представляет собой температурный коэффициент объемного расширения. Данный коэффициент у жидкостей в десятки раз превышает значение такого же у твердых тел.
Пример 1
К примеру, у воды в случае, если температура равна 20 ° С β в ≈ 2 · 10 – 4 К – 1 , у стали β с т ≈ 3 , 6 · 10 – 5 К – 1 , у кварцевого стекла β к в ≈ 9 · 10 – 6 К – 1 .
Тепловое расширение воды обладает важным для жизни на Земле эффектом. В условиях температуры ниже 4 ° С вода начинает расширяется при снижении температуры β < 0 . Максимальную плотность ρ в = 10 3 к г / м 3 вода приобретает при температуре 4 ° С .
Замерзая, вода расширяется, из-за чего лед продолжает плавать на поверхности замерзающего водоема. Температура замерзающей воды подо льдом эквивалентна величине в 0 ° С . У дна водоема, то есть слоях воды, обладающих большей плотностью, температура держится около 4 ° С .
Поверхностное натяжение
Наличие свободной поверхности в жидкостях является одной из самых интересных ее особенностей. В отличие от газов, жидкость не заполняет весь объем сосуда, в котором она находится. Между жидкостью и газом, возможно паром, возникает граница раздела, находящаяся в особых условиях по сравнению с остальной массой жидкости. В отличие от молекул в глубине жидкости, молекулы, располагающиеся в пограничном ее слое, окружены другими молекулами этой же жидкости не со всех сторон. В среднем воздействующие на одну из молекул внутри жидкости со стороны соседних молекул силы межмолекулярного взаимодействия взаимно скомпенсированы. Каждая отдельно взятая молекула в пограничном слое притягивается находящимися внутри жидкости молекулами. При этом, силами, которые оказывают воздействие на такую молекулу жидкости со стороны молекул газа можно пренебречь. Вследствие этого возникает некая направленная вглубь жидкости равнодействующая сила. Поверхностные молекулы втягиваются внутрь жидкости, с помощью действия сил межмолекулярного притяжения. Однако все молекулы, в том числе и принадлежащие пограничному слою, должны находиться в состоянии равновесия. Оно достигается за счет сокращения расстояния между молекулами в пограничном слое и ближайшими их соседями в жидкости. Как проиллюстрировано на рисунке 3 . 1 . 2 , в процессе уменьшения расстояния расстояния между молекулами появляются силы отталкивания. В случае, когда средняя величина расстояния между молекулами в жидкости равна r 0 , молекулы поверхностного слоя расположены плотнее, и по этой причине по сравнению с внутренними молекулами они имеют дополнительным запас потенциальной энергии, что можно увидеть на рисунке 3 . 1 . 2 .
Замечание 1
Стоит обратить внимание на то, что более плотного поверхностного слоя не приводит к сколь-нибудь заметному изменению объема жидкости по причине чрезвычайно низкой сжимаемости.
Силы межмолекулярного взаимодействия совершают положительную работу, в случае, когда молекула перемещается с поверхности внутрь жидкости. И наоборот, чтобы достать некоторое количество молекул на поверхность из глубины жидкости, то есть повысить площадь поверхности жидкости, внешним силам необходимо произвести пропорциональную изменению Δ S площади поверхности положительную работу Δ A в н е ш :
Δ A в н е ш = σ ∆ S ,
где коэффициент σ носит название коэффициента поверхностного натяжения ( σ > 0 ) .
Определение 2
Из всего вышесказанного следует, что коэффициент поверхностного натяжения – это величина равная работе, необходимой для увеличения площади поверхности жидкости при постоянной температуре на единицу.
В С И коэффициент поверхностного натяжения измеряется в джоулях на метр квадратный ( Д ж / м 2 ) или же в ньютонах на метр ( 1 Н / м = 1 Д ж / м 2 ) .
Таким образом, по сравнению с молекулами внутри жидкости молекулы поверхностного слоя жидкости обладают избыточной потенциальной энергией. Потенциальная энергия E р поверхности жидкости пропорциональна ее площади и выражается в виде следующей формулы:
E р = A в н е ш = σ S .
Из раздела механики известно, что равновесным состояниям системы соответствует минимальное значение ее потенциальной энергии. Следовательно, свободная поверхность жидкости стремится уменьшить свою площадь. По данной причине свободная капля жидкости принимает шарообразную форму.
Определение 3
Жидкость ведет себя таким образом, будто по касательной к ее поверхности действуют сокращающие данную поверхность силы. Такие силы называются силами поверхностного натяжения.
Силы поверхностного натяжения влияют на поверхность жидкости таким образом, что она становится похожей на упругую растянутую пленку, с той лишь разницей, что упругие силы в пленке зависят от площади ее поверхности, то есть от степени деформированности пленки, а силы поверхностного натяжения, зависимости от площади поверхности жидкости не имеют.
Пример 2
Некоторые жидкости, например, мыльная вода, имеют способность формировать тонкие пленки. Хорошо известные каждому человеку мыльные пузыри обладают правильной сферической формой, в чем также проявляется воздействие сил поверхностного натяжения. В случае, когда в мыльный раствор опускают проволочную рамку с одной подвижной стороной, вся она затягивается пленкой жидкости, как это показано на рисунке 3 . 5 . 3 .
Рисунок 3 . 5 . 3 . Подвижная сторона проволочной рамки в равновесии под действием внешней силы F в н → и результирующей сил поверхностного натяжения F н → .
Силы поверхностного натяжения действуют на уменьшение поверхности пленки. Ради равновесия подвижной стороны рамки к ней необходимо приложить внешнюю силу
F в н → = – F н → . Если воздействие силы F в н → спровоцирует перемещение перекладины на некоторое Δ x , то будет произведена работа Δ A в н = F в н Δ x = Δ E p = σ Δ S , где Δ S = 2 L Δ x является увеличением площади поверхности обеих сторон мыльной пленки. По той причине, что модули сил F в н → и F н → эквивалентны, справедливой будет запись:
F н ∆ x = σ 2 L ∆ x или σ = F н 2 L .
Определение 4
Исходя из этого, можно заявить, что коэффициент поверхностного натяжения σ может быть определен как модуль силы поверхностного натяжения, действующей на единицу длины линии, ограничивающей поверхность.
По причине воздействия сил поверхностного натяжения на капли жидкости и их действия внутри мыльных пузырей появляется некоторое избыточное давление Δ p . При мысленном разрезании сферической капли с радиусом R на две равные части каждая из половин должна находиться в равновесии под действием приложенных к границе разреза длиной 2 π R и сил избыточного давления, действующих на площадь π R 2 сечения (рис. 3 . 5 . 4 ) сил поверхностного натяжения. Условие равновесия может быть записано в следующем виде:
σ 2 π R = ∆ p πR 2 .
Исходя из этого, можно заявить, что избыточное давление внутри капли эквивалентно:
∆ p = 2 σ R (капля жидкости).
Рисунок 3 . 5 . 4 . Сечение сферической капли жидкости.
Из-за того, что пленка обладает двумя поверхностями, величина избыточного давления внутри мыльного пузыря в два раза выше, чем в капле:
∆ p = 4 σ R (мыльный пузырь).
Пренебрегая взаимодействием с молекулами газа, можно сказать, что поблизости с границей между твердым телом, жидкостью и газом форма свободной поверхности жидкости зависима от сил взаимодействия молекул жидкости с молекулами твердого тела.
Определение 5
В случае, когда данные силы превышают силы взаимодействия между молекулами жидкости, жидкость смачивает поверхность твердого тела. В таком случае жидкость подходит к поверхности твердого тела под некоторым характерным для данной пары жидкость – твердое тело острым углом θ . Такой угол носит название краевого угла.
Краевой угол θ является тупым (рисунок 3 . 5 . 5 ), в случае, если силы взаимодействия между молекулами жидкости превосходят силы их взаимодействия с молекулами твердого тела. В подобном случае можно сказать, что поверхность твердого тела не смачивается жидкостью. В условиях полного смачивания θ = 0 , полного несмачивания θ = 180 ° .
Рисунок 3 . 5 . 5 . Краевые углы смачивающей ( 1 ) и несмачивающей ( 2 ) жидкостей.
Капиллярные явления
Определение 6
Капиллярными явлениями называют процесс подъема или опускания жидкости в трубках малого диаметра, другими словами, в капиллярах.
Смачивающие жидкости поднимаются по капиллярам, несмачивающие – опускаются. На рисунке 3 . 5 . 6 проиллюстрирована опущенная нижним концом в смачивающую жидкость плотности ρ капиллярная трубка, обладающая некоторым радиусом r . При этом верхний конец капилляра является открытым. Подъем жидкости в капилляре будет происходить до тех пор, пока сила тяжести F т → , оказывающая воздействие на столб жидкости в капилляре, не станет эквивалентна по модулю результирующей F н действующих вдоль границы соприкосновения жидкости с поверхностью капилляра сил поверхностного натяжения: F т = F н , где F т = m g = ρ h π r 2 g , F н = σ 2 π r cos θ .
Из этого следует:
h = 2 σ cos θ ρ g r .
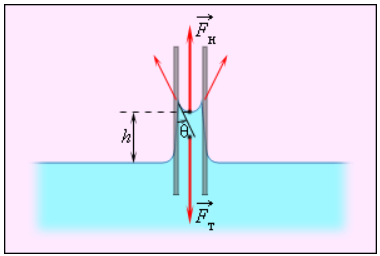
Рисунок 3 . 5 . 6 . Подъем смачивающей жидкости в капилляре.
При полном смачивании θ = 0 , cos θ = 1 . В таком случае:
h = 2 σ ρ g r .
При полном несмачивании θ = 180 ° , cos θ = – 1 и, соответственно, h < 0 . Уровень несмачивающей жидкости в капилляре опускается ниже уровня жидкости в сосуде, в которую опущен капилляр.
Вода почти полностью смачивает чистую поверхность стекла. Ртуть же, строго наоборот, полностью не смачивает стеклянную поверхность. По этой причине уровень ртути в стеклянном капилляре опускается ниже, чем уровень в сосуде.
Источник
