Нейрогенное влияние на сосуды
Оглавление темы “Сосудистый тонус. Эндотелий сосудов. Кровоснабжение головного мозга. Кровоснабжение сердца ( миокарда ).”: Нервная регуляция тонуса сосудов. Парасимпатические воздействия на сосуды. Влияние симпатической нервной системы на сосуды.Нейрогенное сужение сосудов осуществляется путем возбуждения адренергических волокон, которые действуют на гладкие мышцы сосудов путем высвобождения в области нервных окончаний медиатора адреналина. Торможение импульсов в симпатических нервных волокнах влияет на гладкие мышцы сосудов путем снижения их тонуса. Парасимпатические вазодилататорные волокна холинергической природы доказаны для группы волокон сакрального отдела, идущих в составе п. pelvicus. В блуждающих нервах отсутствуют сосудорасширяющие волокна для органов брюшной полости. В скелетных мышцах доказано наличие симпатических вазодилататорных нервных волокон, которые являются холинергическими. Внутрицен-тральный путь этих волокон начинается в моторной зоне коры мозга. Тот факт, что эти волокна могут возбуждаться при стимуляции двигательной области коры мозга, позволяет предположить, что они вовлекаются в системную реакцию, способствующую увеличению кровотока в скелетных мышцах в начале их работы. Гипоталамическое представительство этой системы волокон указывает на их участие в эмоциональных реакциях организма.
У теплокровных отсутствует «дилататорный» центр с особой системой «дилататорных» волокон. Вазомоторные сдвиги бульбоспинального уровня осуществляются исключительно путем изменения числа возбужденных констрикторных волокон и частоты их разрядов, т. е. сосудодвигательные эффекты возникают только путем возбуждения или торможения констрикторных волокон симпатических нервов. Адренергические волокна при электрической стимуляции могут передавать импульсацию с частотой 80—100 в 1 с. Однако в физиологическом покое частота импульсов в них составляет 1—3 в 1 с и может увеличиваться при прессорном рефлексе только до 12—15 имп/с. Из сказанного ясно, что практически весь диапазон величин сосудистых реакций, которые можно получить при электрической стимуляции нервов, соответствует увеличению частоты импульсов всего лишь на 1—12 в 1 мин, что вегетативная нервная система в норме функционирует при частоте разрядов значительно меньшей 10 имп/с. Электрическая стимуляция соответствующих симпатических волокон приводит к достаточно сильному повышению сопротивления сосудов скелетных мышц, кишечника, селезенки, кожи, печени, почки, жира; эффект выражен слабее в сосудах мозга, сердца. В сердце и почке этой вазоконстрикции противостоят местные вазодилататорные влияния, опосредованные активацией функций основных или специальных клеток ткани, одновременно запускаемые нейрогенным адренергическим механизмом. В результате такой суперпозиции двух механизмов выявление адренергической нейрогенной вазоконстрикции в сердце и почке составляет более сложную, чем для других органов, задачу. Общая закономерность все же состоит в том, что во всех органах стимуляция симпатических волокон вызывает активацию гладких мышц сосудов, иногда маскируемую одновременными или вторичными тормозными эффектами. При рефлекторном возбуждении симпатических нервных волокон, как правило, имеет место повышение сопротивления сосудов всех изученных областей (рис. 9.22). При торможении симпатической нервной системы (рефлексы с полостей сердца, депрессорный синокаротидный рефлекс) наблюдается обратный эффект. Различия между рефлекторными вазомоторными реакциями органов в основном количественные, качественные — обнаруживаются значительно реже. Одновременная параллельная регистрация сопротивления в различных сосудистых областях свидетельствует о качественно однозначном характере активных реакций сосудов при нервных влияниях. Учитывая небольшую величину рефлекторных констрикторных реакций сосудов сердца и мозга, можно полагать, что в естественных условиях кровоснабжения этих органов симпатические вазоконстрикторные влияния наних нивелируются метаболическими и общими гемодинамическими факторами, в результате чего конечным эффектом может быть расширение сосудов сердца и мозга. Этот суммарный дилататорный эффект обусловлен сложным комплексом влияний на указанные сосуды, а не только нейро-генных. Кроме того, эти отделы сосудистой системы обеспечивают обмен веществ в жизненно важных органах, поэтому слабость вазоконстриктор-ных рефлексов в этих органах обычно интерпретируют тем, что выраженные симпатические констрикторные влияния на сосуды мозга и сердца биологически нецелесообразно, так как это значительно уменьшало бы их кровоснабжение. – Также рекомендуем “Влияние простогландинов на сосуды. Воздействие кининов на стенку сосуда.” |
Источник
Гуморально-гормональная регуляция тонуса сосудов. Нейрогенная регуляция сосудов
Следует отметить, что одним из важных стимуляторов синтеза оксида азота является механическая деформация эндотелиальных клеток потоком крови – так называемая деформация сдвига эндотелия.
Помимо оксида азота эндотелий вырабатывает другие вазодилататоры: простациклин (простагландин I2), эндотелиальный фактор гиперполяризации, адреномедулин, натрийуретический пептид С-типа. В эндотелии функционирует калликреин-кининовая система, продуцирующая мощнейший пептидный дилататор брадикинин (Куликов В.П., Киселев В.И., Тезов А.А., 1987).
Эндотелий вырабатывает и вазоконстрикторы: эндотелины, тромбоксан (простагландин А2), ангиотензин II, простагландин Н2. Эндотелии 1 (ЕТ1) является наиболее мощным из всех известных вазоконстрикторов.
Эндотелиальные факторы влияют на адгезию и агрегацию тромбоцитов. Простациклин – важнейший антиагрегант, а тромбоксан, напротив, стимулирует адгезию и агрегацию тромбоцитов.
Нарушение этого баланса обозначается как дисфункция эндотелия, которая играет важную роль в патогенезе сердечно-сосудистых заболеваний. Важнейшими лабораторными маркерами дисфункции эндотелия являются эндотелины и фактор Виллебранда.
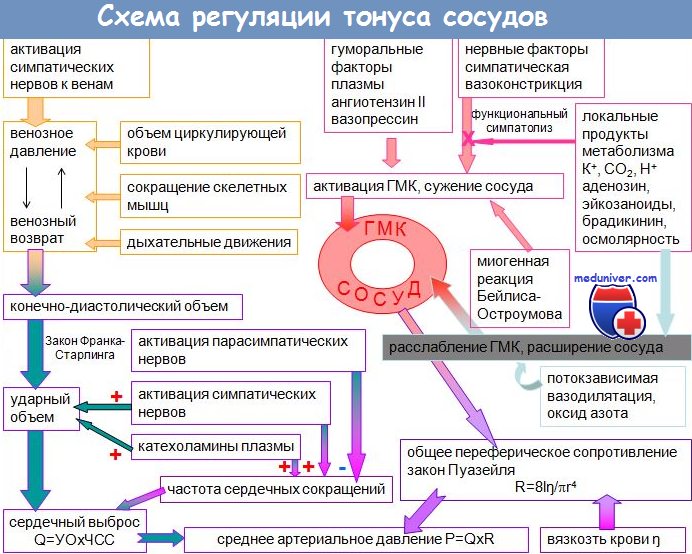
Гуморально-гормональная регуляция. В основном осуществляется посредством баланса активности прессорной ренин-ангиотензин-альдостероновой и депрессорной калликреин-кининовой систем крови. Эти системы связаны посредством ангиотензин превращающего фермента (АПФ). АПФ превращает неактивный ангиотензин I в ангиотензин II, который является вазоконстриктором и стимулирует выработку альдостерона в коре надпочечников, что сопровождается задержкой воды в организме и способствует подъему АД. Одновременно АПФ является основным ферментом разрушения брадикинина и таким образом устраняет его депрессорный эффект. Поэтому ингибиторы АПФ эффективно снижают АД при гипертензии, изменяя баланс систем в сторону кининовой.
Нейрогенная регуляция. Как уже отмечалось, ведущим эфферентным звеном в нейрогенном контроле сосудистого тонуса является симпатическая нервная система. Известна так называемая ишемическая реакция ЦНС. При значительном снижении системного АД возникает ишемия сосудодвигательного центра и активация симпатической нервной системы. Медиатором последней является норадреналин, вызывающий тахикардию (1-рецепторы) и увеличение тонуса сосудов (1 и 2-рецепторы).
Афферентное звено нейрогенной регуляции сосудистого тонуса представлено барорецепторами и хеморецепторами, расположенными в дуге аорты и каротидном синусе.
Барорецепторы реагируют на степень и скорость растяжения стенки сосудов. Хеморецепторы реагируют на изменение в крови концентрации СО2. Чувствительные волокна от барорецепторов и хеморецепторов дуги аорты и каротидного синуса проходят в составе синокаротидного нерва, ветвей языкоглоточного нерва и депрессорного нерва.
Нейрогенная регуляция обеспечивает постоянный (тонический) контроль над резистивными сосудами большинства сосудистых областей и экстренное рефлекторное регулирование, например, при приеме ортостатического положения. В этом и других случаях, когда давление в каротидном синусе и дуге аорты резко падает, включается каротидный барорефлекс, который через активацию барорецепторов и симпатическую нервную систему суживает сосуды, активирует работу сердца и обеспечивает подъем АД. Барорецепторный рефлекс срабатывает, наоборот, на повышение АД, что обеспечивает его снижение через торможение симпатических влияний и активацию блуждающего нерва. Хеморецепторный рефлекс обеспечивает подъем артериального давления посредством активации симпатических влияний в условиях гипоксии, когда в крови накапливается углекислым газ.
– Также рекомендуем “Признаки изменения сосудистой резистентности. Упругость и эластичность сосудов”
Оглавление темы “Норма и патология сосудов”:
1. Сосудистый тонус. Контроль тонуса сосудов
2. Гуморально-гормональная регуляция тонуса сосудов. Нейрогенная регуляция сосудов
3. Признаки изменения сосудистой резистентности. Упругость и эластичность сосудов
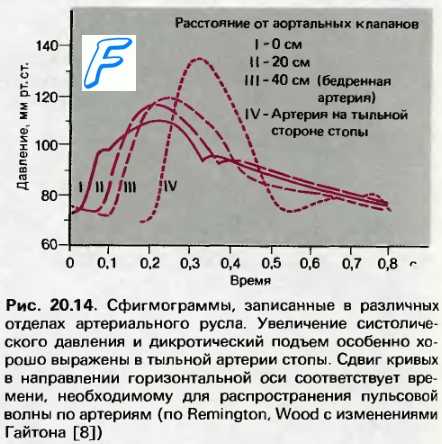
4. Пульсативность артерий. Винтовое движение крови
5. Доказательство винтового движения крови. Импульсно-волновая допплерография кровотока
6. Типовые нарушения регионального кровообращения. Артериальная гиперемия
7. Коллатеральный кровоток. Местные нарушения кровообращения
8. Гемодинамическая значимость сосудистых поражений. Факторы влияющие на значимость нарушений кровотока
9. Ультразвук. Характеристика и параметры ультразвука
10. Физические параметры ультразвука. Диагностический ультразвук
Источник
Оглавление темы “Сосудистый тонус. Эндотелий сосудов. Кровоснабжение головного мозга. Кровоснабжение сердца ( миокарда ).”:
1. Регионарное кровообращение. Сосудистый тонус. Эффект Остроумова—Бейлисса.
2. Ауторегуляция кровотока. Теории механизма ауторегуляции кровотока. Миогенная, нейрогенная теория. Теория тканевого давления. Обменная теория.
3. Базальный тонус сосудов. Растяжимость сосудов. Трансмуральное давление. Мобилизация крови из вен.
4. Депонирование крови. Причина головокружения ( обморока ) при вставании. Рабочая ( или функциональная ) гиперемия.
5. Реактивная ( постокклюзионная ) гиперемия. Ауторегуляторная реакция. Функциональная гиперемия органов.
6. Нервная регуляция тонуса сосудов. Парасимпатические воздействия на сосуды. Влияние симпатической нервной системы на сосуды.
7. Влияние простогландинов на сосуды. Воздействие кининов на стенку сосуда.
8. Эндотелий сосудов. Роль ( значение ) эндотелия в регуляции просвета сосудов.
9. Кровоснабжение головного мозга. Интенсивность кровотока в сосудах мозга. Миогенная, гуморальная регуляция мозгового кровотока.
10. Кровоснабжение сердца ( миокарда ). Интенсивность кровотока в сосудах сердца ( миокарда ). Миогенная, гуморальная регуляция коронарного кровотока.
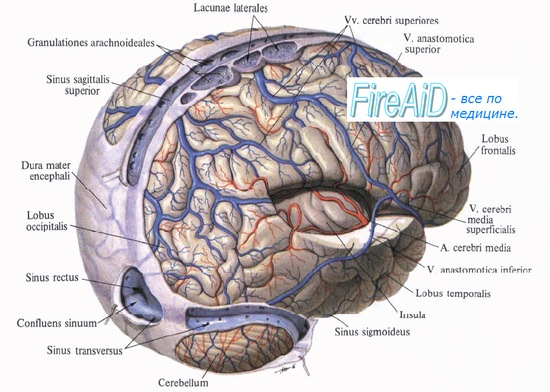
Кровоснабжение головного мозга. Интенсивность кровотока в сосудах мозга. Миогенная, гуморальная регуляция мозгового кровотока.
Интенсивность кровотока в сосудах мозга высока и составляет в состоянии покоя человека 55—60 мл/100 г/мин, т. е. около 15 % сердечного выброса. При относительно небольшой массе (2 % от массы тела) мозг потребляет до 20 % всего кислорода и 17 % глюкозы, которые поступают в организм человека. Интенсивность потребления кислорода мозгом составляет в среднем 3—4 мл/100 г/мин. В отличие от других органов мозг практически не располагает запасами кислорода.
При относительном постоянстве общего мозгового кровотока локальный кровоток в различных отделах мозга не постоянен и зависит от интенсивности их функционирования. Так, при напряженной умственной работе локальный кровоток в коре головного мозга человека может возрастать в 2—3 раза по сравнению с состоянием покоя.
В условиях герметичности и жесткости черепа общее сопротивление сосудистой системы головного мозга мало зависит от изменений давления в его артериях. Так, при повышении АД происходит расширение мозговых артерий, что ведет к повышению давления ликвора, сжатию вен мозга и оттоку ликвора в спинальную полость. При этом сопротивление артерий падает, а вен — возрастает, так что общее сопротивление сосудистой системы мозга в целом практически не меняется.
Миогенная регуляция мозгового кровотока осуществляется за счет реакции гладких мышц артериальных сосудов мозга на изменение давления в них. Повышение АД приводит к возрастанию тонуса миоцитов и сужению артерий, снижение АД — к снижению тонуса и расширению артерий. Миогенная регуляция мозгового кровообращения считается центральным звеном системы ауторегуляции кровообращения в мозге.

Гуморальная регуляция. Мощным регулятором мозгового кровотока является уровень напряжения углекислого газа в артериальной крови и связанный с этим уровень рН спинномозговой жидкости. На каждый миллиметр изменения напряжения С02 величина мозгового кровотока изменяется примерно на 6 %. Возрастание напряжения С02 в крови (гипер-капния) сопровождается расширением мозговых сосудов, а гипокапния — их сужением, столь значительным, что достигается порог кислородной недостаточности мозга (одышка, судороги, потеря сознания). Увеличение мозгового кровотока при гиперкапнии обеспечивает быстрое «вымывание» углекислоты и возвращение уровня напряжения С02 и концентрации водородных ионов к исходной величине.
Метаболическая реакция клеток мозга играет существенную роль при локальных перераспределениях крови между областями мозга, имеющими разный уровень функциональной активности в каждой конкретной ситуации. Локальное повышение функциональной активности нервных клеток приводит к росту в межклеточной среде концентрации аденозина и ионов калия, что ведет к местному расширению сосудов и усилению в них кровотока.
Поскольку уровень концентрации ионов калия в межклеточной среде головного мозга может меняться в течение долей секунды от момента усиления функциональной активности нейронов, описанный механизм считается быстрым контуром регуляции. Более медленный контур регуляции мозгового кровотока связан с повышением напряжения С02 в мозговом веществе вследствие активного потребления кислорода работающими клетками. Это вызывает локальное снижение рН в межклеточной среде и приводит к расширению сосудов активно функционирующей области мозга.
Биологически активные вещества и гормоны могут оказывать как прямое, так и опосредованное влияние на сосуды мозга. К внутрисосудистым вазоконстрикторам относятся: вазопрессин, ангиотензин, простагландины группы F, катехоламины. Сосудорасширяющий эффект оказывают: аце-тилхолин, гистамин (средние и крупные артерии), брадикинин (мелкие артерии).
Нейрогенная регуляция сосудов головного мозга менее эффективна, чем метаболическая. Основной зоной приложения нейрогенных влияний являются мелкие артериальные мозговые сосуды диаметром до 25—30 мкм. Доказано существование адренергических, холинергических, серотонинергических и пептидергических нервных волокон, обеспечивающих регуляцию тонуса мозговых сосудов, Нервные влияния на стенку сосудов головного мозга опосредуются через а- и (B-адренорецепторы (норад-реналин), М-холинорецепторы (ацетилхолин, вазоинтестинальный пептид), D-рецепторы (серотонин).
Основной источник нервных влияний на сосуды мозга — постганглио-нарные симпатические волокна, начинающиеся в верхних шейных ганглиях. Существование парасимпатических влияний на мозговые сосуды не доказано.
Нейрогенные влияния на кровоснабжение мозга во многом зависят от выраженности ауторегуляции, исходного тонуса сосудов, напряжения СO2, O2, состава и концентрации ионов, присутствия биологически активных веществ в спинномозговой жидкости и тканях мозга. Именно поэтому конечный эффект нейрогенных влияний на мозговой кровоток не однозначен.
– Также рекомендуем “Кровоснабжение сердца ( миокарда ). Интенсивность кровотока в сосудах сердца ( миокарда ). Миогенная, гуморальная регуляция коронарного кровотока.”
Источник
Вегетативная регуляция мозгового кровотока. Влияние реологии кровиМозговые сосуды богато иннервированы. В проводящих путях, регулирующих мозговой кровоток, принимают участие различные нейромедиаторы. Нейрогенные факторы играют важную роль в модуляции ответа кровотока на изменяющиеся метаболические потребности в каждой конкретной ситуации. Суще ствуют противоречивые данные относительно важности вегетативного контроля мозгового кровотока. Симпатическая нервная система: Парасимпатическая нервная система:
Тригеминоваскулярные нервы: Изменение реологических свойств крови может оказывать комплексное воздействие на церебральный кровоток и доставку кислорода: – Также рекомендуем “Церебральный метаболизм. Регуляция” Оглавление темы “Нервная система с точки зрения анестезиолога”:
|
Источник