Нейрогенный и миогенный тонус сосудов
Под тонусом сосудов понимают непрерывно поддерживаемую определённую степень сократительной активности сосудистых гладких мышц, которая не сопровождается развитием утомления и определяет противодействие растягивающему сосуд давлению крови. Таким образом, тонус сосудов формируется исключительно деятельностью их гладких мышц. Усиление тонуса сопровождается увеличением сопротивления потоку крови, ослабление – уменьшением сопротивления. На сопротивление сосудов, помимо их тонуса, оказывают влияние многие факторы: вязкость крови (а, следовательно, температура, гематокрит ,содержание белков, скорость кровотока, деформируемость эритроцитов), экстраваскулярная компрессия, состояние коллагеново – эластинового каркаса и др.
Наличие сосудистого тонуса определяют 2 основных механизма – нейрогенный и миогенный.
Миогенный тонус возникает, когда некоторые гладкомышечные клетки сосудов начинают спонтанно генерировать нервный импульс. Возникающее возбуждение распространяется на другие клетки, и происходит сокращение. Тонус поддерживается за счёт базального механизма. Разные сосуды обладают разным базальным тонусом: максимальный тонус наблюдаются в коронарных сосудах, скелетных мышцах, почках, а минимальный – в коже и слизистой оболочке. Его значение заключается в том, что сосуды с высоким базальным тонусом на сильное раздражение отвечают расслаблением, а с низким – сокращением.
Нервный механизм возникает в гладкомышечных клетках сосудов под влиянием импульсов из ЦНС. За счёт этого происходит ещё большее увеличение базального тонуса. Такой суммарный тонус – тонус покоя, с частотой импульсов 1 – 3 в секунду.
Кроме того, на сосудистый тонус оказывают влияние гуморальные механизмы, которые осуществляются за счёт веществ местного и системного действия.
Эти механизмы и предстоит рассмотреть при изучении регуляции сосудистого тонуса.
Происхождение сосудистого тонуса
Нейрогенный компонент сосудистого тонуса определяется исключительно тонической активностью симпатических адренергических вазоконстрикторных нервных волокон (симпатические и парасимпатические холинергические вазодилататорные волокна тонической активностью не обладают). Считается установленным, что в условиях физиологического покоя тоническая симпатическая вазоконстрикторная импульсация не превышает 1 – 2 имп/с .Однако электрофизиологические исследования показывают, что эфферентная симпатическая импульсация в покое имеет нерегулярный характер , с непериодическим чередованием отдельных импульсов и пачек импульсов, с разным расстоянием между импульсами, с разным числом импульсов в пачках и по частоте, следовательно, может значительно превышать 1 – 2 имп/с.
Нейрогенный механизм сосудистого тонуса выявлен во многих участках сосудистого русла, причём величина его в разных органах существенно различается. Это связано, очевидно, не столько с различиями эфферентной симпатической посылки к разным органам, сколько с органными особенностями плотности симпатической иннервации сосудов, плотности распределения в них и чувствительности адренорецепторов. Децентрализация приводит к умеренной вазодилатации в скелетных мышцах (нестойкой) , в кишечнике (устойчивой), в коже (наиболее стойкой), слабая вазодилатация наблюдается в печени, миокарде, непостоянно выявляется в мозге и почке.
Нейрогенный компонент не является решающим фактором формирования сосудистого тонуса; даже в органах с высокой плотностью иннервации он определяет, очевидно, не более 15 – 20 % суммарного тонуса сосудов. После выключения всех нервных и гуморальных влияний (в основном циркулирующих в крови катехоламинов) в сосудах сохраняется так называемый основной или базальный тонус (именуемый так же «периферическим» или «миогенным»). Он сохраняется так же при выключении реагирования сосудов на изменения внутрисосудистого давления. Кроме того, внутрисосудистое давление не является постоянно действующим раздражителем. Например, в децентрализованных скелетных мышцах многие артериолы полностью закрыты (что отражает их высокий тонус), хотя давление крови в них практически равно нулю. Следовательно, миогенная реакция сосудов на растяжение (феномен Остроумова – Бейлисса) не является главенствующим фактором, ответственным за формирование базального тонуса. Считается, что в основе базального тонуса лежит автоматия сосудистых гладких мышц, т.е. присущая им способность развивать и поддерживать сократительную активность за счёт внутренних биохимических и регуляторных процессов. Таким образом, по своему происхождению базальный тонус сосудов является миогенным.
Базальный тонус неодинаков в сосудах разных органов и имеет разное функциональное значение. Он высок в артериолах и значительно ниже в венозных сосудах. Хорошо выражен базальный тонус в сосудах скелетных мышц, слюнных желёз, кишечника, печени, сердца, менее выражен в сосудах мозга, сравнительно низок в сосудах почки и жировой ткани и практически отсутствует в артериовенозных анастомозах кожи. Миогенный (базальный) тонус сосудов и представляет собой ту основу, на которой реализуется влияние различных местных факторов регуляции – механических, метаболических, гормональных, что и обеспечивает осуществление важных процессов ауторегуляции кровотока и функциональной гиперемии.
От величины просвета сосудов, от их тонуса и количества выбрасываемой в них сердцем крови зависит кровоснабжение органов. Поэтому при рассмотрении регуляции функции сосудов прежде всего должна идти речь о механизмах поддержания сосудистого тонуса и о взаимодействии сердца и сосудов.
Источник
Сосудистый тонус. Контроль тонуса сосудов
Сосудистый тонус – напряжение сосудистой стенки, которое создается сокращением ее гладкомышечных клеток и изменяет диаметр просвета сосудов. Изменение сосудистого тонуса – главный механизм регуляции периферического и регионального сосудистого сопротивления. К активному изменению тонуса способны сосуды мышечного типа (мелкие артерии и вены, артериолы и венулы, сфинктеры).
Существует два вида сосудистого тонуса, принципиально различающихся механизмами его регуляции.
Центральный (нейрогенный) тонус регулируется вегетативной нервной системой. Иннервация сосудов в основном осуществляется симпатической нервной системой. Большинство сосудов внутренних органов, кожи содержат а-адренорецепторы. Через них осуществляется сосудосуживающее влияние нервной системы. Сосуды мозга и миокарда содержат в основном бета-адренорецепторы, через которые осуществляется сосудорасширяющее действие.
Периферический (базальный) тонус – напряжение сосудистом стенки, которое сохраняется после полной денервации сосудов. Это указывает на то, что помимо нервной системы существуют другие сосудодвигательные механизмы. Базальный тонус регулируется за счет воздействия вазоактивных тканевых метаболитов, эндотелиальных факторов, биологически активных веществ и гормонов. Кроме того, важную роль играет так называемая миогенная регуляция.

Миогенная регуляция сосудистого тонуса (эффект Бейлиса-Остроумова) основана на реакции гладкомышечных клеток сосудов на растяжение. Колебания АД изменяют растяжение стенки и гладкомышечных клеток сосудов. При повышении АД растяжение гладкомышечных клеток возрастает, но в ответ на растяжение происходит их сокращение и тонус артерий возрастает, они суживаются, сосудистое сопротивление увеличивается. Благодаря этому механизму повышение АД сопровождается сокращением гладкой мускулатуры артериол органов, в результате чего не допускается гиперперфузия органов. Напротив, при снижении АД, растяжение стенки сосудов ослабевает, гладкие мышцы сосудов расслабляются, что позволяет поддерживать региональное кровообращение в этих условиях.
Метаболическая регуляция сосудистого тонуса направлена на поддержание соответствия перфузии и метаболизма в органах. Большинство метаболитов энергетического обмена обладают выраженной вазодилатирующей активностью. Это аденозин, С02, молочная кислота, Н+ и другие. В интенсивно работающем органе продукты метаболизма накапливаются, резистивные сосуды расширяются и перфузия органа увеличивается. Этот же механизм действует, когда продукты метаболизма накапливаются из-за ухудшения притока крови к органу.
Эндотелиальная регуляция сосудистого тонуса осуществляется благодаря выработке эндотелиоцитами биологически активных веществ с сосудодвигательной активностью. Эндотелий вырабатывает соединения с дилататорным и констрикторным эффектом на тонус резистивных сосудов. Важнейшим эндотелиальным вазодилататором является оксид азота.
– Также рекомендуем “Гуморально-гормональная регуляция тонуса сосудов. Нейрогенная регуляция сосудов”
Оглавление темы “Норма и патология сосудов”:
1. Сосудистый тонус. Контроль тонуса сосудов
2. Гуморально-гормональная регуляция тонуса сосудов. Нейрогенная регуляция сосудов
3. Признаки изменения сосудистой резистентности. Упругость и эластичность сосудов
4. Пульсативность артерий. Винтовое движение крови
5. Доказательство винтового движения крови. Импульсно-волновая допплерография кровотока
6. Типовые нарушения регионального кровообращения. Артериальная гиперемия
7. Коллатеральный кровоток. Местные нарушения кровообращения
8. Гемодинамическая значимость сосудистых поражений. Факторы влияющие на значимость нарушений кровотока
9. Ультразвук. Характеристика и параметры ультразвука
10. Физические параметры ультразвука. Диагностический ультразвук
Источник
Оглавление темы “Сосудистый тонус. Эндотелий сосудов. Кровоснабжение головного мозга. Кровоснабжение сердца ( миокарда ).”: Базальный тонус сосудов. Растяжимость сосудов. Трансмуральное давление. Мобилизация крови из вен.Сосуды, лишенные нервных и гуморальных влияний, как оказалось, сохраняют (хотя и в меньшей мере) способность оказывать сопротивление кровотоку. Денервация сосудов скелетных мышц, например, увеличивает кровоток в них примерно в два раза, но последующее введение ацетилхо-лина в кровоток этой сосудистой области может вызвать дальнейшее десятикратное увеличение в ней кровотока, свидетельствующее о сохраняющейся в этом случае способности сосудов к вазодилатации. Для обозначения этой особенности денервированных сосудов оказывать сопротивление кровотоку введено понятие «базальный тонус сосудов». Базальный тонус сосудов определяется структурными и миогенными факторами. Структурная часть его создается жесткой сосудистой «сумкой», образованной коллагеновыми волокнами, которая определяет сопротивление сосудов, если активность их гладких мышц полностью исключена. Миогенная часть базального тонуса обеспечивается напряжением гладких мышц сосудов в ответ на растягивающее усилие артериального давления. Следовательно, изменения сопротивления сосудов под влиянием нервных или гуморальных факторов наслаиваются на базальный тонус, который для определенной сосудистой области более или менее постоянен. Если нервные и гуморальные влияния отсутствуют, а нейрогенный компонент сопротивления сосудов равен нулю, сопротивление их кровотоку определяется базальным тонусом.
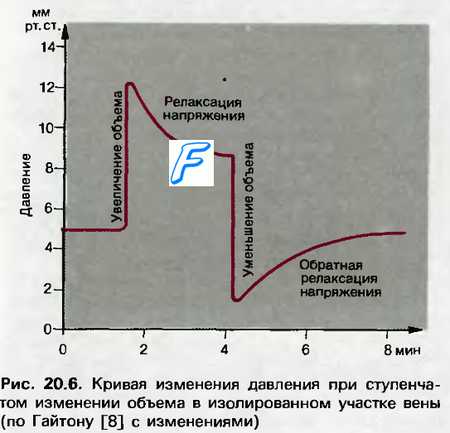
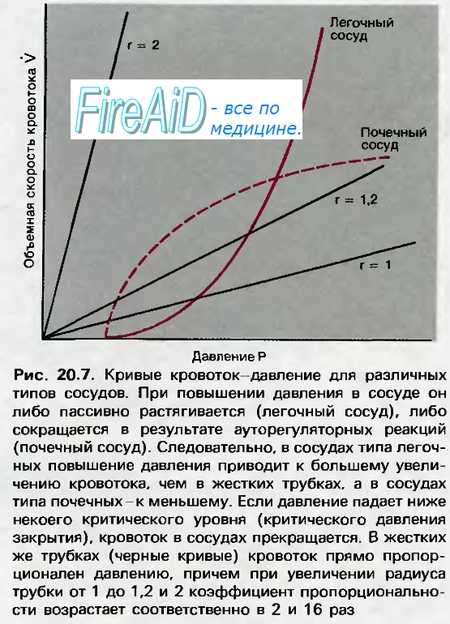
Поскольку одной из биофизических особенностей сосудов является их способность к растяжению, то при активной констрикторной реакции сосудов изменения их просвета находятся в зависимости от двух противоположно направленных влияний: сокращающихся гладких мышц сосудов, которые уменьшают их просвет, и повышенного давления в сосудах, которое их растягивает. Растяжимость сосудов различных органов значительно отличается. При повышении артериального давления только на 10 мм рт. ст. (со ПО до 120 мм рт. ст.) кровоток в сосудах кишечника увеличивается на 5 мл/мин, а в сосудах миокарда в 8 раз больше — на 40 мл/мин. На величине реакций сосудов могут сказываться и различия их исходного просвета. При этом имеет значение отношение толщины стенки сосуда к его просвету. Чем выше указанное отношение (стенка/просвет), т. е. чем больше масса стенки находится внутри «линии силы» укорочения гладких мышц, тем более выражено сужение просвета сосудов. В этом случае при одной и той же величине сокращения гладких мышц в артериальных и венозных сосудах уменьшение просвета всегда будет более выражено в артериальных сосудах, так как структурные «возможности» уменьшения просвета в большей степени присущи сосудам с высоким отношением стенка/просвет. На этой основе строится одна из теорий развития гипертонической болезни у человека. Изменения трансмурального давления (разность внутри- и внесосудистого давлений) влияют на просвет кровеносных сосудов и, следовательно, на их сопротивление кровотоку и содержание в них крови, что особенно сказывается в венозном отделе, где растяжимость сосудов велика и значительные изменения объема содержащейся в них крови могут иметь место при небольших сдвигах давления. Поэтому изменения просвета венозных сосудов будут вызывать соответствующие изменения трансмурального давления, что может привести к пассивно-эластической отдаче крови из этой области.
Следовательно, выброс крови из вен, возникающий при усилении импульсации в вазомоторных нервах, может быть обусловлен как активным сокращением гладкомышечных клеток венозных сосудов, так и их пассивно-эластической отдачей. Относительная величина пассивного выброса крови в этой ситуации будет зависеть от исходного давления в венах. Если исходное давление в них низкое, дальнейшее его уменьшение может вызвать спадение вен, ведущее к весьма выраженному пассивному выбросу крови. Нейрогенная констрикция вен в этой ситуации не вызовет сколько-нибудь значительного выброса из них крови и в результате может быть сделано ошибочное заключение, что нервная регуляция этого отдела незначительна. Напротив, если исходное трансмуральное давление в венах высокое, то уменьшение этого давления не повлечет за собой спадение вен и пассивно-эластическая их отдача будет минимальной. В этом случае активная констрикция вен вызовет значительно больший выброс крови и покажет истинное значение нейрогенной регуляции венозных сосудов. Пассивный компонент мобилизации крови из вен при низком давлении в них очень выражен, но становится весьма малым при давлении 5—10 мм рт. ст. В этом случае вены имеют циркулярную форму и выброс крови из них при нейрогенных влияниях обусловлен активными реакциями указанных сосудов. Однако при подъеме венозного давления выше 20 мм рт. ст. величина активного выброса крови вновь уменьшается, что является следствием «перенапряжения» гладкомышечных элементов венозных стенок. – Также рекомендуем “Депонирование крови. Причина головокружения ( обморока ) при вставании. Рабочая ( или функциональная ) гиперемия.” |
Источник
Гуморально-гормональная регуляция тонуса сосудов. Нейрогенная регуляция сосудов
Следует отметить, что одним из важных стимуляторов синтеза оксида азота является механическая деформация эндотелиальных клеток потоком крови – так называемая деформация сдвига эндотелия.
Помимо оксида азота эндотелий вырабатывает другие вазодилататоры: простациклин (простагландин I2), эндотелиальный фактор гиперполяризации, адреномедулин, натрийуретический пептид С-типа. В эндотелии функционирует калликреин-кининовая система, продуцирующая мощнейший пептидный дилататор брадикинин (Куликов В.П., Киселев В.И., Тезов А.А., 1987).
Эндотелий вырабатывает и вазоконстрикторы: эндотелины, тромбоксан (простагландин А2), ангиотензин II, простагландин Н2. Эндотелии 1 (ЕТ1) является наиболее мощным из всех известных вазоконстрикторов.
Эндотелиальные факторы влияют на адгезию и агрегацию тромбоцитов. Простациклин – важнейший антиагрегант, а тромбоксан, напротив, стимулирует адгезию и агрегацию тромбоцитов.
Нарушение этого баланса обозначается как дисфункция эндотелия, которая играет важную роль в патогенезе сердечно-сосудистых заболеваний. Важнейшими лабораторными маркерами дисфункции эндотелия являются эндотелины и фактор Виллебранда.
Гуморально-гормональная регуляция. В основном осуществляется посредством баланса активности прессорной ренин-ангиотензин-альдостероновой и депрессорной калликреин-кининовой систем крови. Эти системы связаны посредством ангиотензин превращающего фермента (АПФ). АПФ превращает неактивный ангиотензин I в ангиотензин II, который является вазоконстриктором и стимулирует выработку альдостерона в коре надпочечников, что сопровождается задержкой воды в организме и способствует подъему АД. Одновременно АПФ является основным ферментом разрушения брадикинина и таким образом устраняет его депрессорный эффект. Поэтому ингибиторы АПФ эффективно снижают АД при гипертензии, изменяя баланс систем в сторону кининовой.
Нейрогенная регуляция. Как уже отмечалось, ведущим эфферентным звеном в нейрогенном контроле сосудистого тонуса является симпатическая нервная система. Известна так называемая ишемическая реакция ЦНС. При значительном снижении системного АД возникает ишемия сосудодвигательного центра и активация симпатической нервной системы. Медиатором последней является норадреналин, вызывающий тахикардию (1-рецепторы) и увеличение тонуса сосудов (1 и 2-рецепторы).
Афферентное звено нейрогенной регуляции сосудистого тонуса представлено барорецепторами и хеморецепторами, расположенными в дуге аорты и каротидном синусе.
Барорецепторы реагируют на степень и скорость растяжения стенки сосудов. Хеморецепторы реагируют на изменение в крови концентрации СО2. Чувствительные волокна от барорецепторов и хеморецепторов дуги аорты и каротидного синуса проходят в составе синокаротидного нерва, ветвей языкоглоточного нерва и депрессорного нерва.
Нейрогенная регуляция обеспечивает постоянный (тонический) контроль над резистивными сосудами большинства сосудистых областей и экстренное рефлекторное регулирование, например, при приеме ортостатического положения. В этом и других случаях, когда давление в каротидном синусе и дуге аорты резко падает, включается каротидный барорефлекс, который через активацию барорецепторов и симпатическую нервную систему суживает сосуды, активирует работу сердца и обеспечивает подъем АД. Барорецепторный рефлекс срабатывает, наоборот, на повышение АД, что обеспечивает его снижение через торможение симпатических влияний и активацию блуждающего нерва. Хеморецепторный рефлекс обеспечивает подъем артериального давления посредством активации симпатических влияний в условиях гипоксии, когда в крови накапливается углекислым газ.
– Также рекомендуем “Признаки изменения сосудистой резистентности. Упругость и эластичность сосудов”
Оглавление темы “Норма и патология сосудов”:
1. Сосудистый тонус. Контроль тонуса сосудов
2. Гуморально-гормональная регуляция тонуса сосудов. Нейрогенная регуляция сосудов
3. Признаки изменения сосудистой резистентности. Упругость и эластичность сосудов
4. Пульсативность артерий. Винтовое движение крови
5. Доказательство винтового движения крови. Импульсно-волновая допплерография кровотока
6. Типовые нарушения регионального кровообращения. Артериальная гиперемия
7. Коллатеральный кровоток. Местные нарушения кровообращения
8. Гемодинамическая значимость сосудистых поражений. Факторы влияющие на значимость нарушений кровотока
9. Ультразвук. Характеристика и параметры ультразвука
10. Физические параметры ультразвука. Диагностический ультразвук
Источник