От чего лопаются сосуды в печени
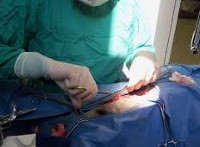
Травма печени – одно из наиболее тяжелых, трудно диагностируемых и опасных для жизни пациента абдоминальных повреждений. Обычно сопровождается массивным кровотечением из ткани печеночной паренхимы и крупных сосудов печени. Возможно также излитие желчи в брюшную полость с последующим развитием желчного перитонита. Причиной такой травмы может стать автокатастрофа, падение с высоты, удар в область живота, ножевое или огнестрельное ранение и т. д. Наблюдаются симптомы острой кровопотери в сочетании с болью и напряжением мышц в области правого подреберья. Подозрение на повреждение печени является показанием для немедленной доставки больного в стационар. Лечение хирургическое, производится в экстренном порядке. Объем оперативного вмешательства и прогноз зависит от характера и тяжести травмы печени.
Общие сведения
Травма печени – опасное для жизни пациента повреждение, сопровождающееся внутренним кровотечением. В отсутствие специализированной помощи смерть в большинстве случаев наступает от потери крови. При небольшом кровотечении через некоторое время развивается перитонит, обычно желчный. Малейшее подозрение на травму печени является показанием для срочной транспортировки пациента в специализированное мед. учреждение, детального обследования и, при подтверждении диагноза – экстренного оперативного лечения.
Травмы печени составляют чуть более 20% от общего количества повреждений органов брюшной полости. Из них 18,7% приходится на закрытые повреждения и 81,3 – на открытые. Повреждения печени редко бывают изолированными и, как правило (в 77,6% случаев) наблюдаются при множественных или сочетанных травмах.

Травмы печени
Классификация травм печени
Специалистами в области травматологии все травмы печени делятся на открытые и закрытые.
Закрытые повреждения в свою очередь подразделяются на несколько групп:
С учетом механизма травмы: полученные вследствие непосредственного удара в живот, дорожной травмы, падения с высоты и сдавления между двумя предметами. Кроме того, в эту группу относят разрывы, возникающие вследствие напряжения брюшного пресса – такая патология может наблюдаться у новорожденных, а также у пациентов с патологически измененной печенью.
С учетом характера повреждения: чрезкапсулярные разрывы (повреждения с нарушением целостности капсулы), субкапсулярные разрывы (подкапсульные повреждения), гематомы печени или центральные разрывы (нарушение целостности ткани в центре органа при неизмененных периферических отделах), повреждения сосудов печени и внепеченочных желчных путей.
С учетом степени повреждения: разрывы глубиной до двух сантиметров и поверхностные трещины, разрывы глубиной менее половины толщи печени, разрывы глубиной более половины толщи печени, множественные разрывы с расчленением органа на отдельные фрагменты, а также размозжение частей органа.
С учетом наличия или отсутствия повреждения внутрипеченочных структур: с поражением или без поражения желчных протоков, внутри- и внепеченочных сосудов.
Кроме того, закрытую травму печени классифицируют с учетом локализации повреждения (нарушения целостности сегментов или долей).
Открытые травмы печени, как и закрытые, подразделяются на группы с учетом характера, локализации и объема повреждения. Кроме того, в этом случае учитывается вид ранения: колотое, резаное, рубленое, огнестрельное (дробовое, пулевое или осколочное) и т. д. Как правило, такие травмы печени сочетаются с повреждением других органов брюшной полости.
Закрытые травмы печени
Особенности повреждения зависят от механизма травмы. При прямом ударе чаще возникают разрывы нижней поверхности или одновременно нижней и верхней. При сдавлении и противоударе чаще страдает верхняя поверхность органа. При этом для сдавления характерны не только множественные линейные разрывы, но и очаги размозжения.
При переломах ребер справа внизу возможно разрушение части печени внедрившимся в нее отломком. Падение с большой высоты может стать причиной отрыва органа от его связочного аппарата. Центральные и подкапсульные гематомы образуются преимущественно при резком перегибе или крутом повороте туловища.
Состояние больного тяжелое, быстро ухудшающееся. Наблюдаются симптомы травматического шока и внутреннего кровотечения. Дыхание по грудному типу, кожные покровы бледные, отмечается вялость, холодный пот, снижение АД и тахикардия. При этом быстрое нарастание тахикардии является прогностически неблагоприятным признаком.
Пациент жалуется на усиливающиеся боли в правом подреберье. Часто отмечается иррадиация в правую надключичную область. Резко выраженный болевой синдром в первые часы после повреждения для изолированных травм печени нехарактерен – его наличие может свидетельствовать об одновременном нарушении целостности полого органа.
Пальпация правого подреберья болезненна, выявляется умеренное напряжение мышц и тупость при перкуссии. Определяется положительный симптом Щеткина-Блюмберга. В анализах крови – нарастающая анемия при быстром увеличении количества лейкоцитов.
Без экстренной медицинской помощи пациент обычно погибает от кровотечения в первые часы или сутки после травмы печени. При небольших повреждениях больной может выжить, однако на 2-3 день в таких случаях развивается перитонит, вызванный излитием желчи или крови в брюшную полость.
Центральные и субкапсулярные гематомы на начальной стадии протекают более благоприятно. Однако на 1-3 сутки гематома может разорваться, что влечет за собой обильное кровоизлияние в брюшную полость. Такие травмы печени носят название двухфазных разрывов.
Диагностика закрытых травм печени достаточно сложна, особенно – при сочетанных и множественных травмах, когда есть другие, более заметные повреждения, обуславливающие кровотечение и развитие травматического шока. Еще одним фактором, затрудняющим постановку диагноза, являются нарушения сознания, вызванные тяжелым шоком, массивной кровопотерей, черепно-мозговой травмой или алкогольным опьянением.
Диагноз выставляется на основании осмотра пациента, данных анализов крови и дополнительных исследований. Для выявления повреждения может использоваться УЗИ, компьютерная томография и ангиография. Наиболее информативным методом исследования является лапароскопия. Во время этой процедуры в брюшную полость через небольшой разрез вводится эндоскоп, через который можно непосредственно осмотреть различные органы, установить факт кровотечения и выявить его источник, а также примерно оценить объем кровопотери.
Лечение закрытых травм печени оперативное, проводится в экстренном порядке. Выжидательная тактика используется только в тех редких случаях, когда повреждение не удается четко диагностировать, кровопотеря незначительна и не увеличивается.
В ходе операции выполняется ревизия печени. Небольшие разрывы и трещины ушивают. При глубоких разрывах и обильном кровотечении предварительно производят перевязку поврежденных сосудов. При размозжении выполняют резекцию печени. При тяжело останавливаемом кровотечении осуществляют тампонаду с использованием мышцы или сальника больного либо гемостатической губки. Брюшную полость промывают, рану зашивают.
Хирургическое вмешательство проводят на фоне переливания крови и кровезаменителей. Если внутренние органы не повреждены, возможно переливание собранной в брюшной полости и предварительно отфильтрованной крови.
Открытые травмы печени
Открытые травмы печени часто сочетаются с повреждением других органов (легких, желудка и поперечно-ободочной кишки). Для колотых и резаных ран характерно обильное наружное кровотечение, для огнестрельных – массивные повреждения с разрывом и контузией органа на значительном протяжении. Кровотечение при открытых травмах печени, как правило, более интенсивное, чем при закрытых. Прогноз неблагоприятный, особенно – при обширной травме, запоздалой специализированной помощи и одновременном повреждении легких.
Показано экстренное хирургическое вмешательство. Операцию проводят незамедлительно, не дожидаясь купирования симптомов травматического шока. В ходе операции осуществляется переливание крови.
При колотых и резаных ранениях выполняют ушивание раны печени. При огнестрельных ранениях производится удаление инородных тел и иссечение нежизнеспособных участков печеночной паренхимы с последующим ушиванием.
Источник
Варикозное расширение вен пищевода и желудка находят у 60% больных циррозом печени, из которых 25% погибают от острых пищеводно-желудочно-кишечных кровотечений. Острое кровотечение из варикозно расширенных вен пищевода и кардии – наиболее частая причина пищеводно-желудочно-кишечных кровотечений и непосредственная причина смерти 1/3 больных циррозом печени. Сопутствующие циррозу печени эрозивно-язвенные поражения верхних отделов пищеварительного канала в редких случаях и обычно в терминальном периоде заболевания являются причиной обильных желудочно-кишечных кровотечений. Продолжительность жизни больных циррозом печени с варикозным расширением вен пищевода зависит от стадии варикоза и степени активности патологических изменений в печени и колеблется от 1,5 до 25 лет.
Летальность после первого кровотечения составляет от 30 до 60%. На фоне кровотечения резко ухудшается функциональная способность печени, часто образуются массивные гипоксические некрозы в ней. При кровотечениях у больных возникают или нарастают желтуха, энцефалопатия, прогрессивно ухудшаются показатели функциональных проб печени, хотя при этом величина асцита и размеры селезенки могут уменьшаться в связи с переходом асцитической жидкости в сосудистое русло и снижением портального давления.
Кровотечение возникает в периоде портального гипертонического криза, когда внезапное повышение портального давления вызывает разрыв аневризм расширенной пищеводной или желудочной вены. Вероятность кровотечения положительно коррелирует с размерами варикозных узлов: в I стадии при эндоскопии видны линейные розовато-голубые вены в слизистой оболочке диаметром менее 2 мм, во II стадии – выдающиеся в просвет синеватые флебэктазии с нодулярными выпячиваниями диаметром 2-3 мм; в III стадии – узловато-извитые синие змеевидные стволы, часто доходящие до свода желудка и выступающие в просвет пищевода до середины его диаметра; в IV стадии – гроздевидные, заполняющие почти весь просвет пищевода темно-синие сосудистые пучки диаметром более 4 мм.
Наибольший риск острого кровотечения из варикозно расширенных вен пищевода и желудка отмечается у больных (с более чем 15-20 мм) расширенной венечной веной желудка, определяемой при ангиографии. Причиной повышения портального давления чаще всего является тяжелая сосудистая и паренхиматозная декомпенсация цирроза печени. У больных с отечно-асцитическим синдромом кровотечения развиваются значительно чаще, чем у больных циррозом без асцита, и в 2 раза чаше заканчивается летальным исходом. Прогноз кровотечения относительно благоприятный у больных в доасцитическую стадию, без желтухи и с нормальным уровнем альбумина крови и неблагоприятен при наличии асцита, гипокалиемии, алкалоза, выраженной гепатоцеллюлярной недостаточности и активности воспалительного процесса в печени (уровень билирубина крови > 51 мкмоль/л, альбумина < 30 г/л, протромбиновый индекс < 40%, активность АсАТ > 1,1 мкмоль/л/ч) и при значительных кровопотерях, требующих для возмещения более 2 л крови или ее заменителей в комплексе с эритроцитной массой. У 15% больных циррозом печени острое массивное кровотечение из верхних отделов пищеварительного канала бывает первым проявлением латентно протекавшего заболевания. У них в отличие от больных с неповрежденной печенью при кровотечении из язвы желудка или двенадцатиперстной кишки или из других источников часто имеет место гипераммониемия. Это следствие эндогенной нагрузки катаболитами белка из-за скопления крови и продуктов ее распада в толстой кишке. После впервые возникшего кровотечения возрастает риск повторных кровотечений.
Классически кровотечение проявляется рвотой темной венозной кровью или «кофейной гущей». Первоначально может возникнуть необильная рвота, а спустя 0,5-1 ч появляется обильная кровавая рвота до 1,5-2 л и более крови. Через несколько часов появляется жидкий или вязкий дегтеобразный стул – мелена. Возможна спонтанная остановка кровотечения в пределах 12-24 ч с его повторением через 7-14 дней. Иногда первым и единственным симптомом бывает мелена. В таком случае кровотечение развивается исподволь, значительных нарушений гемодинамики в течение первых суток после начала кровотечения может не быть.
При эндоскопии через 6-12 ч после начала кровотечения разрыв варикозной вены у 70% больных определяется на уровне гастроэзофагеального перехода или над ним. У части больных кровоточат расширенные вены проксимальных отделов малой кривизны желудка под переходом в пищевод или вены нижней трети пищевода. Редкими причинами кровотечений из верхних отделов пищеварительного канала у больных циррозом являются острые и хронические язвы или эрозии, геморрагический гастрит или эзофагит и синдром Мэллори-Вейса (разрыв слизистой оболочки в области пищеводно-желудочного соустья при длительной неукротимой рвоте).
При проведении эзофагогастродуоденоскопии при кровотечениях необходимо проявлять осторожность в отношении введения больших доз седативных препаратов из-за опасности прогрессирования энцефалопатии и аспирации крови в бронхиальное дерево легких. Эндоскопию при нарастающих кровотечениях следует выполнять после восстановления объема крови путем экстренного введения в вену плазмозамещающих растворов и одногруппной крови, эритроцитной массы с раствором альбумина или реополиглюкина. Перед эндоскопией желудок промывают несколькими литрами воды для удаления скопившейся в нем крови и сгустков.
Источник
Сосудистые заболевания печени могут быть обусловлены поражением различных звеньев ее кровеносной сети: капилляров (синусоидов), артериального русла (от уровня крупных артерий до артериол), сосудов системы воротной вены (от крупных ветвей до венул) и венозной системы (от центральных до печеночных вен).
Патология микроциркуляторного русла имеет характер диффузного поражения паренхимы, тогда как вовлечение крупных кровеносных стволов – ограниченного.
В лекции освещены лишь заболевания сосудов портальной системы и печеночных вен. Главное внимание уделено тромбозу.
Поражение сосудов системы воротной вены
К ним относятся развитие внутрипеченочной портокавальной фистулы и обструкция воротной вены и ее ветвей.
Внутрипеченочные портокавальные фистулы чаще развиваются на фоне портальной гипертензии. Крайне редко встречаются врожденные фистулы. При шунтировании большого объема крови (свыше 60%) из системы воротной вены возможно появление энцефалопатии.
Уменьшение притока крови по системе воротной вены способно приводить к нодулярной перестройке структуры печени, напоминающей множественную фокальную узловую регенераторную гиперплазию.
Целесообразно различать обструкцию основного ствола воротной вены и обструкцию ее ветвей. Развитию последней могут способствовать четыре различных фактора, из которых два первых встречаются наиболее часто:
- хронические заболевания печени, сопровождающиеся портальным воспалением и фиброзом;
- шистосомоз, осложнившийся эмболизацией ветвей воротной вены яйцами паразитов и обструкцией гранулемами и разрастаниями соединительной ткани;
- недостаточно изученное состояние, при котором развивается, как предполагают, первичная облитерация портальных венул (“нецирротическая портальная гипертензия”, “печеночно-портальный цирроз”, “идиопатическая портальная гипертензия”);
- врожденный фиброз печени, наследуемый по аутосомно-рецессивному типу.
Обструкция крупных печеночных вен может быть вызвана их воспалительной компрессией, например, при панкреатите, сдавлением и прорастанием опухолью печени, желчных протоков, поджелудочной железы. Это наиболее частые причины нарушений портального кровотока.
Альтернативный механизм – тромбоз, который обозначается терминами
“пилефлебит” – в острую фазу и “кавернома” – в хроническую.
Согласно современным воззрениям, венозный тромбоз является суммирующим результатом врожденных или приобретенных прокоагулянтных нарушений и действия местных факторов.
Перечень врожденных расстройств свертывания крови включает дефицит естественных ингибиторов свертывания, факторов II и V, тогда как к приобретенным расстройствам можно отнести миелопролиферативные заболевания, антифосфолипидный синдром, пароксизмальную ночную гемоглобинурию; они также сопровождают воспалительные и онкологические заболевания и отмечаются на фоне применения пероральных контрацептивов, беременности, гипергомоцистеинемии.
Для выявления миелопролиферативного заболевания могут потребоваться специальные методы. У 60% больных при тромбозе вен внутренних органов отмечается гиперкоагуляция, у 25% первостепенное значение имеет влияние локальных факторов. Комбинация действия причинных факторов при тромбозе воротной вены обнаруживается в 30 раз чаще, чем в его отсутствие. В 20% случаев развитие тромбоза не находит исчерпывающего объяснения.
По нашему опыту, миелопролиферативные заболевания и дефицит протеина S являются ведущими этиологическими факторами тромбоза в системе воротной вены. Каждый из них выявляется примерно у четверти пациентов.
Кровоснабжение кишечника выше уровня тромбоза портальной вены (по ходу кровотока) сохраняется удовлетворительным до тех пор, пока сохраняется кровоток по дугообразным сосудам кишечника. Если же они тромбируются, развивается ишемия кишки. Этому, вероятно, способствует отсутствие сосудистых коллатералей.
Последствием ишемии может явиться некроз кишки с развитием перитонита, полиорганной недостаточности, а в четверти случаев – летальный исход даже после резекции некротизированного участка кишки.
Напротив, ниже уровня тромбоза не развивается клинически значимых нарушений функции печени, поскольку ее кровоснабжение поддерживается благодаря увеличению притока крови по печеночной артерии (вследствие расширения ее ветвей) и развитию портальных коллатералей (которые, очевидно, образуют так называемую каверному). Портальный кровоток поддерживается за счет повышения перфузионного давления.
Клинические проявления нарушений венозного кровотока в 90-х годах изменились. Доля пациентов, у которых отмечались боли в животе, возросла, тогда как доля больных с пищеводными кровотечениями уменьшилась. Это можно объяснить повышением эффективности ранней диагностики благодаря совершенствованию методов визуализации.
Распознавание тромбозов облегчилось благодаря применению спиральной компьютерной томографии и ультразвукового сканирования. Желудочно-кишечное кровотечение и рецидивирующий тромбоз – основные клинические проявления тромбоза воротной вены, обусловливающие в ряде случаев летальный исход.
Современные способы ведения больных с синдромом портальной гипертензии с применением фармакологических или эндоскопических методов продемонстрировали свою эффективность в лечении и предупреждении желудочно-кишечных кровотечений. В то же время терапия антикоагулянтами считается безопасным и эффективным методом профилактики рецидивов тромбоза. Она способствует также восстановлению кровотока на ранних стадиях тромбоза.
Нарушение кровотока по печеночным венам
Нарушения этого типа обычно развиваются вследствие обструкции печеночных вен. Термину “нарушение венозного оттока от печени” целесообразно отдавать предпочтение перед термином “синдром Бадда-Киари” для обозначения обструкции печеночных венул, вен или терминальной части нижней полой вены.
Обструкция, ограниченная уровнем печеночных венул, может развиваться по одному или двум механизмам: как нетромботическая окклюзия (веноокклюзионная болезнь) и как тромбоз.
Веноокклюзионная болезнь обычно обусловлена воздействием токсических факторов:
- подготовкой к пересадке костного мозга с применением химио- и лучевой терапии;
- иммуносупрессивной терапии азатиоприном и кортикостероидами после трансплантации;
- приемом некоторых растительных алкалоидов.
Тромбоз печеночных венул развивается очень редко.
Обструкцию крупных вен печени могут вызвать механическое сдавление, в том числе воспалительным инфильтратом (например, при амебном абсцессе печени), прорастание злокачественной опухолью, инвазия эхинококка. Однако наиболее частой причиной нарушения оттока крови по печеночным венам является тромбоз.
Выделяют три разновидности тромбоза в зависимости от стадии, на которой выявляют свежий тромб, локальное фиброзное сужение, полную облитерацию вены.
Установленные на сегодняшний день причинные факторы тромбоза печеночных вен сходны с таковыми при тромбозе воротной вены, хотя при этих состояниях их частота различна. Главное значение имеют миелопролиферативные заболевания, дефицит протеина С, фактора V и антифосфолипидный синдром. Локальные факторы выявляются редко. Применение пероральных контрацептивов и беременность могут усиливать влияние скрытого причинного фактора.
Обструкция печеночных вен может иметь два последствия:
- нарастание давления в синусоидах вызывает развитие синдрома портальной гипертензии, увеличение продукции лимфы, что приводит к накоплению в брюшной полости богатой белком асцитической жидкости и развитию коллатералей, функция которых заключается в обходе сдавленных печеночных вен и сохранении перфузии печени;
- внезапное нарушение оттока крови по печеночным венам ведет к развитию ишемических некрозов и печеночной недостаточности.
Неравномерным нарушением печеночной перфузии можно объяснить развитие активной регенерации ткани печени в областях с поддерживаемым уровнем перфузии. Это обстоятельство приводит к ее крупноузловой трансформации.
Тромбоз печеночных вен может иметь длительное бессимптомное течение. Не отмечено четкой корреляции между выраженностью клинических и патоморфологических изменений. Остро возникающие клинические проявления обычно обусловлены острыми нарушениями кровоснабжения, наслаивающимися на уже имеющиеся хронические.
Существуют три основных варианта клинических проявлений нарушения оттока крови по венам печени:
- острый – включает появление болей в верхних отделах живота, увеличение печени, уровня активности сывороточных аминотрансфераз, снижение активности свертывающей системы крови, нарушение функции почек;
- хронический – встречается наиболее часто, проявляется как хроническое заболевание печени в фазе декомпенсации;
- бессимптомный – тромбоз печеночных вен выявляется случайно.
Рост числа больных с бессимптомным течением связан, по-видимому, с совершенствованием диагностических методов визуализации и с пониманием сути заболевания. В течении болезни может либо наступить полная спонтанная ремиссия с вероятностью рецидива, либо заболевание непрерывно прогрессирует.
У половины пациентов 10-летняя выживаемость составляет более 90%, у остальных летальность в течение 10 лет составляет 50%; большая часть летальных исходов регистрируется в первые 12-18 мес с момента развития симптоматики.
Прогноз у больного с тромбозом печеночных вен обычно определяется сопутствующим тромбозом воротной вены. Из других (независимых) факторов, определяющих прогноз, важное значение имеют возраст и степень нарушения функций печени по классификации Чайльда-Пью.
Вследствие того что эта патология не является распространенной, эффективность различных методов лечения тромбоза печеночных вен требует дальнейшего изучения. Таким больным логично назначать антикоагулянты.
Особенности симптоматической терапии по поводу кровотечений, портальной гипертензии и асцита также необходимо исследовать. У пациентов с клинически манифестной формой болезни следует попытаться восстановить отток крови по венам консервативными методами лечения, такими, как чрескожная ангиопластика с установкой стентов (при непротяженных стенозах печеночных вен или нижней полой вены).
К настоящему времени не доказаны эффективность и безопасность восстановления венозного кровотока с помощью тромболитических средств при свежем тромбозе.
В качестве меры, облегчающей проявление клинической симптоматики, при отсутствии печеночной недостаточности можно предложить портокавальное шунтирование. Однако маловероятно, что это вмешательство способно продлить жизнь пациента.
Определенные надежды связаны с таким относительно новым методом лечения, как трансъюгулярный портосистемный шунт (TIPS). По предварительным оценкам, трансплантация печени в наиболее тяжелых случаях позволяет повысить 10-летнюю выживаемость пациентов с 50 до 70%.
Источник
