Плацента из двух сосудов
Оглавление темы “Система нижней полой вены.”:
1. Система нижней полой вены. Нижняя полая вена ( v. cava inferior ).
2. Воротная вена ( v. portae ). Вены образующие воротную вену.
3. Общие подвздошные вены ( Vv. iliacae communes ).
4. Внутренняя подвздошная вена ( v. iliaca interna ).
5. Портокавальные и каво-кавальные анастомозы. “Голова медузы.”
6. Наружная подвздошная вена ( v. iliaca externa ).
7. Вены нижней конечности ( ноги ). Глубокие и поверхностные вены ноги.
8. Закономерности распределения вен.
9. Особенности кровообращения плода. Плацентарное кровообращение.
10. Рентгенологическое исследование кровеносных сосудов.
Особенности кровообращения плода. Плацентарное кровообращение
Кислород и питательные вещества доставляются плоду из крови матери при помощи плаценты – плацентарное кровообращение. Оно происходит следующим образом. Обогащенная кислородом и питательными веществами артериальная кровь поступает из плаценты матери в пупочную вену, которая входит в тело плода в области пупка и направляется вверх к печени, ложась в ее левую продольную борозду. На уровне ворот печени v. umbilicalis делится на две ветви, из которых одна тотчас впадает в воротную вену, а другая, называемая ductus venosus, дроходит по нижней поверхности печени до ее заднего края, где впадает в ствол нижней полой вены.
Тот факт, что одна из ветвей пупочной вены доставляет печени через воротную вену чистую артериальную кровь, обусловливает относительно большую величину печени; последнее обстоятельство связано с необходимой для развивающегося организма функцией кроветворения печени, которая преобладает у плода и уменьшается после рождения. Пройдя через печень, кровь по печеночным венам вливается в нижнюю полую вену.
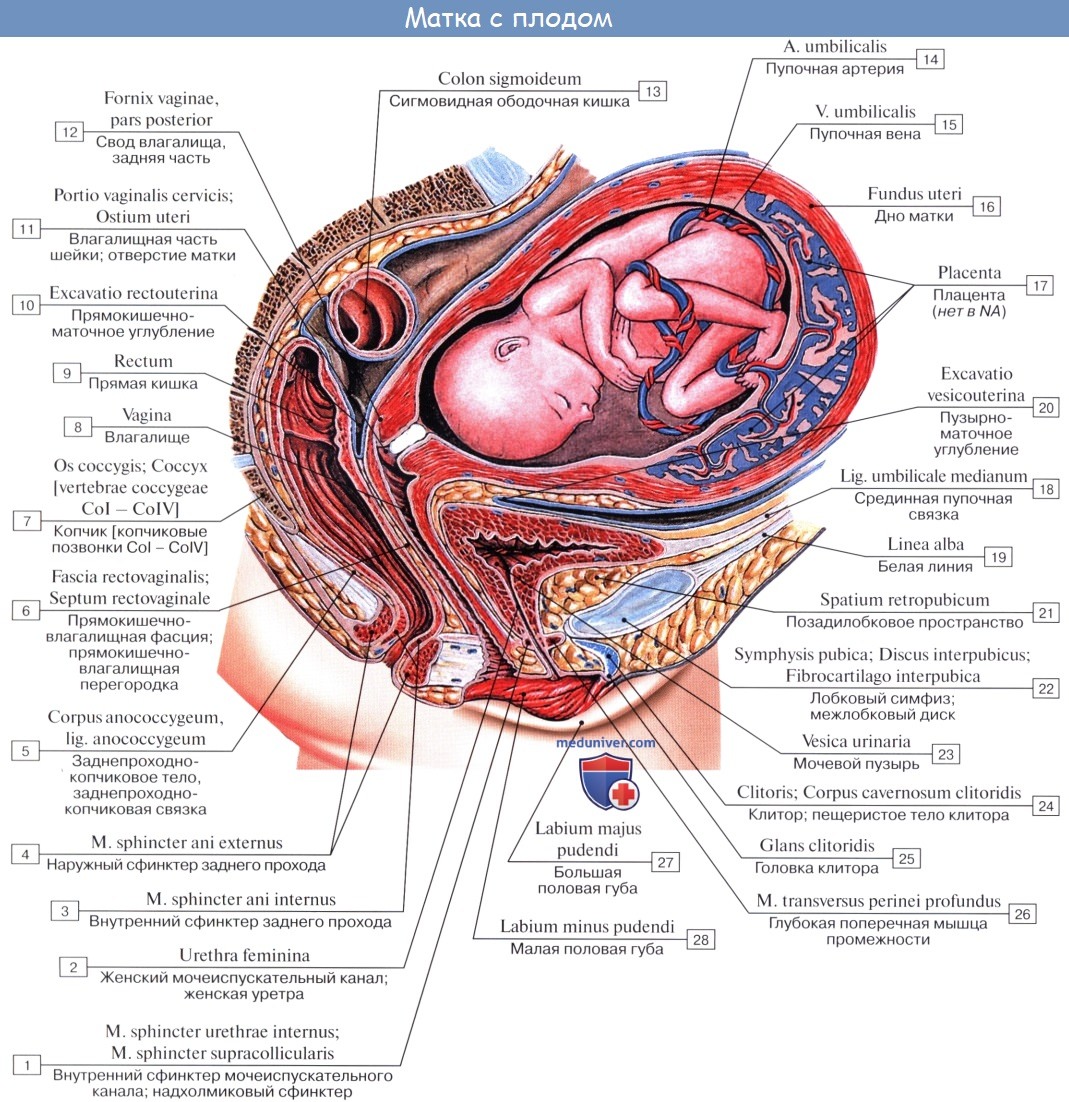
Таким образом, вся кровь из v. umbilicalis или непосредственно (через ductus venosus), или опосредованно (через печень) попадает в нижнюю полую вену, где примешивается к венозной крови, оттекающей по vena cava inferior от нижней половины тела плода.
Смешанная (артериальная и венозная) кровь по нижней полой вене течет в правое предсердие. Из правого предсердия она направляется заслонкой нижней полой вены, valvula venae cavae inferioris, через foramen ovale (расположенно в перегородке предсердий) в левое предсердие. Из левого предсердия смешанная кровь попадает в левый желудочек, затем в аорту, минуя не функционирующий еще легочный круг кровообращения.
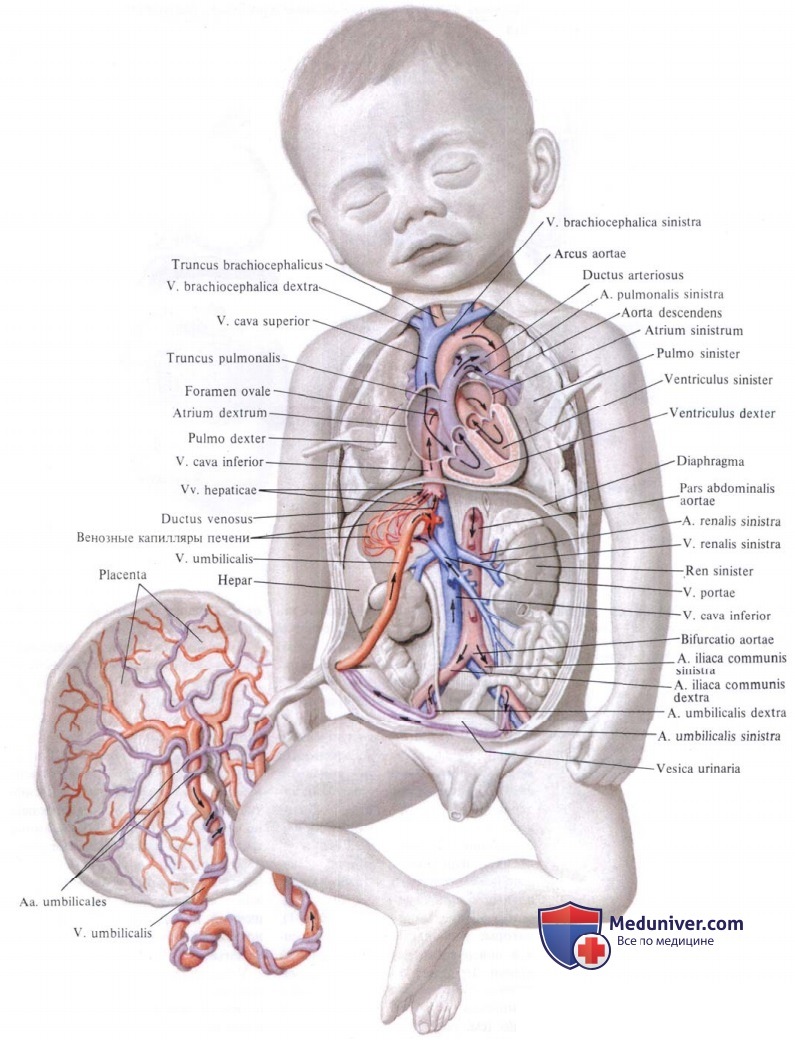
В правое предсердие впадают, кроме нижней полой вены, еще верхняя полая вена и венозный (венечный) синус сердца. Венозная кровь, поступающая в верхнюю полую вену от верхней половины тела, далее попадает в правый желудочек, а из последнего в легочный ствол. Однако, вследствие того что легкие еще не функционируют как дыхательный орган, только незначительная часть крови поступает в паренхиму легких и оттуда по легочным венам в левое предсердие. Большая часть крови из легочного ствола по ductus arteriosus переходит в нисходящую аорту и оттуда к внутренностям и нижним конечностям.
Таким образом, несмотря на то что вообще по сосудам плода течет смешанная кровь (за исключением v. umbilicalis и ductus venosus до его впадения в нижнюю полую вену), качество ее ниже места впадения ductus arteriosus значительно ухудшается. Следовательно, верхняя часть тела (голова) получает кровь, более богатую кислородом и питательными веществами. Нижняя же половина тела питается хуже, чем верхняя, и отстает в своем развитии. Этим объясняются относительно малые размеры таза и нижних конечностей новорожденного.
Акт рождения представляет скачок в развитии организма, при котором происходят коренные качественные изменения жизненно важных процессов. Развивающийся плод переходит из одной среды (полость матки с ее относительно постоянными условиями: температура, влажность и пр.) в другую (внешний мир с его меняющимися условиями), в результате чего коренным образом изменяются обмен веществ, а также способы питания и дыхания. Вместо питательных веществ, получаемых ранее через кровь, пища поступает в пищеварительный тракт, где она подвергается пищеварению и всасыванию, а кислород начинает поступать не из крови матери, а из наружного воздуха благодаря включению органов дыхания. Все это отражается и на кровообращении.
При рождении происходит резкий переход от плацентарного кровообращения к легочному. При первом вдохе и растяжении легких воздухом легочные сосуды сильно расширяются и наполняются кровью. Тогда ductus arteriosus спадается и в течение первых 8 – 10 дней облитерируется, превращаясь в ligamentum arteriosum.
>Пупочные артерии зарастают в течение первых 2 – 3 дней жизни, пупочная вена – несколько позднее (6 – 7 дней). Поступление крови из правого предсердия в левое через овальное отверстие прекращается тотчас после рождения, так как левое предсердие наполняется кровью, поступающей сюда из легких, и различие в давлении крови между правым и левым предсердиями выравнивается. Закрытие овального отверстия происходит значительно позднее, чем облитерация ductus arteriosus, и часто отверстие сохраняется в течение первого года жизни, а в 1/3 случаев – всю жизнь. Описанные изменения подтверждены исследованием на живом с помощью рентгеновских лучей.
Учебное видео анатомия кровообращения у плода
N!B! На видео – 4:02 ОШИБКА: “Лёгочные вены несут артериальную кровь из лёгких в правое предсердие.”
ВЕРНО: Лёгочные вены несут артериальную кровь из лёгких в ЛЕВОЕ предсердие.
На видео всё правильно, но комментатор перепутал. Другие видео уроки по данной теме находятся: Здесь
– Также рекомендуем “Рентгенологическое исследование кровеносных сосудов.”
Источник

Журнал “SonoAce Ultrasound”
Содержит актуальную клиническую информацию по ультрасонографии и ориентирован на врачей ультразвуковой диагностики, выходит с 1996 года.
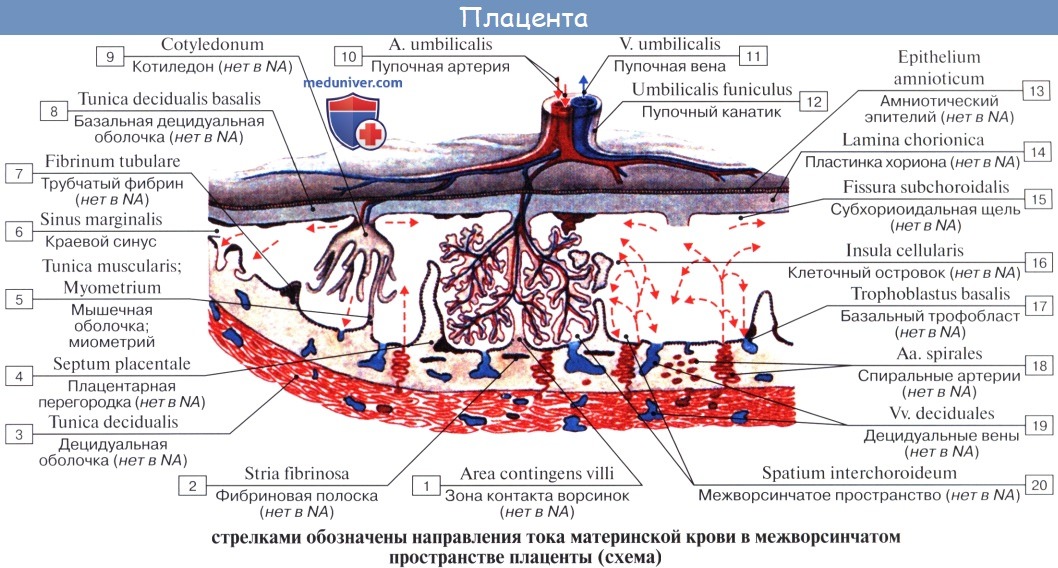
С самого начала беременности и вплоть до ее окончания формируется и функционирует система мать-плацента-плод. Важнейшим компонентом этой системы является плацента, которая представляет собой комплексный орган, в формировании которого принимают участие производные трофобласта и эмбриобласта, а также децидуальная ткань. Функция плаценты, в первую очередь, направлена на обеспечение достаточных условий для физиологического течения беременности и нормального развития плода. К этим функциям относятся: дыхательная, питательная, выделительная, защитная, эндокринная. Все метаболические, гормональные, иммунные процессы во время беременности обеспечиваются через сосудистую систему матери и плода. Несмотря на то, что кровь матери и плода не смешивается, так как их разделяет плацентарный барьер, все необходимые питательные вещества и кислород плод получает из крови матери. Основным структурным компонентом плаценты является ворсинчатое дерево.
При нормальном развитии беременности имеется зависимость между ростом плода, его массой тела и размерами, толщиной, массой плаценты. До 16 недель беременности развитие плаценты опережает темпы роста плода. В случае смерти эмбриона (плода) происходит торможение роста и развития ворсин хориона и прогрессирование инволюционно-дистрофических процессов в плаценте. Достигнув необходимой зрелости в 38-40 недель беременности, в плаценте прекращаются процессы образования новых сосудов и ворсин.
Схема структуры плаценты и маточно плацентарного кровообращения
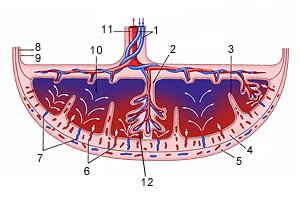
1 – артерии пуповины
2 – стволовая ворсина
3 – децидуальная перегородка
4 – децидуальный слой
5 – миометрий
6 – вены
7 – спиральные артерии
8 – хорион
9 – амнион
10 – межворсинчатое пространство
11 – вена пуповины
12 – котиледон
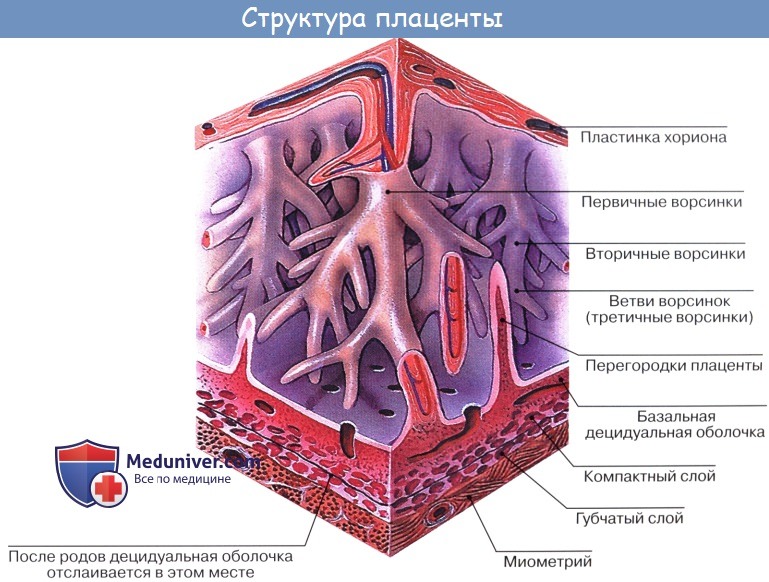
Зрелая плацента представляет собой дискообразную структуру диаметром 15-20 см и толщиной 2,5 – 3,5 см. Ее масса достигает 500-600 гр. Материнская поверхность плаценты, которая обращена в сторону стенки матки, имеет шероховатую поверхность, образованную структурами базальной части децидуальной оболочки. Плодовая поверхность плаценты, которая обращена в сторону плода, покрыта амниотической оболочкой. Под ней видны сосуды, которые идут от места прикрепления пуповины к краю плаценты. Строение плодовой части плаценты представлено многочисленными ворсинами хориона, которые объединяются в структурные образования – котиледоны. Каждый котиледон образован стволовой ворсиной с разветвлениями, содержащими сосуды плода. Центральная часть котиледона образует полость, которая окружена множеством ворсин. В зрелой плаценте насчитывается от 30 до 50 котиледонов. Котиледон плаценты условно сравним с деревом, в котором опорная ворсина I порядка является его стволом, ворсины II и III порядка – крупными и мелкими ветвями, промежуточные ворсины – маленькими ветками, а терминальные ворсины – листьями. Котиледоны отделены друг от друга перегородками (септами), исходящими из базальной пластины.
Межворсинчатое пространство с плодовой стороны образовано хориальной пластиной и прикрепленными к ней ворсинами, а с материнской стороны оно ограничено базальной пластиной, децидуальной оболочкой и отходящими от неё перегородками (септами). Большинство ворсин плаценты свободно погружены в межворсинчатое пространство и омываются материнской кровью. Различают также и якорные ворсины, которые фиксируются к базальной децидуальной оболочке и обеспечивают прикрепление плаценты к стенке матки.
Схема циркуляции крови в организме плода
1 – верхняя полая вена
2 – овальное отверстие
3 – нижняя полая вена
4 – венозный проток
5 – портальный синус
6 – воротная вена
7 – вена пуповины
8 – артерии пуповины
9 – плацента
10 – надчревные артерии
11 – артериальный проток
Спиральные артерии, которые являются конечными ветвями маточной и яичниковой артерий, питающих беременную матку, открываются в межворсинчатое пространство 120-150 устьями, обеспечивая постоянный приток материнской крови, богатой кислородом, в межворсинчатое пространство. За счет разницы давления, которое выше в материнском артериальном русле по сравнению с межворсинчатым пространством, кровь, насыщенная кислородом, из устьев спиральных артерий направляется через центр котиледона к ворсинам, омывает их, достигает хориальной пластины и по разделительным септам возвращается в материнский кровоток через венозные устья. При этом кровоток матери и плода отделены друг от друга. Т.е. кровь матери и плода не смешивается между собой.
Переход газов крови, питательных веществ, продуктов метаболизма и других субстанций из материнской крови в плодовую и обратно осуществляется в момент контакта ворсин с кровью матери через плацентарный барьер. Он образован наружным эпителиальным слоем ворсины, стромой ворсины и стенкой кровеносного капилляра, расположенного внутри каждой ворсины. По этому капилляру течет кровь плода. Насыщаясь таким образом кислородом, кровь плода из капилляров ворсин собирается в более крупные сосуды, которые в конечном итоге объединяются в вену пуповины, по которой насыщенная кислородом кровь оттекает к плоду. Отдав кислород и питательные вещества в организме плода, кровь, обедненная кислородом и богатая углекислым газом, оттекает от плода по двум артериям пуповины к плаценте, где эти сосуды делятся радиально в соответствии с количеством котиледонов. В результате дальнейшего ветвления сосудов внутри котиледонов кровь плода вновь попадает в капилляры ворсин и вновь насыщается кислородом, и цикл повторяется. За счет перехода через плацентарный барьер газов крови и питательных веществ реализуется дыхательная, питательная и выделительная функция плаценты. При этом в кровоток плода попадает кислород и выводится углекислый газ и другие продукты метаболизма плода. Одновременно в сторону плода осуществляется транспорт белков, липидов, углеводов, микроэлементов, витаминов, ферментов и многого другого.
Схема строения плацентарного барьера
1 – эндотелий капилляров терминальных ворсин
2 – капилляр ворсины
3 – строма ворсины
4 – эпителиальный покров ворсин
Плацента осуществляет важную защитную (барьерную функцию) посредством плацентарного барьера, который обладает избирательной проницаемостью в двух направлениях. При нормальном течении беременности проницаемость плацентарного барьера увеличивается до 32 -34 недель беременности, после чего определенным образом снижается. Однако, к сожалению, через плацентарный барьер сравнительно легко проникают в плодовый кровоток достаточно большое количество лекарственных препаратов, никотин, алкоголь, наркотические вещества, пестициды, другие токсические химические вещества, а также целый ряд возбудителей инфекционных заболеваний, что оказывает неблагоприятное воздействие на плод. Кроме того, под воздействием патогенных факторов барьерная функция плаценты нарушается еще в большей степени.
Плацента анатомически и функционально связана с амнионом (водная оболочка), который окружает плод. Амнион представляет собой тонкую мембрану, которая выстилает поверхность плаценты, обращенной к плоду, переходит на пуповину и сливается с кожей плода в области пупочного кольца. Амнион активно участвует в обмене околоплодных вод, в ряде обменных процессов, а также выполняет и защитную функцию.
Плаценту и плод соединяет пуповина, которая представляет собой шнуровидное образование. Пуповина содержит две артерии и одну вену. По двум артериям пуповины течет обедненная кислородом кровь от плода к плаценте. По вене пуповины к плоду течет кровь, обогащенная кислородом. Сосуды пуповины окружены студенистым веществом, которое получило название “вартонов студень”. Эта субстанция обеспечивает упругость пуповины, защищает сосуды и обеспечивает питание сосудистой стенки. Пуповина может прикрепляться (чаще всего) в центре плаценты и реже сбоку пуповины или к оболочкам. Длина пуповины при доношенной беременности в среднем составляет около 50 см.
Плацента, плодные оболочки и пуповина вместе образуют послед, который изгоняется из матки после рождения ребенка.

Журнал “SonoAce Ultrasound”
Содержит актуальную клиническую информацию по ультрасонографии и ориентирован на врачей ультразвуковой диагностики, выходит с 1996 года.
Источник
Vasa Previa (Предлежание Сосудов, ПС) может иметь катастрофические последствия для жизни плода и новорожденного. На самом деле существует всего несколько пренатальных ультразвуковых диагнозов, которые имеют настолько выраженное, прямое влияние на исход родов и так значительно повышают выживаемость среди тех, у кого было своевременно диагностировано данное состояние. Исключение ПС с помощью ультразвука занимает менее минуты и обязательно должно входить в стандартные скрининговые ультразвуковые исследования.
«Vasa Previa отняла у нас нашего прекрасного мальчика, нашего первого ребёнка, и мы никогда уже не будем такими, как прежде. Всё о чем мы можем мечтать, это чтобы хоть у кого-то одного из медицинского персонала хватило предусмотрительности сканировать нас на предмет наличия такого состояния.» – Natalie Samat, чей ребёнок Henry Cameron Samat умер врезультате не диагностированного предлежания сосудов в 2005 году.
Что такое Vasa Previa?
Vasa Previa (Предлежание Сосудов) – (от лат. vasa – сосуд, prеvia – находящийся перед, спереди от) – это состояние, характеризующееся наличием сосудов, имеющих связь с плодово-плацентарным кровотоком, проходящих свободно во внеплацентарных плодных оболочках, расположенных между предлежащей частью плода и шейкой матки.
Эти сосуды проходят незащищёнными ни Вартоновым студнем, ни тканью плаценты, вследствие чего легко ранимы и подвержены сдавлению на любом этапе беременности, хотя большинство осложнений происходит в родах.
Vasa Previa является патологическим состоянием, не имеющим клинических проявлений, приводящим в некоторых случаях к развитию плодного кровотечения во время беременности и родов, и как следствие, ведущее к смерти плода/новорожденного.
Различают два типа ПС
1-й тип – наличие над внутренним зевом свободных сосудов пуповины, не защищенных Вартоновым студнем при оболочечном прикреплении пуповины (ОПП) – состояние, при котором пуповина прикрепляется не к ткани плаценты, а к околоплодным оболочкам на некотором расстоянии от края плаценты. ОПП является одной из первых причин ПС, описанных в литературе. Диагностируется анте- или постнатально в среднем от 0,4 до 1,8% случаев всех беременностей, приводя при этом к ПС от 1 до 3% случаев, или в среднем один случай VP на 50 случаев ОПП. При многоплодной беременности частота ОПП намного увеличивается и встречается от 3,6 до 16% в случаях беременностью двойней. У моноамниональных монохориональных двоен ОПП наблюдается в 16%, у диамниональных монохориональных двоен – в 13%, а у дихориональных двоен – в 7% случаев. В случаях беременности тройней ОПП встречается в 28,2% случаев.
2-й тип – наличие над внутренним зевом незащищенных сосудов, соединяющих между собой доли плаценты при двудольной плаценте, или при наличии дополнительных долей, при возможно нормальном прикреплении пуповины к основной доле плаценты.
Из всех случаев ПС тип 1 встречается почти в 90% обнаружения ПС.
Частота встречаемости ПС примерно 1:2500 родов, но есть вероятность того, что на самом деле эта цифра недооценена, так как часть случаев могут проходить без осложнений и не попадать в отчёты. При этом есть работы показывающие, что частота ПС после ЭКО 1:300 беременностей.
В чём опасность?
Учитывая тот факт, что ПС является патологическим состоянием без каких-либо клинических проявлений, данная патология остается одной из опаснейших по развитию осложнений со стороны плода, таких как смерть в результате кровотечения при разрыве ПС либо внутриутробной асфиксии, при пережатии сосудов.
Одними из самых опасных осложнений ПС являются разрыв и возникающее плодное кровотечение. В большинстве случаев повреждение ПС происходит одномоментно с разрывом плодных оболочек, имея при этом «общую точку разрыва». Описаны случаи разрывов сосудов, проходящих свободно в оболочках, расположенных на расстоянии от места первоначального разрыва оболочек. В данных случаях сосуды повреждаются из-за продолжающегося разрыва плодных оболочек во время продвижения плода в процессе родов, что объясняет случаи кровотечения через 12 и более часов после момента разрыва плодных оболочек.
Учитывая тот факт, что объем циркулирующей крови плода к 38 неделям беременности составляет 80-110 мл/кг веса, то начавшееся кровотечение из ПС требует экстренной операции кесарева сечения, так как потеря уже 100 мл плодной крови может привести к развитию геморрагического шока и к смерти плода. Коварной чертой такого кровотечения является то, что состояние матери при этом не меняется, остаётся стабильным.
Перинатальная смертность при не диагностированном ПС составляет 55-75%.
История
Первым ПС при оболочечном прикреплении пуповины описал H. A. Wrisberg в 1773 году, он публиковал свои находки о «свободных сосудах в оболочках, выходящих из плаценты и связывающих ее с пуповиной плода в нижней части матки в месте ее расширения при родах».
В 1778 году E. Sandifort доложил о следующем случае обнаружения «прикрепления пуповины к краю плаценты» и о «свободных сосудах в оболочках, выходящих с противоположной месту прикрепления пуповины стороны плаценты и входящих в сеть сосудов пуповины плода».
В 1801 J.-F. Lobstein первым высказал предположение о «возможном разрыве свободных сосудов, проходящих в оболочках между пуповиной и плацентой, а также между плацентой и ее дополнительными долями, с возможным кровотечением, которое может привести к быстрой смерти плода» .
Но только в 1831 году R. Benckiser в своей «Dissertation inaugurale» сообщил о первом случае смерти новорожденного вследствие кровотечения, связанного с «разрывом венозной ветви, проходящей в 6 см от края плаценты над отверстием матки, во время разрыва амниотических оболочек». Именно после этого случая в европейской, в частности во франкоязычной, литературе за кровотечением, возникающим вследствие разрыва VP, закрепилось название «кровотечение Бенкизера»
Первое ультразвуковое описание ПС было в 1987 году. Gianopoulos и соавторы описали случай УЗ диагностики предлежания сосудов у беременной с добавочной долей плаценты.
В 1990г Nelson впервые сообщил об использовании цветового допплеровского картирования (ЦДК) для диагностики ПС.
И лишь в 1996 году описан первый случай выявления ПС во время скринингового УЗИ во втором триместре, благодаря чему на 35 неделе родился здоровый ребёнок путём операции кесарево сечение.
Но проблема Vasa Previa так и оставалась в разряде «отдельных научных статей, о которых мало кто знал» до очередной трагедии, которая случилась в семье адвокатов Natalie и Daren Samat, когда в 2005 году в результате не диагностированного ПС на 13-м дне жизни скончался их ребёнок Henry. Проблема получила широкую огласку именно благодаря стараниям этих людей, основанному ими благотворительному фонду https://vasaPrevia.co.uk/ и требованию к NHS National Screening Committee Великобритании включить исследование на предмет ПС в скрининг второго триместра.

Natalie и Daren Samat
В 2008 году National Screening Committee ответил, что на данный момент не достаточно доказательств необходимости включения данного обследования в программу скрининга и что есть обеспокоенность о гипердиагностике, которая повлечёт ненужные операции кесарево сечение.
Роль УЗИ в диагностике Предлежания Сосудов
В январе 2014 года в журнале Journal of Ultrasound in Medicine была опубликована статья «Natural History of Vasa Previa Across Geion Using a Screening Protocol», в которой описывается большое исследование, проводившееся с июня 2005 по июнь 2012гг, включившее в себя 27 573 беременных, которым целенаправленно проводилось УЗ исследование на предмет Vasa Previa во время скрининга второго и третьего триместров.
Показаниями для проведения исследования были:
Предлежание плаценты на более ранних сроках, которая «поднялась»
Vasa Previa в прошлые беременности
Оболочечное прикрепление сосудов в области нижнего сегмента матки
Добавочная доля плаценты в области нижнего сегмента матки
Беременность двойней
Диагноз Предлежание Сосудов выставлялся в случае обнаружения оболочечного прикрепления сосудов в пределах 2-х сантиметров от внутреннего зева при трансвагинальном исследовании с использованием серой шкалы, ЦДК и энергетического Доплера.
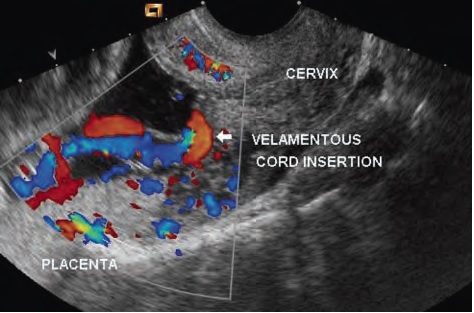
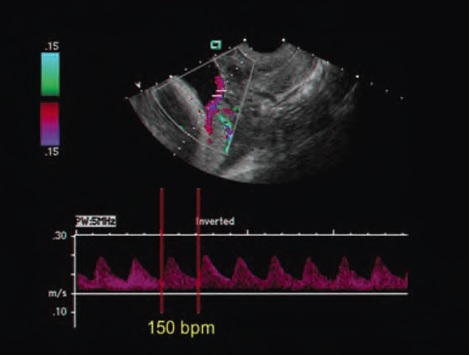
Был выявлен 31 случай ПС, что соответствовало частоте 1.1:1000 беременностей. У авторов нет информации о пропущенных случаях ПС.
В заключении сказано, что использование стандартизированного скрининга ПС является эффективным методом диагностики ПС, благодаря которому достигается 100% выживаемость. Было показано, что примерно в 24% случаев, ПС диагностированное во втором триместре (<26 недель) самостоятельно разрешается благодаря смещению сосудов вверх к третьему триместру, но не было ни одного случая смещения сосудов кверху при диагностике ПС в третьем триместре.
Вероятность ПС минимальна в случаях, когда корень пуповины выходит из ткани плаценты, и при отсутствии добавочной доли плаценты или билобарной плаценты. Учитывая, что описание плаценты уже включено в стандартный протокол УЗИ, необходимо сместить приоритет к исключению оболочечного прикрепления сосудов пуповины, так как такое состояние является предпосылкой для наиболее частого варианта ПС, тип 1. Диагностика нормального прикрепления пуповины к плаценте во время скрининга второго триместра сама по себе имеет большое значение. Помимо ПС существует ещё масса осложнений при оболочечном прикреплении пуповины: повышенный риск отслойки плаценты, задержки роста плода, низкой оценки Апгар при рождении, преждевременных родов. Это не значит, что если Вам поставили диагноз ОПП, то всё это непременно случится, но такая беременность требует повышенного внимания со стороны акушера-гинеколога и более осмотрительного поведения со стороны беременной.
Несколько исследований показали, что определение места прикрепления пуповины к плаценте во время скрининга первого или второго триместра занимает меньше минуты и не требует каких-то особых умений. До 11 недель данное исследование невозможно, так как трофобласт в это время покрывает значительную площадь полости матки.
Определение места прикрепления пуповины к плаценте во время скрининга первого триместра в 11-14 недель предпочтительно, так как на этом сроке это совсем не сложно сделать. При многоплодной беременности, а также при беременности после ЭКО следует рекомендовать трансвагинальное исследование в тех случаях, когда осмотр области внутреннего зева затруднён при трансабдоминальном доступе.
Важно подчеркнуть, что необходимо целенаправленно исключать ОПП, так как если не делать этого специально, то с большой долей вероятности ОПП будет пропущено.
Корень пуповины может располагаться в центре плаценты или эксцентрично, но в ткани плаценты (90%). Либо на краю плаценты (10%) , т.н. краевое прикрепление пуповины к плаценте, в этом случае бывает сложно с помощью УЗ однозначно утверждать, что часть сосудов не расположены оболочечно. И в 1% беременностей определяется оболочечное прикрепление пуповины в стороне от края плаценты. Важно убедиться, что определён именно корень пуповины, а не свободные петли пуповины на поверхности плаценты. В этом может помочь режим ЦДК, показывающий вход сосудов пуповины в хориальную пластину.
В случае, когда отчётливо определено место вхождения пуповины в плаценту, вероятность 1 типа ПС крайне мала и никаких дополнительных исследований не требуется.
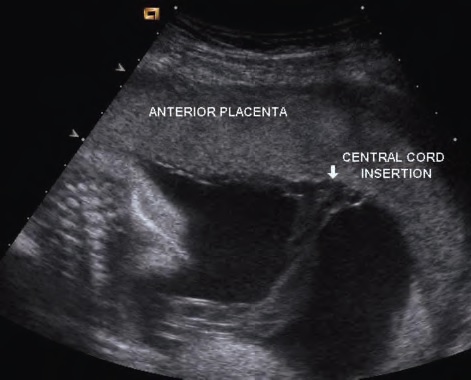
показан корень пуповины входящий в центр плаценты
И, наоборот, в случае, когда не удаётся отчётливо определить место вхождения пуповины, специалисту УЗД необходимо приложить дополнительные усилия, чтобы не пропустить ОПП. Когда не удаётся выявить ОПП в верхнем сегменте матки с помощью трансабдоминального датчика, необходимо провести трансвагинальное исследование с использованием ЦДК.
Кроме того не следует забывать о ПС 2 типа, и осматривать стенки полости матки на предмет добавочных долей плаценты.
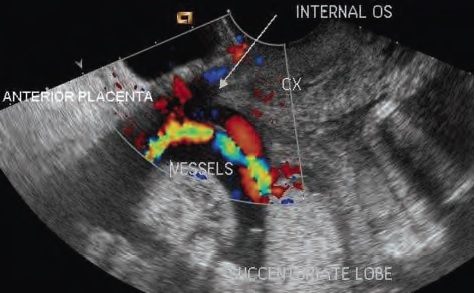
показана плацента по передней стенке матки, добавочная доля плаценты и ПС 2 тип
В случае низкой плацентации во втором триместре беременности, необходимо убедиться, что сосуды не определяются рядом с внутренним зевом, и если это так, то никаких дополнительных действий не требуется.
Низкая плацентация во втором триместре беременности – это состояние, когда край плаценты определяется на расстоянии менее 3-х сантиметров от внутреннего зева, но не перекрывает его. В этом случае не требуется каких-то дополнительных действий или лечения «на всякий» случай. Достаточно повторной оценки расположения плаценты в третьем триместре.
Во время скрининга первого триместра и тем более до 11 недель, не следует ставить диагноз Низкое расположение хориона, так как нижний сегмент матки ещё значительно растянется, и в подавляющем большинстве случаев к 20 неделям уже не будет низкой плацентации.
В настоящее время широко используется трансвагинальное исследование шейки матки с целью исключения истмико-цервикальной недостаточности (ИЦН). Не редко женщины сами, без назначения врача, приходят на цервикометрию просто на всякий случай, потому что им так спокойнее.
Врачу УЗД, проводящему данное исследование следует помнить о Vasa Previa и использовать эту уникальную возможность для того, чтобы, затратив меньше минуты своего времени, лишний раз посмотреть, включить режим ЦДК и, может быть, предотвратить трагедию.
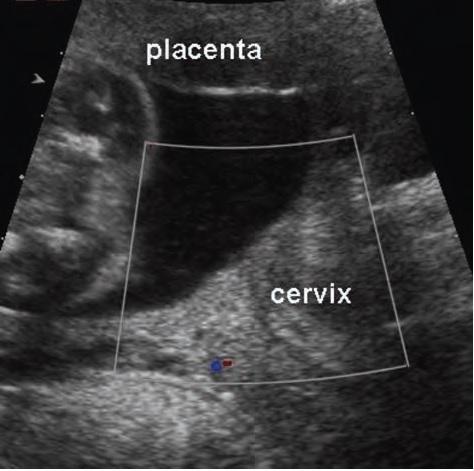
показано отсутствие предлежащих сосудов при трансвагинальном исследовании шейки матки
В заключении хочу предложить диагностический алгоритм для исключения Vasa Previa во время скрининга второго триместра, разработанный командой Philippe Jeanty:
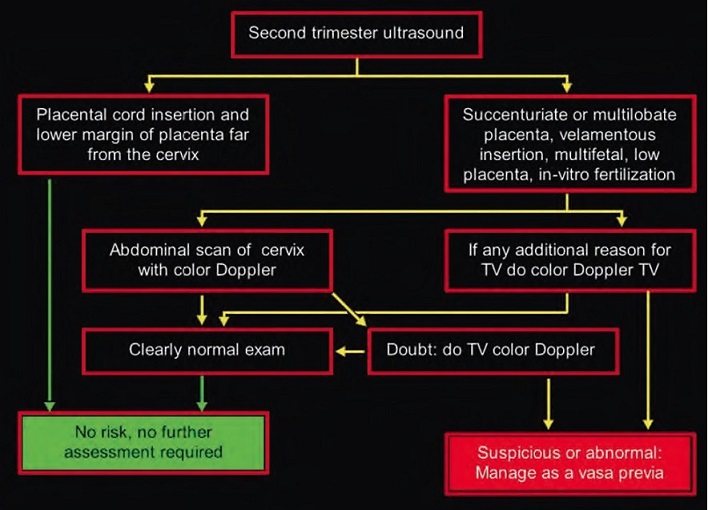
Если Вам поставили диагноз Предлежание Сосудов во втором триместре, не нужно пугаться, но нужно понимать, что к такой беременности нужно относиться с ещё большим трепетом и выполнять все рекомендации наблюдающего Вас врача. Помните, что в 24 % случаев к третьему триместру сосуды могут сместиться кверху, и диагноза ПС уже не будет. Если же и в третьем триместре диагноз подтверждается, то Вам будет показана госпитализация в стационар ближе к 35 неделям беременности, проведение профилактики респираторного дистресс синдрома и родоразрешение путём операции кесарево сечение на сроке 35-36 недель беременности.
Источник
