Процесс сжатие воздуха в сосуде

Сжатый воздух на сегодняшний день является важнейшим и незаменимым источником энергии для промышленных предприятий, сравнимым по важности разве что с электричеством.
В данной статье мы подробно расскажем о том, что же такое сжатый воздух, какие он имеет особенности и характеристики при сжатии, и как следует с ним обращаться в рамках рабочего процесса.
По своей сути, сжатый воздух представляет собой воздух под давлением, которое превышает атмосферное, то есть сжатый атмосферный воздух. Состав атмосферного воздуха известен, это сочетание следующих газов:
- азот в концентрации около 78%;
- кислород в концентрации около 21%;
- остальные газы в общем соотношении около 1%.
Основными параметрами описания состояния воздуха являются следующие:
- давление (bar);
- температура (°C);
- удельный объем (л. или м3).
Последний параметр (удельный объем) обычно используется для расчета объема ресивера или расхода сжатого воздуха компрессором.
В процессе сжатия воздух проходит следующие этапы:
- Атмосфера;
- Компрессор;
- Пневмомагистраль;
- Потребитель.
Основной процесс сжатия воздуха происходит в компрессоре, после него по пневмомагистрали сжатый воздух поступает к потребителю. Для задач сжатия воздуха наибольшее распространение получили поршневые, винтовые и турбокомпрессоры.
Далее посмотрим, как меняются параметры воздуха в процессе сжатия.
Температура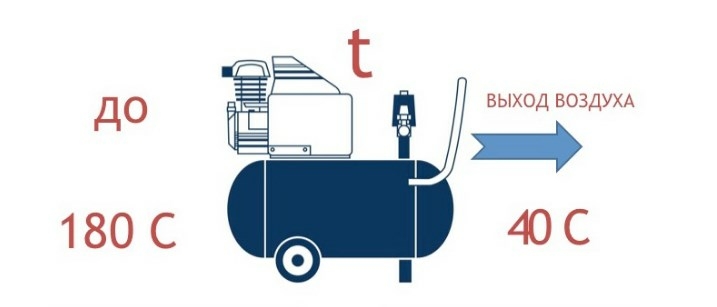
После всасывания воздуха в компрессор, он начинает сжиматься. При сжатии воздуха в компрессоре температура может повыситься до 180 градусов, но после попадания в ресивер, температура снижается примерно до 40 градусов. В течение процесса понижения температуры начинает образовываться конденсат, то есть выпадение влаги.
Особенности сжатия воздуха:
- в процессе сжатия воздуха его температура всегда повышается, поскольку молекулы начинают двигаться быстрее, и выделяется тепло, при этом существует прямая зависимость повышения температуры от степени сжатия. Другими словами, чем сильнее мы сжимаем воздух, тем больше становится его температура. Это справедливо и для небольших величин давления.
- пары воды также сжимаются и впоследствии конденсируются
- конденсат представляет собой загрязнение, аккумулирующее в себе частицы пыли, масла, окалины и т.д.
- Конденсат и прочие загрязнения необходимо удалять, иначе они могут повредить пневмосистеме, являясь причиной коррозии, повышенного износа и поломки.
Состав сжатого воздуха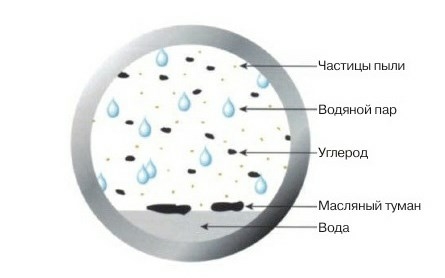
Поступающий в компрессор воздух может содержать до 2 миллиардов частиц пыли, что уже является загрязнением в виде твердых частиц. Далее к ним прибавляется влага, масляные пары и частицы углерода. Масляный туман может повредить компрессор во время работа, а если мы эксплуатируем компрессор в условиях медицинского, фармацевтического производства или при производстве продуктов питания, вредные вещества могут попасть в организм человека или в продукты. Масляный туман сложно отделить от основного потока воздуха. Соответственно, для предотвращения износа оборудования и обеспечения его долгосрочной работы, воздух необходимо очищать. Кроме того, важным моментом является обеспечение соответствия качества сжатого воздуха нормам и стандартам DIN ISO 8573-1:2001 или ГОСТ 17433-80.
Очистка сжатого воздуха
Для соответствия высоким требованиям к сжатому воздуху, предъявляемым современными производствами, и, как следствие, к продукту, необходимо использовать комплексные системы подготовки и очистки воздуха.
В последнее время производство качественного сжатого воздуха приобрело особое значение, так как современная промышленность предъявляет высокие требования к оборудованию, а потребитель – к качеству выпускаемой продукции.
В связи с этим существуют комплексные системы подготовки и очистки сжатого воздуха. Например, для удаления влаги применяются охладители воздуха, которые способствуют выпадению конденсата путем охлаждения воздуха примерно до 10 градусов относительно температуры окружающей среды. Далее используются осушители воздуха для получения сжатого воздуха с требуемым содержанием влаги (точкой росы). Чтобы удалить примеси и загрязнения, например пыль, окалину, ржавчину, масляные пары необходимо использовать фильтры очистки.
Преимущества использования сжатого воздуха
- Безопасность – по сравнению с электричеством, куда более безопасным является использование сжатого воздуха. В этом случае исключены перегрузки, поражение током, возгорание и прочий ущерб, особенно при работе в условиях повышенной влажности.
- Удобство применения – проще использовать на удаленных строительных объектах, буровых установках, шахтах. Важными особенностями является возможность работы с переменной частотой и крутящим моментом.
- Меньший вес и эргономичность – удобство работы, снижение утомляемости персонала и расходов на эксплуатацию.
- Стоимость – по последним подсчетам, стоимость электричества ниже, чем стоимость сжатого воздуха, но само оборудование для получения сжатого воздуха стоит существенно дешевле, при этом отличается простотой конструкции и большей долговечностью.
- Сжатый воздух является отличной универсальной, гибкой и безопасной средой для хранения и передачи энергии. Учитывая все возрастающее потребление сжатого воздуха в промышленности, стоит заметить, что правильное использование указанных выше средств подготовки и очистки воздуха позволит длительно эксплуатировать вашу пневмосистему и избежать поломок и выхода из строя.

Источник
04 Апреля 2012
В современном высокотехнологическом мире сжатый воздух незаменим, он используется повсеместно и на сегодняшний день является вторым по важности источником энергии после электричества для очень многих промышленных предприятий.
Что же представляет из себя сжатый воздух? Какие существуют принципы и особенности сжатия воздуха, и что следует помнить при работе с ним?
Начнем с определения: сжатый воздух – это воздух, который находится под давлением, превышающим атмосферное. По сути, сжатый воздух – это сжатый атмосферный воздух, то есть тот воздух, которым мы дышим, который состоит из различных газов:
– 78% азот
– 21% кислород
– 1% другие газы.
Состояние воздуха (газа) можно описать тремя параметрами:
– давление (Р);
– температура (С);
– удельный объем (Vуд.);
В технологии сжатия воздуха все три параметра измеряются в конкретных величинах:
– рабочее давление (давление сжатия) измеряется в барах;
– температура сжатого воздуха измеряется в градусах Цельсия;
– объем используют как для определения размеров ресивера, так и для расхода компрессорами сжатого воздуха, выраженный в лит./мин или куб.м./час
Одним из средств сжатия воздуха является его “выработка” компрессорным оборудованием. Таким образом, сжатый воздух начинает свой путь в компрессоре.
Прежде чем попасть к потребителю сжатый воздух проходит следующие этапы:
На каждом из этих этапов происходит своего рода трансформация воздуха из одного состояния в другое. Рассмотрим основные принципы и особенности сжатого воздуха.
Температура.
В процессе поступления воздуха из атмосферы в компрессор воздух начинает сжиматься. В момент сжатия воздуха в компрессоре его температура может достигать до 180 С, однако через какое-то время, когда воздух попадает дальше, в ресивер, его температура начинает падать, к примеру, на “выходе” из поршневого компрессора она равняется примерно 40-45 С.

Таким образом, падение температуры сжатого воздуха “на лицо”, и воздух, действительно, остывает. В тот момент, когда его температура начинает понижаться, идет процесс возникновения конденсата или другими словами влаги. Таким образом, о сжатии воздуха важно знать следующее:
– при сжатии всегда происходит повышение температуры. Чем сильнее сжимается воздух, тем выше поднимается температура, и даже при сжатии воздуха до невысокого давления происходит значительное возрастание температуры.
– повышение температуры происходит не из-за механического трения частей компрессора и тому подобного, а из-за самого сжатия.
– водяные пары также сжимаются, и при последующем понижении температуры – конденсируются.
– при сжатии воздуха пары воды становятся основным загрязнением.
– в сжатом воздухе сконденсировавшаяся вода является загрязнением, которое улавливает и переносит другие загрязнения.
– концентрация вредных веществ возрастает, и может стать опасной, если их не удалить.
Самое главное – то, что в итоге сжатия воздуха после падения температуры воздуха возникает конденсат, и это может стать настоящей проблемой для потребителя.
Значительное содержание воды в сжатом воздухе становится причиной коррозии пневмосети. Взвешенные частицы и ржавчина действуют как абразив на элементы пневмоавтоматики. Всё это приводит к серьезным повреждениям пневматического оборудования, тем самым вызывая простои оборудования, повышение эксплуатационных расходов и повреждение производимых изделий.
Состав сжатого воздуха.
При подаче в компрессор обычный воздух содержит около 1,8 миллиардов частиц пыли. Таким образом, воздух, попадающий в компрессор, уже содержит загрязнения в виде твердых частиц. К этому надо добавить и то, что мы уже выяснили – некоторое количество влаги или водяного пара, который при сжатии конденсируется, тоже образует загрязнение воздуха. Но и это еще не все: в процессе работы маслянных компресоров в воздушный поток (в результате нагревания масла) могут попадать масляные пары и образовавшийся углерод.
 Масляный туман или пар, исходящий из потока сжатого воздуха, может стать причиной сбоя в работе компрессора, сколов краски от корпуса либо появления отверстий (пробоин) на нем. При эксплуатации компрессора в пищевой отрасли либо в медицинской сфере существует риск попадания вредных веществ в организм человека. Масляный туман является наиболее трудновыводимым элементом при его отделении от воздушного потока.
Масляный туман или пар, исходящий из потока сжатого воздуха, может стать причиной сбоя в работе компрессора, сколов краски от корпуса либо появления отверстий (пробоин) на нем. При эксплуатации компрессора в пищевой отрасли либо в медицинской сфере существует риск попадания вредных веществ в организм человека. Масляный туман является наиболее трудновыводимым элементом при его отделении от воздушного потока.
Все это в целом приводит к тому, что загрязнения в атмосферном воздухе с наличием водяных паров и масляного тумана, в процессе работы компрессора превращаются в 2 миллиарда частиц пыли и 0,03 мг/м.куб. масляных паров в выходном воздушном потоке.
Попадая в пневматическую систему, такая агрессивная смесь приводит к ускоренному износу оборудования и выходу его из строя.
Поэтому встает вопрос о качестве воздуха, которое определяется содержанием частиц пыли, масляного тумана и водяных паров. Требование к качеству сжатого воздуха определяет производитель оборудования и нормируется по DIN ISO 8573-1:2001 или ГОСТ 17433-80. Существуют следующие стандарты ISO для типов сжатого воздуха:
Очистка сжатого воздуха.
В последнее время производство качественного сжатого воздуха приобрело особое значение, так как современная промышленность предъявляет высокие требования к оборудованию, а потребитель – к качеству выпускаемой продукции. В связи с этим существуют комплексные системы подготовки и очистки сжатого воздуха. Если коротко остановится на основных этапах, то они выглядят так.
Для принудительного удаления влаги из сжатого воздуха на первом этапе применяют охладители воздуха, которые охлаждают горячий, содержащий влагу воздух до температуры +10 С по отношению к температуре окружающей среды. В результате резкого охлаждения происходит процесс конденсации. На выходе из охладителя сжатый воздух содержит влагу в виде взвеси капелек воды – водяного конденсата и пара. На следующем этапе получения сжатого воздуха с необходимой точкой росы (содержанием влаги) используются осушители сжатого воздуха.
Для удаления содержащихся в сжатом воздухе других посторонних примесей (песок, пыль, частицы метала от трущихся элементов компрессора, продукты окисления пневматической магистрали, пары масел и т. п.), применяются магистральные фильтры.
Таким образом, какими бы ни были требования по чистоте воздуха, современные системы подготовки и очистки воздуха позволяют эффективно подготовить и очистить воздух до необходимого уровня.
DIN ISO 8573-1:2001 Качество сжатого воздуха
| Класс качества | Грязь | Вода | Масло | |
| Размер частиц (мкм) | Макс. концентрация (мг/м. куб) | Точка росы при макс. давлении (С) | Макс. концентрация (мг/м. куб) | |
| Класс 0 зарезервирован под более высокие требования, оговариваются специально | ||||
| 1 | 0,1 | 0,1 | -70 | 0,01 |
| 2 | 1 | 1 | -40 | 0,1 |
| 3 | 5 | 5 | -20 | 1 |
| 4 | 15 | 8 | 3 | 5 |
| 5 | 40 | 10 | 7 | 25 |
| 6 | – | – | 10 | – |
Стандарт качества сжатого воздуха для каждой категории применения
| Применение | Класс качества | ||
| Грязь | Вода | Масло | |
| Фотография | 1 | 1 | 1 |
| Продукты питания/напитки | 2 | 3 | 1 |
| Пневмоцилиндр | 3 | 3 | 3 |
| Воздух для общего приминения | 4 | 4 | 5 |
Пневмомагазин.ру
Источник
Автор статьи — профессиональный репетитор, автор учебных пособий для подготовки к ЕГЭ Игорь Вячеславович Яковлев
Темы кодификатора ЕГЭ: изопроцессы — изотермический, изохорный, изобарный процессы.
На протяжении этого листка мы будем придерживаться следующего предположения: масса и химический состав газа остаются неизменными. Иными словами, мы считаем, что:
• , то есть нет утечки газа из сосуда или, наоборот, притока газа в сосуд;
• , то есть частицы газа не испытывают каких-либо изменений (скажем, отсутствует диссоциация — распад молекул на атомы).
Эти два условия выполняются в очень многих физически интересных ситуациях (например, в простых моделях тепловых двигателей) и потому вполне заслуживают отдельного рассмотрения.
Если масса газа и его молярная масса фиксированы, то состояние газа определяется тремя макроскопическими параметрами: давлением, объёмом и температурой. Эти параметры связаны друг с другом уравнением состояния (уравнением Менделеева — Клапейрона).
Термодинамический процесс (или просто процесс) — это изменение состояния газа с течением времени. В ходе термодинамического процесса меняются значения макроскопических параметров — давления, объёма и температуры.
Особый интерес представляют изопроцессы — термодинамические процессы, в которых значение одного из макроскопических параметров остаётся неизменным. Поочерёдно фиксируя каждый из трёх параметров, мы получим три вида изопроцессов.
1. Изотермический процесс идёт при постоянной температуре газа: .
2. Изобарный процесс идёт при постоянном давлении газа: .
3. Изохорный процесс идёт при постоянном объёме газа: .
Изопроцессы описываются очень простыми законами Бойля — Мариотта, Гей-Люссака и Шарля. Давайте перейдём к их изучению.
Изотермический процесс
Пусть идеальный газ совершает изотермический процесс при температуре . В ходе процесса меняются только давление газа и его объём.
Рассмотрим два произвольных состояния газа: в одном из них значения макроскопических параметров равны , а во втором — . Эти значения связаны уравнением Менделеева-Клапейрона:
Как мы сказали с самого начала,масса и молярная масса предполагаются неизменными.
Поэтому правые части выписанных уравнений равны. Следовательно, равны и левые части:
(1)
Поскольку два состояния газа были выбраны произвольно, мы можем заключить, что в ходе изотермического процесса произведение давления газа на его объём остаётся постоянным:
(2)
Данное утверждение называется законом Бойля — Мариотта.
Записав закон Бойля — Мариотта в виде
(3)
можно дать и такую формулировку: в изотермическом процессе давление газа обратно пропорционально его объёму. Если, например, при изотермическом расширении газа его объём увеличивается в три раза, то давление газа при этом в три раза уменьшается.
Как объяснить обратную зависимость давления от объёма с физической точки зрения? При постоянной температуре остаётся неизменной средняя кинетическая энергия молекул газа, то есть, попросту говоря, не меняется сила ударов молекул о стенки сосуда. При увеличении объёма концентрация молекул уменьшается, и соответственно уменьшается число ударов молекул в единицу времени на единицу площади стенки — давление газа падает. Наоборот, при уменьшении объёма концентрация молекул возрастает, их удары сыпятся чаще и давление газа увеличивается.
Графики изотермического процесса
Вообще, графики термодинамических процессов принято изображать в следующих системах координат:
• -диаграмма: ось абсцисс , ось ординат ;
• -диаграмма: ось абсцисс , ось ординат ;
• -диаграмма: ось абсцисс , ось ординат .
График изотермического процесса называется изотермой.
Изотерма на -диаграмме — это график обратно пропорциональной зависимости .
Такой график является гиперболой (вспомните алгебру — график функции ). Изотерма-гипербола изображена на рис. 1.

Рис. 1. Изотерма на -диаграмме
Каждая изотерма отвечает определённому фиксированному значению температуры. Оказывается, что чем выше температура, тем выше лежит соответствующая изотерма на –диаграмме.
В самом деле, рассмотрим два изотермических процесса, совершаемых одним и тем же газом (рис. 2). Первый процесс идёт при температуре , второй — при температуре .

Рис. 2. Чем выше температура, тем выше изотерма
Фиксируем некоторое значение объёма . На первой изотерме ему отвечает давление , на второй — . Но при фиксированном объёме давление тем больше, чем выше температура (молекулы начинают сильнее бить по стенкам). Значит, .
В оставшихся двух системах координат изотерма выглядит очень просто: это прямая, перпендикулярная оси (рис. 3):

Рис. 3. Изотермы на и -диаграммах
Изобарный процесс
Напомним ещё раз, что изобарный процесс — это процесс, проходящий при постоянном давлении. В ходе изобарного процесса меняются лишь объём газа и его температура.
Типичный пример изобарного процесса: газ находится под массивным поршнем, который может свободно перемещаться. Если масса поршня и поперечное сечение поршня , то давление газа всё время постоянно и равно
где — атмосферное давление.
Пусть идеальный газ совершает изобарный процесс при давлении . Снова рассмотрим два произвольных состояния газа; на этот раз значения макроскопических параметров будут равны и .
Выпишем уравнения состояния:
Поделив их друг на друга, получим:
В принципе, уже и этого могло бы быть достаточно, но мы пойдём немного дальше. Перепишем полученное соотношение так, чтобы в одной части фигурировали только параметры первого состояния, а в другой части — только параметры второго состояния (иными словами, «разнесём индексы» по разным частям):
(4)
А отсюда теперь — ввиду произвольности выбора состояний! — получаем закон Гей-Люссака:
(5)
Иными словами, при постоянном давлении газа его объём прямо пропорционален температуре:
(6)
Почему объём растёт с ростом температуры? При повышении температуры молекулы начинают бить сильнее и приподнимают поршень. При этом концентрация молекул падает, удары становятся реже, так что в итоге давление сохраняет прежнее значение.
Графики изобарного процесса
График изобарного процесса называется изобарой. На -диаграмме изобара является прямой линией (рис. 4):

Рис. 4. Изобара на -диаграмме
Пунктирный участок графика означает, что в случае реального газа при достаточно низких температурах модель идеального газа (а вместе с ней и закон Гей-Люссака) перестаёт работать. В самом деле, при снижении температуры частицы газа двигаются всё медленнее, и силы межмолекулярного взаимодействия оказывают всё более существенное влияние на их движение (аналогия: медленный мяч легче поймать, чем быстрый). Ну а при совсем уж низких температурах газы и вовсе превращаются в жидкости.
Разберёмся теперь, как меняется положение изобары при изменении давления. Оказывается, что чем больше давление, тем ниже идёт изобара на –диаграмме.
Чтобы убедиться в этом, рассмотрим две изобары с давлениями и (рис. 5):

Рис. 5. Чем ниже изобара, тем больше давление
Зафиксируем некоторое значение температуры . Мы видим, что . Но при фиксированной температуре объём тем меньше, чем больше давление (закон Бойля — Мариотта!).
Стало быть, .
В оставшихся двух системах координат изобара является прямой линией, перпендикулярной оси (рис. 6):

Рис. 6. Изобары на и -диаграммах
Изохорный процесс
Изохорный процесс, напомним, — это процесс, проходящий при постоянном объёме. При изохорном процессе меняются только давление газа и его температура.
Изохорный процесс представить себе очень просто: это процесс, идущий в жёстком сосуде фиксированного объёма (или в цилиндре под поршнем, когда поршень закреплён).
Пусть идеальный газ совершает изохорный процесс в сосуде объёмом . Опять-таки рассмотрим два произвольных состояния газа с параметрами и . Имеем:
Делим эти уравнения друг на друга:
Как и при выводе закона Гей-Люссака, «разносим» индексы в разные части:
(7)
Ввиду произвольности выбора состояний мы приходим к закону Шарля:
(8)
Иными словами, при постоянном объёме газа его давление прямо пропорционально температуре:
(9)
Увеличение давления газа фиксированного объёма при его нагревании — вещь совершенно очевидная с физической точки зрения. Вы сами легко это объясните.
Графики изохорного процесса
График изохорного процесса называется изохорой. На -диаграмме изохора является прямой линией (рис. 7):

Рис. 7. Изохора на -диаграмме
Смысл пунктирного участка тот же: неадекватность модели идеального газа при низких температурах.
Далее, чем больше объём, тем ниже идёт изохора на –диаграмме (рис. 8):

Рис. 8. Чем ниже изохора, тем больше объём
Доказательство аналогично предыдущему. Фиксируем температуру и видим, что . Но при фиксированной температуре давление тем меньше, чем больше объём (снова закон Бойля — Мариотта). Стало быть, .
В оставшихся двух системах координат изохора является прямой линией, перпендикулярной оси (рис. 9):

Рис. 9. Изохоры на и -диаграммах
Законы Бойля — Мариотта, Гей-Люссака и Шарля называются также газовыми законами.
Мы вывели газовые законы из уравнения Менделеева — Клапейрона. Но исторически всё было наоборот: газовые законы были установлены экспериментально, и намного раньше. Уравнение состояния появилось впоследствии как их обобщение.
Источник
