Разрастание сосудов в печени
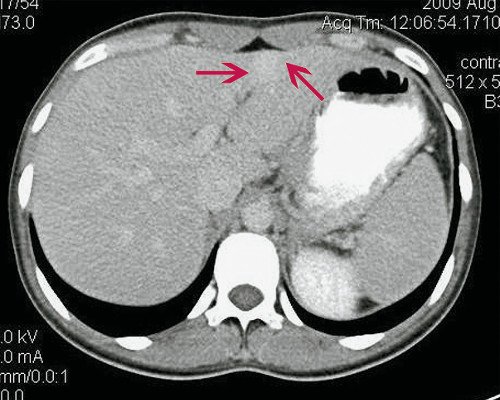
Гемангиома печени – опухолевое образование доброкачественного характера, которое появляется на одной или обеих долях внутреннего органа. В среднем, размер новообразования достигает 5 см.
Классификация
В мировой медицинской практике существует несколько разновидностей данной опухоли:
- кавернозная гемангиома печени, представляющая собой сразу несколько свободных полостей, соединяющихся в единую;
- капиллярная гемангиома печени образует большое число маленьких полостей, в каждой из которых размещается кровеносный или венозный сосуд.
Наряду с самыми распространенными также могут встречаться венозная, гроздевидная гемангиома, гемангиоэндотелиома.
Симптоматика недуга
Симптомы гемангиомы печени появляются далеко не сразу. Из-за небольших размеров образования даже в лабораторных условиях не всегда можно заметить наличие новых клеток. Это же касается клинических проявлений.
При разрастании опухоли до размеров от 10 см можно обнаружить нехарактерные для здорового состояния особенности:
- увеличение печени в объемах;
- тошнота, небольшая рвота;
- неприятные, болезненные ощущения под ребрами с правой стороны.
Все эти симптомы возникают в результате того, что новообразование давит на соседние органы и сдавливает расположенные рядом сосуды.
В некоторых случаях гемангиома печени может проявить себя после травмы живота (например, сильного удара) или интенсивной физической нагрузки тела. Разорвавшись от натуги, она вызывает внутреннее кровотечение и острую боль в области живота.
Причины появления
Признаки гемангиомы печени может ощутить на себе абсолютно каждый человек вне зависимости от возраста или пола. Тем не менее, отмечено, что у женщин она может разрастаться интенсивнее ввиду повышенного уровня гормона эстрогена.
Несмотря на огромное количество проведенных исследований данного образования, точная причина его появления до сих пор не выявлена. Ученые-медики считают, что предпосылки формируются еще во внутриутробном периоде развития плода.
Существует мнение о том, что разрастание клеток, образующих впоследствии гемангиому печени, активизируется в результате перенесенных организмом кровоизлияний, а также склонности к увеличению капиллярных и венозных сосудов и тромбозам.
Диагностика образования
В исключительно резких случаях, лишь при случайном стечении обстоятельств, гемангиома печени у ребенка или взрослого может быть обнаружена на ранней стадии. В подавляющем большинстве случаев ее находят, когда размеры достигают серьезных объемов.
В качестве методов диагностики применяются следующие:
- УЗИ желчного пузыря и печени (может показать опухоль круглой формы с четкими границами);
- МРТ желчевыводящих путей и печени (помимо очертаний образования покажет и его содержимое);
- МСКТ брюшной полости (послойно продемонстрирует границы и содержимое опухоли).
При обнаружении опухоли необходимо определить ее качественные особенности. Для подтверждения гемангиомы проводится ангиография чревного ствола, может также понадобиться статическая сцинтиграфия печени. Чтобы определить степень доброкачественности (злокачественности) атипичных клеток, назначается гепатосцинтиграфия.
Наряду с этим проводятся клинические анализы:
- печеночные пробы;
- общий анализ крови, биохимия крови;
- анализ крови на генетические маркеры.
Особенности лечения
Методика избавления от новообразования во многом зависит от его размеров и формы.
Небольшие опухоли (до 5-6 см в объеме) не требуют особенных действий. За ними осуществляется наблюдение и УЗ-контроль спустя 3 месяца с момента обнаружения. При отсутствии какой-либо динамики ультразвуковая диагностика назначается каждые 6-12 месяцев.
Необходимость в хирургическом удалении определяется индивидуально. К такому ходу событий приводят:
- стремительное разрастание гемангиомы печени – более чем на 50% от первоначальных размеров за год;
- объем более 5-6 см;
- кровотечение атипичной ткани;
- агрессивное проявление симптомов;
- неточное определение доброкачественности опухоли.
Питание
Питание при гемангиоме печени играет существенную роль в избавлении от нее. Пациенту в обязательном порядке назначается диета, чтобы не спровоцировать ухудшение ситуации (резкое разрастание атипичных клеток).
Диета при гемангиоме печени у взрослых и детей подразумевает исключение из рациона таких продуктов, как:
- газированные напитки;
- алкоголь и слабоалкогольные напитки;
- любой шоколад;
- яичные желтки;
- острые специи;
- груши, дыни;
- свежий хлеб.
Следует ограничить потребление жирной, жареной, копченой, соленой пищи.
Вместо этого необходимо сделать упор на:
- нежирные сорта рыбы;
- печень;
- молочные продукты;
- вязкие каши;
- овощи;
- не кислые фрукты.
Может быть дополнительно назначен прием витамина В12.
Ответы на распространенные вопросы
Какая профилактика при гемангиомах?
Так как точная причина появления гемангиомы не определена, грамотной профилактической мерой является проведение один раз в год ультразвуковой диагностики печени. При наличии каких-либо сомнений следует дополнительно сделать КТ или МРТ.
Обязательно ли соблюдать диету при гемангиоме печени?
Правильный подбор питания обязателен в случае, если пациент настроен на положительный результат. Употребление недопустимых в рационе заболевшего продуктов может спровоцировать резкий рост и разрыв гемангиомы.
Чем опасна гемангиома печени?
Ее главная опасность заключается в возможном разрыве тканей и последующим за ним кровотечением. Также существует вероятность, что из-за больших размеров опухоли будут сдавлены соседние органы, в связи с чем будет нарушена их работа.
Как лечить гемангиому печени?
Лечение данного недуга подбирается в зависимости от его размеров и скорости разрастания. Специалист может подобрать гормональную терапию, малоинвазивные методы (например, лучевую терапию), а также хирургическое вмешательство. Для закрепления эффекта от лечения необходимо соблюдать специальную диету.
Не нашли ответа на свой вопрос?
Наши специалисты готовы проконсультировать вас по телефону:
Источник
Нодулярная гиперплазия печени – очаговое образование в паренхиме печени, морфологически представляющее собой разрастание нормальных гепатоцитов вокруг сосудистой мальформации. Причины развития данной патологии неизвестны, определенная роль отводится сосудистым аномалиям, приему гормональных препаратов. В течение длительного времени заболевание может никак не проявляться; при достижении опухолью определенных размеров беспокоит болевой синдром, диспепсические явления. Диагностика включает проведение УЗИ печени, КТ, МРТ, обязательна биопсия. Лечение при малых размерах гиперплазии не требуется, при крупном образовании с тенденцией к росту проводится энуклеация опухоли или сегментарная резекция печени.
Общие сведения
Нодулярная гиперплазия печени (очаговый цирроз, паренхиматозная гамартома) является второй по частоте доброкачественной опухолью печени после гемангиомы. Согласно данным аутопсий, распространенность нодулярной гиперплазии составляет около 2%. Диагностироваться данная патология может в любом возрасте, но в 95% случаев выявляется у женщин 30-40 лет. Чаще всего это одиночное образование, не имеющее капсулы и не превышающее в диаметре 5 см; крайне редко встречается множественное поражение.
В гастроэнтерологии выделяют два типа нодулярной гиперплазии печени: классический (диагностируется в 80% случаев) и неклассический. Классический тип характеризуется наличием трех признаков: аномальной структуры дольки, извилистых толстостенных сосудов и гиперплазии желчных протоков; в 60% наблюдений обнаруживается центральный рубец с измененными сосудами разного калибра. При неклассическом типе всегда есть гиперплазия протоков, а один из оставшихся признаков (измененные сосуды или аномальная узловая архитектура) может отсутствовать. Неклассический тип подразделяют на три подтипа: аденоматозный гиперпластический, телеангиэктатический и нодулярную гиперплазию печени с клеточной атипией.
Нодулярная гиперплазия печени
Причины нодулярной гиперплазии печени
Этиология нодулярной гиперплазии печени окончательно не изучена. Предполагают, что гиперплазия печеночной паренхимы связана с наличием сосудистых мальформаций, нарушающих локальный кровоток, применением глюкокортикостероидов, высокодозированных комбинированных оральных контрацептивов, эндогенной гиперэстрогенией. Довольно часто нодулярная гиперплазия печени сочетается с гемангиомами; зарегистрированы случаи ее развития на фоне кавернозной трансформации или врожденного отсутствия воротной вены, воспалительных заболеваний печени, тромбоза печеночных вен, артериовенозного внутриорганного шунтирования, наследственных геморрагических телеангиэктазий и цереброваскулярных заболеваний.
Нодулярная гиперплазия печени макроскопически представляет собой плотный узел серо-коричневого цвета, четко отграниченный от окружающих тканей. Его размеры могут быть различными: от 1 до 25 сантиметров в диаметре. На разрезе определяется центральный рубец – фиброзная ткань, которая распространяется к периферии и разделяет образование на дольки. Микроскопическими признаками нодулярной гиперплазии печени являются дезорганизация печеночных долек: имеют место воспалительные клеточные инфильтраты, пролиферированные протоки, утолщенные сосуды и фиброзная ткань.
Симптомы нодулярной гиперплазии печени
В большинстве случаев данная патология протекает бессимптомно и выявляется при проведении обследования по поводу других заболеваний. Клинические признаки имеют место менее чем у половины пациентов, при этом они неспецифичны. Наиболее частый симптом – боль в животе, локализованная в правом подреберье. Чаще боль постоянная, ноющего характера, возможно чувство тяжести. Болевой синдром при нодулярной гиперплазии является следствием растяжения капсулы печени или сдавления соседних органов.
При нодулярной гиперплазии печени пациента также могут беспокоить диспепсические явления: тошнота, снижение аппетита. В случае больших размеров образования возможна его пальпация через переднюю брюшную стенку. Не установлена связь между размером опухоли и наличием симптомов, поскольку более важна локализация образования относительно окружающих органов. Крайне редко развиваются такие осложнения нодулярной гиперплазии печени, как механическая желтуха, кровотечение из опухоли и малигнизация.
Диагностика нодулярной гиперплазии печени
Консультация гастроэнтеролога обычно выявляет неспецифические признаки заболевания: диспепсические явления, болевой синдром малой интенсивности. При объективном обследовании пациента опухоль большого размера может быть обнаружена пальпаторно, в случае нарушения оттока желчи определяется желтушность кожи и склер. Лабораторные методы исследования не выявляют никаких специфических для нодулярной гиперплазии печени признаков. Редко обнаруживается некоторое повышение уровня аланинаминотрансферазы, билирубина. С целью дифференциальной диагностики со злокачественными новообразованиями печени обязательно проводится определение онкомаркеров: альфа-фетопротеина, СА 19-9, СЕА.
Диагностика нодулярной гиперплазии печени основана на инструментальных методиках. Характерным признаком данной патологии является «звездчатый шрам» в центре образования, но он выявляется не у всех пациентов, кроме того, может быть обнаружен при фиброламеллярной карциноме, внутрипеченочной холангиокарциноме и других заболеваниях. Это диагностическое ограничение относится ко всем методикам визуализации: УЗИ печени, КТ и МРТ печени. При проведении УЗИ органов брюшной полости единственным признаком нодулярной гиперплазии печени может быть смещение сосудов, иногда определяется гипоэхогенный ободок опухоли (сдавленные образованием сосуды и паренхима). Более информативно исследование в режиме допплеровского сканирования, при котором визуализируется гипертрофированная центральная артерия.
При проведении компьютерной томографии выявляется хорошо отграниченное образование, накопление контрастного вещества в области гиперплазии. МРТ дает аналогичные результаты: гиперинтенсивность контрастирования в артериальную фазу и гипоинтенсивность – в венозную. Неинвазивные методики обладают специфичностью только при классическом типе нодулярной гиперплазии печени. Высокой информативностью при проведении дифференциальной диагностики с другими гиперваскулярными образованиями обладает сцинтиграфия печени. В затруднительных случаях может быть выполнена ангиография, но данный метод также неспецифичен.
При невозможности установить диагноз в ходе неинвазивных исследований проводится биопсия, при этом большими критериями диагностики является наличие толстостенных сосудов, фиброзной прослойки, пролиферирующих протоков, узловой вид опухоли; малыми критериями – перисинусоидальный фиброз и синусоидальная дилатация. Диагноз достоверен при наличии трех больших критериев, вероятный – при определении двух больших и 1-2 малых.
Дифференциальная диагностика нодулярной гиперплазии проводится с другими доброкачественными и злокачественными образованиями печени, крупноузловым циррозом, а также с регенеративной гиперплазией при системных заболеваниях соединительной ткани.
Лечение и прогноз нодулярной гиперплазии печени
В большинстве случаев лечение нодулярной гиперплазии печени не требуется. Если опухоль не достигла больших размеров, не сдавливает соседние органы, не имеет тенденции к увеличению, основной целью является устранение этиологического фактора (если он известен). Отмены гормонального контрацептива, снижения дозировки системных глюкокортикостероидов может быть достаточно для уменьшения размеров образования и его полной регрессии. Однако пациент должен регулярно проходить обследование с целью контроля размеров опухоли и своевременного выявления показаний к хирургическому лечению.
Если нодулярная гиперплазия печени крупная, нарушает отток желчи, препятствует кровообращению или сдавливает соседние органы, проводится энуклеация опухоли или сегментарная резекция печени. Оперативное лечение также требуется в случаях, когда диагноз окончательно не установлен, и опухоль имеет тенденцию к увеличению (в такой ситуации удаление образования проводится даже при нормальных результатах биопсии).
Прогноз при нодулярной гиперплазии печени благоприятный. Заболевание в течение длительного времени может никак не беспокоить пациента, а осложнения развиваются крайне редко. Специфической профилактики не существует. Необходимо обоснованное назначение гормональных препаратов, а при установленном диагнозе обязательно регулярное проведение УЗИ печени для контроля над течением заболевания.
Источник
УЗИ сканер HS60
Профессиональные диагностические инструменты. Оценка эластичности тканей, расширенные возможности 3D/4D/5D сканирования, классификатор BI-RADS, опции для экспертных кардиологических исследований.
Еще сравнительно недавно фокальная нодулярная гиперплазия печени (ФНГ) относилась к редким (3%) объемным образованиям печени. Однако, учитывая применение современных методов визуализации, в настоящее время ФНГ занимает 3-е место среди доброкачественных образований печени после гемангиомы и аденомы [8, 10, 14].
Согласно морфологической классификации опухолей печени, ФНГ относится к опухолеподобным процессам и характеризуется гиперплазией печеночной паренхимы, разделенной на узлы фиброзными прослойками в виде звездчатого рубца [14]. Гиперпластические узлы без четких границ переходят в окружающую ткань, не сдавливая ее. Опухоль состоит из гепатоцитов, элементов желчных протоков, купферовских клеток и фиброзной ткани.
Происхождение гиперпластических узлов не совсем ясно. Не исключено, что составной их частью является доброкачественная опухоль – аденома, для которой характерно наличие соединительнотканной капсулы. Подобные узлы регенераторнорепаративного характера могут встретиться и в плотной цирротически измененной печени, подвергшейся субмассивному некрозу. По мнению некоторых авторов, сущность процесса заключается в том, что на месте полной гибели паренхимы отмечается запустение сосудистой системы с исчезновением сети аргирофильных волокон и развитием фиброзной соединительной ткани. Наряду с этим из сохранившихся остатков паренхимы могут образовываться новые узлы с характерными для них особенностями [8, 10, 14]. Считается, что ФНГ является реакцией гепатоцитов на локальные сосудистые мальформации (врожденные или приобретенные). Местные изменения кровотока ведут к появлению участков паренхимы с повышенным артериальным кровоснабжением и гиперплазии клеток печени.
ФНГ развивается в любом возрасте, одинаково часто у лиц разного пола. В то же время имеются данные о том, что подобные новообразования чаще диагностируются у женщин (в 82,2% случаев) [10, 17].
ФНГ встречается у 66,7% пациентов моложе 40 лет, в печени без гепатита и цирроза – у 83,3% [8, 9, 14, 17], в 57,7% случаев ФНГ расположена подкапсульно, в 33,7% – внутрипеченочно [9, 10, 17].
Макроскопически очаговая узловая гиперплазия представляет собой мягкоэластичный, четко ограниченный, иногда инкапсулированный узел серовато-коричневого цвета размером от 0,5 до 6 см. Узлы могут быть как одиночными, так и множественными и располагаться в периферических отделах правой (чаще) и левой доли. Иногда узлы заметно выбухают на поверхности печени, в редких случаях они имеют ножку. Узлы имеют дольчатую структуру с наличием фиброзных прослоек, отходящих, как правило, от центрально расположенного рубца.
При микроскопическом исследовании узлов определяют нормальные гепатоциты, содержащие гликоген и формирующие трабекулярные структуры. Местами наблюдается полиморфизм величины и формы зрелых гепатоцитов, они образуют синцитий. В центре печеночной доли, как правило, располагается центральная вена, имеются синусоиды, выстланные купферовскими клетками (звездчатые ретикулоэндотелиоциты). Портальные прослойки сформированы правильно, достаточно деликатны. В зоне звездчатого рубца и по ходу стромы располагаются сосуды. Сосу дис тый компонент весьма разнообразен как по содержанию (венозные, толстостенные артериальные сосуды с миксоматозной дегенерацией среднего слоя), так и по форме (гемангиоматоз). По ходу портальных септ определяются пролиферирующие желчные протоки, единичные мелкие узлы регенерации и лимфоплазмоцитарные инфильтраты. Эти признаки служат основными дифференциально-диагностическими критериями, позволяющими отличить ФНГ от печеночно-клеточной аденомы [17].
Выделяют 2 типа ФНГ: классическая и неклассическая. При классическом типе выделяют все 3 признака: аномальная нодулярная структура, извилистые толстостенные сосуды, гиперплазия желчных протоков. Центральный рубец присутствует в 65% наблюдений. Он всегда содержит измененные сосуды разного калибра: большие извилистые артерии с гипертрофией интимы и медии, крупные и мелкие вены, капилляры. При неклассическом типе отсутствует один из двух признаков (нодулярная структура или измененные сосуды), но гиперплазия протоков есть всегда. Централь ный рубец отсутствует. В свою очередь неклассический тип делится на 3 подтипа: телеангиэктатический (склонный к кровотечениям), аденоматозный и ФНГ с клеточной атипией.
Опухоль в большинстве случаев (66,7-80,8% пациентов) не проявляет себя клинически и может быть случайно обнаружена при проведении ультразвукового исследования (УЗИ) по иному поводу [18]. Специфичные лабораторные симптомы отсутствуют. ФНГ не озлокачествляется и край не редко вызывает осложнения в виде внутрибрюшного кровотечения.
Ультразвуковая картина ФНГ
Так, при УЗИ в В-режиме вид ФНГ неспецифичен и вариабелен. Чаще всего ФНГ печени выглядит как единичное очаговое образование с нечеткими или четкими, ровными или неровными контурами, несколько неоднородное по своей внутренней структуре, без капсулы. В 80% случаев (рис. 1) очаг изоэхогенный или гипоэхогенный [3, 8, 9, 11-14].
Рис. 1. Ультразвуковая картина ФНГ печени.
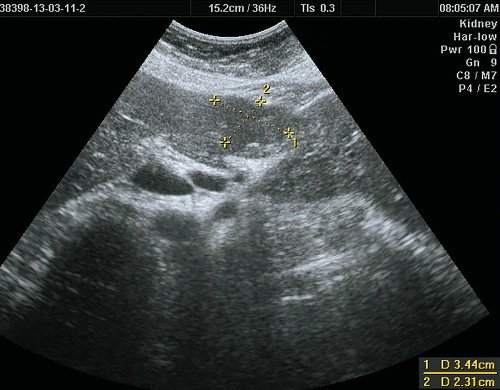
а) В-режим. В IV сегменте печени, выходя на контур печени, деформируя его, визуализируется тканевой плотности гипоэхогенное, несколько неоднородное по эхоструктуре образование размерами 50 х 40 мм, неправильной формы, с четкими ровными контурами.
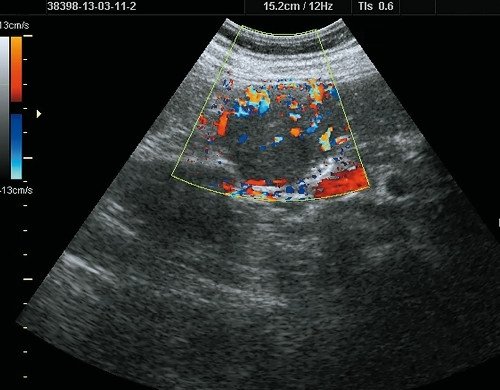
б) В режиме ЦДК выраженный кровоток в виде “баскетбольной корзинки”, определяется “питающая” артерия.
Использование режима цветового допплеровского картирования (ЦДК) выявляет высокую степень кровоснабжения образования (гиперваскулярное, с активным пульсирующим внутренним кровотоком). Типичным признаком ФНГ является “питающая” артерия. В очаге определяются множественные сосуды, которые имеют типичную картину “баскетбольной корзины” или “колеса со спицами”, характерную для ФНГ, обусловленную расходящимися от центра к периферии артериями. При допплерографии определяются артериальные сосуды в центре опухоли (с высокой скоростью: систолическая скорость 0,71 м/с, средняя систолическая скорость 0,33 м/с (20,0 ± 11,3 см/с), высокая диастолическая скорость, низкий индекс допплеровской перфузии печени, низкий пульсационный индекс 0,9 ± 0,35) и венозные по периферии [1, 2, 5 10, 14, 15]. Соотношение вен и артерий внутри образований 33 и 44% соответственно.
Для ФНГ характерно отсутствие артериовенозного шунтирования внутри опухоли, обычно кровоснабжение идет одной артерией.
При двухфазной динамической контрастной эхографии типичными признаками являются выраженная васкуляризация образования и быстрое контрастное усиление в раннюю артериальную фазу. В венозную паренхиматозную фазу контрастирования структура образования становится изо- или гиперэхогенной. Центральный рубец остается гипоэхогенным в артериальную и портальную фазы. Сохранение усиления в портальную и паренхиматозную фазы не характерно для метастазов и аденом, что является важным моментом в дифференциальной диагностике [3, 11, 16].
По данным некоторых авторов, чувствительность УЗИ в серошкальном режиме в диагностике ФНГ составляет 93,5%, чувствительность УЗИ с контрастом в диагностике ФНГ достигает 96% [11].
КТ фокальной узловой гиперплазии
На нативных компьютерных томограммах ФНГ представлена негомогенным (иногда гомогенным) образованием гиподенсной (пониженной) плотности (по данным некоторых авторов, гиподенсное у 69% пациентов) или изоденсным с зоной очень низкой плотности в центре (центральный рубец выявляется у 80% пациентов, как зона очень низкой плотности в центре) [9,10, 12, 14].
При нативном исследовании ФНГ может быть неотличима от гемангиомы печени: ФНГ гиподенсна, как и гемангиома, а зона пониженной плотности в узле может иметь звездчатый вид и ошибочно трактоваться как “гиалиновая щель” [9, 10, 17].
После контрастирования образование активно накапливает контраст в артериальную фазу (у 71-96% пациентов), становится гиперденсным при сравнении с окружающей тканью.
Контрастирование равномерно, за исключением зоны центрального рубца, после контрастного “усиления” рубец становится более гиперденсным. В отличие от гемангиомы, гиперконтрастные лакуны которой хотя и могут иметь высокую интенсивность, сравнимую с аортой, узел ФНГ буквально “заливает” контрастом всю площадь, хотя и не совсем равномерно, кроме центрального рубца. В венозную фазу гиперконтрастность сохраняется [9, 12, 14, 17, 18]. По данным других авторов, в венозную фазу в 53,3% случаев образование становится гомогенным и в 73,3% – изоденсным [18].
В позднюю (отсроченную) фазу контрастирования через 4-5 мин после введения контраста центральный рубец ФНГ интенсивно накапливает контрастное вещество и становится особенно хорошо заметен. Сам же узел ФНГ становится гиподенсным по отношению к паренхиме печени (в отличие от гемангиомы, которая на отсроченных сканах гиперденсна) [9, 12, 14, 17, 18].
Чувствительность КТ с контрастом в диагностике узловой гиперплазии достигает 80-100% [17, 18].
МРТ фокальной узловой гиперплазии
При МРТ на Т1- и Т2-взвешенных изображениях данная опухоль проявляется как гомогенное (у 66,7-94% пациентов), иногда неправильной формы, с нечеткими неровными контурами изоинтенсивное образование по сравнению с неизмененной паренхимой. В центре указанного образования визуа лизируется низкоинтенсивная структура линейной формы – соединительнотканный рубец. На Т1-взвешенных изображениях центральный рубец гипоинтенсивный, однако на Т2-взвешенных изображениях центральный рубец дает сильный сигнал – это объясняется тем, что рубец состоит из богато васкуляризированной молодой соединительной ткани [7-10, 12, 14, 17, 18].
Контрастное “усиление” при МРТ имеет такой же, как и при КТ, механизм накопления контраста. При контрастировании отмечается гомогенное усиление образования в раннюю фазу (25 с), кроме соединительнотканного рубца, и только позднее, после 45 с, центральный рубец дает на Т1взвешенных изображениях сильный сигнал. При отсроченном исследовании с контрастированием интенсивность сигнала от образования снижается с усилением контрастирования соединительнотканного рубца. Центральный рубец патогномоничен для ФНГ. Точность МРТ с контрастом в диагностике гиперплазии составляет 80-100% [7-10, 12, 14, 17, 18].
Ангиография узловой гиперплазии
Образование гиперсосудистое, гомогенное, контрастирование, выраженное в артериальную фазу [1, 2, 14]. Чувствительность ангиографии в диагностике узловой гиперплазии в пределах 82-97,3% [1, 2, 14].
Дифференциальная диагностика проводится с аденомой печени (рис. 2), а также с метастазами печени (рис. 3).
Рис. 2. Ультразвуковая картина аденомы печени.
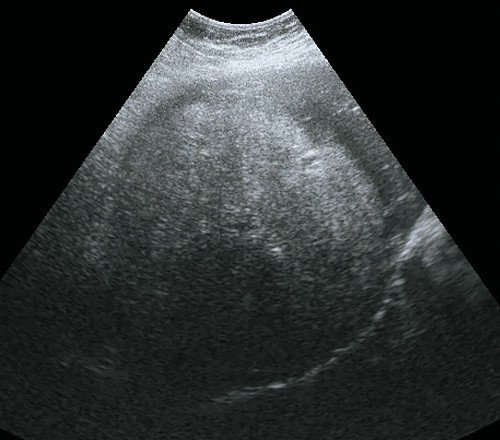
а) В-режим. Объемное образование VI-VII сегмента правой доли печени, гетерогенное, преимущественно повышенной эхогенности, с мелкими гипоэхогенными зонами, с ровными четкими контурами, гипоэхогенным ободком.
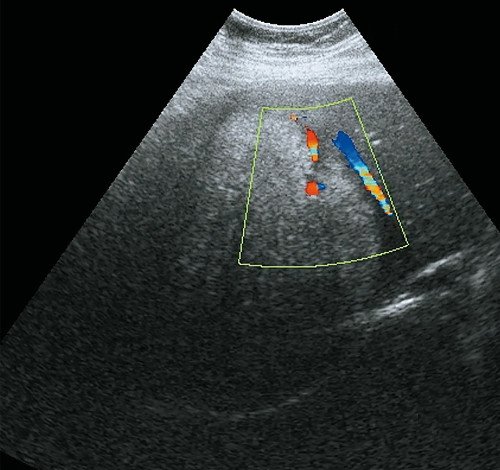
б) Режим ЦДК. Образование малососудистое, с отсутствием внутреннего кровотока.
Рис. 3. Ультразвуковая картина метастаза печени.
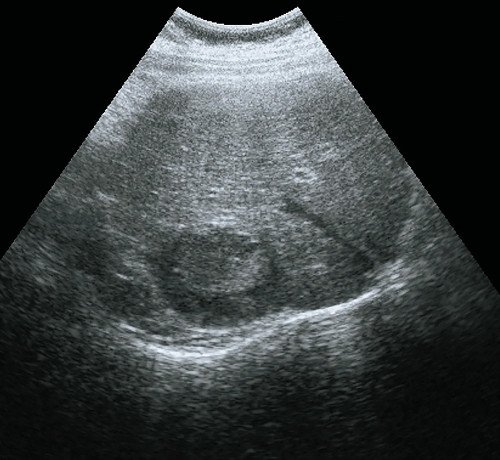
а) В-режим. В заднедиафрагмальных отделах печени визуализируется объемное образование размерами 50 х 37 мм, тканевой плотности, изоэхогенное, неоднородное по эхоструктуре, с выраженным гипоэхогенным ободком.
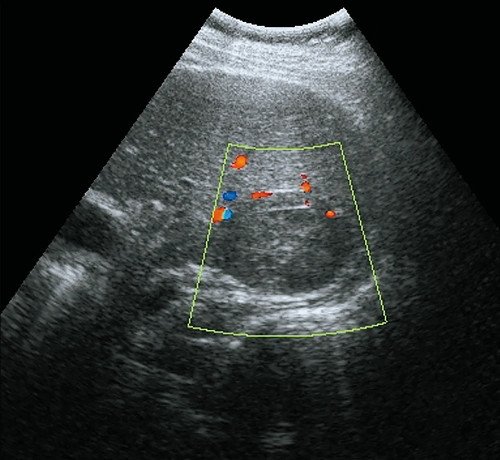
б) Режим ЦДК. Образование аваскулярное.
Лечение узловой гиперплазии
ФНГ требует динамического наблюдения с использованием радиологических методов [8]. Считая узловую гиперплазию гиперваскулярным образованием, одни авторы считают эффективным лечением данной патологии химиоэмболизацию печеночной артерии [1, 2, 5], другие рекомендуют выполнять оперативное лечение [4, 6].
Клиническое наблюдение 1
Пациентка Г., поступила с диагнозом: хронический гастродуоденит.
При УЗИ выявлено образование в печени (рис. 4).
Рис. 4. Ультразвуковая картина ФНГ печени у пациентки Г.
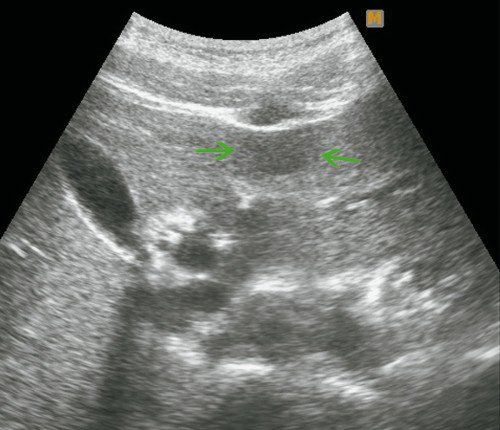
а) В-режим. В левой доле печени, в III сегменте, подкапсульно визуализируется гипоэхогенное образование размерами 28 х 16 мм, с четкими ровными контурами.
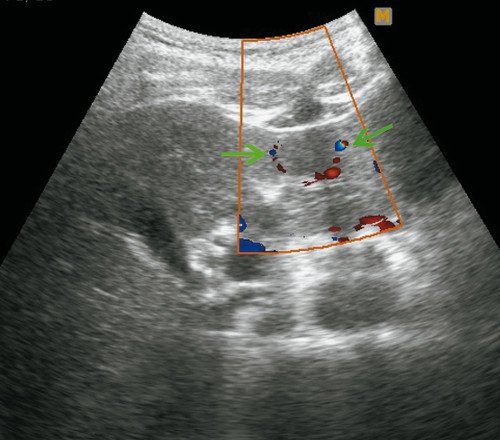
б) Режим ЦДК. Определяется “питающая” артерия.
Проведенная КТ (рис. 5) подтвердила диагноз ФНГ.
Рис. 5. Компьютерные томограммы ФНГ печени у пациентки Г.
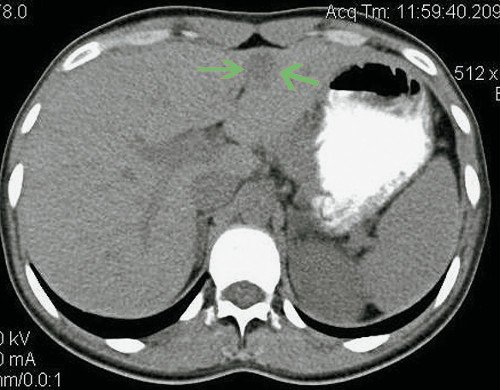
а) Нативная фаза. В проекции СII-III левой доли печени определяется очаговое образование пониженной плотности, с достаточно плотным контуром, размерами 27 х 15 мм.
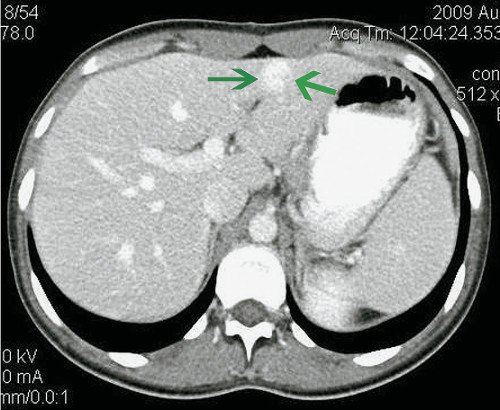
б) Артериальная фаза. При внутривенном контрастировании в артериальную фазу диффузно интенсивно “в виде вспышки” накапливает контрастное вещество.

в) Выделительная фаза. В отсроченную фазу происходит медленное вымывание контраста.
Клиническое наблюдение 2
Пациентка Р. поступила с диагнозом: аксиальная кардиофундальная грыжа пищеводного отдела диафрагмы.
При УЗИ выявлено образование в печени (рис. 6), которое при КТ печени (рис. 7) расценено как ФНГ.
Рис. 6. Ультразвуковая картина ФНГ печени у пациентки Р.
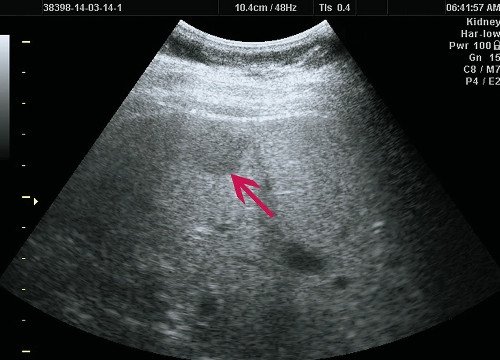
а) В-режим. В правой доле печени визуализируется гипоэхогенное образование до 20 мм, с четкими ровными контурами.
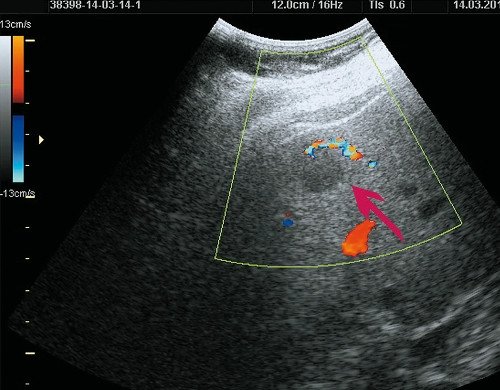
б) Режим ЦДК. Определяется “питающая” артерия.
Рис. 7. Компьютерные томограммы ФНГ печени у пациентки Р.
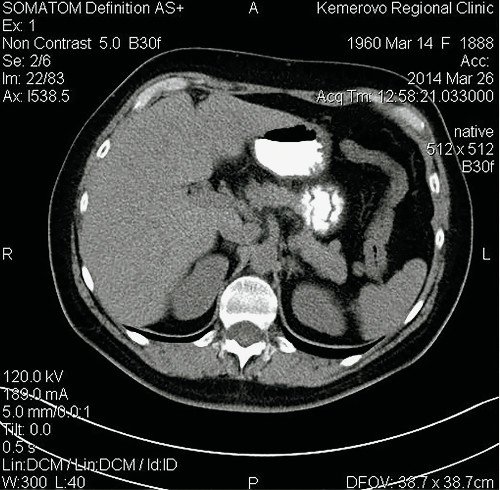
а) Нативная фаза.
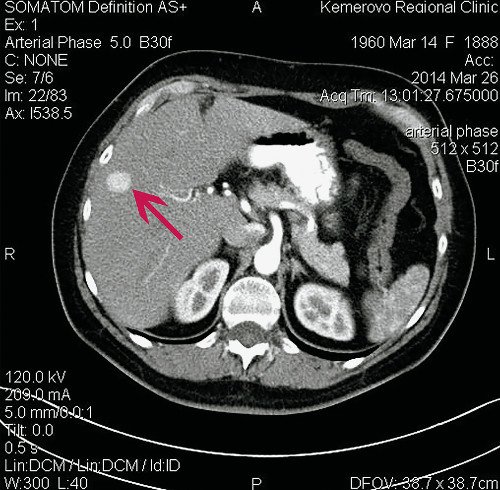
б) Артериальная фаза.
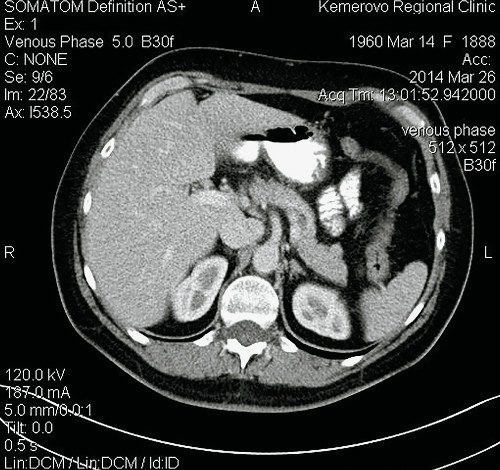
в) Выделительная фаза.
На границе СVIII/VII округлое образование размерами 15 х 15 х 18 мм, визуализируемое только в артериальную фазу. Заключение: гиперваскулярное образование правой доли печени. КТ-картина ФНГ.
В описанных клинических наблюдениях произведена диагностическая пункция образований под ультразвуковым контролем. Гистологическая верификация: ФНГ печени. Рекомендовано динамическое наблюдение.
Заключение
Таким образом, ФНГ – редко встречающееся заболевание печени, которое выявляется случайно при проведении УЗИ. Обязательным в дифференциально-диагностическом поиске должно быть проведение КТ брюшной полости. Сочетанное применение УЗИ и КТ в некоторых случаях позволяет поставить правильный диагноз и не применять пункционную биопсию или диагностическую лапаротомию. В сомнительных случаях, на наш взгляд, необходимо проведение биопсии образования с последующей гистологической верификацией.
Литература
- Акинфеев В.В., Дударев В.С., Дзюбан В.П., Хоружик С.А., Карман А.В., Ребеко И.В., Жарков В.В., Дорош Д.Д., Русинович В.М., Шавликова Л.А. // Материалы 5-го съезда лучевых диагностов Беларуси. 3-4 ноября 2005 г. Минск, 2005: 316-319.
- Дударев В.С., Аникфеев В.В., Дзюбан В.П., Фрадкин С.З., Машевский А.А., Жарков В.В., Кохнюк В.Т., Ребеко И.В., Дорош Д.Д. Диагностическая и интервенционная радиология при опухолевых заболеваниях печени // Материалы 5-го съезда лучевых диагностов Беларуси. 3-4 ноября 2005 г. Минск, 2005: 327-329.
- Зубарев А.В. Новые возможности ультразвука в диагностике объемных поражений печени и поджелудочной железы // Эхография. 2000; 2: 140-146.
- Ивашкин В.Г. Болезни печени и желчевыводящих путей. М.: М-Вести, 2005. 536 с.
- Кунцевич Г.И., Гаврилин А.В., Вишневский В.А., Бурцева Е.А. Комплексная ультразвуковая диагностика метастатического поражения печени // Ультразвуковая диагностика. 2004; 3: 13-20.
- Коваленко Ю.А., Чжао А.В., Чугунов А.О. Выбор объема оперативного вмешательства при очаговых заболеваниях печени // Анналы хирургической гепатологии. 2009; 14 (4): 79-87.
- Ратников В.А., Лубашев Я.А. Сложности и ошибки диагностики заболеваний печени при использовании комплексной МРТ // Материалы 9-й Российской конференции “Гепатология сегодня”. 22-24 марта 2004 г. Москва // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2004; 1 (Приложение № 12): 59.
- Шахиджанова С.В., Шария М.А. Диагностика очаговой узловой гиперплазии печени (данные комплексного обследования – магнитно-резонансная томография, компьютерная томография, ультразвуковое исследование // Вестник рентгенологии и радиологии. 2001; 1: 43-45.
- Attal P., Vilgrain V., Brancatelli G., Paradis V., Terris B., Belghiti J., Taouli B., Y. Telangiectatic focal nodular hyperplasia: US, CT, and MR imaging findings with histopathologic correlation in 13 cases // Radiology. 2003; 228 (2): 465-472.
- Buscarini E., Danesino C., Plauchu H., de Fazio C., Olivieri C., Brambilla G., Menozzi F., Reduzzi L., Blotta P., Gazzaniga P., Pagella F., Grosso M., Pongiglione G., Cappiello J., Zambelli A. High prevalence of hepatic focal nodular hyperplasia in subjects with hereditary hemorrhagic telangiectasia // Ultrasound Med Biol. 2004; 30 (9): 1089-1097.
- Bleuzen A., Tranquart F. Incidental liver lesions: diagnostic value of cadence contrast pulse sequencing (CPS) and SonoVue // Eur Radiol. 2004; 14 (Suppl. 8): 53-62.
- Fabre A., Audet P., Vilgrain V., Nguyen B.N., Valla D., Belghiti J., Degott C. Histologic scoring of liver biopsy in focal nodular hyperplasia with atypical presentation // Hepatology. 2002; 35 (2): 414-420.
- Harvey C.J., Albrecht T. Ultrasound of focal liver lesions // Eur Radiol. 2001; 11: 1578-1593.
- Kehagias D., Moulopoulos L., Antoniou A., Hatziioannou A., Smyrniotis V., Trakadas S., Lahanis S., Vlahos L. Focal nodular hyperplasia: imaging findings // Eur Radiol. 2001; 11 (2): 202-212.
- Kudo M., Tochio H., Zhou P. Differentiation of hepatic tumors by color Doppler imaging: role of the maximum velocity and the pulsatility index of the intratumoral blood flow al // Intervirology. 2004; 47 (3-5): 154-161.
- Leen E., Moug S.J., Horgan P. Potential impact and utilization of ultrasound contrast // Eur Radiol. 2004; 14: 16-24.
- Schmitz D., Kohler H.H., Heussel C.P., Lohr H.F., Galle P.R. Lymphoma-simulating presentation of focal nodular hyperplasia (FNH) of the liver // Z Gastroenterol. 2001; 39 (3): 219-224.
- Ye Q., Tang Z., Ma Z., Wu Z., Fan J., Qin L., Wang W. Differential diagnosis between hepatic focal nodular hyperplasia and hepatocellular carcinoma with negative alhpa-fetoprotein // Zhonghua Gan Zang Bing Za Zhi. 2000; 8 (3): 136-138.

УЗИ сканер HS60
Профессиональные диагностические инструменты. Оценка эластичности тканей, расширенные возможности 3D/4D/5D сканирования, классификатор BI-RADS, опции для экспертных кардиологических исследований.
Источник
