Сколько литров воздуха в сосуде
Воздух – неосязаемая величина, его невозможно пощупать, понюхать, он находится повсюду, но для человека он невидим, узнать, сколько весит воздух непросто, но возможно. Если поверхность Земли, как в детской игре расчертить на мелкие квадратики, размером 1х1 см, то вес каждого из них будет равен 1 кг, то есть в 1см2 атмосферы содержится 1 кг воздуха.
Можно ли это доказать? Вполне. Если соорудить весы из обычного карандаша и двух воздушных шаров, закрепив конструкцию на нити, карандаш будет находиться в равновесии, поскольку вес двух накачанных шариков одинаков. Стоит проткнуть один из шаров, перевес окажется в сторону надутого шарика, потому как воздух из поврежденного шарика вышел наружу. Соответственно, простой физический опыт доказывает, что воздух имеет некий вес. Но, если взвесить воздух на равнинной поверхности и в горах, то его масса окажется различной – горный воздух значительно легче, чем тот, которым мы дышим возле моря. Причин разного веса несколько:
Состав воздуха
Вес 1 м3 воздуха составляет 1,29 кг.
Можно ли доказать, что воздух имеет вес? Вполне. Если соорудить весы из обычного карандаша и двух воздушных шаров, закрепив конструкцию на нити, карандаш будет находиться в равновесии, поскольку вес двух накачанных шариков одинаков. Стоит проткнуть один из шаров, перевес окажется в сторону надутого шарика, потому как воздух из поврежденного шарика вышел наружу. Соответственно, простой физический опыт доказывает, что воздух имеет некий вес. Но, если взвесить воздух на равнинной поверхности и в горах, то его масса окажется различной – горный воздух значительно легче, чем тот, которым мы дышим возле моря.
Причин разного веса несколько:
- чем выше поднимается воздух, тем более разряженным он становится, то есть высоко в горах, давление воздуха будет составлять не 1 кг на см2, а вполовину меньше, но и содержание необходимого для дыхания кислорода так же уменьшается ровно вполовину, что способно вызвать головокружение, тошноту и боль в ушах;
- содержание воды в воздухе.
В состав воздушной смеси входят:
- Азот – 75,5%;
- Кислород – 23,15%;
- Аргон – 1,292%;
- Углекислый газ – 0,046%;
- Неон – 0,0014%;
- Метан – 0,000084%;
- Гелий – 0,000073%;
- Криптон – 0,003%;
- Водород – 0,00008%;
- Ксенон – 0,00004%.
Рассмотрим, что из себя представляют газы, которые формируют воздух?
Азот
Содержание азота в воздухе – 78% по объему и 75% по массе, то есть этот элемент доминирует в атмосфере, имеет звание одного из самых распространенных на Земле, и, кроме того, содержится и за пределами зоны обитания человека – на Уране, Нептуне и в межзвездных пространствах. Итак, сколько азота в воздухе, мы уже разобрались, остался вопрос о его функции. Азот необходим для существования живых существ, он входит в состав:
- белков;
- аминокислот;
- нуклеиновых кислот;
- хлорофилла;
- гемоглобина и др.
В среднем около 2% живой клетки составляют как раз атомы азота, что объясняет, зачем столько азота в воздухе в процентах объема и массы.
Азот также является одним из инертных газов, добываемых из атмосферного воздуха. Из него синтезируют аммиак, используют для охлаждения и в других целях.
Кислород
Содержание кислорода в воздухе – один из самых популярных вопросов. Сохраняя интригу, отвлечемся на один забавный факт: кислород открыли дважды – в 1771 и 1774 годах, однако из-за разницы в публикациях открытия, почести открытия элемента достались английскому химику Джозефу Пристли, который фактически выделил кислород вторым. Итак, доля кислорода в воздухе колеблется около 21% по объему и 23% по массе. Вместе с азотом эти два газа образуют 99% всего земного воздуха. Однако процент кислорода в воздухе меньше, чем азота, и при этом мы не испытываем проблем с дыханием. Дело в том, что количество кислорода в воздухе оптимально рассчитано именно для нормального дыхания, в чистом виде этот газ действует на организм подобно яду, приводит к затруднениям в работе нервной системы, сбоям дыхания и кровообращения. При этом недостаток кислорода также негативно сказывается на здоровье, вызывая кислородное голодание и все связанные с ним неприятные симптомы. Поэтому сколько кислорода в воздухе содержится, столько и нужно для здорового полноценного дыхания.
Аргон
Аргон в воздухе занимает третье место, он не имеет запаха, цвета и вкуса. Значимой биологической роли этого газа не выявлено, однако он обладает наркотическим эффектом и даже считается допингом. Добытый из атмосферы аргон используют в промышленности, медицине, для создания искусственной атмосферы, химического синтеза, пожаротушения, создания лазеров и пр.
Углекислый газ
Углекислый газ составляет атмосферу Венеры и Марса, его процент в земном воздухе куда ниже. При этом огромное количество углекислоты содержится в океане, он регулярно поставляется всеми дышащими организмами, выбрасывается за счет работы промышленности. В жизни человека углекислый газ используется в пожаротушении, пищевой промышленности как газ и как пищевая добавка Е290 – консервант и разрыхлитель. В твердом виде углекислота – один из самых известных хладагентов «сухой лед».
Неон
Тот самый загадочный свет дискотечных фонарей, яркие вывески и современные фары используют пятый по распространенности химический элемент, который также вдыхает человек – неон. Как и многие инертные газы, неон оказывает на человека наркотическое действие при определенном давлении, однако именно этот газ используют в подготовке водолазов и других людей, работающих при повышенном давлении. Также неоново-гелиевые смеси используются в медицине при расстройствах дыхания, сам неон используют для охлаждения, в производстве сигнальных огней и тех самых неоновых ламп. Однако, вопреки стереотипу, неоновый свет не синий, а красный. Все остальные цвета дают лампы с другими газами.
Метан
Метан и воздух имеют очень древнюю историю: в первичной атмосфере, еще до появления человека, метан был в куда большем количестве. Сейчас этот газ, добываемый и используемый как топливо и сырье в производстве, не так широко распространен в атмосфере, но по-прежнему выделяется из Земли. Современные исследования устанавливают роль метана в дыхании и жизнедеятельности организма человека, однако авторитетных данных на этот счет пока нет.
Гелий
Посмотрев, сколько гелия в воздухе, любой поймет, что этот газ не относится к числу первостепенных по важности. Действительно, сложно определить биологическое значение этого газа. Не считая забавного искажения голоса при вдыхании гелия из шарика. Однако гелий широко применяется в промышленности: в металлургии, пищевой промышленности, для наполнения воздухоплавающих судов и метеорологических зондов, в лазерах, ядерных реакторах и т.д.
Криптон
Речь не идет о родине Супермена. Криптон – инертный газ, который в три раза тяжелее воздуха, химически инертен, добывается из воздуха, используется в лампах накаливания, лазерах и все еще активно изучается. Из интересных свойств криптона стоит отметить, что при давлении в 3,5 атмосферы он оказывает наркотический эффект на человека, а при 6 атмосферах приобретает резкий запах.
Водород
Водород в воздухе занимает 0,00005% по объему и 0,00008% по массе, но при этом именно он – самый распространенный элемент во Вселенной. О его истории, производстве и применении вполне можно написать отдельную статью, поэтому сейчас ограничимся небольшим списком отраслей: химическая, топливная, пищевая промышленности, авиация, метеорология, электроэнергетика.
Ксенон
Последний в составе воздуха, изначально и вовсе считавшийся только примесью к криптону. Его название переводится как «чужой», а процент содержания и на Земле, и за ее пределами минимальный, что обусловило его высокую стоимость. Сейчас без ксенона не обходятся: производство мощных и импульсных источников света, диагностика и наркоз в медицине, двигатели космических аппаратов, ракетное топливо. Кроме того, при вдыхании ксенон значительно понижает голос (обратный эффект гелию), а с недавнего времени вдыхание этого газа причислено к списку допингов.
Количество ингредиентов в составе воздуха может меняться и, соответственно, масса воздуха так же претерпевает изменения в сторону увеличения или уменьшения.
- воздух всегда содержит пары воды. Физическая закономерность такова, что чем выше температура воздуха, тем больше воды в нем содержится. Этот показатель называется влажностью воздуха и влияет на его вес.
В чем измеряется вес воздуха? Существует несколько показателей, которые определяют его массу.
Сколько весит куб воздуха?
При температуре, равной 0° по Цельсию вес 1 м3 воздуха составляет 1,29 кг.
То есть, если в комнате мысленно выделить пространство высотой, шириной и длиной, равными 1м, то в этом воздушном кубе будет находиться именно это количество воздуха.
Если воздух имеет вес и вес, достаточно ощутимый, почему человек не чувствует тяжести? Такое физическое явление, как атмосферное давление, подразумевает, что на каждого жителя планеты давит воздушный столб весом 250 кг. Площадь ладони взрослого человека, в среднем, равна 77 см2. То есть, в соответствии с физическим законами, каждый из нас держит на ладони 77 кг воздуха! Это равноценно тому, что мы постоянно носим в каждой руке по 5 пудовых гирь. В реальной жизни это не под силу даже тяжелоатлету, однако, с такой нагрузкой каждый из нас справляется легко, потому что атмосферное давление давит с двух сторон, как снаружи человеческого организма, так и изнутри, то есть разница в конечном итоге равна нулю.
Свойства воздуха таковы, что он по-разному действует на организм человека. Высоко в горах, из-за недостатка кислорода у людей возникают зрительные галлюцинации, а на большой глубине, соединение кислорода и азота в особую смесь – «веселящий газ» может создавать чувство эйфории и ощущение невесомости.
Зная эти физические величины можно рассчитать массу атмосферы Земли – то количество воздуха, которое удерживается в околоземном пространстве силами тяготения. Верхняя граница атмосферы заканчивается на высоте 118 км, то есть, зная вес м3 воздуха, можно поделить всю заемную поверхность на воздушные столбы, с основанием 1х1 м и сложить полученную массу таких колонн. В конечном итоге, она будет равна 5,3*1015 тонн. Вес воздушной брони планеты достаточно велик, но и он составляет лишь одну миллионную долю от общей массы земного шара. Атмосфера Земли служит своеобразным буфером, сохраняющим Землю от неприятных космических сюрпризов. От одних только солнечных бурь, которые достигают поверхности планеты, атмосфера теряет в год до 100 тысячи тонн от своей массы! Такой невидимый и надежный щит – воздух.
Сколько весит литр воздуха?
Человек не замечает, что его постоянно окружает прозрачный и практически невидимый воздух. Можно ли увидеть этот неосязаемый элемент атмосферы? Наглядно, перемещение воздушных масс ежедневно транслируется на телевизионном экране – теплый или холодный фронт приносит долгожданное потепление или обильный снегопад.
Что еще мы знаем о воздухе? Наверное, то, что он жизненно необходим всем живым существам, обитающим на планете. Человек каждые сутки вдыхает и выдыхает порядка 20 кг воздуха, четвертая часть которого потребляется мозгом.
Вес воздуха можно измерять в разных физических величинах, в том числе и в литрах.
Вес одного литра воздуха будет равняться 1,2930 грамм, при давлении 760 мм рт. столба и температуре, равной 0°С.
Кроме привычного газообразного состояния воздух может встречаться и в жидком виде. Для перехода субстанции в данное агрегатное состояние потребуется воздействие огромного давления и очень низких температур. Астрономы предполагают, что существуют планеты, поверхность которых полностью покрыта жидким воздухом.
Источниками кислорода, необходимого для существования человека, являются леса Амазонии, которые продуцируют до 20% этого важного элемента на всей планете.
Леса – это действительно «зеленые» легкие планеты, без которых существование человека попросту невозможно. Поэтому живые комнатные растения в квартире являются не просто предметом интерьера, они очищают воздух в помещении, загрязнение которого в десятки раз выше, чем на улице.
Чистый воздух давно стал дефицитом в мегаполисах, загрязненность атмосферы настолько велика, что люди готовы покупать чистый воздух. Впервые «продавцы воздуха» появились в Японии. Они производили и продавали чистый воздух в консервных банках и любой житель Токио мог на ужин открыть баночку чистейшего воздуха, и насладиться его свежайшим ароматом.
Чистота воздуха оказывает значительное влияние не только на здоровье человека, но и животных. В загрязненных районах экваториальных вод, возле населенных людьми мест десятками гибнут дельфины. Причиной смерти млекопитающих является загрязненная атмосфера, на вскрытии животных легкие дельфинов напоминают легкие шахтеров, забитые угольной пылью. Очень чувствительны к загрязнению воздуха и обитатели Антарктиды – пингвины, если воздух содержит большое количество вредных примесей, они начинают тяжело и прерывисто дышать.
Для человека чистота воздуха так же очень важна, поэтому после работы в офисе врачи рекомендуют совершать ежедневные часовые прогулки в парке, лесу, за городом. После такой «воздушной» терапии, жизненные силы организма восстанавливаются и значительно улучшается самочувствие. Рецепт этого бесплатного и эффективного лекарства известен с давних времен, многие ученые, правители считали обязательным ритуалом ежедневные прогулки на свежем воздухе.
Для современного городского жителя лечение воздухом очень актуальна: небольшая порция живительного воздуха, вес которой равен 1-2 кг, является панацеей от многих современных недугов!
Физические свойства воздуха
Как и у всякой смеси веществ, сегодня можно установить физические свойства воздуха.
| Свойство | Значение |
|---|---|
| Средняя молярная масса (средняя масса одного моля вещества) | 28,98 г/моль |
| Плотность сухого воздуха при нормальном атмосферном давлении | 1,29 кг/м3 |
| Средняя удельная теплоемкость при постоянном давлении | 1,005 кДж / (кг·К) |
| Средняя удельная теплоемкость при постоянном объеме | 0,717 кДж/(кг·К) |
| Показатель адиабаты (отношение теплоемкости при постоянном давлении к теплоемкости при постоянном объеме) | 1,40 |
| Теплопроводность при 0℃ | 0,0243 Вт / (м·К) |
| Скорость звука в воздухе при нормальных условиях | 331 м/с (1193 км/ч) |
| Средний коэффициент теплового расширения в интервале температур 0–100°C (изменение объема при постепенном увеличении температуры при постоянном давлении) | 3,67·10−3 1/К |
| Коэффициент динамической вязкости воздуха при нормальных условиях (динамическая вязкость – внутреннее сопротивление молекул движению внутри вещества согласно закону Ньютона) | 17,2 мкПа·с |
| Растворимость воздуха в воде | 29,18 см3/л |
| Показатель преломления при нормальных условиях (показатель преломления означает изменение угла движения световых и любых других волн в веществе) | 1,0002926 |
| Коэффициент изменения показателя преломления | 2,8·10−9 1/Pa |
| Средняя поляризуемость молекулы | 1,7·10−30 |
Источник
Задача 62.
Вычислить массу: а) 2л Н2 при 15 °С и давлении 100,7кПа (755мм рт. ст.); 6) 1м3 N2 при 10 °С и давлении 102,9 кПа (772мм рт. ст.); в) 0,5 м3 Cl2 при 20 °С и давлении 99,9 кПа (749,3мм рт. ст.).
Решение:
Зависимость между объёмом газа, давлением и температурой выражается общим уравнением, объединяющим законы Гей-Люссака и Бойля-Мариотта:
где P и V – давление и объём газа при температуре T; P0 (101,325кПа) и V0 – давление и объём газа при нормальных условиях; T0 (273К) – абсолютная температура. Преобразуя уравнение, получим выражение для расчета объёма газов при нормальных условиях:
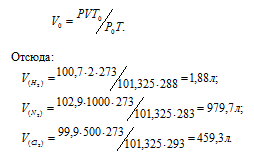
Рассчитаем массу каждого газа, учитывая, что мольный объём газа равен 22,4л и, зная молекулярную массу газов, получим:
Ответ: а) 0,168г; б) 1.23кг; в) 1,456кг.
Задача 63.
Определить объем, занимаемый 0,07кг N2 при 21°С и давлении 142 кПа (106 мм рт. ст.).
Решение:
Зная мольный объём и мольную массу азота (28г/моль), находим объём, который будет занимать 0,07кг (70г) азота при нормальных условиях:
Затем приведём полученный объём к температуре Т = 21оС (294К) и Р = 142кПа, используя выражение, объединяющее законы Гей-Люссака и Бойля-Мариотта:
где P и V – давление и объём газа при температуре T; P0 (101,325кПа) и V0 – давление и объём газа при нормальных условиях; (273 К) – абсолютная температура. Преобразуя уравнение, получим выражение для расчета объёма газа при заданной температуре
Ответ: 43л.
Задача 64.
Бертолетова соль при нагревании разлагается с образованием КСI и О2. Сколько литров кислорода при 0 °С и давлении 101,3 кПа можно получить из 1 моля КСIО3?
Решение:
Уравнение реакции термического разложения бертолетовой соли имеет вид:
Из уравнения реакции следует, что из двух молей бертолетовой соли образуется три моля кислорода, т.е. из одного моля соли образуется полтора моля кислорода (2:3 = 1:х; x = 1.3/2 = 1,5моль).
Объём кислорода при нормальных условиях (T0 =0 °С и P0 =101.325кПа) можно рассчитать по формуле:
V(B) – объём газа, л;
(B) – количество газа, моль;
V(M) – мольный объём, 22,4л.
Тогда
V(кислорода) = 1,5 . 22,4 = 33,6л.
Ответ: 33,6л.
Задача 65.
Сколько молей содержится в 1м3 любого газа при нормальных условиях?
Решение:
Зная, что один моль любого газа при нормальных условиях (Т0 =0 °С и Р0 =101.325 кПа) занимает 22,4л, рассчитаем количество молей газа в 1м3 (1000 л) из пропорции:
Ответ: 44,64моль.
Задача 66.
Чему равно атмосферное давление на вершине Казбека, если при 0 °С масса 1л взятого там воздуха равна 700 мг?
Решение:
Мольная масса воздуха равна 29 г/моль. Нормальными условиями для газов являются температура 0 °С и давление 101,325 кПа (760 мм рт ст.). Масса одного литра воздуха при нормальных условиях равна 1296,64 мг:
Теперь рассчитаем атмосферное давление на вершине Казбека из пропорции:
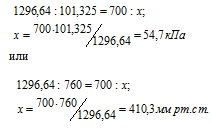
Ответ: 54,7к Па (410,3 мм рт. ст.).
Задача 67.
При взаимодействии одного объема СО и одного объема Сl2 образуется один объем фосгена. Установить формулу фосгена.
Решение:
По условию задачи выходит, что из молекулы угарного газа и одной молекулы хлора образуется одна молекула фосгена. Так как молекула угарного газа СО состоит из одного атома углерода и одного атома кислорода, а молекула хлора Cl2 состоит из двух атомов хлора, то, следовательно, молекула фосгена будет состоять из одного атома углерода, одного атома кислорода и двух атомов хлора. Тогда формула фосгена будет иметь вид: CCl2O.
Уравнение реакции будет иметь вид:
СО + Cl2 → ССl2O.
Ответ: ССl2O.
Задача 68.
Какой объем СО2 получается при сгорании 2л бутана? Объемы обоих газов измерены при одинаковых условиях.
Решение:
Уравнение реакции горения бутана имеет вид:
2С4Н10 + 13О2 = 8СО2 + 10Н2О
Из уравнения реакции следует, что при сгорании одного моля бутана образуется четыре моля углекислого газа. Известно, что при одинаковых условиях одинаковое количество газов занимают одинаковый объём. Один моль любого газа при нормальных условиях занимает объём в 22,4 л.
Исходя, из этих утверждений рассчитаем объём выделившегося углекислого газа при сгорании 2 л бутана, составив пропорцию:
Ответ: 8л.
Задача 69.
В замкнутом сосуде при 120°С и давлении 600 кПа находится смесь, состоящая из трех объемов О2 и одного объема СН4. Каково будет давление в сосуде, если взорвать смесь и привести содержимое сосуда к первоначальной температуре?
Решение:
Уравнение реакции имеет вид:
CH4 + 2O2 → CO2 + 2H2O
Из уравнения реакции следует, что из одной молекулы метана и двух молекул кислорода образуются одна молекула углекислого газа и две молекулы воды, т. е. реакция протекает без изменения объёма. Начальный объём системы состоял из одного объёма метана и трёх объёмов кислорода, после реакции в системе остался один объём не прореагировавшего кислорода и три объёма продуктов реакции (один объём метана и два объёма паров воды). Поскольку реакция протекает без изменения объёма, а по окончании реакции содержимое сосуда приводится к первоначальной температуре, а общее число молекул газов не изменилось, то давление в системе останется прежним, т. е. 600 кПа.
Ответ: не изменится.
Задача 70. После взрыва 0,020 л смеси водорода с кислородом осталось 0,0032 л кислорода. Выразить в процентах по объему первоначальный состав смеси.
Решение:
Находим объём газов, вступивших в реакцию:
0,020 – 0,0032 = 0,0168 л.
Уравнение реакции горения водорода имеет вид:
2Н2 + О2 = 2Н2О
При взаимодействии водорода с кислородом из двух молекул водорода и одной молекулы кислорода получаются две молекулы воды, следовательно, из трёх молекул образовавшихся газов одна молекула будет принадлежать кислороду. Таким образом, объём кислорода, вступившего в реакцию, будет составлять одну треть объёма смеси газов – продуктов реакции. Отсюда количество кислорода, вступившего в реакцию, составляет 0,00565 л (0 0168/3 = 0,0056).
Следовательно, общее количество кислорода до реакции составляло 0,0088л (0,0056 + 0,0032 = 0,0088).
Тогда содержимое водорода до реакции составляло 0,0112л (0,02 – 0,0088 = 0.0112).
Рассчитаем в процентах первоначальный состав газовой смеси:
Ответ: 56%Н2; 44%О2.
Источник
