Сколько молекул газа содержит сосуд объемом 1л

- Главная
- Вопросы & Ответы
- Вопрос 15637655
Мари Умняшка
более месяца назад
Просмотров : 4
Ответов : 1
Лучший ответ:
Таня Масян
чтобы найти число молекул нужно использовать формулу: n=N/Na
Найдем n из формулы: р=2/3nE
n=3p/2E = 6*10^5/12*10²¹= 0,5*10^-16
И теперь найдем число молекул N=nNa=0,5*10^-16*6*10^23= 3*10^7
более месяца назад
Ваш ответ:
Комментарий должен быть минимум 20 символов
Чтобы получить баллы за ответ войди на сайт

Лучшее из галереи за : неделю месяц все время































Другие вопросы:
Суррикат Мими
морфологический разбор слова слышится 5 класс
более месяца назад
Смотреть ответ
Просмотров : 1
Ответов : 1
Главный Попко
сколько протонов находится в ядре изотопа урана с массовым числом 238? число нейтронов в данном изотопе больше числа протонов на 54.
более месяца назад
Смотреть ответ
Просмотров : 1
Ответов : 1
Суррикат Мими
Ответьте на вопрос . Для чего люди используют интернет (4 предложения ) пожалуйста помогите !!!
более месяца назад
Смотреть ответ
Просмотров : 1
Ответов : 1
Главный Попко
Помогите сделать тест
более месяца назад
Смотреть ответ
Просмотров : 1
Ответов : 1
Картинок: 1
Энджелл
Высота равностороннего треугольника равна 11 корней 3. Найдите сторону. Помогите пожалуйста!
более месяца назад
Смотреть ответ
Просмотров : 1
Ответов : 1
Источник
- Главная
- Вопросы & Ответы
- Вопрос 33017
Суррикат Мими
более месяца назад
Просмотров : 62
Ответов : 1
Лучший ответ:
Васян Коваль
Чтобы найти число молекул нужно использовать формулу: n=N/NaНайдем n из формулы: р=2/3nEn=3p/2E = 6*10^5/12*10²¹= 0,5*10^-16И теперь найдем число молекул N=nNa=0,5*10^-16*6*10^23= 3*10^7
более месяца назад
Ваш ответ:
Комментарий должен быть минимум 20 символов
Чтобы получить баллы за ответ войди на сайт

Лучшее из галереи за : неделю месяц все время































Другие вопросы:
Васян Коваль
Облака-Именительный падеж. Единственное число. Кто?Что?Облака И.п.
более месяца назад
Смотреть ответ
Просмотров : 25
Ответов : 1
Зачетный Опарыш
Выполните действия: 1)(7/15-1/6)+2/5; 2)(3/8-1/9)+25/36; 3)(8/9-5/6)+2/3; 4)(7/8-13/20)+9/10; 5)(7/18-1/12)+5/6; 6)(3/4-8/15)+17/20;наверное вы знаете что это/-дробь
более месяца назад
Смотреть ответ
Просмотров : 5
Ответов : 1
Онтонио Веселко
В треугольнике ABC AB равен BC равен 10 Найдите медиану проведенную из вершины B к стороне AD C если A C равно 8
более месяца назад
Смотреть ответ
Просмотров : 13
Ответов : 1
Энджелл
Для приготовления пирожного Картошка, на 16 порции использовали 80 грамм масла (сливочного) Сколько понадобится масла на 18 порции? на 22 порции? Пропорции
более месяца назад
Смотреть ответ
Просмотров : 4
Ответов : 1
Васян Коваль
Назовите причины восстания народов Поволжья с 1552 – 1584 года?
более месяца назад
Смотреть ответ
Просмотров : 22
Ответов : 1
Источник
Задачи для самостоятельного решения Сколько молекул газа содержит сосуд объемом 1 л, если средняя кинетическая энергия поступательного движения молекулы 6*10-21Дж? Давление в сосуде 2*1015Па. Молекула массой 10-24кг движется со средней квадратичной скоростью 400 м/с. Определите изменение концентрации молекул при изменении давления от 1015 до 4*104 Па. Определите среднюю квадратичную скорость молекул гелия при температуре 100 °С Определите, во сколько раз средняя квадратичная скорость молекул водорода больше средней квадратичной скорости молекул кислорода, если энергии поступательного движения молекул равны. Во сколько раз изменится давление одноатомного газа в результате уменьшения его объема в 3 раза и увеличения средней кинетической энергии молекул в 2 раза? Во сколько раз средняя квадратичная скорость молекул водяного пара в летний день при температуре 30°С больше, чем в зимний день при температуре -30 °С?
Слайд 15 из презентации ««Тепловое движение атомов и молекул»
Размеры: 720 х 540 пикселей, формат: .jpg.
Чтобы бесплатно скачать слайд для использования на уроке,
щёлкните на изображении правой кнопкой мышки и нажмите «Сохранить изображение как…».
Скачать всю презентацию ««Тепловое движение атомов и молекул.ppt» можно
в zip-архиве размером 1646 КБ.
Молекулярная физика
краткое содержание других презентаций о молекулярной физике
«Расположение молекул» – Очень слабое взаимодействие между молекулами. Озон. Твердое. Золото. Вещество. Слабое взаимодействие между молекулами. Жидкое. Большие Расстояния Между молекулами. Масло. Невидимая. Различие в молекулярном строении твердых тел, жидкостей и газов. Видимая. Лед. Промежутки между молекулами малы, но притяжение мало и форма не сохраняется.
«Масса и размеры молекул» – Самая маленькая молекула. Число молекул. Количество вещества. Найти формулы. Объём слоя масла. Массы молекул. Молекула. Масса и размеры молекул. Фотографии молекул. Решить задачи. Учитель. Синквейн. Размер молекулы. Постоянная Авогадро.
«Игра «Вещества»» – Две сестры. Капля масла. Цена деления приборов. Процесс диффузии. Диффузия. Определите цену деления. Детский резиновый шар. Значение между двумя ближайшими штрихами. Весы. Строение вещества. Стоматологи. С помощью какого прибора можно увидеть молекулу. Урок проводится по типу телевизионной передачи.
«Строение вещества, молекулы» – Гераклит. Молекула. Из чего состоят вещества. Электронный микроскоп. Рефлексия. Физические тела. Атом. Михаил Васильевич Ломоносов. Мир строения вещества. Вода окрасилась синим цветом. Стальной шарик. Атомы принято означать символами. Окружающие нас тела называются физическими телами. Молекула воды.
«Химические элементы» – Подгруппа щелочных металлов. Таблица Мейера. Простейшее водородное соединение ВН3-бороводород. Подгруппа углерода. Закон Мозли. Современная формулировка периодического закона. Значение периодического закона. Формула водородных соединений НЭ. Энергия ионизации. Атомные объемы. Закон триад. Подгруппа бериллия.
«Строение вещества физика» – При каких условиях ? 4. закрытая бутылка наполовину заполнена керосином. Решение качественных задач Домашнее задание: § 9, задание 2(1). Урок № 5 «Различия в молекулярном строении газов, жидкостей, тв.тел. Примеры диффузии в природе. Наблюдения и опыты». Свойства газов (по рис.) Решение задач: 1. Почему возд.
Всего в теме
«Молекулярная физика»
21 презентация
Источник
Задача 62.
Вычислить массу: а) 2л Н2 при 15 °С и давлении 100,7кПа (755мм рт. ст.); 6) 1м3 N2 при 10 °С и давлении 102,9 кПа (772мм рт. ст.); в) 0,5 м3 Cl2 при 20 °С и давлении 99,9 кПа (749,3мм рт. ст.).
Решение:
Зависимость между объёмом газа, давлением и температурой выражается общим уравнением, объединяющим законы Гей-Люссака и Бойля-Мариотта:
где P и V – давление и объём газа при температуре T; P0 (101,325кПа) и V0 – давление и объём газа при нормальных условиях; T0 (273К) – абсолютная температура. Преобразуя уравнение, получим выражение для расчета объёма газов при нормальных условиях:
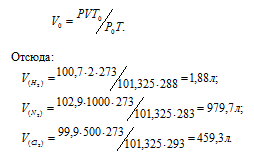
Рассчитаем массу каждого газа, учитывая, что мольный объём газа равен 22,4л и, зная молекулярную массу газов, получим:
Ответ: а) 0,168г; б) 1.23кг; в) 1,456кг.
Задача 63.
Определить объем, занимаемый 0,07кг N2 при 21°С и давлении 142 кПа (106 мм рт. ст.).
Решение:
Зная мольный объём и мольную массу азота (28г/моль), находим объём, который будет занимать 0,07кг (70г) азота при нормальных условиях:
Затем приведём полученный объём к температуре Т = 21оС (294К) и Р = 142кПа, используя выражение, объединяющее законы Гей-Люссака и Бойля-Мариотта:
где P и V – давление и объём газа при температуре T; P0 (101,325кПа) и V0 – давление и объём газа при нормальных условиях; (273 К) – абсолютная температура. Преобразуя уравнение, получим выражение для расчета объёма газа при заданной температуре
Ответ: 43л.
Задача 64.
Бертолетова соль при нагревании разлагается с образованием КСI и О2. Сколько литров кислорода при 0 °С и давлении 101,3 кПа можно получить из 1 моля КСIО3?
Решение:
Уравнение реакции термического разложения бертолетовой соли имеет вид:
Из уравнения реакции следует, что из двух молей бертолетовой соли образуется три моля кислорода, т.е. из одного моля соли образуется полтора моля кислорода (2:3 = 1:х; x = 1.3/2 = 1,5моль).
Объём кислорода при нормальных условиях (T0 =0 °С и P0 =101.325кПа) можно рассчитать по формуле:
V(B) – объём газа, л;
(B) – количество газа, моль;
V(M) – мольный объём, 22,4л.
Тогда
V(кислорода) = 1,5 . 22,4 = 33,6л.
Ответ: 33,6л.
Задача 65.
Сколько молей содержится в 1м3 любого газа при нормальных условиях?
Решение:
Зная, что один моль любого газа при нормальных условиях (Т0 =0 °С и Р0 =101.325 кПа) занимает 22,4л, рассчитаем количество молей газа в 1м3 (1000 л) из пропорции:
Ответ: 44,64моль.
Задача 66.
Чему равно атмосферное давление на вершине Казбека, если при 0 °С масса 1л взятого там воздуха равна 700 мг?
Решение:
Мольная масса воздуха равна 29 г/моль. Нормальными условиями для газов являются температура 0 °С и давление 101,325 кПа (760 мм рт ст.). Масса одного литра воздуха при нормальных условиях равна 1296,64 мг:
Теперь рассчитаем атмосферное давление на вершине Казбека из пропорции:
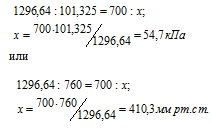
Ответ: 54,7к Па (410,3 мм рт. ст.).
Задача 67.
При взаимодействии одного объема СО и одного объема Сl2 образуется один объем фосгена. Установить формулу фосгена.
Решение:
По условию задачи выходит, что из молекулы угарного газа и одной молекулы хлора образуется одна молекула фосгена. Так как молекула угарного газа СО состоит из одного атома углерода и одного атома кислорода, а молекула хлора Cl2 состоит из двух атомов хлора, то, следовательно, молекула фосгена будет состоять из одного атома углерода, одного атома кислорода и двух атомов хлора. Тогда формула фосгена будет иметь вид: CCl2O.
Уравнение реакции будет иметь вид:
СО + Cl2 → ССl2O.
Ответ: ССl2O.
Задача 68.
Какой объем СО2 получается при сгорании 2л бутана? Объемы обоих газов измерены при одинаковых условиях.
Решение:
Уравнение реакции горения бутана имеет вид:
2С4Н10 + 13О2 = 8СО2 + 10Н2О
Из уравнения реакции следует, что при сгорании одного моля бутана образуется четыре моля углекислого газа. Известно, что при одинаковых условиях одинаковое количество газов занимают одинаковый объём. Один моль любого газа при нормальных условиях занимает объём в 22,4 л.
Исходя, из этих утверждений рассчитаем объём выделившегося углекислого газа при сгорании 2 л бутана, составив пропорцию:
Ответ: 8л.
Задача 69.
В замкнутом сосуде при 120°С и давлении 600 кПа находится смесь, состоящая из трех объемов О2 и одного объема СН4. Каково будет давление в сосуде, если взорвать смесь и привести содержимое сосуда к первоначальной температуре?
Решение:
Уравнение реакции имеет вид:
CH4 + 2O2 → CO2 + 2H2O
Из уравнения реакции следует, что из одной молекулы метана и двух молекул кислорода образуются одна молекула углекислого газа и две молекулы воды, т. е. реакция протекает без изменения объёма. Начальный объём системы состоял из одного объёма метана и трёх объёмов кислорода, после реакции в системе остался один объём не прореагировавшего кислорода и три объёма продуктов реакции (один объём метана и два объёма паров воды). Поскольку реакция протекает без изменения объёма, а по окончании реакции содержимое сосуда приводится к первоначальной температуре, а общее число молекул газов не изменилось, то давление в системе останется прежним, т. е. 600 кПа.
Ответ: не изменится.
Задача 70. После взрыва 0,020 л смеси водорода с кислородом осталось 0,0032 л кислорода. Выразить в процентах по объему первоначальный состав смеси.
Решение:
Находим объём газов, вступивших в реакцию:
0,020 – 0,0032 = 0,0168 л.
Уравнение реакции горения водорода имеет вид:
2Н2 + О2 = 2Н2О
При взаимодействии водорода с кислородом из двух молекул водорода и одной молекулы кислорода получаются две молекулы воды, следовательно, из трёх молекул образовавшихся газов одна молекула будет принадлежать кислороду. Таким образом, объём кислорода, вступившего в реакцию, будет составлять одну треть объёма смеси газов – продуктов реакции. Отсюда количество кислорода, вступившего в реакцию, составляет 0,00565 л (0 0168/3 = 0,0056).
Следовательно, общее количество кислорода до реакции составляло 0,0088л (0,0056 + 0,0032 = 0,0088).
Тогда содержимое водорода до реакции составляло 0,0112л (0,02 – 0,0088 = 0.0112).
Рассчитаем в процентах первоначальный состав газовой смеси:
Ответ: 56%Н2; 44%О2.
Источник
