Сосуды пуповины не спазмируются
Пуповина представляет собой спиралевидно закрученную трубку, которая соединяет плод с плацентой. Снаружи пуповина покрыта плодными оболочками. Она содержит две артерии и одну вену.
По вене пуповины течет артериальная кровь, несущая кислород к органам плода. По пупочным артериям течет венозная кровь от плода к плаценте, эта кровь содержит продукты обмена веществ плода. Сосуды пуповины находятся в особом студнеобразном веществе, которое фиксирует их и предохраняет от травм, а также осуществляет обмен веществ между кровью плода и амниотической жидкостью. Пуповина начинает формироваться с 2-3 недели беременности и растет вместе с малышом. К моменту рождения ее длина составляет 45-60 см (длина пуповины в среднем соответствует росту ребенка), а диаметр – 1,5-2 см.
Пуповина может по-разному прикрепляться к плаценте. В одних случаях прикрепление происходит в центре плаценты (центральное прикрепление), в других – сбоку (боковое прикрепление). Иногда пуповина прикрепляется к плодным оболочкам, не доходя до самой плаценты (оболочечное прикрепление). В этих случаях сосуды пуповины подходят к плаценте между плодными оболочками. Такое прикрепление плаценты является фактором риска по возникновению плодово-плацентарной недостаточности.
У пуповины могут быть и такие особенности, как истинные и ложные узлы. Ложные узлы представляют собой местные утолщения пуповины вследствие варикозного расширения вены пуповины или скопления вартонова студня. Они не влияют на развитие плода и процесс родов. Истинные узлы пуповины образуются на ранних сроках беременности, когда плод еще мал, что позволяет ему проскочить через петлю пуповины. Истинные узлы пуповины могут повлиять на исход родов. При натяжении пуповины узел затягивается, прекращаются поступление и отток крови по сосудам. В этом случае возникает острая гипоксия плода.
Патологией развития пуповины является также состояние, при котором сформирована только одна артерия пуповины вместо двух, у некоторых плодов с одной артерией пуповины наблюдаются различные пороки развития. Причиной такого формирования пуповины могут стать факторы, вызывающие пороки развития плода – так называемые тератогенные факторы (химические вещества, некоторые лекарственные препараты, ионизирующая радиация, генетические заболевания родителей).
Некоторые проблемы могут возникнуть и в связи с укорочением пуповины. Укорочение пуповины можно подразделить на абсолютное и относительное. При абсолютном укорочении пуповины длина пуповины составляет менее 45 см. В течение беременности это состояние никак не сказывается на развитии малыша. Во время родов как при относительной, так и при абсолютной короткости пуповины из-за ее натяжения преждевременно может отслоиться плацента, которую пуповина тянет за собой, что создает прямую угрозу жизни плода.
Ложное укорочение пуповины возникает при обвитии пуповины вокруг шеи и туловища плода. Причиной обвития пуповины может являться чрезмерно большая ее длина (более 70 см), а также повышенная двигательная активность плода, которая может быть связана с хронической внутриутробной гипоксией плода. Причины хронической нехватки кислорода различны – это и заболевания матери, и заболевания плода, и патология плаценты. Обвитие пуповины может быть однократным, двукратным и даже трехкратным. Во время беременности это состояние, как правило, не влияет на плод, но во время родов могут возникнуть проблемы. Натяжение или пережатие сосудов пуповины приводит к нарушению тока крови.
Такие состояния, как укорочение пуповины (абсолютное и относительное) и истинные узлы пуповины, во время родов могут привести к острой внутриутробной гипоксии плода. Она проявляется изменением числа сердцебиений. (В норме сердцебиение плода составляет 120-160 ударов в минуту). При возникновении острой внутриутробной гипоксии плода в околоплодных водах появляется первородный кал (меконий), воды окрашиваются в зеленый цвет. Появление всех этих симптомов требует неотложной терапии. В первую очередь необходимо устранить причину гипоксии, что достигается путем скорейшего родоразрешения. Метод родоразрешения зависит от периода родов и оттого, как далеко продвинулась предлежащая часть плода (головка или тазовый конец) по родовым путям. Если острая гипоксия возникла во время беременности или в первый период родов, женщине делают кесарево сечение. Во втором периоде родов, когда головка или тазовый конец уже близко к выходу из малого таза, применяют различные акушерские пособия, ускоряющие завершение второго периода родов.
К счастью, подобное состояние возникает не часто. Поэтому обвитие пуповины и узлы пуповины не являются абсолютным показанием к плановой операции кесарева сечения (абсолютную короткость пуповины диагностировать до родов невозможно). Эти состояния являются относительным показанием к операции, т.е. кесарево сечение делают лишь в тех случаях, когда кроме них, имеются еще и другие относительные показания к операции (возраст женщины старше 30 лет, нетяжёлые формы гестоза и т.п.).
Единственным методом, позволяющим предположить патологию пуповины, является ультразвуковое сканирование. С помощью УЗИ можно выявить аномалии пуповины, такие, как неправильное развитие сосудов (единственная артерия пуповины), истинные и ложные узлы пуповины, обвитие пуповиной. А вот длину пуповины во время беременности определить практически невозможно.
Особо надо сказать о диагностике обвития пуповины. Порой при исследовании видны только петли пуповины в области шеи, но определить, обвивают ли они шею, невозможно. В этих случаях помогает допплерометрическое исследование, в ходе которого можно изучить движение крови по сосудам – в том числе и пуповины. Кроме того во время родов используют метод кардиотокографии, который позволяет следить за числом сердечных сокращений, или выслушивают сердце¬биение плода при помощи стетоскопа.
Таким образом, во время беременности патологию пуповины можно лишь заподозрить. Однако своевременно проведенные ультразвуковые исследования помогут врачам сделать ваши роды безопасными.
Источник
Нарушение маточно-плацентарного кровотока – симптомокомплекс, развивающийся во время беременности вследствие расстройства функций плаценты или происходящих в ее строении морфологических изменений. Со стороны матери клиника может отсутствовать. На фоне акушерской патологии возникает гипоксия плода, проявляющаяся учащением или замедлением сердечных сокращений, снижением активности. Диагностика нарушений маточно-плацентарного кровотока осуществляется посредством УЗИ, КТГ, допплерометрии. Лечение проводится в стационаре консервативным путем с использованием препаратов, улучшающих гемодинамику в сосудах плаценты.
Общие сведения
Нарушение маточно-плацентарного кровотока – акушерская патология, возникающая вследствие расстройства функций гемодинамики в системе «женщина-плацента-ребенок». Диагностируется такая аномалия примерно у 4% беременных. В 25% случаев заболевание развивается на фоне уже имеющихся экстрагенитальных заболеваний пациентки. Нарушение маточно-плацентарного кровотока представляет угрозу для здоровья и жизни плода, поскольку может приводить к недостаточному поступлению питательных веществ, что осложняется задержкой внутриутробного развития, гипоксией и даже возможной гибелью ребенка.
Опасность нарушения маточно-плацентарного кровотока зависит от выраженности и продолжительности существования данной акушерской патологии. Чем меньше питательных веществ поступает к ребенку, тем выше вероятность формирования отклонений. По статистике, около 85% новорожденных, подверженных такой патологии, появляются на свет с признаками гипоксии или врожденными аномалиями различной степени выраженности. Нарушение маточно-плацентарного кровотока способно возникать на разных этапах беременности, чаще всего оно диагностируется во 2-3 триместре вынашивания. Расстройство гемодинамики, развившееся до 16 недель, нередко заканчивается самопроизвольными выкидышами.
Нарушение маточно-плацентарного кровотока
Причины нарушения маточно-плацентарного кровотока
Нарушение маточно-плацентарного кровотока развивается вследствие неправильного формирования ворсинчатого слоя плодных оболочек еще в период закладки плаценты или в результате влияния на организм матери неблагоприятных факторов, становящихся причиной расстройства гемодинамики в нормальной плаценте. Патогенез заболевания заключается в неполноценной маточно-плацентарной перфузии, приводящей к недостаточному поступлению кислорода к плоду. Как следствие, нарушение маточно-плацентарного кровотока запускает механизм гипоксических изменений, способствующих задержке развития плода.
Спровоцировать нарушение маточно-плацентарного кровотока могут эндогенные и экзогенные причины. К первой группе относятся факторы, влияющие изнутри организма будущей матери. Риск развития патологии наблюдается при наличии у женщины сахарного диабета, заболеваний почек, сердца и сосудов, на фоне дисфункции щитовидной железы. Формированию нарушения маточно-плацентарного кровотока способствует отягощенный акушерский анамнез – поздний гестоз, угрозы прерывания, множественные аборты и выкидыши, доброкачественные опухоли матки. Высокий риск расстройства гемодинамики наблюдается на фоне беременности с резус-конфликтом, а также, если пациентка страдала бесплодием.
Нарушение маточно-плацентарного кровотока нередко развивается на фоне генетических нарушений у плода и при наличии врожденных пороков репродуктивной системы матери (при двурогой или седловидной матке, перегородках в полости органа). Вероятность возникновения акушерской патологии существует и при половых инфекциях, а также, если больная перенесла вирусные заболевания, к примеру, грипп, ОРВИ. К экзогенным факторам, способствующим нарушению маточно-плацентарного кровотока относится работа на вредных производствах, употребление наркотиков и алкоголя, курение. Неблагоприятным образом сказывается и нерациональное питание. В группу риска по развитию нарушения маточно-плацентарного кровотока входят женщины в возрасте до 18 и старше 35 лет. Риск аномальной гемодинамики присутствует при постоянных стрессах, интенсивных физических нагрузках.
Классификация нарушения маточно-плацентарного кровотока
В зависимости от локализации патологических изменений в акушерстве различают несколько степеней тяжести нарушения маточно-плацентарного кровотока:
- 1а – характеризуется расстройством гемодинамики между маткой и плацентой, при этом к ребенку попадает достаточное количество питательных веществ.
- 1б – нарушение кровообращения происходит в круге «плод-плацента».
- 2 степень – нарушение маточно-плацентарного кровотока наблюдается в круге «плод-плацента-мать», однако гипоксия выражена незначительно.
- 3 степень – сопровождается критическим расстройством показателей гемодинамики, может привести к гибели ребенка или самопроизвольному аборту.
Учитывая срок гестации, на котором происходит нарушение маточно-плацентарного кровотока, можно выделить следующие виды патологии:
- Первичная – возникает в первом триместре, обычно развивается на фоне аномальной имплантации, нарушений в формировании или прикреплении плаценты.
- Вторичная – диагностируется после 16 недель эмбриогенеза, как правило, провоцируется негативными внешними факторами или состоянием здоровья матери.
Симптомы нарушения маточно-плацентарного кровотока
Клинические проявления нарушения маточно-плацентарного кровотока зависят от выраженности акушерской аномалии. Со стороны матери патологические признаки наблюдаются не всегда. У пациентки может развиться гестоз, нередко присутствует угроза выкидыша или преждевременных родов, что сопровождается болью в животе и в области паха. Возможно появление кровянистой слизи из половых путей. На фоне нарушения маточно-плацентарного кровотока происходит активизация деятельности условно-патогенной флоры, нередко возникают кольпиты. Это осложнение нарушения маточно-плацентарного кровотока может стать причиной внутриутробного инфицирования плода.
Нарушение маточно-плацентарного кровотока более выражено со стороны ребенка. Заподозрить признаки гипоксии плода в ряде случаев может сама пациентка. Патологическое состояние проявляется снижением двигательной активности ребенка. В ходе осмотра акушер-гинеколог выявляет учащение или уменьшение частоты сердечных сокращений у малыша, что также является достоверным признаком нарушения маточно-плацентарного кровотока. Недостаток питательных компонентов способен вызвать преждевременную отслойку плаценты. При этом состояние женщины и плода стремительно ухудшается, возможно возникновение угрозы для жизни.
Диагностика и лечение нарушения маточно-плацентарного кровотока
Выявить нарушение маточно-плацентарного кровотока можно в ходе УЗИ. О наличии акушерской патологии свидетельствуют патологии плаценты и внутриутробная задержка развития плода, проявляющаяся несоответствием размеров анатомических частей сроку гестации. Оценить степень нарушения маточно-плацентарного кровотока удается с помощью допплерографии. Для оценки функциональности сердечно-сосудистой системы ребенка используется КТГ. Характерным признаком является тахикардия или брадикардия, возникшая на фоне гипоксии.
Лечение нарушения маточно-плацентарного кровотока проводится в условиях стационара. Больной показан постельный режим, исключение стрессов и интенсивных физических нагрузок. Консервативная терапия заключается в использовании препаратов для купирования нарушений маточно-плацентарного кровотока и улучшения оксигенации плода. Также используются антиагреганты и средства, улучшающие питание тканей головного мозга. При нарушении маточно-плацентарного кровотока показано употребление витаминов, блокаторов кальциевых каналов. Последние применяются для устранения гипертонуса матки.
При нарушении маточно-плацентарного кровотока все усилия специалистов направлены на продление ведения беременности до 37-38 недель. При условии достаточной эффективности медикаментозной терапии через 4 недели пациентку переводят на амбулаторное лечение. Если справиться с признаками нарушения маточно-плацентарного кровотока не удается и состояние плода продолжает ухудшаться, осуществляют преждевременное родоразрешение методом экстренного кесарева сечения. Если беременность удалось доносить до 38 недель, роды могут происходить естественным путем. Во втором периоде показано использование вакуум-экстракции плода или наложение акушерских щипцов. В случае развития нарушения маточно-плацентарного кровотока на фоне других заболеваний у матери осуществляется плановое кесарево сечение в сроке 38 недель.
Прогноз и профилактика нарушения маточно-плацентарного кровотока
Своевременное лечение нарушения маточно-плацентарного кровотока позволяет женщине продлить беременность до 37 недель гестации и родить абсолютно здорового младенца. При первичной форме патологии возможна внутриутробная гибель плода или самопроизвольный выкидыш. Профилактика нарушения маточно-плацентарного кровотока состоит в устранении экстрагенитальных патологий еще до момента зачатия, ранней постановке на учет к акушеру-гинекологу и выполнении всех его рекомендаций. Беременная должна придерживаться рационального питания, отказаться от вредных привычек, стрессов и тяжелой физической работы. Уменьшить вероятность развития нарушения маточно-плацентарного кровотока позволяет также исключение контактов с возможными источниками инфекций.
Источник
Vasa Previa (Предлежание Сосудов, ПС) может иметь катастрофические последствия для жизни плода и новорожденного. На самом деле существует всего несколько пренатальных ультразвуковых диагнозов, которые имеют настолько выраженное, прямое влияние на исход родов и так значительно повышают выживаемость среди тех, у кого было своевременно диагностировано данное состояние. Исключение ПС с помощью ультразвука занимает менее минуты и обязательно должно входить в стандартные скрининговые ультразвуковые исследования.
«Vasa Previa отняла у нас нашего прекрасного мальчика, нашего первого ребёнка, и мы никогда уже не будем такими, как прежде. Всё о чем мы можем мечтать, это чтобы хоть у кого-то одного из медицинского персонала хватило предусмотрительности сканировать нас на предмет наличия такого состояния.» – Natalie Samat, чей ребёнок Henry Cameron Samat умер врезультате не диагностированного предлежания сосудов в 2005 году.
Что такое Vasa Previa?
Vasa Previa (Предлежание Сосудов) – (от лат. vasa – сосуд, prеvia – находящийся перед, спереди от) – это состояние, характеризующееся наличием сосудов, имеющих связь с плодово-плацентарным кровотоком, проходящих свободно во внеплацентарных плодных оболочках, расположенных между предлежащей частью плода и шейкой матки.
Эти сосуды проходят незащищёнными ни Вартоновым студнем, ни тканью плаценты, вследствие чего легко ранимы и подвержены сдавлению на любом этапе беременности, хотя большинство осложнений происходит в родах.
Vasa Previa является патологическим состоянием, не имеющим клинических проявлений, приводящим в некоторых случаях к развитию плодного кровотечения во время беременности и родов, и как следствие, ведущее к смерти плода/новорожденного.
Различают два типа ПС
1-й тип – наличие над внутренним зевом свободных сосудов пуповины, не защищенных Вартоновым студнем при оболочечном прикреплении пуповины (ОПП) – состояние, при котором пуповина прикрепляется не к ткани плаценты, а к околоплодным оболочкам на некотором расстоянии от края плаценты. ОПП является одной из первых причин ПС, описанных в литературе. Диагностируется анте- или постнатально в среднем от 0,4 до 1,8% случаев всех беременностей, приводя при этом к ПС от 1 до 3% случаев, или в среднем один случай VP на 50 случаев ОПП. При многоплодной беременности частота ОПП намного увеличивается и встречается от 3,6 до 16% в случаях беременностью двойней. У моноамниональных монохориональных двоен ОПП наблюдается в 16%, у диамниональных монохориональных двоен – в 13%, а у дихориональных двоен – в 7% случаев. В случаях беременности тройней ОПП встречается в 28,2% случаев.
2-й тип – наличие над внутренним зевом незащищенных сосудов, соединяющих между собой доли плаценты при двудольной плаценте, или при наличии дополнительных долей, при возможно нормальном прикреплении пуповины к основной доле плаценты.
Из всех случаев ПС тип 1 встречается почти в 90% обнаружения ПС.
Частота встречаемости ПС примерно 1:2500 родов, но есть вероятность того, что на самом деле эта цифра недооценена, так как часть случаев могут проходить без осложнений и не попадать в отчёты. При этом есть работы показывающие, что частота ПС после ЭКО 1:300 беременностей.
В чём опасность?
Учитывая тот факт, что ПС является патологическим состоянием без каких-либо клинических проявлений, данная патология остается одной из опаснейших по развитию осложнений со стороны плода, таких как смерть в результате кровотечения при разрыве ПС либо внутриутробной асфиксии, при пережатии сосудов.
Одними из самых опасных осложнений ПС являются разрыв и возникающее плодное кровотечение. В большинстве случаев повреждение ПС происходит одномоментно с разрывом плодных оболочек, имея при этом «общую точку разрыва». Описаны случаи разрывов сосудов, проходящих свободно в оболочках, расположенных на расстоянии от места первоначального разрыва оболочек. В данных случаях сосуды повреждаются из-за продолжающегося разрыва плодных оболочек во время продвижения плода в процессе родов, что объясняет случаи кровотечения через 12 и более часов после момента разрыва плодных оболочек.
Учитывая тот факт, что объем циркулирующей крови плода к 38 неделям беременности составляет 80-110 мл/кг веса, то начавшееся кровотечение из ПС требует экстренной операции кесарева сечения, так как потеря уже 100 мл плодной крови может привести к развитию геморрагического шока и к смерти плода. Коварной чертой такого кровотечения является то, что состояние матери при этом не меняется, остаётся стабильным.
Перинатальная смертность при не диагностированном ПС составляет 55-75%.
История
Первым ПС при оболочечном прикреплении пуповины описал H. A. Wrisberg в 1773 году, он публиковал свои находки о «свободных сосудах в оболочках, выходящих из плаценты и связывающих ее с пуповиной плода в нижней части матки в месте ее расширения при родах».
В 1778 году E. Sandifort доложил о следующем случае обнаружения «прикрепления пуповины к краю плаценты» и о «свободных сосудах в оболочках, выходящих с противоположной месту прикрепления пуповины стороны плаценты и входящих в сеть сосудов пуповины плода».
В 1801 J.-F. Lobstein первым высказал предположение о «возможном разрыве свободных сосудов, проходящих в оболочках между пуповиной и плацентой, а также между плацентой и ее дополнительными долями, с возможным кровотечением, которое может привести к быстрой смерти плода» .
Но только в 1831 году R. Benckiser в своей «Dissertation inaugurale» сообщил о первом случае смерти новорожденного вследствие кровотечения, связанного с «разрывом венозной ветви, проходящей в 6 см от края плаценты над отверстием матки, во время разрыва амниотических оболочек». Именно после этого случая в европейской, в частности во франкоязычной, литературе за кровотечением, возникающим вследствие разрыва VP, закрепилось название «кровотечение Бенкизера»
Первое ультразвуковое описание ПС было в 1987 году. Gianopoulos и соавторы описали случай УЗ диагностики предлежания сосудов у беременной с добавочной долей плаценты.
В 1990г Nelson впервые сообщил об использовании цветового допплеровского картирования (ЦДК) для диагностики ПС.
И лишь в 1996 году описан первый случай выявления ПС во время скринингового УЗИ во втором триместре, благодаря чему на 35 неделе родился здоровый ребёнок путём операции кесарево сечение.
Но проблема Vasa Previa так и оставалась в разряде «отдельных научных статей, о которых мало кто знал» до очередной трагедии, которая случилась в семье адвокатов Natalie и Daren Samat, когда в 2005 году в результате не диагностированного ПС на 13-м дне жизни скончался их ребёнок Henry. Проблема получила широкую огласку именно благодаря стараниям этих людей, основанному ими благотворительному фонду https://vasaPrevia.co.uk/ и требованию к NHS National Screening Committee Великобритании включить исследование на предмет ПС в скрининг второго триместра.

Natalie и Daren Samat
В 2008 году National Screening Committee ответил, что на данный момент не достаточно доказательств необходимости включения данного обследования в программу скрининга и что есть обеспокоенность о гипердиагностике, которая повлечёт ненужные операции кесарево сечение.
Роль УЗИ в диагностике Предлежания Сосудов
В январе 2014 года в журнале Journal of Ultrasound in Medicine была опубликована статья «Natural History of Vasa Previa Across Geion Using a Screening Protocol», в которой описывается большое исследование, проводившееся с июня 2005 по июнь 2012гг, включившее в себя 27 573 беременных, которым целенаправленно проводилось УЗ исследование на предмет Vasa Previa во время скрининга второго и третьего триместров.
Показаниями для проведения исследования были:
Предлежание плаценты на более ранних сроках, которая «поднялась»
Vasa Previa в прошлые беременности
Оболочечное прикрепление сосудов в области нижнего сегмента матки
Добавочная доля плаценты в области нижнего сегмента матки
Беременность двойней
Диагноз Предлежание Сосудов выставлялся в случае обнаружения оболочечного прикрепления сосудов в пределах 2-х сантиметров от внутреннего зева при трансвагинальном исследовании с использованием серой шкалы, ЦДК и энергетического Доплера.
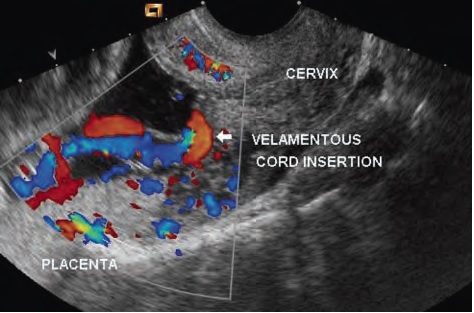
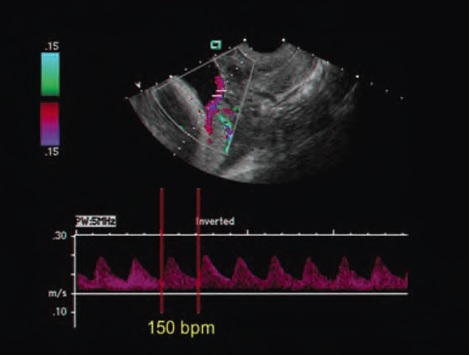
Был выявлен 31 случай ПС, что соответствовало частоте 1.1:1000 беременностей. У авторов нет информации о пропущенных случаях ПС.
В заключении сказано, что использование стандартизированного скрининга ПС является эффективным методом диагностики ПС, благодаря которому достигается 100% выживаемость. Было показано, что примерно в 24% случаев, ПС диагностированное во втором триместре (<26 недель) самостоятельно разрешается благодаря смещению сосудов вверх к третьему триместру, но не было ни одного случая смещения сосудов кверху при диагностике ПС в третьем триместре.
Вероятность ПС минимальна в случаях, когда корень пуповины выходит из ткани плаценты, и при отсутствии добавочной доли плаценты или билобарной плаценты. Учитывая, что описание плаценты уже включено в стандартный протокол УЗИ, необходимо сместить приоритет к исключению оболочечного прикрепления сосудов пуповины, так как такое состояние является предпосылкой для наиболее частого варианта ПС, тип 1. Диагностика нормального прикрепления пуповины к плаценте во время скрининга второго триместра сама по себе имеет большое значение. Помимо ПС существует ещё масса осложнений при оболочечном прикреплении пуповины: повышенный риск отслойки плаценты, задержки роста плода, низкой оценки Апгар при рождении, преждевременных родов. Это не значит, что если Вам поставили диагноз ОПП, то всё это непременно случится, но такая беременность требует повышенного внимания со стороны акушера-гинеколога и более осмотрительного поведения со стороны беременной.
Несколько исследований показали, что определение места прикрепления пуповины к плаценте во время скрининга первого или второго триместра занимает меньше минуты и не требует каких-то особых умений. До 11 недель данное исследование невозможно, так как трофобласт в это время покрывает значительную площадь полости матки.
Определение места прикрепления пуповины к плаценте во время скрининга первого триместра в 11-14 недель предпочтительно, так как на этом сроке это совсем не сложно сделать. При многоплодной беременности, а также при беременности после ЭКО следует рекомендовать трансвагинальное исследование в тех случаях, когда осмотр области внутреннего зева затруднён при трансабдоминальном доступе.
Важно подчеркнуть, что необходимо целенаправленно исключать ОПП, так как если не делать этого специально, то с большой долей вероятности ОПП будет пропущено.
Корень пуповины может располагаться в центре плаценты или эксцентрично, но в ткани плаценты (90%). Либо на краю плаценты (10%) , т.н. краевое прикрепление пуповины к плаценте, в этом случае бывает сложно с помощью УЗ однозначно утверждать, что часть сосудов не расположены оболочечно. И в 1% беременностей определяется оболочечное прикрепление пуповины в стороне от края плаценты. Важно убедиться, что определён именно корень пуповины, а не свободные петли пуповины на поверхности плаценты. В этом может помочь режим ЦДК, показывающий вход сосудов пуповины в хориальную пластину.
В случае, когда отчётливо определено место вхождения пуповины в плаценту, вероятность 1 типа ПС крайне мала и никаких дополнительных исследований не требуется.
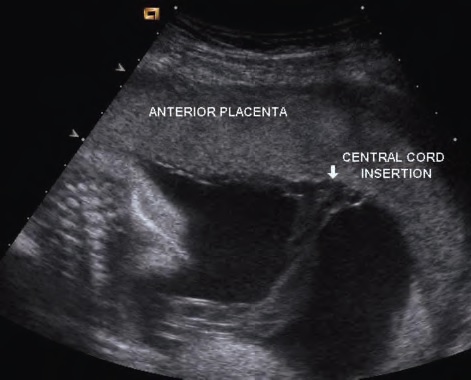
показан корень пуповины входящий в центр плаценты
И, наоборот, в случае, когда не удаётся отчётливо определить место вхождения пуповины, специалисту УЗД необходимо приложить дополнительные усилия, чтобы не пропустить ОПП. Когда не удаётся выявить ОПП в верхнем сегменте матки с помощью трансабдоминального датчика, необходимо провести трансвагинальное исследование с использованием ЦДК.
Кроме того не следует забывать о ПС 2 типа, и осматривать стенки полости матки на предмет добавочных долей плаценты.
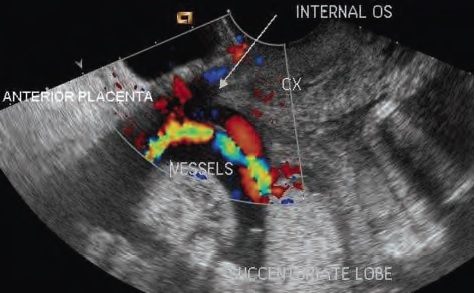
показана плацента по передней стенке матки, добавочная доля плаценты и ПС 2 тип
В случае низкой плацентации во втором триместре беременности, необходимо убедиться, что сосуды не определяются рядом с внутренним зевом, и если это так, то никаких дополнительных действий не требуется.
Низкая плацентация во втором триместре беременности – это состояние, когда край плаценты определяется на расстоянии менее 3-х сантиметров от внутреннего зева, но не перекрывает его. В этом случае не требуется каких-то дополнительных действий или лечения «на всякий» случай. Достаточно повторной оценки расположения плаценты в третьем триместре.
Во время скрининга первого триместра и тем более до 11 недель, не следует ставить диагноз Низкое расположение хориона, так как нижний сегмент матки ещё значительно растянется, и в подавляющем большинстве случаев к 20 неделям уже не будет низкой плацентации.
В настоящее время широко используется трансвагинальное исследование шейки матки с целью исключения истмико-цервикальной недостаточности (ИЦН). Не редко женщины сами, без назначения врача, приходят на цервикометрию просто на всякий случай, потому что им так спокойнее.
Врачу УЗД, проводящему данное исследование следует помнить о Vasa Previa и использовать эту уникальную возможность для того, чтобы, затратив меньше минуты своего времени, лишний раз посмотреть, включить режим ЦДК и, может быть, предотвратить трагедию.
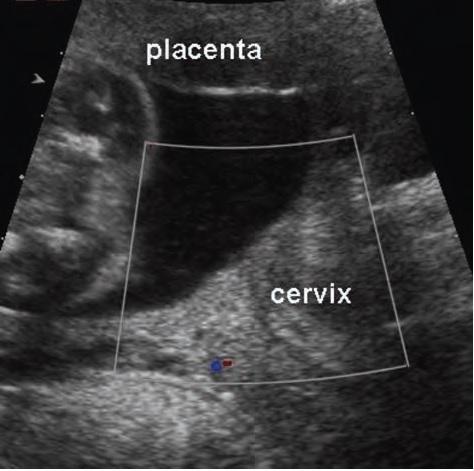
показано отсутствие предлежащих сосудов при трансвагинальном исследовании шейки матки
В заключении хочу предложить диагностический алгоритм для исключения Vasa Previa во время скрининга второго триместра, разработанный командой Philippe Jeanty:
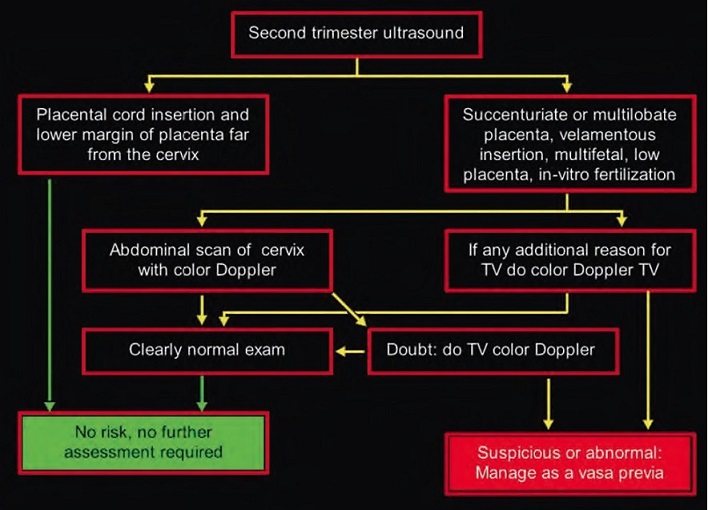
Если Вам поставили диагноз Предлежание Сосудов во втором триместре, не нужно пугаться, но нужно понимать, что к такой беременности нужно относиться с ещё большим трепетом и выполнять все рекомендации наблюдающего Вас врача. Помните, что в 24 % случаев к третьему триместру сосуды могут сместиться кверху, и диагноза ПС уже не будет. Если же и в третьем триместре диагноз подтверждается, то Вам будет показана госпитализация в стационар ближе к 35 неделям беременности, проведение профилактики респираторного дистресс синдрома и родоразрешение путём операции кесарево сечение на сроке 35-36 недель беременности.
Источник
