Срез через 3 сосуда патология
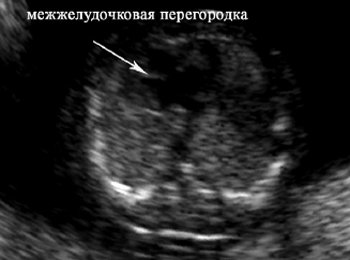
Ïëîä → Ñåðäöå ïëîäà
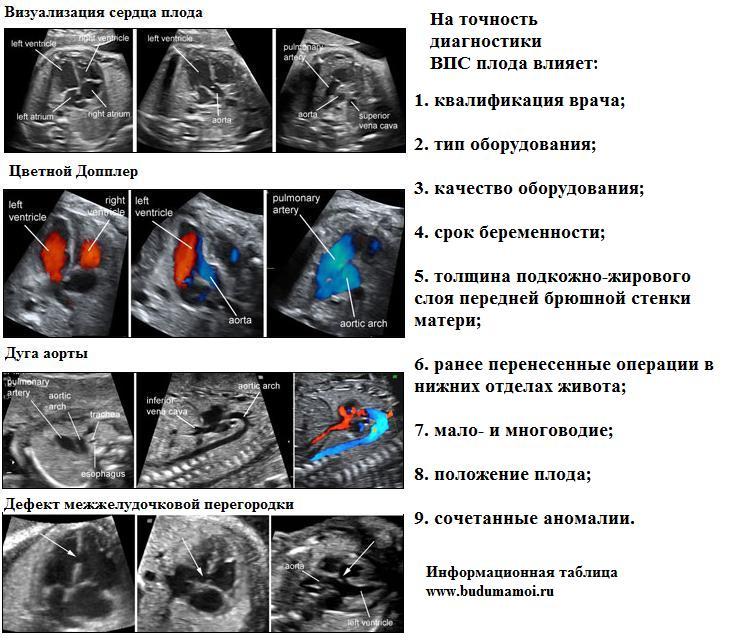
Âðîæäåííûå ïîðîêè ñåðäöà (ÂÏÑ) ÿâëÿþòñÿ äîñòàòî÷íî ðàñïðîñòðàíåííûìè, ïîýòîìó èõ îáíàðóæåíèþ îòäàåòñÿ áîëüøîå çíà÷åíèå. Èõ ìîæíî ñâîåâðåìåííî äèàãíîñòèðîâàòü, åñëè â îáÿçàòåëüíîì ïîðÿäêå ïðîâîäèòü ñêðèíèíãîâûå ÓÇÈ âî II òðèìåñòðå íà àïïàðàòàõ ýêñïåðòíîãî èëè âûñîêîãî êëàññà. Îáû÷íàÿ ñõåìà îáñëåäîâàíèÿ: îöåíêà ÷åòûðåõêàìåðíîãî ñðåçà ñåðäöà è ñðåçà ÷åðåç òðè ñîñóäà. Ýòî ïîìîãàåò õîðîøî ðàçãëÿäåòü âñå ñòðóêòóðû ñåðäöà, äàæå ñàìûå ìåëü÷àéøèå. Íà ñîâðåìåííîì îáîðóäîâàíèè âðà÷ ìîæåò ïîñìîòðåòü êðîõîòíûå ñîñóäû èëè ïåðåãîðîäêè, óâèäåòü ðàáîòó êëàïàíîâ.
×åòûðåõêàìåðíûé ñðåç
Ïðè îöåíêå ÷åòûðåõêàìåðíîãî ñðåçà ñåðäöà ïëîäà óòî÷íÿþò, êàêîå ïîëîæåíèå çàíèìàåò ñåðäöå, êàê ðàñïîëàãàåòñÿ îñü, ðàçìåðû ïðåäñåðäèé è æåëóäî÷êîâ, íàëè÷èå äåôåêòîâ ìåææåëóäî÷êîâîé ïåðåãîðîäêè, ïîëîæåíèå àòðèîâåíòðèêóëÿðíûõ êëàïàíîâ, åñòü ëè èçìåíåíèÿ ýíäîêàðäà, ìèîêàðäà è ïåðèêàðäà. Èìåííî ýòîò ñðåç è ïîçâîëÿåò óçíàòü âñå ïîäðîáíîñòè ñòðîåíèÿ êðîõîòíîãî äåòñêîãî ñåðäå÷êà. Ñëîæíî îöåíèòü ðàáîòó îðãàíà, åñëè ñìîòðåòü íà íåãî òîëüêî â îáúåìå, à ñðåç ïîìîãàåò çàãëÿíóòü âíóòðü, ïîíÿòü íîðìó àíàòîìèè.
Íîðìàëüíîå ðàñïîëîæåíèå ñåðäöå ïëîäà
Îöåíêó ïðîâîäÿò ïî îòíîøåíèþ ê êâàäðàíòàì, ó÷èòûâàÿ äâå ëèíèè ïðè ïîïåðå÷íîì ñêàíèðîâàíèè ãðóäíîé êëåòêè ïëîäà (â ñàãèòòàëüíîì è ïîïåðå÷íîì íàïðàâëåíèè). Íîðìàëüíîå ðàñïîëîæåíèå – â ïåðåäíåì ëåâîì êâàäðàíòå (ñåðäöå ðàñïîëàãàåòñÿ òàì íå ïîëíîñòüþ, íî â áîëüøåé ñâîåé ÷àñòè), ïðè ýòîì îñíîâíûì êðèòåðèåì ÿâëÿåòñÿ ïîëîæåíèå åãî âåðõóøêè.
Íîðìàëüíûå ðàçìåðû ñåðäöà
 íîðìå ñåðäöå çàíèìàåò íå áîëåå 1/3 ïîïåðå÷íîãî ñðåçà ãðóäíîé êëåòêè. Ñóùåñòâóþò ðàçíûå òàáëèöû, êîòîðûå òî÷íî ïîìîãàþò îïðåäåëèòü íîðìó.
Ðàñïîëîæåíèå îñè ñåðäöà
Îöåíêó îñè ñåðäöà ïðîâîäÿò ïî îòíîøåíèþ ê ñàãèòòàëüíîìó íàïðàâëåíèþ.  íîðìå óãîë ìåæäó îñüþ ñåðäöà ïëîäà (ñìîòðÿò äâå ïåðåãîðîäêè -ìåææåëóäî÷êîâóþ è ìåæïðåäñåðäíóþ), è ñàãèòòàëüíûì íàïðàâëåíèåì ñîñòàâëÿåò 45 ãðàäóñîâ. Òàêàÿ íîðìà âåðíà äëÿ âòîðîé ïîëîâèíû áåðåìåííîñòè, à íîðìàëüíûå çíà÷åíèÿ +/- ìîãóò áûòü äàæå îò 30 äî 60 ãðàäóñîâ, ïîýòîìó îöåíêîé äîëæåí çàíèìàòüñÿ îïûòíûé ñïåöèàëèñò, êîòîðûé ó÷òåò âñå îñîáåííîñòè êðîõîòíîãî îðãàíèçìà.
Ðàçìåðû ïðåäñåðäèé è æåëóäî÷êîâ
Ïðåäñåðäèÿ è æåëóäî÷êè ñåðäöà ïëîäà äîëæíû áûòü ïî÷òè ðàâíûìè ïî ðàçìåðó. Ïðåäñåðäèÿ íà ÓÇÈ ïîõîæè íà ñôåðè÷åñêèå îáðàçîâàíèÿ, à æåëóäî÷êè èìåþò êîíè÷åñêóþ ôîðìó. Îïðåäåëåíèå äèñïðîïîðöèè ðàçìåðîâ ïîìîãàåò â äèàãíîñòèêå âðîæäåííûõ ïîðîêîâ ñåðäöà.
Äåôåêòû ìåææåëóäî÷êîâîé ïåðåãîðîäêè
Äåôåêòû ìåææåëóäî÷êîâîé ïåðåãîðîäêè ÿâëÿþòñÿ íàèáîëåå ÷àñòîé ôîðìîé âðîæäåííûõ ïîðîêîâ ñåðäöà. Îá ýòîì ïîðîêå ñëûøàëè, âåðîÿòíî, ìíîãèå ðîäèòåëè. Ïåðåãîðîäêà ïëîäà èìååò î÷åíü ìàëûå ðàçìåðû, à îñîáåííîñòè ïîëîæåíèÿ ïëîäà äîïîëíèòåëüíî îñëîæíÿþò îáñëåäîâàíèå, ïîýòîìó äèàãíîñòèêà äåôåêòà òðåáóåò âíèìàòåëüíîñòè ñïåöèàëèñòà. Îïðåäåëåíèå äåôåêòà îñíîâûâàåòñÿ íà âûÿâëåíèè â ñòðóêòóðå ýõîíåãàòèâíîé çîíû.
Ïîëîæåíèå àòðèîâåíòðèêóëÿðíûõ êëàïàíîâ
Íàäåæíûì êðèòåðèåì ïàòîëîãèè ÿâëÿåòñÿ çíà÷èòåëüíîå ñìåùåíèå ñòâîðîê òðèêóñïèäàëüíîãî êëàïàíà âãëóáü ïðàâîãî æåëóäî÷êà íà 4 ìì è áîëåå. Ñòâîðêè ìèòðàëüíîãî (ýòî äâóñòâîð÷àòûé êëàïàí, êîòîðûé íàõîäèòñÿ ìåæäó ëåâûì ïðåäñåðäèåì è æåëóäî÷êîì ñåðäöà) è òðèêóñïèäàëüíîãî (ýòî òð¸õñòâîð÷àòûé êëàïàí, êîòîðûé íàõîäèòñÿ ìåæäó ïðàâûì ïðåäñåðäèåì è æåëóäî÷êîì ñåðäöà) êëàïàíîâ ïîñòîÿííî «ðàáîòàþ» (îòêðûâàþòñÿ è çàêðûâàþòñÿ).
Èçìåíåíèÿ ýíäîêàðäà, ìèîêàðäà è ïåðèêàðäà
 íîðìå ýíäîêàðä, êîòîðûé òàêæå íàçûâàþò âíóòðåííåé îáîëî÷êîé ñåðäöà èìååò ñðåäíþþ ýõîãåííîñòü. Âûðàæåííîå èñòîí÷åíèå èëè óòîëùåíèå ìèîêàðäà «ãîâîðèò» î ïàòîëîãèè. Ïðè âèçóàëèçàöèè ïåðèêàðäà íå äîëæåí îïðåäåëÿòüñÿ ïåðèêàðäèàëüíûé âûïîò èëè êàêèå-òî äîïîëíèòåëüíûå îáðàçîâàíèÿ.
Ñðåç ÷åðåç òðè ñîñóäà
Äàííûé âàðèàíò îáñëåäîâàíèÿ ÿâëÿåòñÿ äîïîëíèòåëüíûì «ïîìîùíèêîì» íà ÓÇÈ äëÿ äèàãíîñòèêè âðîæäåííûõ ïîðîêîâ ñåðäöà. Îí ïîçâîëÿåò óâèäåòü àíîìàëèè, êîòîðûå ñîïðîâîæäàþòñÿ èçìåíåíèåì ãëàâíûõ àðòåðèé.
Îïðåäåëåíèå òðåõ ñîñóäîâ
 íîðìå óäàåòñÿ îïðåäåëèòü òðè ñîñóäà ñåðäöà ïëîäà, ïðè ýòîì ïî öåíòðó ïðîõîäèò îñíîâíîé ñòâîë ëåãî÷íîé àðòåðèè, ñïðàâà âîñõîäÿùàÿ àîðòà, à ïðàâåå âåðõíÿÿ ïîëàÿ âåíà.
Ðàñïîëîæåíèå ñîñóäîâ â îäíó ëèíèþ
Îñíîâàíèå ëåãî÷íîé àðòåðèè, âîñõîäÿùåé àîðòû è ïîïåðå÷íûé ñðåç âåðõíåé ïîëîé âåíû ðàñïîëàãàþòñÿ â îäíó ëèíèþ, ÷òî õîðîøî âèäíî âî âðåìÿ îáñëåäîâàíèÿ è ÿâëÿåòñÿ íîðìîé.
Ðàçìåðû ñîñóäîâ
Ëåãî÷íàÿ àðòåðèÿ áîëüøå àîðòû, à àîðòà áîëüøå âåðõíåé ïîëîé âåíû, íî ýòî óâåëè÷åíèå îäíîãî îòíîñèòåëüíî äðóãîãî íå ñîñòàâëÿåò áîëåå ÷åì â 1,3 ðàçà.
Àâòîð: aêóøåð-ãèíåêîëîã Íèêîëàåâà Î. Ï.
Äàòà ïóáëèêàöèè: 29.05.2013
Ïåðåïå÷àòêà áåç àêòèâíîé ññûëêè çàïðåùåíà
Âíèìàíèå! Ýòî ÂÀÆÍÎ!
Âñÿ èíôîðìàöèÿ â ñòàòüå, à òàêæå
íîðìû è òàáëèöû ïðåäñòàâëåíû òîëüêî äëÿ îáùåãî îçíàêîìëåíèÿ. Îíà íå äàåò
îñíîâàíèé ñòàâèòü ñåáå äèàãíîç èëè íàçíà÷àòü ëå÷åíèå ñàìîñòîÿòåëüíî.
Âñåãäà îáðàùàéòåñü ê âðà÷ó!
Источник
УЗИ сканер HS60
Профессиональные диагностические инструменты. Оценка эластичности тканей, расширенные возможности 3D/4D/5D сканирования, классификатор BI-RADS, опции для экспертных кардиологических исследований.
Введение
Общий предсердно-желудочковый канал является пороком, при котором сочетаются дефекты межпредсердной и межжелудочковой перегородок с расщеплением атриовентрикулярных клапанов [1]. Частота порока составляет 3-7% среди всех пороков сердца у новорожденных. Удельный вес аномалии у плодов, конечно, выше. В группе пациентов высокого риска доля порока достигает 11% [2]. Порок часто (до 60%) сочетается с анеуплоидиями, среди которых наиболее частой является трисомия 21 и другими синдромами (до 50%), преимущественно синдромом гетеротаксии [3]. Различают полную и неполную форму порока. При неполной форме порока атриовентрикулярные клапаны разделены. Существует коммуникация между предсердиями или между левым желудочком и правым предсердием. При этом правый клапан чаще интактен, а левый расщеплен на три створки с образованием щели между передней и задней створками. При полной форме порока первичные дефекты перегородок сочетаются с расщеплением створок клапанов и образуют общий атриовентрикулярный канал с единым пятистворчатым клапаном [1].
Прогноз в большинстве случаев неблагоприятный в связи с частыми сочетанными пороками и хромосомными аномалиями. Этими обстоятельствами определяется акушерская тактика. Недостаточность клапана является плохим прогностическим признаком. При изолированной форме порока и своевременной, квалифицированной хирургической помощи благоприятные исходы возможны более чем в 80% случаев [1].
Перерыв дуги аорты является пороком, при котором отсутствует сообщение между восходящей и нисходящей аортой [4]. Сообщение сердца и сосудов нижней половины туловища обеспечивается артериальным протоком. Классификация основана на отношении брахиоцефальных сосудов и зоны перерыва дуги аорты: тип А (42%) – дистальнее левой подключичной артерии, тип В (43%) – дистальнее левой общей сонной артерии, тип С (4%) – дистальнее брахиоцефального ствола [5].
Наиболее частые сочетанные аномалии – это синдром Di George, другие аномалии дуги аорты, внутрисердечные аномалии (дефект межжелудочковой перегородки), обструктивное поражение выходящего тракта левого желудочка, аберрантные или изолированные левая или правая подключичная артерии, общий артериальный ствол, синдром CHARGE [6].
Большинство новорожденных погибают в ранний неонатальныи период. Если ребенок остается в живых, то возможна хирургическая коррекция порока.
Акушерская тактика зависит от наличия других пороков и хромосомных аномалий. Рекомендуется прерывание беременности до периода жизнеспособности плода. В более позднем сроке оценивается состояние плода, степень сердечной недостаточности. В случае удовлетворительного состояния плода – родоразрешение в центре с возможной кардиохирургической помощью [4].
Приводим описание наблюдений пренатальнои диагностики общего предсердно-желудочкового канала и перерыве дуги аорты.
Материалы и методы
Пациентка А., 27 лет, паритет 2/1, поступила в роддом для пренатальнои диагностики в связи с выявленным ультразвуковым маркером хромосомных аномалий (увеличение ТВП до 5,6 мм) (рис. 1). Срок беременности составил 13 нед 6 дней. Выполнена трансабдоминальная хорионбиопсия, диагностирована трисомия 21. Повторно пациентка поступила через 4,5 нед (срок беременности 18 нед 4 дня) для прерывания беременности по медицинским показаниям.
Пациентка В., 39 лет, паритет 4/2, поступила в родильный дом для прерывания беременности по медицинским показаниям. В связи с возрастом пациентки и величиной воротникового пространства у плода 3,5 мм (ультразвуковое исследование выполнено в 13 нед) в 16 нед беременности был выполнен амниоцентез и диагностирован синдром Дауна. При поступлении в стационар срок беременности составил 21 нед 4 дня.
Ультразвуковые исследования выполнялись на аппарате SonoAce-8000 Ex (компании Medison) с применением абдоминального конвексного датчика 3-7 МГц и внутриполостного конвексного датчика 4-9 МГц.
Результаты
Возможности визуализации сканера SonoAce-8000 Ex позволяют оценить практически все основные плоскости сканирования сердца плода в 12-14 нед гестации. Программа исследования сердца плода позволяет добиться значительного успеха в визуализации интракардиальных структур у нормостеников даже при трансабдоминальной методике. Применение внутриполостного датчика существенно расширяет возможности. Основная часть исследования сердца плода в I триместре выполняется именно этим датчиком. Учитывая такую, вполне удовлетворительную визуализацию сердца плода (и других, конечно, структур), алгоритм исследования в I триместре был расширен до программы исследования сердца плода во II триместре. Визуализирован нормальный срез через 3 сосуда (рис. 2). Изучение четырехкамерного среза сердца позволило выявить дефект нижней части межпредсердной и верхней части межжелудочковой перегородок, единый аномальный атриовентрикулярный клапан (рис. 3). Кроме того, у этого плода не визуализировалась носовая кость, была обнаружена «сандалевидная щель» (рис. 4, 5). Исследование при сроке 18-19 нед подтвердило все находки. Отмечалось увеличение шейной складки (рис. 6), тазового угла (рис. 7), гипоплазия носовых костей.
По данным аутопсии диагноз общего предсердно-желудочкового канала полностью подтвержден (верифицирована полная форма порока).
Во втором наблюдении при исследовании дуги аорты оказалось, что визуализировать дугу на всем протяжении невозможно (рис. 8). Определялись восходящая аорта и отходящие от нее плечеголовной ствол и левая сонная артерия. Затем изображение дуги аорты отсутствовало и, далее, определялась дистальная часть дуги, левая подключичная артерия и нисходящая аорта (рис. 9).
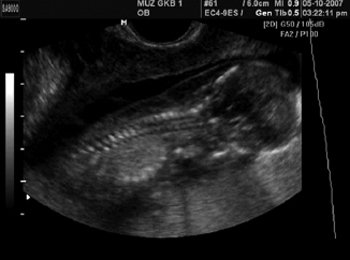
Рис. 1. Увеличенное воротниковое пространство. Сагиттальная плоскость.
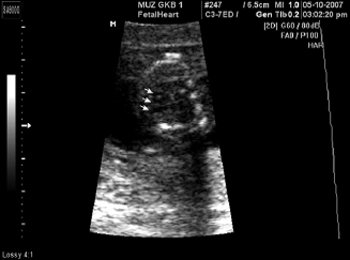
Рис. 2. Срез через три сосуда.

Рис. 3. Четырехкамерный срез сердца плода в 13 нед 6 дней.
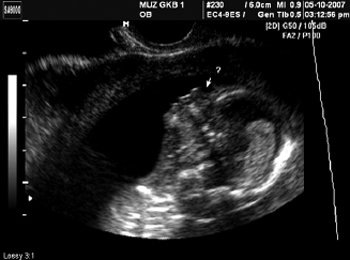
Рис. 4. Лицо плода. Отсутствие носовой кости. Срок беременности 13 нед 6 дней.
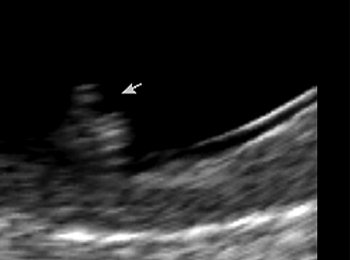
Рис. 5. «Сандалевидная щель». Срок беременности 13 нед 6 дней.
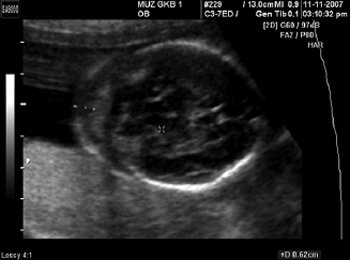
Рис. 6. Увеличение шейной складки. Срок беременности 18 нед 4 дня.
Топография сосудов в аксиальных сечениях также была изменена. В сечении, расположенном на уровне отхождения основных сосудов визуализировались 3 сосуда (рис. 10). Однако взаимоотношения дуги аорты, легочной артерии и артериального протока были нарушены. Получить характерное «У»-образное изображение дуги аорты и артериального протока (рис. 11) оказалось невозможным.
По данным аутопсии, диагноз перерыва дуги аорты полностью подтвержден.
Обсуждение
Ранняя диагностика аномалий развития является, несомненно, приоритетной задачей. Решение вопросов о вынашивании беременности в I триместре сопряжено с меньшими медицинскими, социальными, психологическими проблемами и экономически более выгодно. Современные технические возможности позволяют сместить акцент именно на I триместр [7]. Сканер SonoAce-8000 Ex позволяет в большинстве случаев значительно расширить программу исследования плода в I триместре. Увеличение ТВП требует тщательного изучения сердца плода [7]. Полученный результат можно считать вполне закономерным. Планомерное изучение основных сечений позволило диагностировать общий предсердно-желудочковый канал и выявить другие аномалии.
Ошибки в пренатальной диагностике общего предсердно-желудочкового канала (а это может привести к решению о прерывании беременности) связывают в первую очередь с расширением коронарного синуса, что бывает при персистенции левой верхней полой вены. Эта аномалия может сочетаться с общим предсердно-желудочковым каналом или быть изолированной. Изолированная аномалия в виде персистенции верхней левой полой вены не ухудшает качество жизни и, как правило, является случайной находкой, в том числе и у спортсменов [8].
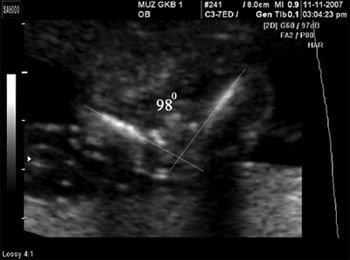
Рис. 7. Увеличение тазового угла. Срок беременности 18 нед 4 дня.
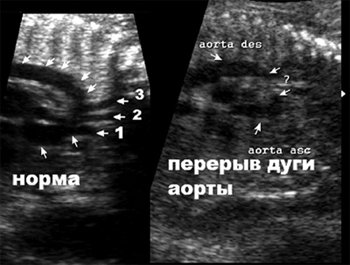
Рис. 8. Дуга аорты в норме и при ее перерыве. Срез через дугу аорты. Ветви дуги аорты:
1- брахиоцефальный ствол, 2 – левая сонная, 3 – левая подключичная артерии.
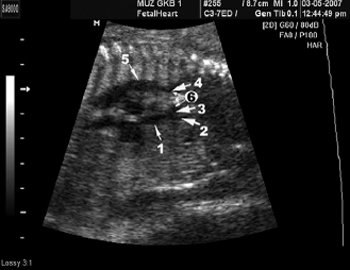
Рис. 9. Срез через дугу аорты (перерыв дуги аорты тип В).
1 – восходящая аорта, 2 – брахиоцефальный ствол, 3 – левая сонная артерия, 4 – левая подключичная артерия, 5 – нисходящая аорта, 6 – отсутствующая часть дуги аорты.
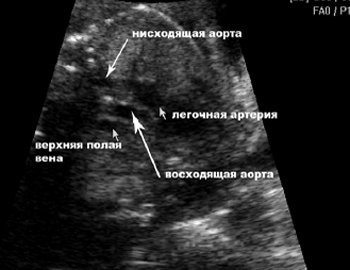
Рис. 10. Аксиальное сечение грудной клетки плода на уровне отхождения основных сосудов.
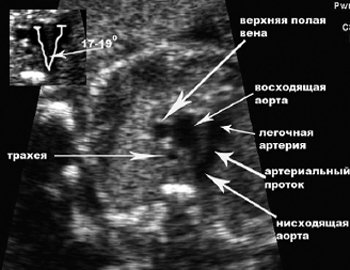
Рис. 11. Нормальное аксиальное сечение грудной клетки плода. Хорошо видно «У»-образное взаимоотношение артериального протока и дуги аорты.
Коронарный синус визуализируется у 97,4% плодов. Его величина изменяется с течением беременности от 1 до 3,2 мм.
При персистирующей верхней полой вене синус может увеличиваться более чем в 3 раза. Синус впадает в правое предсердие очень близко к основанию створок атрио-вентрикулярного клапана, поэтому при его расширении может создаться впечатление об артриовентрикулярном канале. Тщательное мультиплоскостное исследование, прицельный поиск возможной персистирующей верхней левой полой вены позволит избежать трагической ошибки [9, 10].
Для успешной диагностики аномалий дуги аорты необходимо визуализировать трахею, главные сосуды, артериальный проток и нисходящую аорту в аксиальном сечении верхней половины грудной клетки. Ключевым моментом в диагностике является обнаружение аномальной позиции нисходящей аорты, отсутствия нормального «У»-образного соотношения артериального протока и дуги аорты (см. рис. 2), аномальное соотношение восходящей аорты и основного ствола легочной артерии в трехсосудистом срезе, а также обнаружение аномального сосуда позади трахеи с образованием сосудистой петли или кольца вокруг трахеи [11, 12]. Дифференциальную диагностику необходимо проводить со стенозом аорты, атрезией аорты, коарктацией и тубулярной гипоплазией дуги аорты.
Для дифференциальной диагностики аномалий главных артерий важно оценить отношение диаметров легочная артерия/ аорта, измеренных в трехсосудистом срезе. Этот показатель позволяет с чувствительностью 86% и ложноположительными результатами 5% прогнозировать патологию главных артерий. Медиана значений во II триместре (19-24 нед) составляет 1,16. При патологии это отношение увеличивается и превышает 95-й процентиль [13].
Заключение
Успешное выявление врожденных пороков сердца требует соблюдения современных принципов и методических приемов эхокардиографического исследования плода. Тщательное изучение четырехкамерного сечения сердца, венозного возврата, сечения через три сосуда необходимо для дифференциальной диагностики общего предсердно-желудочкового канала.
Исследование аксиальных сечений верхней половины грудной клетки плода с визуализацией трахеи, главных сосудов, артериального протока, нисходящей аорты, «У»-образного соотношения артериального протока и дуги аорты, визуализация аномального сосуда позади трахеи, сечения через дугу аорты с визуализацией ветвей дуги аорты, а также исследование внутрисердечного кровотока и кровотока в главных артериях необходимо для успешной диагностики аномалий дуги аорты.
Литература
- Медведев М. В. Сердце // Пренатальная эхография/ Под ред. Медведева М. В. 1-е изд., – М.: Реальное Время, 2005. С. 371-429.
- Allan L., Hornberger L. K., Sharland G. Textbook of Fetal Cardiology.Greenwich Medical Media Publishing. 2000.
- Bronshtein M., Egenburg S., Auslander R., Zimmer E. Z. Atrioventricular septal defect in a fetus: a false negative diagnosis in early pregnancy // Ultrasound Obstet. Gynecol. 2000. V. 16. P. 98-99.
- Wheeler T.C., Jeanty P. Aortic arch interruption // www. TheFetus. net
- Celoria G.C., Patton R. B. Congenital absence of the aortic arch // Am. Heart J. 1959. V. 58. P. 407-413.
- Conley M. E., Beckwith J. В., Mancer J., et al: The spectrum of DiGeorge syndrome // J. Pediatr. 1979. V. 94. P. 883-890.
- Nicolaides K. H. The 11 – 13+6 weeks scan. Fetal Medicine Foundation. London. 2004. 112p.
- Kinoshita N., Hasegawa K., Oguma Y., Katsukawa F., Onishi S., Yamazaki H. Fortuitously discovered persistent left superior vena cava in young competitive athletes //Clinical implications of sports physicians. J. Sports Med. Phy.s Fitnes.s 2001. V. 41. P. 275-277.
- Rein A.J., Nir A., Nadjari M. The coronary sinus in the fetus. // Ultrasound Obstet. Gynecol. 2000. V. 5. P. 468-472.
- Park J.K., Taylor D. K., Skeels M., Towner D. R. Dilated coronary sinus in a fetus: misinterpretation as an atrioventricular canal defect // Ultrasound Obstet. Gynecol. 1997. V. 10. P. 126-129.
- Yoo S.J., Min J. Y., Lee Y. H., Roman K., Jaeggi E., Smallhorn J. Fetal sonographic diagnosis of aortic arch anomalies // Ultrasound Obstet. Gynecol. 2003. V. 22. P. 535-546
- Marasini M., Pongiglione G., Lituania M., Cordone M., Porro E., Garello-Cantoni L. Aortic arch interruption: two-dimensional echocardiographic recognition in utero // Pediatr. Cardiol // 1985. V. 6. P. 147-149.
- Wong S.F., Ward C, Lee-Tannock A., Le S., Chan F. Y. Pulmonary artery/aorta ratio in simple screening for fetal outflow tract abnormalities during the second trimester // Ultrasound Obstet. Gynecol. 2007. V. 30. P. 275-280.

УЗИ сканер HS60
Профессиональные диагностические инструменты. Оценка эластичности тканей, расширенные возможности 3D/4D/5D сканирования, классификатор BI-RADS, опции для экспертных кардиологических исследований.
Источник
