Свойства стенок кровеносных сосудов
3. Свойства кровеносных сосудов.
Кровеносные сосуды по своим свойствам и функциям подразделяются на четыре типа: артерии эластичного типа, артерии мышечного типа, капилляры и вены.
l Артерии эластичного типа можно назвать аккумуляторами давления крови: благодаря им поддерживается непрерывный ток крови во время диастолы, когда сердце отдыхает. Стенки таких сосудов содержат значительное количество эластических волокон, благодаря чему в ходе функционирования артерий этого типа их радиус способен при упругих деформациях увеличиваться в 1,1 раза (на 10%), что соответствует увеличению площади сечения на 20%.
В ходе нарастания давления крови в процессе сокращения желудочков, информация об этом передается вдоль системы сосудов со скоростью звука (это порядка 1000 м/с). Вследствие этого все артерии эластического типа слегка увеличиваются в диаметре; их стенки слегка напрягаются (закон Гука); создается некоторый запас крови повышенного давления.
Помимо этого, начиная с аорты, вдоль всей системы артерий начинает распространяться пульсовая волна, расходясь по разветвлениям и постепенно затухая. В возникновении и распространении этой волны, помимо эластичности сосудов, играет роль инерционность жидкости. Благодаря инерционности, для жидкости легче образовать вздутие сосуда (благо он это позволяет), чем устремляться вдоль сосуда. Вздутие развивается до той поры, пока возрастающие силы упругости не уравновесят внутренние силы статического давления. Далее – кровь выдавливается из зоны вздутия упругими силами стенок, с тем, чтобы образовать вздутие в соседних сечениях; и т.д.
Упругие и инерционные свойства системы «кровь – аорта» определяют скорость распространения пульсовой волны:
(8)
Здесь Е – модуль упругости стенки; r – плотность крови; r – внутренний радиус сосуда; b – толщина его стенки.
С возрастом, по мере уменьшения эластичности сосудов, растет модуль упругости Е, что отслеживается ростом скорости распространения пульсовой волны.
Измерить скорость пульсовой волны можно следующим образом. Можно установить два датчика пульсовых колебаний на некотором расстоянии Dl друг от друга, и записать две кривые артериального пульса. Такие записи называются санмограммами. По двум таким записям легко определяется временной сдвиг Dt одной из них по отношению к другой. Скорость пульсовой волны:
Зная Vп, можно с помощью формулы (8) вычислить модуль упругости Е как показатель состояния сосудистой стенки. А можно обойтись и без вычислений, сравнивая измеренные значения Vп со значениями, характерными для нормы.
Наряду с эластичными волокнами, стенки сосудов данного типа имеют значительное количество коллагеновых волокон, природное предназначение которых – обеспечение прочности тканей. Однако прочностные способности этих волокон способны проявиться лишь при значительных деформациях стенок сосудов. Это объясняется рыхлой укладкой коллагеновых волокон. Они как бы спутаны, и начинают проявлять прочность только когда распрямляются при больших деформациях стенок.
Наличие прочных нитей коллагеновых волокон обеспечивает возможность работы сосудов в условиях очень больших нагрузок на систему кровообращения, вплоть до десятикратного роста артериального давления.
l Артерии мышечного типа, меняя тонус, меняют распределение давления крови по органам и тканям. В системе кровообращения нет кранов и задвижек, но есть артерии мышечного типа – артериолы. Их численность – несколько сот тысяч; суммарная площадь сосудистого русла получается весьма внушительной, а потому перепад давлений на системе артериол достаточно велик, несмотря на параллельную работу их ветвей. Так, если давление в аорте во время систолы достигает 115-130 мм рт.ст., то у начала артериол оно составляет 70-80 мм, а у начала капилляров – 20-40 мм рт.ст. Природная логика здесь примерно такова: артериола должна иметь заметное гидравлическое сопротивление, и тогда она может своим мышечным тонусом менять его в обе стороны: как в сторону понижения, так и в сторону повышения. Будь у нее очень малое сопротивление, она могла бы работать, регулируя систему только на повышение давления, что было бы гораздо менее эффективно.
Изменения тонуса в отдельных звеньях системы артериол обеспечивают повышенный кровоток в тех органах, которые в данный момент в этом нуждаются, как в связи с физическими нагрузками, так и в ходе регулирования теплообмена организма с окружающей средой.
Помимо изложенного, система артериол передает пульсовую волну, которая окончательно затухает лишь на входе в капилляры.
Примеры системных нарушений в работе этого участка кровеносной системы – гипертония и гипотония.
l Капилляры – та часть системы кровообращения, ради которой эта система существует.
Гидравлическое сопротивление всей системы капилляров невелико: если на входе в капилляры давление крови 20-40 мм рт.ст., то на выходе – 8-15 мм рт.ст., и это несмотря на впечатляющую суммарную их протяженность. Объяснение тому – очень малая скорость движения крови в этих сосудах: порядка 0,5 мм/с.
Система капилляров – та часть кровеносной системы, которая выходит из строя при декомпрессии. Имеется в виду ситуация, когда резко уменьшается давление воздуха, который окружает человека (и которым он дышит). Например, если водолаз, в нарушение инструкций, будет быстро всплывать с больших глубин на поверхность, то давление воздуха в его скафандре будет автоматически уменьшаться вслед за уменьшением внешнего гидростатического давления, и при этом воздух, растворившийся в его крови при больших давлениях в скафандре, начинает выделяться в виде микроскопических пузырьков как в самих капиллярах, так и в потоке крови, поступающей к ним. Эти пузырьки способны закупорить капилляры.
Дело в том, что в связи с явлением поверхностного натяжения под изогнутой поверхностью жидкости возникает избыточное давление (давление Лапласа), величина которого, где s – коэффициент поверхностного натяжения; r – радиус пузырька или капилляра, в котором он обосновался.
При радиусе капилляра r = 5 мкм = 5×10-6м и при s = 0,05 Н/м давление в пузырьке: p = 20 кПа = 150 мм рт.ст., т.е. превосходит «рабочее» давление крови в капиллярах и вполне годится в качестве пробки для них. Такой пузырек, вместе с его внутренним давлением, будет постепенно вытолкнут из капилляра, но навредить он успеет, поскольку ток в капилляре будет существенно замедлен. А дальше что? Спустя небольшое время значительная часть этих пузырьков вернется, пройдя сердце, в систему капилляров на повторное вредительство.
Радикальным выходом из подобных ситуаций, приводящих к кессонной болезни, является помещение пострадавших в барокамеры с повышенным давлением воздуха, выдерживание их в камерах в течение долгих часов, пока воздух из пузырьков опять растворится в крови, затем – медленное поэтапное снижение давления в барокамере до нормального атмосферного давления. Чем раньше начинается такая восстановительная процедура, тем меньше остаточные явления.
Чтобы оказаться в обозначенном круге проблем, не обязательно быть водолазом или космонавтом. В медицинской практике – камеры гипербарической оксигенации: пациента помещают в герметичную камеру, в которой воздух заменен кислородом высокого давления. Это предпринимается для эффективного насыщения крови кислородом в случаях, когда обычное легочное дыхание плохо справляется с этой задачей.
Вывод пациента из барокамеры должен быть растянут во времени, с медленным снижением избыточного давления, во избежание кессонной болезни.
l Вены – сложная разветвленная сеть сосудов, замыкающая выход капилляров с предсердиями. Эта система работает в условиях низкого давления; оно достигает нулевой отметки, и даже, как уже говорилось, может быть отрицательным. В этих условиях, в правом предсердии возникает еще более низкое давление, чтобы всасывать кровь, если она поступает слабо.
Если же организм работает в режиме повышенных физических нагрузок, то давление на входе в предсердия – повышенное, и имеет место хорошая заполняемость предсердий и желудочков. Это означает, что мышечные волокна миокарда растянуты значительно. Для сердца это является указанием на то, что от него требуется сократительная деятельность повышенной мощности. В этом проявляется закон Старлинга: сила сердечного сокращения прямо пропорциональна исходной длине миокардиальных волокон перед началом систолы. Таким путем, не дожидаясь команд из «центра» – ЦНС, сердце автоматически регулирует свою деятельность. Способность сердца автономно выполнять сократительную деятельность, даже находясь вне организма, поражала еще древних медиков.
Разумеется, сказанное не означает, что сердце работает совершенно независимо от центральной нервной системы. Хорошо известно, что эмоциональные перегрузки способны оказывать сильнейшее влияние, как положительное, так и отрицательное, на работу сердца и всей сердечно-сосудистой системы.
l Автоматическое регулирование собственных параметров системой кровообращения просто обязано быть под контролем центральной нервной системы. Без этого система может «далеко зайти».
В самом деле, легко представима такая ситуация: работая по закону Старлинга, сердце начинает, в ответ на хорошую заполненность предсердий, совершать более энергичные сокращения; это приводит к еще более хорошему заполнению предсердий, сердце начинает работать еще энергичнее, и т.д., – сердце «пошло в разнос».
Нечто подобное можно представить себе и в работе системы артериол: давление крови повысилось – артериолы зажались – сердце вынуждено повысить давление еще больше – артериолы зажались еще сильнее, и т.д.
Следовательно, центральная нервная система по отношению к системе кровообращения должна тонко проводить принцип: «ты саморегулируйся, но знай меру». Это очень деликатная и тонкая работа ведется нервной системой непрерывно, в том числе и тогда, когда мы спим. Одно из двух: либо ЦНС справляется с этой работой, либо – нет, и тогда встают задачи, самые сложные для медика – устранение неполадок в работе ЦНС.
l Памятник – пародия на дурную систему автоматического регулирования установлен в Стокгольме перед музеем техники: на столбе висит фонарь; его включение и выключение осуществляет фотоэлемент. А дальше так: стемнело – фотоэлемент включил фонарь – стало светло – фотоэлемент выключил фонарь – стало темно – и т.д.
l В отношении венозной части системы кровообращения, работающей в условиях низкого давления, а что гораздо важнее – низких перепадов давления (см. закон Пуазейля), природа распорядилась не полагаться полностью на эти перепады. Кровоток в этой части системы кровообращения поддерживается также через механику легочных сокращений, движений диафрагмы; движение крови в венах рук и ног стимулируется сократительной деятельностью мышц. Чтобы такие «подкачивающие насосы» работали эффективно, вены имеют систему клапанов, пропускающих кровь только в сторону предсердий.
Следовательно, лежание на диване не является оптимальной жизненной стратегией в деле поддержания работы сердечно-сосудистой системы на должном уровне. Двигательная активность организма предусмотрена природой как необходимое условие четкой работы этой системы.
l Венозные сосуды имеют тонкие стенки и сравнительно слабые мышечные волокна. Тем не менее, в венах возникает и по ним распространяется своя пульсовая волна. Ее предназначение – сгладить колебания давления крови, погасить эти колебания. Возникновение этих пульсаций давления связано с гидравлическим ударом, а точнее –с его предотвращением. Дело в том, что перед каждым очередным срабатыванием сердца вход в предсердие резко закрывается, и кровотоку в сторону предсердий становится некуда девать свою кинетическую энергию. Вместо опасных пиков давления возникают упругие растяжения стенок вен на входе в предсердия, а дальше все идет, как в артериальной пульсовой волне, только в обратном направлении – против тока крови.
Таким образом, в сторону капилляров идут две пульсовые волны, затухая окончательно на подступах к ним: кровеносная система бережно создает «режим наибольшего благоприятствования» в работе своего основного участка.
В соответствии с формулой (8), скорость венозной пульсовой волны меньше, чем артериальной. Она может быть измерена по записям венного пульса. Такие записи называются флебограммами.
Источник
Строение стенок сосудов
Все кровеносные сосуды выстланы изнутри слоем эндотелия, непосредственно прилегающим к просвету сосуда. Эндотелий обычно построен из одного слоя плоских клеток (около прекапиллярных сфинктеров и в области артериовенозных анастомозов имеется многослойный эпителий). Эндотелий образует гладкую внутреннюю поверхность сосуда; если эта поверхность не повреждена, она препятствует свертыванию крови. Помимо эндотелия во всех сосудах, кроме истинных капилляров, имеются следующие образования: 1) эластические волокна; 2) коллагеновые волокна; 3) гладкомышечные волокна. Количество этих волокон в разных сосудах различно.
Эластические волокна, особенно волокна внутренней оболочки (интимы), образуют относительно густую сеть. Они легко могут быть растянуты в несколько раз. Эти волокна создаютэластическое напряжение, противодействующее кровяному давлению, растягивающему сосуд. На создание такого напряжения не расходуется энергия биохимических процессов.
Коллагеновые волокна средней и наружной оболочек образуют сеть, оказывающую растяжению сосуда гораздо
большее сопротивление, чем эластические волокна. Коллагеновые волокна относительно свободно располагаются в стенке сосуда и иногда образуют складки. В связи с этим они противодействуют давлению только тогда, когда сосуд растянут до определенной степени.
Веретенообразные гладкомышечные клетки (диаметром около 4,7 мкм, длиной около 20 мкм) соединены друг с другом и с эластическими и коллагеновыми волокнами. Главная функция гладкомышечных клеток состоит в создании активного напряжения сосудистой стенки(сосудистого тонуса) и в изменении величины просвета сосудов в соответствии с физиологическими потребностями. Гладкие мышцы кровеносных сосудов иннервируются волокнами вегетативной нервной системы.
Трансмуральное давление, диаметр сосудов и напряжение в стенке
Трансмуральное давление и диаметр сосудов.
Трансмуральным давлением называют разность давлений между внутренней и наружной поверхностями стенки сосуда (Рt = Рв – Рн). Поскольку сосудистая стенка эластична, изменения трансмурального давления сопровождаются соответствующими изменениями диаметра и степени растяжения сосуда.
В большинстве органов внешнее давление (т. е. давление на сосуды со стороны окружающих тканей) невелико, поэтому трансмуральное давление фактически равно внутрисосудистому. Однако в некоторых особых случаях внутрисосудистое давление может оставаться постоянным, а трансмуральное-претерпевать значительные изменения из-за местных колебаний экстрамурального давления (это касается в особенности вен с их легко деформируемыми стенками). В таких ситуациях просвет сосудов меняется, и это влияет на их емкость и скорость кровотока.
Трансмуральное давление и напряжение в стенке сосуда. Растягивающее давление, действующее на стенки сосуда, создает в них противоположно направленное тангенциальное напряжение (Т). Это напряжение зависит не только от трансмурального давления, но также от внутреннего радиуса (rв) и толщины стенок (h). Напряжение, проинтегрированное для всей толщины стенки (Тh), можно рассчитать исходя из видоизмененногоуравнения Лапласа:
Th=Ptrв/h(H/M2). (14)
На рис. 20.5 приведены все факторы, учитываемые в данном уравнении. Трансмуральное давление направлено таким образом, что, если бы сосуд был разделен на две половины продольным разрезом, эти половины расходились бы под действием силы, равной
Fpt = 2 • rв • L • Pt. В норме эта сила уравновешена противодействующей силой, создающейся в стенках: Fth = 2h • L • Th. Как тангенциальное напряжение в стенке, так и трансмуральное давление имеют размерность силы, отнесенной к единице
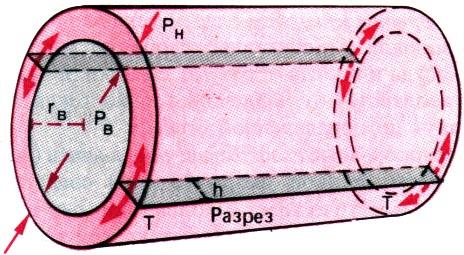
Рис. 20.5. Схема соотношения трансмурального давления и тангенциального напряжения в кровеносном сосуде цилиндрической формы. Рв внутрисосудистое давление; Рн-давление снаружи сосуда; rв -внутренний радиус; h-толщина стенки; Т тангенциальное напряжение в стенке сосуда. Если бы в стенке сосуда был произведен продольный разрез, то края этого разреза разошлись бы под действием силы Т
поверхности, и служат мерой напряжения, испытываемого структурами сосудистой стенки. При данном давлении этонапряжение будет тембольше, чем больше радиус сосуда именьше толщина его стенки.
В табл. 20.1 приведены значения напряжения в стенках различных сосудов. Эти значения рассчитаны для более простых, чем реальные, условий: 1) не учтены градиенты давлений (приняты средние давления для сосудов каждого типа с различным радиусом), 2) в некоторых случаях соотношение между внутренним радиусом и толщиной стенки широко варьирует. Из таблицы видно, что по мере удаления от аорты и крупных артерий к артериолам и более дистальным сосудам напряжение в стенке значительно снижается. Благодаря этой закономерности – низкому напряжению в стенке сосудов с малым радиусом- капилляры, состоящие всего из одного слоя клеток, не разрываются под действием растягивающей силы, обусловленной давлением крови. Мелкие сосуды обладают еще одной особенностью: когда в результате сокращения гладких мышц их радиус снижается, напряжение в их стенке, будучи небольшим уже в состоянии покоя, еще сильнее уменьшается. Это связано не только с уменьшением радиуса сосуда, но и с одновременным утолщением его стенки. В связи с этим
Таблица 20.1. Значения трансмурального давления (Р) и тангенциального напряжения (Т) в различных сосудах [4,6]
Сосуды | r(в), м | r/h | Р, кПа | Т, кПа |
Аорта | 12-10-3 | 8 | 13,3 | 106 |
Артерии | 0,5-3 10-3 | 3-7 | 11,0 | 33-77 |
Артериолы | 10-100 10-6 | 15 | 7,0 | 7-35 |
Капилляры | 3 10-6 | 58 | 3,3 | 17-26 |
Венулы | 10-250 10-6 | 7 -10 | 1,6 | 11-16 |
Вены | 0,75-7,5 10-3 | 7 -10 | 1,3 | 9-13 |
Полые вены | 17 10-3 | 10- 15 | 1,0 | 10-15 |
неудивительно, что при любых физиологических значениях давления сокращение гладкой мускулатуры артериол легко приводит к уменьшению их диаметра.
Взаимосвязь между давлением в сосудах и их объемом
Упругие свойства сосудов. Пределырастяжимости сосудов зависят как от числа эластических и коллагеновых волокон, так и от соотношения между ними. Так, артерии какого-либо отдела большого круга кровообращения в 6-10 раз менее растяжимы, чем вены этого же отдела. В малом же круге кровообращения артерии всего в два раза менее растяжимы, чем вены, которые обладают почти такими же свойствами, как в большом круге.
Коэффициент объемной упругости Е’. Коэффициент объемной упругости Е’ отражает упругие свойства полого образования (или изолированного отрезка сосуда). Этот коэффициент равен отношению прироста давления (ΔР) к приросту объема (AV):
Е’ = ΔP/ΔV(Па/мл) (15)
Если упругий материал легко растяжим, то его Е’ мал, и наоборот. О податливости сосуда можно также судить по такой величине, как
Растяжимость = ΔV/ ΔP(16)
Общая растяжимость системы из полых упругих элементов равна сумме растяжимостей этих элементов.
Соотношение между давлением и объемом как в отдельных сосудах или их частях, так и в кровеносной системе в целом можно представить в виде кривых давление-объем (см. рис. 20.12).
Модуль объемной упругости К отражает упругость, отнесенную к единице объема (т. е. прирост давления, необходимый для относительного изменения объема):
К= ΔP/ΔV=E’ V(Па) (17)
Модуль объемной упругости связан с плотностью крови ρ и скоростью распространения пульсовой волны с (в см/с) следующей зависимостью:
К = ρс2, или с = √K/ρ (18)
Эта зависимость дает возможность судить об упругих свойствах артерий при помощи относительно простого способа измерения скорости распространения пульсовой волны.
Сосудистый тонус. Во многих сосудах имеется некоторое количество гладкомышечных клеток, которые периодически спонтанно деполяризуются (см. разд. 4.5); эти клетки играют роль «пейсмекеров» и возбуждают соседние клетки. Их сокращения не зависят от иннервации сосуда и наблюдаются даже после денервации сосудов. Благодаря этому явлению стенки сосудов даже в покое находятся в состоянии напряжения, или так называемого миогенного базального тонуса (см. рис. 20.25 и 20.26).
Напряжение большинства сосудов в покое обусловлено не только базальным тонусом, но также сокращением гладкомышечных клеток под влиянием сосудосуживающих импульсов, поступающих по вегетативным нервным волокнам. Это суммарное напряжение сосудов называетсятонусом покоя (см. рис. 20.25).
Релаксация напряжения. Если внезапно увеличить объем изолированного участка сосуда, то давление в нем сначала резко повысится, а затем будет постепенно снижаться при том же объеме. Через несколько минут давление может стать лишь немногим больше, чем до увеличения объема (рис. 20.6). Это медленное снижение давления связано с тем, что после первоначального растяжения эластических волокон развивается как бы приспособление тонуса гладких мышц к увеличенному растяжению. Этот процесс называется релаксацией напряжения. Возможно, такоевязкоэластичное поведение сосудистой стенки обусловлено перестройкой актомиозиновых мостиков в растянутых мышечных волокнах, в результате которой миофиламенты медленно скользят относительно друг друга, что и приводит к уменьшению напряжения.
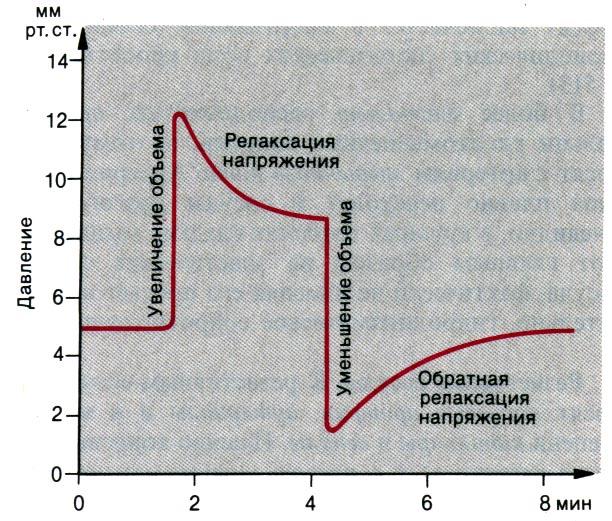
Рис. 20.6. Кривая изменения давления при ступенчатом изменении объема в изолированном участке вены (по Гайтону [8] с изменениями)
При внезапном снижении объема в сосуде происходят обратные процессы (рис. 20.6). Напряжение в гладкомышечных волокнах сначала резко снижается, а в последующие минуты постепенно повышается; вместе с напряжением возрастает и внутрисосудистое давление. Это так называемая обратная релаксация напряжения.
Все эти явления гораздо более выражены в венах, чем в артериях. Благодаря этому, а также вследствие большой емкости вены могут задерживать и выбрасывать значительный объем крови без длительных изменений внутрисосудистого давления. Возможно, релаксация напряжения и обратная релаксация служат важными механизмами поддержания давления наполнения кровеносной системы в соответствии с различными физиологическими потребностями организма.
Соотношение между давлением и скоростью кровотока в сосудах разного типа
Пассивное растяжение. Благодаря эластичности сосудов изменения давления влияют на объемную скорость кровотока не только непосредственно, но также косвенно – путем изменений просвета сосуда.
Вследствие этого в некоторых сосудах объемная скорость кровотока в большей степени зависит от давления, чем в жестких трубках. Для таких сосудов наклон кривых кровоток-давление непрерывно увеличивается. Классическим примером сосудов, пассивно растягивающихся при изменениях давления, служатсосуды легких (рис. 20.7).
Ауторегуляция сосудистого тонуса. В некоторых сосудах, напротив, при увеличении давления прирост объемной скорости кровотока постепенно уменьшается, что сопровождается уменьшением наклона кривой объемная скорость-давление (рис. 20.7). Это явление обусловлено ауторегуляторными реакциями гладких мышц на механические воздействия(эффект Бейлиса): при растяжении гладкие мышцы сокращаются. Чем выше внутрисосудистое давление, тем сильнее сокращаются гладкие мышцы; в результате при увеличении давления объемная скорость кровотока либо не изменяется, либо возрастает незначительно. Этот механизм способствует стабилизации кровоснабжения органа. В некоторых органах объемная скорость не изменяется при колебаниях давления от 120 до 200 мм рт. ст. Классическим примером таких сосудов служатсосуды почек. Эта миогенная ауторегуляция не зависит от вегетативных влияний, поэтому она сохраняется даже после перерезки сосудодвигательных нервов [9, 32].
Соотношение между давлением и объемной скоростью кровотока можно приблизительно описать при
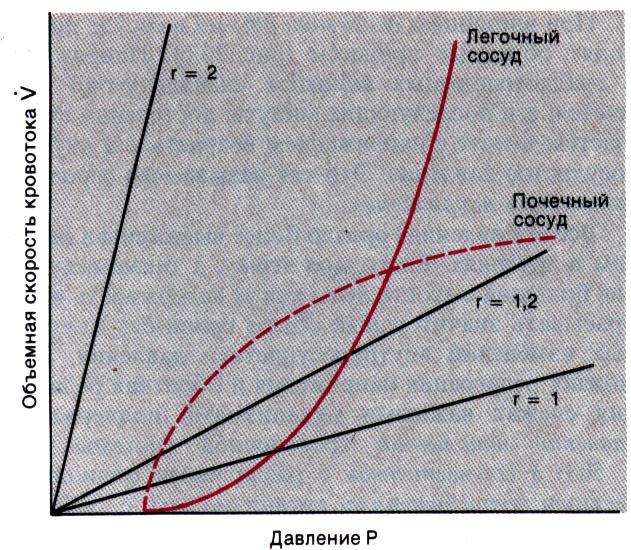
Рис. 20.7. Кривые кровоток -давление для различных типов сосудов. При повышении давления в сосуде он либо пассивно растягивается (легочный сосуд), либо сокращается в результате ауторегуляторных реакций (почечный сосуд). Следовательно, в сосудах типа легочных повышение давления приводит к большему увеличению кровотока, чем в жестких трубках, а в сосудах типа почечных-к меньшему. Если давление падает ниже некоего критического уровня (критического давления закрытия), кровоток в сосудах прекращается. В жестких же трубках (черные кривые) кровоток прямо пропорционален давлению, причем при увеличении радиуса трубки от 1 до 1,2 и 2 коэффициент пропорциональности возрастает соответственно в 2 и 16 раз
помощи степенной функции, аналогичной уравнению Ома, в котором ΔР возводится в степени, не равные 1. Для сосудов типа легочных показатели степени больше 1, а для сосудов типа почечных-меньше 1. При этом на форму и расположение кривой давление-кровоток влияет тонус сосудистых мышц, зависящий от нервных и метаболических факторов, химического состава крови и т.д.
Критическое давление закрытия. Кривые давление-кровоток часто пересекают горизонтальную ось не в области нуля, а в точке, соответствующей некой положительной величине-так называемому критическому давлению закрытия (см. рис. 20.7). При перфузии сосуда кровью это давление составляет около 20 мм рт.ст., а при высоком сосудистом тонусе оно может достигать 60 мм рт.ст. В отсутствие тонуса критическое давление закрытия может снижаться до 1 мм рт.ст.
Считается, что спадение сосуда при критическом давлении характерно для артериол. Это связано с тем, что по мере снижения их радиуса, наступающего в результате уменьшения давления, растягивающая сила убывает быстрее, чем она уменьшалась бы только в
соответствии со снижением давления. Кроме того, к остановке кровотока может приводить увеличение вязкости крови, наблюдающееся при низких скоростях кровотока. В тех участках сосудистой системы, где наружное давление достаточно велико по сравнению с внутрисосудистым, кровоток может прекращаться даже при наличии артериовенозного градиента давления. Это может быть обусловлено либо спадением сосудов (легочные сосуды, вены), либо их сдавлением (коронарные сосуды при систоле). В условиях значительного критического давления при снижении чрезмерно высокого кровяного давления до нормы кровообращение в той или иной сосудистой области может прекратиться. Таким образом, для определения эффективной артериовенозной разницы давлений в сосудистой системе из полученной при измерении величины следует вычитать критическое давление закрытия.
Соседние файлы в папке ССС
- #
- #
- #
- #
- #
- #
- #
Источник
