Температура стенок сосуда при кипении

Êèïåíèå — ýòî èíòåíñèâíûé ïåðåõîä æèäêîñòè â ïàð, ïðîèñõîäÿùèé ñ îáðàçîâàíèåì ïóçûðüêîâ ïàðà ïî âñåìó îáúåìó æèäêîñòè ïðè îïðåäåëåííîé òåìïåðàòóðå.
 îòëè÷èå îò èñïàðåíèÿ, êîòîðîå ïðîèñõîäèò ïðè ëþáîé òåìïåðàòóðå æèäêîñòè, äðóãîé âèä ïàðîîáðàçîâàíèÿ — êèïåíèå — âîçìîæåí ëèøü ïðè ñîâåðøåííî îïðåäåëåííîé (ïðè äàííîì äàâëåíèè) òåìïåðàòóðå — òåìïåðàòóðå êèïåíèÿ.
Ïðè íàãðåâàíèè âîäû â îòêðûòîì ñòåêëÿííîì ñîñóäå ìîæíî óâèäåòü, ÷òî ïî ìåðå óâåëè÷åíèÿ òåìïåðàòóðû ñòåíêè è äíî ñîñóäà ïîêðûâàþòñÿ ìåëêèìè ïóçûðüêàìè. Îíè îáðàçóþòñÿ â ðåçóëüòàòå ðàñøèðåíèÿ ìåëü÷àéøèõ ïóçûðüêîâ âîçäóõà, êîòîðûå ñóùåñòâóþò â óãëóáëåíèÿõ è ìèêðîòðåùèíàõ íå ïîëíîñòüþ ñìà÷èâàåìûõ ñòåíîê ñîñóäà.
Ïàðû æèäêîñòè, êîòîðûå íàõîäÿòñÿ âíóòðè ïóçûðüêîâ, ÿâëÿþòñÿ íàñûùåííûìè. Ñ ðîñòîì òåìïåðàòóðû äàâëåíèå íàñûùåííûõ ïàðîâ âîçðàñòàåò, è ïóçûðüêè óâåëè÷èâàþòñÿ â ðàçìåðàõ. Ñ óâåëè÷åíèåì îáúåìà ïóçûðüêîâ ðàñòåò è äåéñòâóþùàÿ íà íèõ âûòàëêèâàþùàÿ (àðõèìåäîâà) ñèëà. Ïîä äåéñòâèåì ýòîé ñèëû íàèáîëåå êðóïíûå ïóçûðüêè îòðûâàþòñÿ îò ñòåíîê ñîñóäà è ïîäíèìàþòñÿ ââåðõ. Åñëè âåðõíèå ñëîè âîäû åùå íå óñïåëè íàãðåòüñÿ äî 100 °Ñ, òî â òàêîé (áîëåå õîëîäíîé) âîäå ÷àñòü âîäÿíîãî ïàðà âíóòðè ïóçûðüêîâ êîíäåíñèðóåòñÿ è óõîäèò â âîäó; ïóçûðüêè ïðè ýòîì ñîêðàùàþòñÿ â ðàçìåðàõ, è ñèëà òÿæåñòè çàñòàâëÿåò èõ ñíîâà îïóñêàòüñÿ âíèç. Çäåñü îíè îïÿòü óâåëè÷èâàþòñÿ è âíîâü íà÷èíàþò âñïëûâàòü ââåðõ. Ïîïåðåìåííîå óâåëè÷åíèå è óìåíüøåíèå ïóçûðüêîâ âíóòðè âîäû ñîïðîâîæäàåòñÿ âîçíèêíîâåíèåì â íåé õàðàêòåðíûõ çâóêîâûõ âîëí: çàêèïàþùàÿ âîäà øóìèò.
Êîãäà âñÿ âîäà ïðîãðååòñÿ äî 100 °Ñ, ïîäíÿâøèåñÿ ââåðõ ïóçûðüêè óæå íå ñîêðàùàþòñÿ â ðàçìåðàõ, à ëîïàþòñÿ íà ïîâåðõíîñòè âîäû, âûáðàñûâàÿ ïàð íàðóæó. Âîçíèêàåò õàðàêòåðíîå áóëüêàíüå — âîäà êèïèò.
Êèïåíèå íà÷èíàåòñÿ ïîñëå òîãî, êàê äàâëåíèå íàñûùåííîãî ïàðà âíóòðè ïóçûðüêîâ ñðàâíèâàåòñÿ ñ äàâëåíèåì â îêðóæàþùåé æèäêîñòè.
Âî âðåìÿ êèïåíèÿ òåìïåðàòóðà æèäêîñòè è ïàðà íàä íåé íå ìåíÿåòñÿ. Îíà ñîõðàíÿåòñÿ íåèçìåííîé äî òåõ ïîð, ïîêà âñÿ æèäêîñòü íå âûêèïèò. Ýòî ïðîèñõîäèò ïîòîìó, ÷òî âñÿ ïîäâîäèìàÿ ê æèäêîñòè ýíåðãèÿ óõîäèò íà ïðåâðàùåíèå åå â ïàð.
Òåìïåðàòóðà, ïðè êîòîðîé êèïèò æèäêîñòü, íàçûâàåòñÿ òåìïåðàòóðîé êèïåíèÿ.
Òåìïåðàòóðà êèïåíèÿ çàâèñèò îò äàâëåíèÿ, îêàçûâàåìîãî íà ñâîáîäíóþ ïîâåðõíîñòü æèäêîñòè. Ýòî îáúÿñíÿåòñÿ çàâèñèìîñòüþ äàâëåíèÿ íàñûùåííîãî ïàðà îò òåìïåðàòóðû. Ïóçûðåê ïàðà ðàñòåò, ïîêà äàâëåíèå íàñûùåííîãî ïàðà âíóòðè íåãî íåìíîãî ïðåâîñõîäèò äàâëåíèå â æèäêîñòè, êîòîðîå ñêëàäûâàåòñÿ èç âíåøíåãî äàâëåíèÿ è ãèäðîñòàòè÷åñêîãî äàâëåíèÿ ñòîëáà æèäêîñòè.
×åì áîëüøå âíåøíåå äàâëåíèå, òåì áîëüøå òåìïåðàòóðà êèïåíèÿ.
Âñåì èçâåñòíî, ÷òî âîäà êèïèò ïðè òåìïåðàòóðå 100 ºC. Íî íå ñëåäóåò çàáûâàòü, ÷òî ýòî ñïðàâåäëèâî ëèøü ïðè íîðìàëüíîì àòìîñôåðíîì äàâëåíèè (ïðèìåðíî 101 êÏà). Ïðè óâåëè÷åíèè äàâëåíèÿ òåìïåðàòóðà êèïåíèÿ âîäû âîçðàñòàåò. Òàê, íàïðèìåð, â êàñòðþëÿõ-ñêîðîâàðêàõ ïèùó âàðÿò ïîä äàâëåíèåì îêîëî 200 êÏà. Òåìïåðàòóðà êèïåíèÿ âîäû ïðè ýòîì äîñòèãàåò 120°Ñ.  âîäå òàêîé òåìïåðàòóðû ïðîöåññ âàðêè ïðîèñõîäèò çíà÷èòåëüíî áûñòðåå, ÷åì â îáû÷íîì êèïÿòêå. Ýòèì è îáúÿñíÿåòñÿ íàçâàíèå «ñêîðîâàðêà».
È íàîáîðîò, óìåíüøàÿ âíåøíåå äàâëåíèå, ìû òåì ñàìûì ïîíèæàåì òåìïåðàòóðó êèïåíèÿ. Íàïðèìåð, â ãîðíûõ ðàéîíàõ (íà âûñîòå 3 êì, ãäå äàâëåíèå ñîñòàâëÿåò 70 êÏà) âîäà êèïèò ïðè òåìïåðàòóðå 90 °Ñ. Ïîýòîìó æèòåëÿì ýòèõ ðàéîíîâ, èñïîëüçóþùèì òàêîé êèïÿòîê, òðåáóåòñÿ çíà÷èòåëüíî áîëüøå âðåìåíè äëÿ ïðèãîòîâëåíèÿ ïèùè, ÷åì æèòåëÿì ðàâíèí. À ñâàðèòü â ýòîì êèïÿòêå, íàïðèìåð, êóðèíîå ÿéöî âîîáùå íåâîçìîæíî, òàê êàê ïðè òåìïåðàòóðå íèæå 100 °Ñ áåëîê íå ñâîðà÷èâàåòñÿ.
Ó êàæäîé æèäêîñòè ñâîÿ òåìïåðàòóðà êèïåíèÿ, êîòîðàÿ çàâèñèò îò äàâëåíèÿ íàñûùåííîãî ïàðà. ×åì âûøå äàâëåíèå íàñûùåííîãî ïàðà, òåì íèæå òåìïåðàòóðà êèïåíèÿ ñîîòâåòñòâóþùåé æèäêîñòè, ò. ê. ïðè ìåíüøèõ òåìïåðàòóðàõ äàâëåíèå íàñûùåííîãî ïàðà ñòàíîâèòñÿ ðàâíûì àòìîñôåðíîìó. Íàïðèìåð, ïðè òåìïåðàòóðå êèïåíèÿ 100 °Ñ äàâëåíèå íàñûùåííûõ ïàðîâ âîäû ðàâíî 101 325 Ïà (760 ìì ðò. ñò.), à ïàðîâ ðòóòè — âñåãî ëèøü 117 Ïà (0,88 ìì ðò. ñò.). Êèïèò ðòóòü ïðè 357°Ñ ïðè íîðìàëüíîì äàâëåíèè.
Òåïëîòà ïàðîîáðàçîâàíèÿ.
Òåïëîòà ïàðîîáðàçîâàíèÿ (òåïëîòà èñïàðåíèÿ) — êîëè÷åñòâî òåïëîòû, êîòîðîå íåîáõîäèìî ñîîáùèòü âåùåñòâó (ïðè ïîñòîÿííîì äàâëåíèè è ïîñòîÿííîé òåìïåðàòóðå) äëÿ ïîëíîãî ïðåâðàùåíèÿ æèäêîãî âåùåñòâà â ïàð.
Ôèçè÷åñêàÿ âåëè÷èíà, ïîêàçûâàþùàÿ, êàêîå êîëè÷åñòâî òåïëîòû íåîáõîäèìî, ÷òîáû îáðàòèòü æèäêîñòü ìàññîé 1 êã â ïàð áåç èçìåíåíèÿ òåìïåðàòóðû, íàçûâàåòñÿ óäåëüíîé òåïëîòîé ïàðîîáðàçîâàíèÿ.
Óäåëüíóþ òåïëîòó ïàðîîáðàçîâàíèÿ îáîçíà÷àþò áóêâîé r è èçìåðÿþò â äæîóëÿõ íà êèëîãðàìì (Äæ/êã).
Êîëè÷åñòâî òåïëîòû, íåîáõîäèìîå äëÿ ïàðîîáðàçîâàíèÿ (èëè âûäåëÿþùååñÿ ïðè êîíäåíñàöèè). ×òîáû âû÷èñëèòü êîëè÷åñòâî òåïëîòû Q, íåîáõîäèìîå äëÿ ïðåâðàùåíèÿ â ïàð æèäêîñòè ëþáîé ìàññû, âçÿòîé ïðè òåìïåðàòóðå êèïåíèÿ, íóæíî óäåëüíóþ òåïëîòó ïàðîîáðàçîâàíèÿ r óìíîæèòü íà ìàññó m:
Q = rm.
Ïðè êîíäåíñàöèè ïàðà ïðîèñõîäèò âûäåëåíèå òàêîãî æå êîëè÷åñòâà òåïëîòû:
Q = -rm.
Источник
Анонимный вопрос
24 ноября 2018 · 3,0 K
ЕГЭ и поступление в вуз – новости и законы. Веду ютуб-канал и паблик в ВК · vk.com/grandexam
Принято считать, что жидкости кипит при некоторой фиксированной температуре, температуре кипения. Например, для воды при нормальных условиях это 100°С.
Однако если постараться (например, взять идеально чистую дистиллированную воду без пузырьков воздуха), можно нагреть жидкость и немного выше температуры кипения. Такая жидкость будет называться перегретой. Она будет находиться в неустойчивом состоянии и при малейшем воздействии будет стремительно переходить в пар.
До какой максимальной температуры можно нагреть воду?
Бывший школьник, недопсихолог, далеко не генетик и не нейрофизиолог, но…
Имеется в виду жидкая вода или вода вообще?
Как верно заметил оратор выше, с увеличением давления увеличивается и температура кипения, однако продолжаться бесконечно это не может. Каждое вещество имеет критическую температуру фазового перехода — когда давление настолько большое, что различия между фазой жидкости и газа у вещества исчезают (плотность жидкости и её насыщенного пара уравниваются, а поверхностное натяжение вещества доходит до нуля). У воды это проходит при максимальном давлении в 218,3 атмосфер, тогда температура кипения будет равна 647 по Кельвину или примерно 374 по Цельсию.
Если имеется в виду максимальная температура вещества вообще, то здесь она для всех веществ одинаковая. Для начала, после нагрева молекул воды до температуры в несколько тысяч градусов, с орбит атомов слетят электроны и в целом получится уже не вода, а свободные ядра водорода и кислорода. Далее, на температуре около ста миллиардов градусов и ядра развалятся протоны с нейтронами, позже — протоны разделятся на кварки и глюоны.
Что будет, если нагревать дальше? Существует верхний предел температуры (планковская температура) для всех веществ во Вселенной. Выше планковской температуры энергия частиц становится настолько большой, что гравитационные силы между ними становятся сравнимы с остальными фундаментальными взаимодействиями. Проще говоря, вся материя переходит в энергию, ибо сама по себе температура в термодинамике — это кинетическая энергия молекул. Равна эта величина примерно 1,416808*10^32 (141 680 800 000 000 000 000 000 000 000 000 — сто сорок один нониллион, шестьсот восемьдесят октиллионов, восемьсот септиллионов) градуса Кельвина с погрешностью.
Прочитать ещё 1 ответ
На сколько градусов в минуту остывает кипяток (100 градусов) при комнатной температуре (20 градусов)?
Георазведка, путешествия, журналистика, и т.д.
Ответ зависит от того, в какой емкости находится кружка – состав стенки емкости и ее толщина (удельная теплоемкость). Это может быть алюминиевая кружка, а может лютый термостаканище.
По ощущениям, за 5 минут кипяток остывает до вида “можно пить по чуть-чуть” и не обжечься, а за 20 минут до примерно комнатной.
dT = k(T – Tср)*dt, где
dT – разность температуры жидкости, на которую оно охладится за время dt;
T – начальная температура жидкости;
Tср – температура окружающей среды;
k – коэффициент, зависящий от множества условий, таких как форма чашки, толщина ее стенок, покрыта ли она крышкой при остывании, есть ли движение воздуха и т.п.
Источник
Что это за явление?
 Кипение — это процесс перехода воды из жидкого агрегатного состояния в газообразное, то есть ее превращение в пар.
Кипение — это процесс перехода воды из жидкого агрегатного состояния в газообразное, то есть ее превращение в пар.
От обычного испарения оно отличается высокой степенью интенсивности: если на испарение воды может потребоваться несколько дней или недель, то выкипеть такой же ее объем сможет за считанные часы.
При необходимости ёмкость можно прикрыть, тогда часть пара будет конденсироваться обратно, становясь капельками воды.
Процесс кипения условно можно разделить на два этапа:
- сначала вода нагревается до нужной температуры (при нормальном атмосферном давлении — это 100 градусов Цельсия),
- потом происходит её превращение в пар, в течение которого показания термометра уже не меняются.
Однако источник тепла нужен даже на этой стадии, ведь парообразование тоже требует энергетических затрат.
Какие факторы влияют на закипание?
На кипение влияет множество факторов:
- количество воды;
- наличие примесей;
- емкость, в которой она содержится;
- температура окружающей среды;
- высота, где происходит кипячение;
- давление атмосферы;
- мощность источника тепла.
Чем выше изначальная температура воды и воздуха вокруг, тем быстрее начнётся кипение: на нагревание будет затрачено меньше энергии, а значит, меньше времени уйдёт на её получение.
Также часть тепла забирает ёмкость, в которой содержится вода, ведь она должна дойти до нужной температуры ещё раньше, чем ее содержимое. Поэтому посуда с более тонкими стенками, сделанная из легко проводящего тепло материала, например, металла, лучше подходит для кипячения.
От массы, а значит и от объёма вещества, кипение находится в обратной зависимости. Чем больше вес, тем больше энергии требуется на его нагревание, тем дольше будет необходимо ждать.
 При прочих равных условиях вода без соли и других примесей закипает несколько быстрее, чем солёная. Однако, если концентрация соли очень низкая, этой разницы может быть практически незаметно.
При прочих равных условиях вода без соли и других примесей закипает несколько быстрее, чем солёная. Однако, если концентрация соли очень низкая, этой разницы может быть практически незаметно.
Давление также влияет на процесс. Чем оно выше, тем дольше будет закипать вода, потому что давление атмосферы как бы удерживает пузырьки газа внутри, а испаряться она начинает тогда, когда давление пара уравнивается с атмосферным.
Соответственно, влияние оказывает также высота, на которой происходит кипячение, ведь с высотой давление уменьшается, как и температура кипения, потому что слой атмосферы сверху становится тоньше.
Эта разница мало заметна, если сравнивать первый этаж жилого дома с пятым, однако становится ощутима, если речь идёт, например, о подъеме в горы.
В вакууме температура кипения всех веществ очень сильно снижается из-за понижения давления, обычно отличие составляет 100-200 градусов. Для воды она стремится к нулю по мере уменьшения количества воздуха, оставшегося в сосуде.
Не менее важны характеристики источника тепла. Чем больше его мощность, то есть количество выделяемой им энергии за единицу времени, тем быстрее идет процесс кипячения. На практике это означает, что на более сильном огне или при большей температуре конфорки на электроплите вода закипит скорее.
Сколько по времени закипает?
Становится понятно, что время кипения сильно зависит от условий, при которых оно происходит.
Чтобы узнать количество времени (секунд) точно до закипания, можно воспользоваться формулой: t= (c1m1t°C1+ c2m2t°C2 +Lm) / N
Величины:
-
 c1, L — табличные величины, теплоемкость и удельная теплота парообразования воды;
c1, L — табличные величины, теплоемкость и удельная теплота парообразования воды; - m1 — ее масса;
- t°C — разница между изначальной и нужной для кипения температурой;
- N — мощность нагревательного прибора;
- m2 и c2 — характеристики емкости, в которой проводится кипячение (масса и теплоемкость).
Даже эта формула учитывает не все, ведь также существуют потери тепла, которое уходит в окружающую среду.
Однако такая точность редко бывает нужна в быту, кроме того, необходимые данные для расчётов получить затруднительно. Чаще всего кипение литра воды на плите при достаточно большом огне занимает около 10 минут. Здесь некоторую роль играет материал, из которого сделана посуда. Быстрее всего нагревается металл.
Как понять, что жидкость кипит?
По мере приближения к точке кипения в воде появляется все больше пузырьков. Сначала их можно увидеть на стенках сосуда, а потом они начинают всплывать на поверхность, отчего она становится неровной. Пропустить этот момент сложно из-за характерного бурления.
Присмотревшись, над поверхностью воды можно будет увидеть поднимающийся пар. Если нет цели заставить воду выкипать, стоит снять её с плиты.
Даже спустя некоторое время после этого испарение будет продолжаться, потому что температура не сразу опустится ниже точки кипения. Например, от чашки горячего чая еще некоторое время идет пар.
Как быстро остывает после?
 Остывание зависит от тех же факторов, что и нагрев: от объема, температуры окружающей среды.
Остывание зависит от тех же факторов, что и нагрев: от объема, температуры окружающей среды.
Например, электрочайник, вскипевший за пять минут, будет остывать около двух часов, чтобы дойти до комнатной температуры.
Если объем воды большой, то остывание при прочих равных займет более длительный промежуток времени, а чем холоднее воздух вокруг, тем быстрее охладится и сам кипяток. Его температура будет опускаться до того момента, пока не сравняется с окружающей.
Нюансы процесса
Кипение воды в чайнике и кастрюле немного различается между собой, но в обоих случаях оно происходит при 100 градусах. Рассмотрим особенности каждого процесса.
В чайнике
В электрическом чайнике процесс пойдёт быстрее, чем при кипячении в кастрюле, он займёт 3-4 минуты, точное время зависит от конкретной модели и ее мощности. Не потребуется даже выключать прибор – он сделает это автоматически.
Обычный чайник несильно отличается от металлической кастрюли похожей конфигурации и размера, поэтому время закипания у них приблизительно одинаково.
Свист, которым чайник оповещает, что вода кипит, связан с прохождением пара через крышку на его носике.
В кастрюле
 При таком способе кипячения ждать потребуется дольше – около 10 мин. Лучше всего подойдет металлическая кастрюля, она нагреется быстрее, чем емкости из других материалов.
При таком способе кипячения ждать потребуется дольше – около 10 мин. Лучше всего подойдет металлическая кастрюля, она нагреется быстрее, чем емкости из других материалов.
Не стоит наполнять ее до самого верха, потому что в таком случае при кипении брызги будут выплескиваться на плиту. Момент закипания сопровождается громким бурлением. Почти сразу после этого воду можно выключать.
Если накрыть кастрюлю крышкой, можно ускорить нагрев и закипание воды, потому что снизится количество тепла, уходящего в окружающую среду. Однако желательно оставить щель, через которую будет выходить пар.
Видео по теме статьи
О кипении жидкости расскажет видео:
Заключение
Хотя с точки зрения физики кипение — далеко не самый сложный процесс, говорить о нем можно долго, так как он связан со множеством факторов, под воздействием которых особенности его протекания несколько отличаются.
Даже общие знания из этой области могут быть полезны и найдут практическое применение, ведь в быту с необходимостью вскипятить воду регулярно сталкивается каждый.
А какова Ваша оценка данной статье?
Источник
Ход урока
1.Стадии кипения воды.
Кипение – переход жидкости в пар, происходящий
с образованием в объеме жидкости пузырьков пара
или паровых полостей. Пузырьки растут вследствие
испарения в них жидкости, всплывают, и
содержащийся в пузырьках насыщенный пар
переходит в паровую фазу над жидкостью.
Кипение начинается, когда при нагреве жидкости
давление насыщенного пара над её поверхностью
становится равным внешнему давлению.
Температура, при которой происходит кипение
жидкости, находящейся под постоянным давлением,
называется температурой кипения (Ткип). Для
каждой жидкости температура кипения имеет свое
значение и в стационарном процессе кипения не
меняется.
Строго говоря, Ткип соответствует температуре
насыщенного пара (температуре насыщения) над
плоской поверхностью кипящей жидкости, так как
сама жидкость всегда несколько перегрета
относительно Ткип. При стационарном кипении
температура кипящей жидкости не меняется. С
ростом давления Ткип увеличивается
1.1.Классификация процессов кипения.
Кипение классифицируют по следующим признакам:
1)
пузырьковое и пленочное.
Кипение, при котором пар образуется в виде
периодически зарождающихся и растущих пузырей,
называется пузырьковым кипением. При медленном
пузырьковом кипении в жидкости (а точнее, на
стенках или на дне сосуда) появляются пузырьки,
наполненные паром.
При увеличении теплового потока до некоторой
критической величины отдельные пузырьки
сливаются, образуя у стенки сосуда сплошной
паровой слой, периодически прорывающиеся в объём
жидкости. Такой режим называется плёночным.
Если температура дна сосуда значительно
превышает температуру кипения жидкости, то
скорость образования пузырей на дне становится
столь большой, что они объединяются вместе,
образуя сплошную паровую прослойку между дном
сосуда и непосредственно самой жидкостью. В этом
режиме плёночного кипения тепловой поток от
нагревателя к жидкости резко падает (паровая
плёнка проводит тепло хуже, чем конвекция в
жидкости), и в результате скорость выкипания
уменьшается. Режим плёночного кипения можно
наблюдать на примере капли воды на раскалённой
плите.
2)
по виду конвекции у поверхности
теплообмена ? при свободной и вынужденной
конвекции;
При нагревании вода ведет себя неподвижно, и
теплота от нижних слоев к верхним передается
посредством теплопроводности. По мере
нагревания, однако, характер теплопередачи
меняется, поскольку запускается процесс, который
принято называть конвекцией. Нагреваясь вблизи
дна, вода расширяется. Соответственно, удельный
вес придонной разогретой воды оказывается легче,
чем вес равного объема воды в поверхностных
слоях. Это приводит всю водную систему внутри
кастрюли в нестабильное состояние, которое
компенсируется за счет того, что горячая вода
начинает всплывать к поверхности, а на ее место
опускается более прохладная вода. Это свободная
конвекция. При вынужденной конвекции теплообмен
создается с помощь перемешивания жидкости и
движение в воде создается за искусственным
теплоносителем-мешалкой, насосом, вентилятором и
тому подобное.
3)
по отношению к температуре насыщения ? без
недогрева и кипение с недогревом. При кипении с
недогревом пузырьки воздуха растут у основания
сосуда, отрываются и схлопываются. Если
недогрева нет, то пузырьки отрываясь, растут и
всплывают на поверхность жидкости.
4)
по ориентации поверхности кипения в
пространстве ? на горизонтальных наклонных и
вертикальных поверхностях;
Некоторые слои жидкости непосредственно
прилегающие к более горячей теплообменной
поверхности, нагреваются выше и поднимаются как
более легкие пристенные вдоль вертикальной
поверхности. Таким образом, вдоль горячей
поверхности возникает непрерывное движение
среды, скорость которой определяет
интенсивность теплообмена поверхности с
основной массой практически неподвижной среды
5)
по характеру кипения ? развитое и
неразвитое, неустойчивое кипение;
С ростом плотности теплового потока растет
коэффициент парообразования. Кипение переходит
в развитое пузырьковое. Увеличение частоты
отрыва приводит к тому, что пузыри догоняют друг
друга и сливаются. С увеличением температуры
поверхности нагрева число центров
парообразования резко возрастает, все большее
количество оторвавшихся пузырьков всплывает в
жидкости, вызывая ее интенсивное перемешивание.
Такое кипение носит развитый характер.
1.2.Разделение процесса кипения по стадиям.
Кипячение воды представляет собой сложный
процесс, состоящий из четырех ясно отличимых
одна от другой стадий.
Первая стадия начинается с проскакивания со
дна чайника маленьких пузырьков воздуха, а также
появления групп пузырьков на поверхности воды у
стенок чайника.
Вторая стадия характеризуется увеличение
объема пузырьков. Затем постепенно количество
пузырьков, возникающих в воде и рвущихся на
поверхность, всё более увеличивается. На первой
стадии кипения слышим тонкий, едва различимый
сольный звук.
Третья стадия кипения характерна массовым
стремительным подъёмом пузырьков, которые
вызывают сначала легкое помутнение, а затем даже
“побеление” воды, напоминая собой быстро
бегущую воду родника. Это так называемое кипение
“ белым ключом”. Оно — крайне
непродолжительное. Звук становится похожим на
шум небольшого пчелиного роя.
Четвертая — это интенсивное бурление воды,
появление на поверхности больших лопающихся
пузырей, а затем брызганьем. Брызги будут
означать, что вода очень сильно перекипела. Звуки
резко усиливаются, но их равномерность
нарушается, они как бы стремятся опередить друг
друга, нарастают хаотически.
2.Из Китайской церемонии чаепития.
На востоке отношение к чаепитию особое. В Китае
и Японии чайная церемония была частью встреч
философов и художников. Во время традиционного
восточного чаепития произносились мудрые речи,
рассматривались произведения искусства. Чайная
церемония специально оформлялась для каждой
встречи, подбирались букеты цветов.
Использовалась специальная посуда для заварки
чая. Особенное отношение было к воде, которая
бралась для заваривания чая. Важно правильно
вскипятить воду, обращая внимание на “циклы
огня”, которые воспринимаются и воспроизводятся
в кипятке. Вода не должна доводиться до бурного
кипения, так как в результате этого уходит
энергия воды, которая, соединяясь с энергией
чайного листа, и производит в нас искомое чайное
состояние.
Есть четыре стадии внешнего вида кипятка,
которые соответственно называются “рыбий глаз”,
“крабий глаз”, “жемчужные нити” и “бурлящий
источник”. Этим четырем стадиям соответствуют
четыре характеристики звукового сопровождения
закипания воды: тихий шум, средний шум, шум и
сильный шум, которым в разных источниках тоже
иногда даются разные поэтические названия.
Кроме того, отслеживают и стадии образования
пара. Например, легкая дымка, туман, густой туман.
Туман и густой туман указывают на переспелость
кипятка, который уже не подходит для заваривания
чая. Считается, что энергия огня в нем уже
настолько сильна, что подавила энергию воды, и в
результате вода не сможет должным образом войти
в контакт с чайным листом и дать соответствующее
качество энергии человеку, пьющему чаю.
В результате правильного заваривания получаем
вкусный чай, заваривать который водой, не
нагретой до 100 градусов, можно несколько раз,
наслаждаясь тонкими оттенками послевкусия от
каждого нового заваривания.
–
В России стали появляться чайные клубы, которые
прививают культуру чаепития Востока. В чайной
церемонии, которая называется Лу Юй, или
кипячение воды на открытом огне можно наблюдать
все стадии кипения воды. Такие эксперименты с
процессом кипения воды можно провести в домашних
условиях. Предлагаю несколько экспериментов:
– изменения температуры на дне сосуда и на
поверхности жидкости;
изменение температурной зависимости стадий
кипения воды;
– изменение объема кипящей воды с течением
времени;
– распределения температурной зависимости от
расстояния до поверхности жидкости.
3.Эксперименты по наблюдению процесса кипения.
3.1. Исследование температурной зависимости
стадий кипения воды.
Проводилось измерение температуры на всех
четырех стадиях кипениях жидкости. Были получены
следующие результаты:
– первая стадия кипения воды (РЫБИЙ ГЛАЗ)
длилась с 1-ой по 4-ую минуты. Пузырьки на дне
появились при температуре 55 градусов (фото 1).
 Фото1.
Фото1.
– вторая стадия кипения воды (КРАБИЙ ГЛАЗ)
длилась с5-ой по7-ую минуты при температуре около
77 градусов. Мелкие пузырьки на дне увеличивались
в объеме, напоминая глаза краба. (фото 2).
 Фото 2.
Фото 2.
– третья стадия кипения воды (ЖЕМЧУЖНЫЕ
НИТИ) длилась с 8-ой по10-ую минуты. Множество
мелких пузырьков образовывали ЖЕМЧУЖНЫЕ НИТИ,
которые поднимались к поверхности воды, не
достигая её. Процесс начался при температуре в 83
градуса (фото 3).
 Фото 3.
Фото 3.
– четвертая стадия кипения воды (БУРЛЯЩИЙ
ИСТОЧНИК) длилась с 10-ой по12-ую минуты. Пузырьки
росли, поднимались на поверхность воды, и
лопались, создавая бурление воды. Процесс
проходил при температуре 98 градусов (фото 4). Фото
4.
 Фото
Фото
4.
3.2. Исследование изменения объема кипящей воды
с течением времени.
С течением времени, объём кипящей воды
изменяется. Первоначальный объем воды в кастрюле
составлял 1 л. Через 32 минуты объем уменьшился
вдвое. Это хорошо видно на фото 5, отмечено
красными точками.
 Фото 5.
Фото 5.
 Фото 6.
Фото 6.
За следующие 13 минут кипения воды её объем
уменьшился на одну треть, эта линия так же
отмечена красными точками (фото 6).
По результатам измерений была получена
зависимостьизменения объема кипящей воды с
течением времени.
| Зависимость изменения объема кипящей воды от времени. | ||||||||
| Измерение | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| Объем, л | 1 | 0.75 | 0.50 | 0.25 | 0.125 | 0.08 | 0.04 | |
| Время, мин | 16 | 32 | 45 | 50 | 65 | 69 | 80 | |
Рис.1. График изменения объема кипящей
воды от времени
Вывод: Изменение объема обратно
пропорционально времени кипения жидкости(рис.1)
до тех пор, пока от первоначального объема не
осталось1/25 часть. На последней стадии
уменьшение объема замедлилось. Здесь играет роль
режим плёночного кипения. Если температура дна
сосуда значительно превышает температуру
кипения жидкости, то скорость образования
пузырей на дне становится столь большой, что они
объединяются вместе, образуя сплошную паровую
прослойку между дном сосуда и непосредственно
самой жидкостью. В этом режиме скоростьвыкипания
жидкости уменьшается.
3.3. Исследование распределения температурной
зависимости от расстояния до поверхности
жидкости.
В кипящей жидкости устанавливается
определённое распределение температуры (рис 2), у
поверхности нагрева жидкость заметно
перегрета. Величина перегрева зависит от ряда
физико-химических свойств и самой жидкости, а так
же граничных твёрдых поверхностей. Тщательно
очищенные жидкости, лишённые растворённых газов
(воздуха), можно при соблюдении особых мер
предосторожности перегреть на десятки градусов.
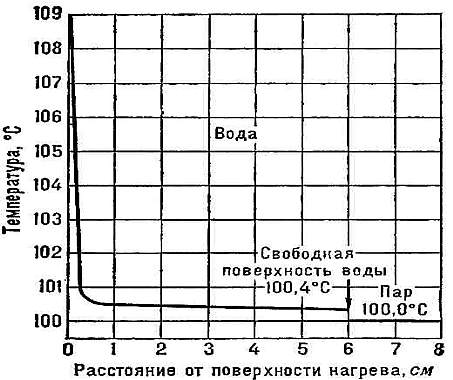
Рис. 2.График зависимости изменения
температуры воды у поверхности от расстояния до
поверхности нагрева.
По результатам измерений можно получить график
зависимости изменения температуры воды от
расстояния до поверхности нагрева.
Вывод: с увеличением глубины жидкости
температура меньше, причем на небольших
расстояниях от поверхности до 1 см температура
резко уменьшается, а потом почти не меняется.
3.4.Исследование изменения температуры на дне
сосуда и у поверхности жидкости.
Было проведено 12 измерений. Воду нагревали от
температуры 7 градусов до момента закипания.
Измерения температуры проводились через каждую
минуту. По результатам измерения было получено
два графика изменения температуры у поверхности
воды и на дне.
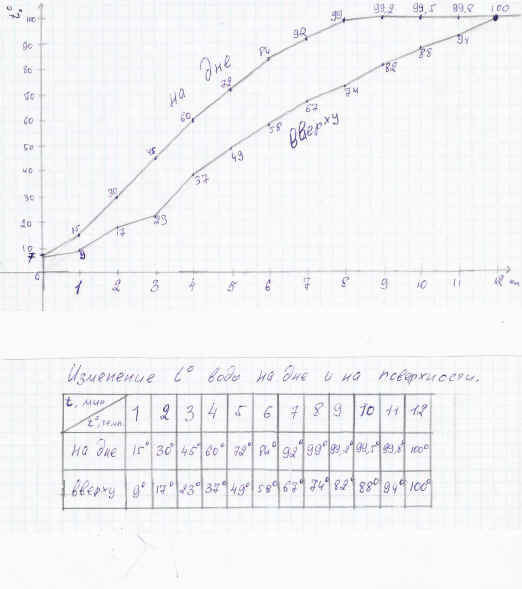
Рис.3.Таблица и график по результатам
наблюдений. (Фото автора)
Выводы: изменение температуры
воды на дне сосуда и на поверхности различно. На
поверхности температура меняется строго по
линейному закону и достигает температуры
кипения позже на три минуты, чем на дне. Это
объясняется тем, что на поверхности жидкость
соприкасается с воздухом и отдаёт часть своей
энергии, поэтому прогревается не так, как на дне
кастрюли.
Выводы по результатам работы.
Было выяснено, что вода при нагревании до
температуры кипения проходит три стадии,
зависящие от теплообмена внутри жидкости с
образованием и ростом внутри жидкости пузырьков
пара. При наблюдении за поведением воды отмечены
характерные особенности каждой стадии.
Изменение температуры воды на дне сосуда и на
поверхности различно. На поверхности
температура меняется строго по линейному закону
и достигает температуры кипения позже на три
минуты, чем на дне.Это объясняется тем, что на
поверхности жидкость соприкасается с воздухом и
отдаёт часть своей энергии.
Так же было определено экспериментально, что с
увеличением глубины жидкости температура
меньше, причем на небольших расстояниях от
поверхности до 1 см температура резко
уменьшается, а потом почти не меняется.
Процесс кипения происходит с поглощение
теплоты. При нагревании жидкости большая часть
энергии идет на разрыв связей между молекулами
воды. При этом растворенный в воде газ выделяется
на дне и стенках сосуда, образуя воздушные
пузырьки. Достигнув определенных размеров,
пузырек поднимается на поверхность и
схлопывается с характерным звуком. Если таких
пузырьков много, то вода “шипит”. Пузырек
воздуха поднимается на поверхность воды и
лопается, если выталкивающая сила, больше силы
тяжести. Кипение представляет собой непрерывный
процесс, при кипении температура воды равна 100
градусов и не меняется в процессе выкипания воды.
Литература
- В.П. Исаченко, В.А. Осипова, А.С. Сукомел
“Теплопередача” М.: Энергия 1969 - Френкель Я.И. Кинетическая теория жидкостей. Л.,
1975 - Крокстон К. А. Физика жидкого состояния. М., 1987
- П.М. Куреннова “ Русский Народный Лечебник”.
- Буздин А., Сорокин В., Кипение жидкостей.
Журнал “Квант”, N6,1987 - https://aquaterm.ur.ru
- www.buyda.ru/Danses/boiling.htm
- kvant@mccme.ru
- https://www.shaku-wind.ru/another_tea.html
Источник
