Теплоизолированный сосуд разделен теплопроводной
Здравствуйте, уважаемый слушатель. Предлагаю Вам 2 занятие по теме: «Молекулярная Кинетическая Теория МКТ». Ирина Станиславовна. Дополнительную информацию по данному вопросу вы можете найти на сайтах
www. school-collection. *****,
https://*****/posters/spectrum/light,
https://www. *****.
https://*****/
В литературе:
1.ЕГЭ 2009.Физика. Федеральный банк экзаменационных материалов/Авт.-сост. , .- М.:Эксмо,2009.-368с.
2. ЕГЭ 2009.Физика. репетитор/ , .- М.:Эксмо,2009.-432с.- (ЕГЭ. Репетитор).
3. ЕГЭ-2012. Физика: типовые экзаменационные варианты : 32 варианта: 9-11 классы / под ред. .- М. : Национальное образование, 201с.- (ЕГЭ. ФИПИ-школе).
Основные положения МКТ:
1. все макроскопические тела состоят из частиц: атомов и молекул.
2. Частицы вещества взаимодействуют между собой: притягиваются и отталкиваются.
3. Частицы вещества находятся в непрерывном хаотичном движении.
Колличество вещества равно отношению числа частиц в теле (атомов – в атомарном веществе, молекул – в молекулярном) к числу молекул в колличестве вещества, равном 1 моль, т. е. к числу Авогадро:
Если массу одной молекулы вещества обозначить черезm0, то малярную массу можно трактовать как массу NA молекул:
Масса m любого колличества вещества, содержащего N молекул, равна:
Откуда колличество вещества равно:
Аморфное тело не имеет упорядоченной (кристаллической) структуры молекул, сохраняет форму только благодаря затрудненности перемещение молекул относительно друг друга.
При нагревании аморфное тело размягчаеться постепенно. Механические, тепловые и другие свойства одинаковы вдоль всех направлений такого тела.
Идеальный газ. Идеальный газ – модель состояния вещества, в которой относительно его молекул принимаются следующие предположения:
1. число молекул в газе велико: N>>1
2. молекулы не взаимодействуют друг с другом.
3. молекулы газа совершают неупорядоченное, хаотичное движение.
Основное уравнение молекулярно – кинетической теории идеального газа. Это уравнение связывает макропараметры системы – давление p и концентрацию молекул
Уравнение Менделеева – Клайперона,
Название процесса | Формулировка закона | Графики | Физический смысл |
Кто открыл Дата | Для газа данной массы произведение давления газа на его объём постоянно, если температура газа не меняется |
| ,т. к |
Закон Бойля Мариотта 17 век Изотермический | |||
Закон Гей-Люссака 1802 г. Изобарный | Для газа данной массы отношение объёма к температуре постоянно при неизменном давлении |
| Увеличиваются силы отталкивания между частицами, а следовательно расстояние между частицами увеличивается |
Закон Шарля 1787 г. Изохорный |
|
Название процесса | Формулировка закона | Графики | Физический смысл |
Газовые законы.
Примеры решения задач.
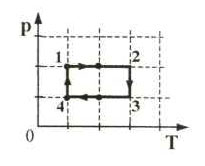
1.В сосуде, закрытом поршнем, находится идеальный газ. График зависимости давления газа от температуры при изменениях его состояния представлен на рисунке. Какому состоянию газа соответствует наименьшее значение объема?
1) А 3) С
2) В 4) D
А В С
D
0 T
Если провести изохоры через все точки, то наименьший угол проходит через точку D, следовательно объем наибольший в точке D, наименьший в точке А.
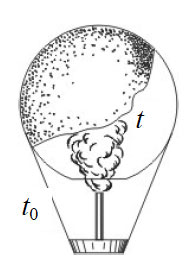
2. воздушный шар объемом 2500 м3 с массой оболочки 400 кг имеет внизу отверстие, через которое воздух в шаре нагревается горелкой. Рассчитайте максимальную массу груза, который может поднять шар, если воздух в нем нагрет до температуры 770С. температура окружающего воздуха 70С, его плотность 1,2 кг/м3. Оболочку шара считать нерастяжимой.
Шар поднимет груз при условии: , где М и m – масса оболочки шара и масса груза, mш – масса воздуха в шаре и – масса такого же по объему воздуха вне шара.
Сокращающее уравнение на g, имеет
При нагревании воздуха в шаре его давление p и объем V не меняются. Следовательно, согласно уравнению Менделеева – Клайпейрона.
, где m- средняя молярная масса воздуха, и – его температуры внутри и вне шара. Отсюда:
,где p- плотность окружающего воздуха;
. Следовательно,
Ответ: m=200 кг
Задача 3
Элементы ответа:
1) Записано уравнение:
2) Получены выражения для
3) Записаны показания приборов:
PA = 746 мм рт. ст. или Па;
PM = 40 мм рт. ст.;
t0 = 450 C
4) Определено давление газа:
мм рт. ст.
5) Выполнен расчет:
(кг/м3)
4 задача.
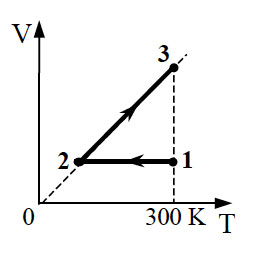
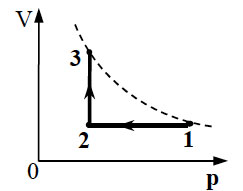
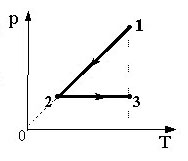
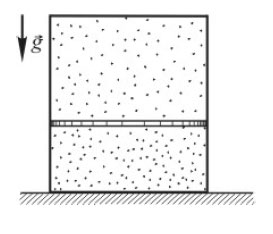
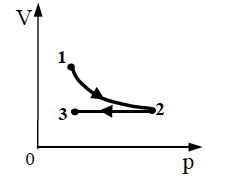
Теплоизолированный сосуд разделен теплопроводной неподвижной перегородкой на две части одинакового объема. В одной части сосуда находится гелий в количестве 2 моль, а в другой – аргон в количестве 2 моль. В начальной момент средняя квадратичная скорость атомов аргона в 2 раза больше скорости атомов гелия. Определите отношение давления гелия к давлению аргона после установления теплового равновесия.
Элементы ответа:
1) После установления теплового равновесия температура газов станет одинаковой и равной Т.
2) Из уравнения Менделеева – Клайпейрона:
. Здесь 2V – объем сосуда.
3) Из уравнений следует ответ:
4) Так как v1=v2, то
5 задача.
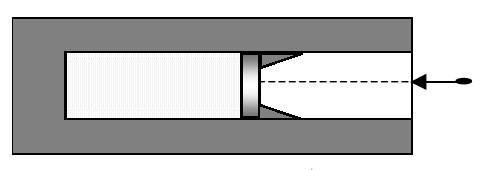
Внутри двух соосных горизонтальных цилиндров сечениями S1 = 2 м2 и S2 = 1 м2 свободно ходят поршни, связанные между собой жестким стержнем. в пространстве между поршнями- вакуум. Первоначально поршни застопорены. Слева от левого поршня в объеме V1= 4м2 находится идеальный газ под давлением р1 = 250 Па, а справа от правого поршня в объеме V2= 2м2 – идеальный газ под давлением р2= 200 Па. Какое давление установиться в газах, когда поршни будут освобождены? Температура системы постоянна.
Обозначим давления и объемы газов слева и справа после установления равновесия через ; и
Условие постоянства длины стержня между поршнями дает:
А условие равновесия системы поршней – равенство сил давления:
Решая эту ситему, получим:
Па; Па
6 задача.
В сосуде объемом V1 находится идеальный одноатомный газ при температуре T1 и давлении р1, в сосуде объемом V2 находится другой идеальный одноатомный газ при температуре T2 и давлении р2. Вентиль В соединяющий сосуды открыли и газы перемешались. Найти температуру установившуюся в сосуде. Сосуды теплонепроницаемы, теплообменом с материалом сосудов можно пренебречь. |
Запишем уравнения состояния для каждого газа и смеси
, (1)
, (2)
Поскольку обмена теплом с окружающей средой нет, то внутренняя энергия смеси равна сумме внутренних энергий смешиваемых газов. Учитывая, что оба газа одноатомные, а следовательно их молярные теплоёмкости при постоянном объеме, а также молярная теплоёмкость смеси, равны, выражение для внутренней энергии смеси можно записать следующим образом
(3)
Из (3) находим выражение для
(4)
Из (1)–(2) выражаем ν1 и ν2. После подстановки в (4) получим искомое выражение для температуры смеси
Задачи для самостоятельного решения.
1 задача.
Воздушный шар с газонепроницаемой оболочкой массой 400 кг заполнен гелием. Он может удерживать в воздухе на высоте, где температура воздуха 170 С, а давление 105 Па, груз массой 225 кг. Какова масса гелия в оболочке шара? Считать, что оболочка шара не оказывает сопротивления изменению объема шара.
2 задача.
В горизонтальной трубке постоянного сечения, запаянного с одного конца, помещен столбик ртути длиной 15 см, который отделяет воздух в трубке от атмосферы. Трубку расположили вертикально запаянным концом вниз и нагрели на 60 К. При этом объем, занимаемым воздухом, не изменился. Давление атмосферы в лаборатории – 750мм. рт. ст.. Какова температура воздуха в лаборатории?
3 задача.
В сосуде постоянного объема находится идеальный газ, массу которого изменяют. На диаграмме (см. рис.) показан процесс изменения состояния газа. В какой из точек диаграммы масса газа наибольшая.
1) А 3) С
2) В 4) D
P
A D
B C
O T
4 задача.
При какой температуре плотность идеального газа будет в 1,5 раза больше его плотности при температуре Т= 402 К, если давление газа постоянно? Ответ выразите в кельвинах (К), округлив до целых чисел.
5 задача.
Воздушный шар объемом 2500 м с массой оболочки 400 кг имеет внизу отверстие, через которое воздух в шаре нагревается горелкой. До какой минимальной температуры нужно нагреть воздух в шаре, чтобы шар взлетел вместе с грузом (корзиной и воздухоплавателем) массой 200 кг? Температура окружающего воздуха 70С, его плотность 1,2 кг/м3. Оболочку шара считать нерастяжимой.
Источник

ТОП 10:
| А 1 | В левой половине сосуда находится 1020 молекул газа, а в правой половине молекул. Сколько примерно молекул окажется в левой половине сосуда через длительное время после того, как уберут перегородку между двумя половинами сосуда (см. рисунок)? |
| 1) 2)3) 4) | |
| С 2 | Теплоизолированный сосуд объемом разделен пористой перегородкой на 2 равные части. Атомы гелия могут свободно проникать через поры в перегородке, а атомы аргона – нет. В начальный момент в одной части сосуда находится моль гелия, а в другой моль аргона. Температура гелия равна , а аргона . Определите температуру гелия после установления равновесия в системе. |
| С 3 | Теплоизолированный цилиндр разделён теплопроводным поршнем на две части. В одной части цилиндра находится гелий, а в другой – аргон. В начальный момент температура гелия равна 300 К, а аргона –900 К; объёмы, занимаемые газами, одинаковы, а поршень находится в равновесии. Поршень медленно перемещается без трения. Теплоёмкость поршня и цилиндра пренебрежимо мала. Чему равно отношение внутренней энергии гелия после установления теплового равновесия к его энергии в начальный момент? |
| С 4 | Теплоизолированный сосуд объемом V = 2 м3 разделён теплоизолирующей перегородкой на две равные части. В одной части сосуда находится 2 моль He, а в другой – такое же количество моль Ar. Температура гелия Т1 = 300 К, а температура аргона Т2 = 600 К. Определите парциальное давление аргона в сосуде после удаления перегородки. |
| С 5 | Теплоизолированный сосуд объемом разделён пористой перегородкой на 2 равные части. Атомы гелия могут свободно проникать через поры в перегородке, а атомы аргона – нет. В начальный момент в одной части сосуда находится гелий массой , а в другой аргон массой . Средняя квадратичная скорость атомов гелия равна средней квадратичной скорости атомов аргона и составляет . Определите температуру гелий-аргоновой смеси после установления равновесия в системе. Молярная масса гелия 0,004 кг/моль, а аргона 0,04 кг/моль. |
| С 6 | Теплоизолированный сосуд объемом разделён пористой перегородкой на 2 равные части. Атомы гелия могут свободно проникать через поры в перегородке, а атомы аргона – нет. В начальный момент в одной части сосуда находится гелий массой , а в другой аргон массой . Средняя квадратичная скорость атомов гелия равна средней квадратичной скорости атомов аргона и составляет . Определите температуру гелий-аргоновой смеси после установления равновесия в системе. Молярная масса гелия 0,004 кг/моль, а аргона 0,04 кг/моль. |
| С 7 | Теплоизолированный сосуд разделён теплопроводной неподвижной перегородкой на две части одинакового объема. В одной части находится моль гелия, а в другой – моль аргона. В начальный момент времени средняя квадратичная скорость атомов аргона в 2 раза больше средней квадратичной скорости атомов гелия. Определите отношение давления гелия к давлению аргона после установления теплового равновесия. Молярная масса гелия 0,004 кг/моль, а аргона 0,04 кг/моль. |
| С 8 | Теплоизолированный сосуд объемом разделён перегородкой на две равные части. В одной части сосуда находится гелий массой , а в другой аргон массой . Средняя квадратичная скорость атомов гелия равна средней квадратичной скорости атомов аргона и составляет . Определите парциальное давление гелия после удаления перегородки. Молярная масса гелия 0,004 кг/моль, а аргона 0,04 кг/моль. |
Источник
Задачи из ДЕМОВАРИАНТОВ (с решениями)
1. Воздушный шар, оболочка
которого имеет массу М = 145 кг и объем V =
230 м3, наполняется горячим воздухом при нормальном
атмосферном давлении и температуре окружающего воздуха tо
= 0оС. Какую минимальную температуру t должен
иметь воздух внутри оболочки, чтобы шар начал подниматься? Оболочка
шара нерастяжима и имеет в нижней части небольшое отверстие.
Образец возможного решения
2. Воздушный
шар с газонепроницаемой оболочкой массой 400 кг заполнен гелием.
Он может удерживать в воздухе на высоте, где температура воздуха
17оС, а давление 105 Па, груз массой 225
кг. Какова масса гелия в оболочке шара? Считать, что оболочка
шара не оказывает сопротивления изменению объема шара.
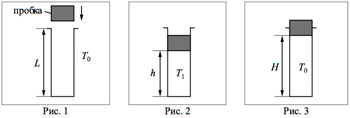
Образец возможного решения2*. В камере, заполненной азотом, при температуре T = 300 К находится открытый цилиндрический сосуд (см. рис. 1). Высота сосуда L = 50 см. Сосуд плотно закрывают цилиндрической пробкой и охлаждают до температуры T1. В результате расстояние от дна сосуда до низа пробки становится равным h = 40 см (см. рис. 2). Затем сосуд нагревают до первоначальной температуры T0. Расстояние от дна сосуда до низа пробки при этой температуре становится равным H = 46 см (см. рис. 3). Чему равна температура T1? Величину силы трения между пробкой и стенками сосуда считать одинаковой при движении пробки вниз и вверх. Массой пробки пренебречь. Давление азота в камере во время эксперимента поддерживается постоянным.
Образец возможного решения
3. В медный
стакан калориметра массой 200 г, содержащий 150 г воды, опустили
кусок льда, имевший температуру 0°С. Начальная температура калориметра
с водой 25°С. В момент времени, когда наступит тепловое равновесие,
температура воды и калориметра стала равной 5°С. Рассчитайте массу
льда. Удельная теплоемкость меди 390 Дж/кг•К, удельная теплоемкость
воды 4200 Дж/кг•К, удельная теплота плавления льда 3,35•105
Дж/кг. Потери тепла калориметром считать пренебрежимо малыми.
Образец возможного решения4. Необходимо расплавить лёд массой 0,2 кг,
имеющий температуру 0оС. Выполнима ли эта задача,
если потребляемая мощность нагревательного элемента – 400 Вт,
тепловые потери составляют 30%, а время работы нагревателя не
должно превышать 5 минут?
Образец возможного решения4*. Теплоизолированный горизонтальный сосуд разделён пористой перегородкой на две равные части. В начальный момент в левой части сосуда находится ν = 2 моль гелия, а в правой – такое же количество моль аргона. Атомы гелия могут проникать через перегородку, а для атомов аргона перегородка непроницаема. Температура гелия равна температуре аргона: Т = 300 К. Определите отношение внутренних энергий газов по разные стороны перегородки после установления термодинамического равновесия.
Образец возможного решения4**. Теплоизолированный цилиндр разделён подвижным теплопроводным поршнем на две части. В одной части цилиндра находится гелий, а в другой – аргон. В начальный момент температура гелия равна 300 К, а аргона – 900 К; объёмы, занимаемые газами, одинаковы, а поршень находится в равновесии. Поршень медленно перемещается без трения. Теплоёмкость поршня и цилиндра пренебрежимо мала. Чему равно отношение внутренней энергии гелия после установления теплового равновесия к его энергии в начальный момент?
Образец возможного решения
5. В вакууме
закреплен горизонтальный цилиндр с поршнем. В цилиндре находится
0,1 моль гелия. Поршень удерживается упорами и может скользить
влево вдоль стенок цилиндра без трения. В поршень попадает пуля
массой 10 г, летящая горизонтально со скоростью 400 м/с, и застревает
в нем. Температура гелия в момент остановки поршня в крайнем левом
положении возрастает на 64 К. Какова масса поршня? Считать, что
за время движения поршня газ не успевает обменяться теплом с поршнем
и цилиндром.
Образец возможного решения6. В горизонтальном цилиндрическом сосуде,
закрытом поршнем, находится одноатомный идеальный газ. Первоначальное
давление газа p1 = 4•105
Па. Расстояние от дна сосуда до поршня равно L. Площадь
поперечного сечения поршня S = 25 см2. В
результате медленного нагревания газ получил количество теплоты
Q = 1,65 кДж, а поршень сдвинулся на расстояние x
= 10 см. При движении поршня на него со стороны стенок сосуда
действует сила трения величиной Fтр = 3•103
Н. Найдите L. Считать, что сосуд находится в вакууме.
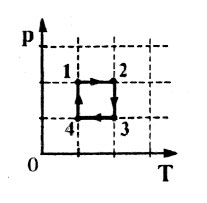
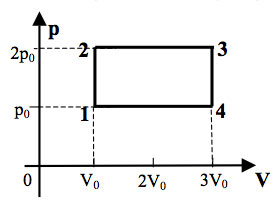
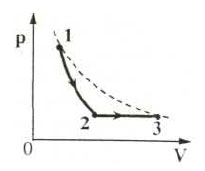
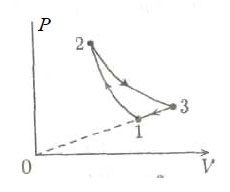
Образец возможного решения7. На pT-диаграмме показан
цикл тепловой машины, у которой рабочим телом является идеальный
газ (см. рисунок). На каком из участков цикла 1 – 2, 2 – 3, 3
– 4, 4 – 1 работа газа наибольшая по модулю?
Образец возможного решения
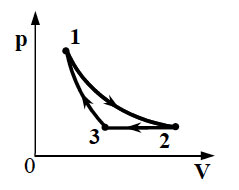
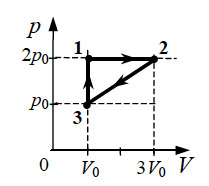
8. 10 моль одноатомного идеального
газа сначала охладили, уменьшив давление в 3 раза, а затем нагрели
до первоначальной температуры 300 К (см. рисунок). Какое количество
теплоты получил газ на участке 2 – 3?
Образец возможного решения
9. 10 моль идеального одноатомного газа охладили,
уменьшив давление в 3 раза. Затем газ нагрели до первоначальной
температуры 300 К (см. рисунок). Какое количество теплоты сообщено
газу на участке 2 – 3?
Образец возможного решения
10. 1 моль идеального одноатомного газа сначала
охладили, а затем нагрели до первоначальной температуры 300
К, увеличив объем газа в 3 раза (см. рисунок). Какое количество
теплоты отдал газ на участке 1 – 2?
Образец возможного решения
10*. Над одноатомным идеальным газом проводится циклический процесс, показанный на рисунке. На участке 1–2 газ совершает работу А12 = 1000 Дж. На адиабате 3–1 внешние силы сжимают газ, совершая работу |A31| = 370 Дж. Количество вещества газа в ходе процесса не меняется. Найдите количество теплоты |Qхол|, отданное газом за цикл холодильнику.
Образец возможного решения
11. Рассчитайте КПД тепловой
машины, использующей в качестве рабочего тела одноатомный идеальный
газ и работающей по циклу, изображенному на рисунке.
Образец возможного решения
Избранные задачи прошлых лет (с ответами)
12. Вертикально расположенный
замкнутый цилиндрический сосуд высотой 50 см разделен подвижным
поршнем весом 110 Н на две части, в каждой из которых содержится
одинаковое количество идеального газа при температуре 361 К. Сколько
молей газа находится в каждой части цилиндра, если поршень находится
на высоте 20 см от дна сосуда? Толщиной поршня пренебречь.
13. В калориметре
находился лед при температуре t1 = – 5 °С.
Какой была масса m1 льда, если после добавления
в калориметр m2 = 4 кг воды, имеющей температуру
t2 = 20 °С, и установления теплового равновесия
температура содержимого калориметра оказалась равной t
= 0 °С, причем в калориметре была только вода?14. Теплоизолированный
цилиндр разделен подвижным теплопроводным поршнем на две части.
В одной части цилиндра находится гелий, а в другой — аргон. В
начальный момент температура гелия равна 300 К, а аргона — 900
К. При этом объемы, занимаемые газами одинаковы. Какую температуру
будут иметь газы в цилиндре после установления теплового равновесия,
если поршень перемещается без трения? Теплоемкостью сосуда и поршня
пренебречь.15. Теплоизолированный
сосуд объемом V = 2 м3 разделен теплопроводящей
перегородкой на две части одинакового объема. В одной части находится
m = 1 кг гелия, а в другой части m = 1 кг аргона.
Средняя квадратичная скорость атомов аргона равна средней квадратичной
скорости атомов гелия и составляет υ = 500 м/с. Рассчитайте
парциальное давление гелия после удаления перегородки.16. Теплоизолированный
сосуд объемом V = 2 м3 разделен пористой перегородкой
на две равные части. В начальный момент в одной части сосуда находится
νHe = 2 моль гелия, а в другой – νAr
= 1 моль аргона. Температура гелия ТHe = 300
К, а температура аргона ТAr = 600 К. Атомы
гелия могут свободно проникать через поры в перегородке, а атомы
аргона – нет. Определите температуру гелия после установления
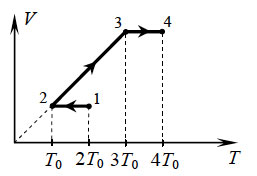
теплового равновесия в системе.17. С одним молем идеального
одноатомного газа совершают процесс 1-2-3-4, показанный на рисунке
в координатах V-Т. Во сколько раз количество теплоты,
полученное газом в процессе 1-2-3-4 больше работы газа в этом
процессе?
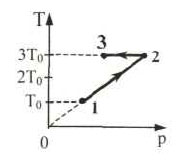
18. Один моль одноатомного
идеального газа совершает процесс 1-2-3 (см. рисунок). На участке
2 – 3 к газу подводят 3 кДж теплоты. Т0 =
100 К. Найдите отношение работы, совершаемой газом в ходе всего
процесса А123, к соответствующему полному
количеству подведенной к нему теплоты Q123.
19. Один моль идеального
одноатомного газа сначала изотермически сжали (Т1
= 300 К). Затем газ изохорно охладили, понизив давление в 3 раза
(см. рисунок). Какое количество теплоты отдал газ на участке 2
– 3?
20. Идеальный одноатомный
газ расширяется сначала адиабатно, а затем изобарно. Конечная
температура газа равна начальной (см. рисунок). За весь процесс
1-2-3 газом совершается работа, равная 5 кДж. Какую работу совершает
газ при адиабатном расширении?
21. На рисунке в координатах
p,T показан цикл тепловой машины, у которой
рабочим телом является идеальный газ. На каком участке цикла работа
газа наименьшая по модулю?
22. Один моль одноатомного
идеального газа совершает цикл, изображенный на pV-диаграмме
(см. рисунок). Участок 1 – 2 –– изотерма, 2 – 3 –– изобара, 3
– 1 –– адиабата. Работа, совершаемая газом за цикл, равна А.
Разность температур в состояниях 1 и 3 составляет ΔТ.
Какую работу совершает газ при изотермическом процессе?
23. Газообразный гелий находится
в цилиндре под подвижным поршнем. Газ сжимают в адиабатическом
процессе, переводя его из состояния 1 в состояние 2 (см. рис.).
Над газом совершается при этом работа сжатия А12
(А12> 0). Затем газ расширяется в изотермическом
процессе 2-3, и, наконец, из состояния 3 газ переводят в состояние
1 в процессе, когда его давление Р прямо пропорционально
объему V. Найти работу А23, которую
совершил газ в процессе изотермического расширения, если во всем
замкнутом цикле 1-2-3-1 он совершил работу А.
24. Температура
гелия увеличилась в k = 3 раза в процессе P2V
= const (Р — давление, V — объем газа), а его
внутренняя энергия изменилась на 100 Дж. Найти: 1) начальный объем
V1 газа; 2) начальное давление P1
газа. Максимальный объем, который занимал газ в процессе нагрева,
равнялся Vmax = 3 л.25. Одноатомный идеальный
газ неизменной массы совершает циклический процесс, показанный
на рисунке. За цикл от нагревателя газ получает количество теплоты
QH = 8 кДж. Чему равна работа газа за цикл?
Ответы к избранным задачам
прошлых лет
Источник



 Изотерма
Изотерма