Толстостенный сосуд в котором нагревают вещества
Посуда химическая лабораторная (п.х.л.) – изделия, изготовленные из стекла, кварца, фарфора и др. материалов, которые применяются
для препаративных и химико-аналитических работ.
Требования, которым должна соответствовать химическая посуда:
- Термоустойчивость, малый коэффициент теплового расширения материала
- Устойчивость к воздействию химических реагентов
- Загрязнения должны легко отмываться
В данной статье мы классифицируем всю химическую посуду на три группы по ее назначению: мерная, немерная и специального применения.
Мерная химическая посуда
Мерная посуда имеет точную градуировку, нагреванию ее не подвергают.
- Пипетки
- Бюретки
- Мерные колбы, мензурки и цилиндры
Пипетки служат для отбора жидкостей (до 100 мл) и газов (от 100 мл)

Применяются для измерения точных объемов, титрования (метод количественного/качественного анализа в аналитической химии)

С помощью мерных колб, мензурок и цилиндров отмеривают и хранят определенные объемы жидкостей.

Немерная химическая посуда (общего назначения)
К такой химической посуде относятся изделия, многие из которых употребляются с нагревом:
пробирки, стаканы, колбы (плоскодонные, круглодонные, конические), реторты.

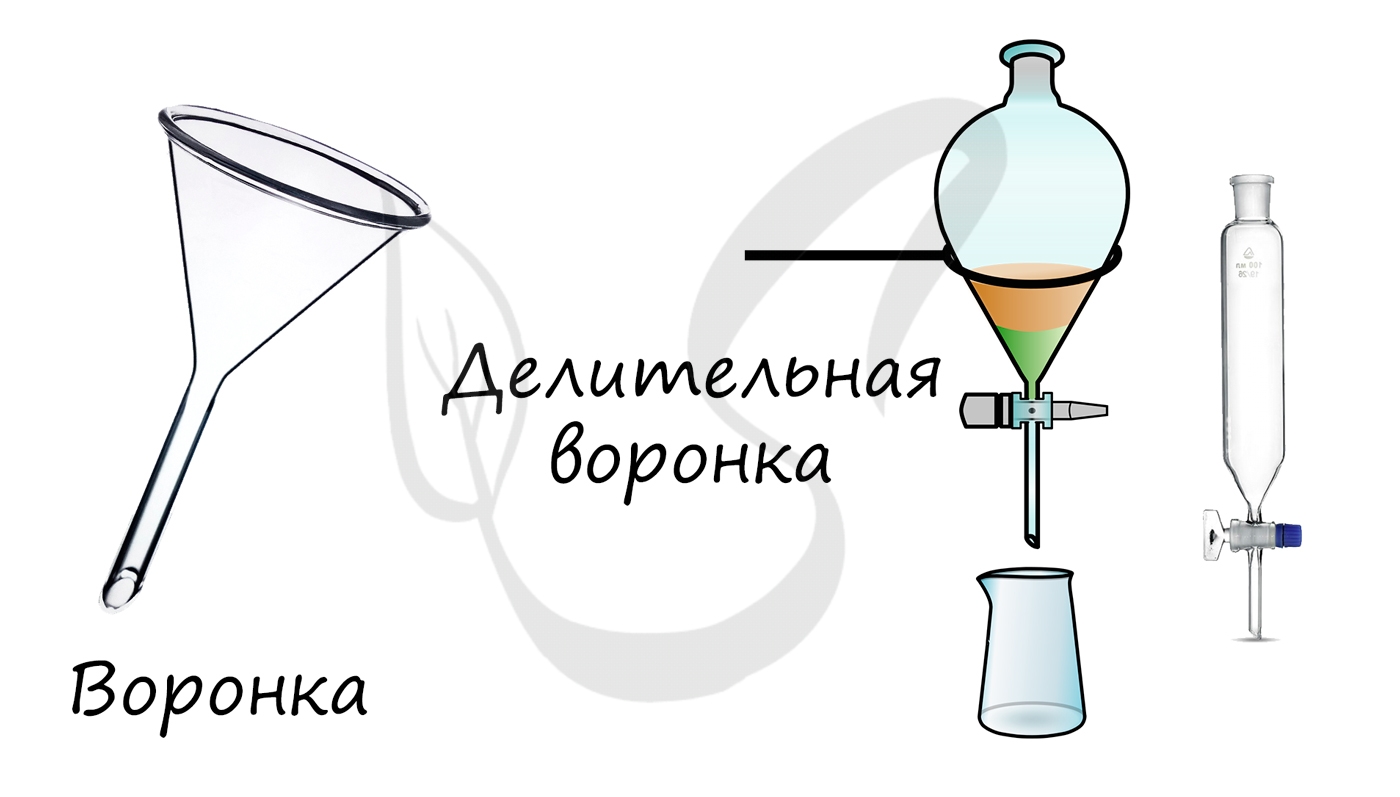
- Воронки, делительные воронки
- Кристаллизатор
- Сифон
- Банки, склянки, бюксы
- Капельница
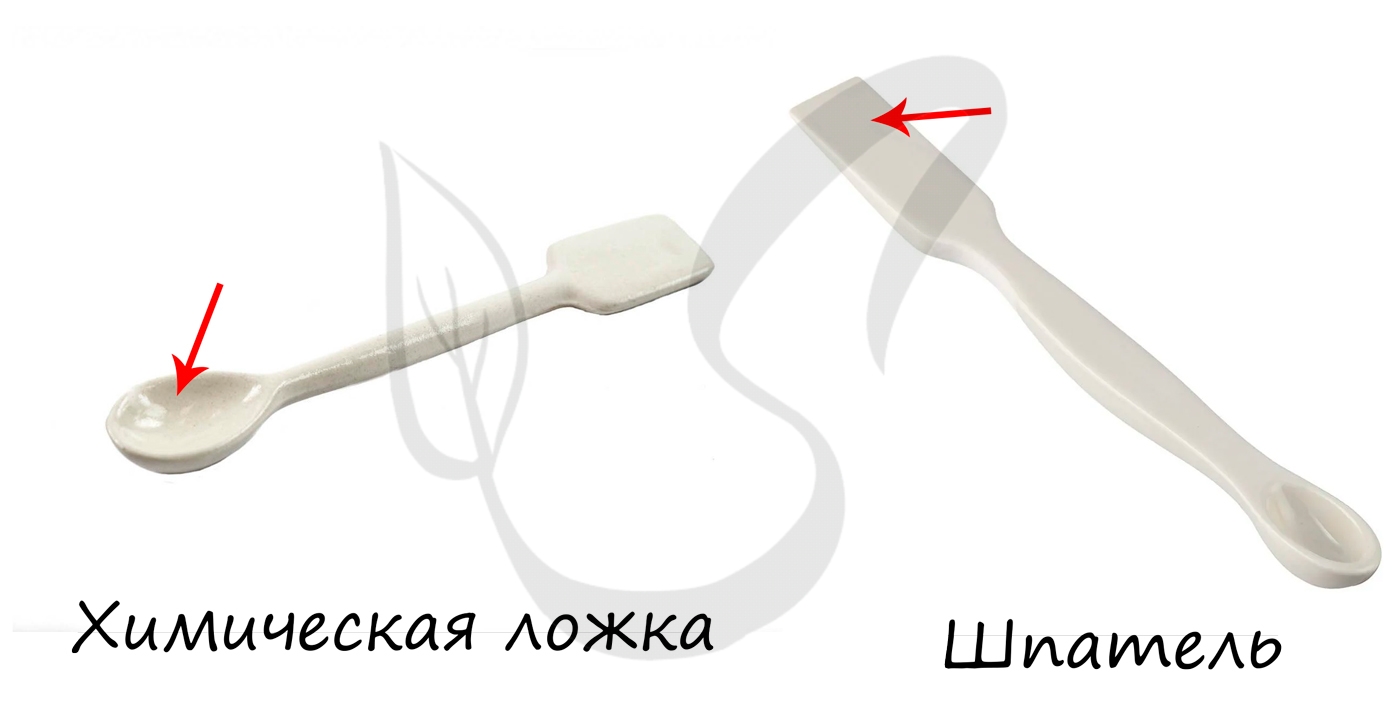
- Химические ложки, шпатели
- Штатив для пробирок
Служат для переливания и фильтрования жидкостей. Делительные воронки применяются для разделения несмешивающихся жидкостей.
Используется для выпаривания растворов и очистки веществ путем перекристаллизации – методе, основанном на различии растворимости вещества
в растворителе при различных температурах.

Сифон химический применяется для безопасного перекачивания жидких сред из бутылей, бочек, канистр. Особенно важен сифон в работе с агрессивными
опасными химическими веществами.

Банки служат для хранения твердых веществ, склянки – для хранения жидких веществ, а также в качестве резервуара, из которого жидкость поступает в другой
раствор, например, в бюретки в ходе титрования.
Бюкс – баночка с притертой пробкой, используется как емкость при исследовании, в ходе которых высушиваются и взвешиваются сыпучие материалы

Химическая капельница применяется для дозирования растворов и индикаторов.

Используются с целью взятия твердых и сыпучих веществ. Могут служить для перемешивания жидкостей.
Применяется для одновременного размещения и закрепления множества пробирок.

Химическая посуда специального назначения
Данная посуда отличается тем, что предназначена для какой-либо одной цели.
- Колбы для дистилляции (колбы Вюрца)
- Колба Бунзена
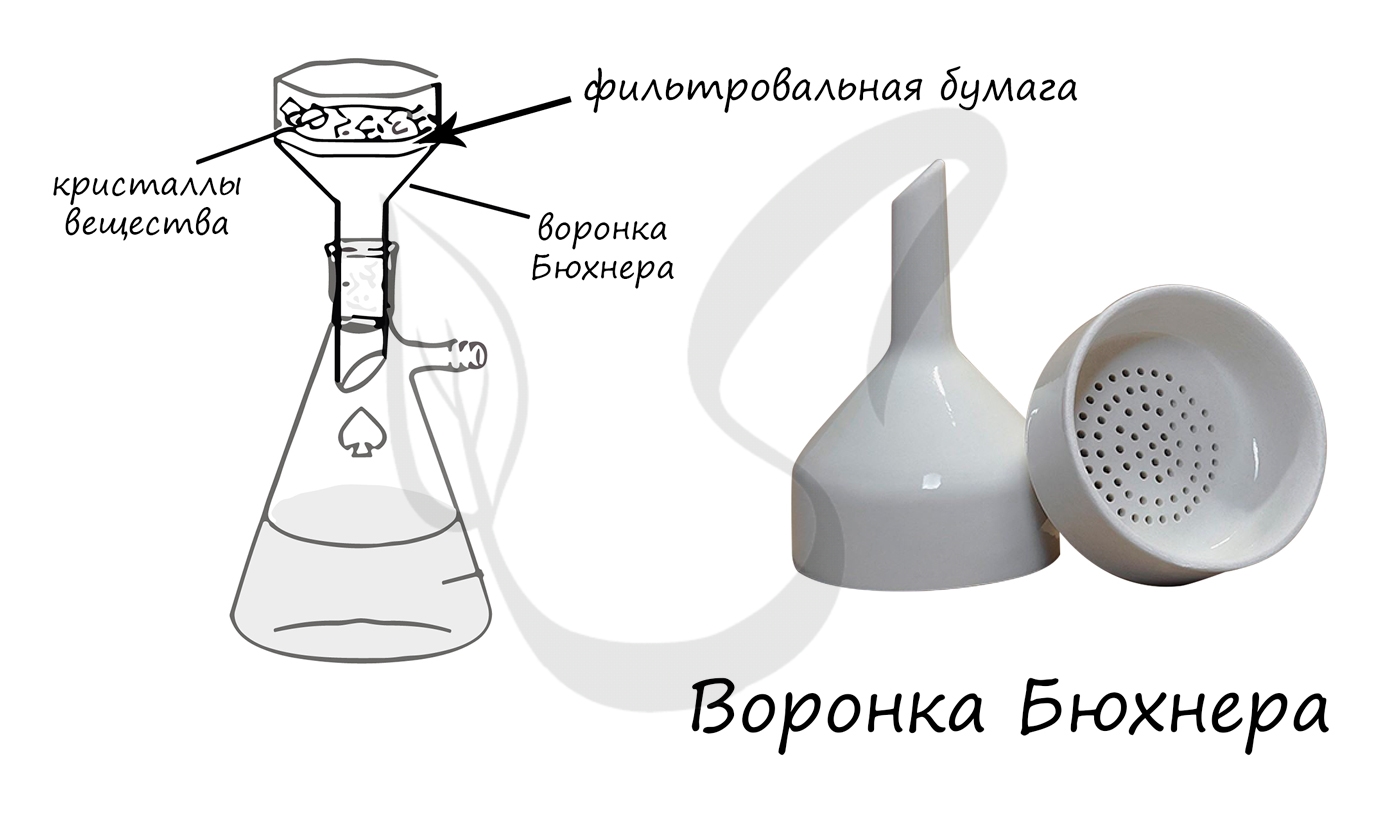
- Воронка Бюхнера
- Воронка (фильтр) Шотта
- Прямой холодильник
- Обратный холодильник
- Аллонж
- Колбы грушевидной формы (колбы Кьельдаля)
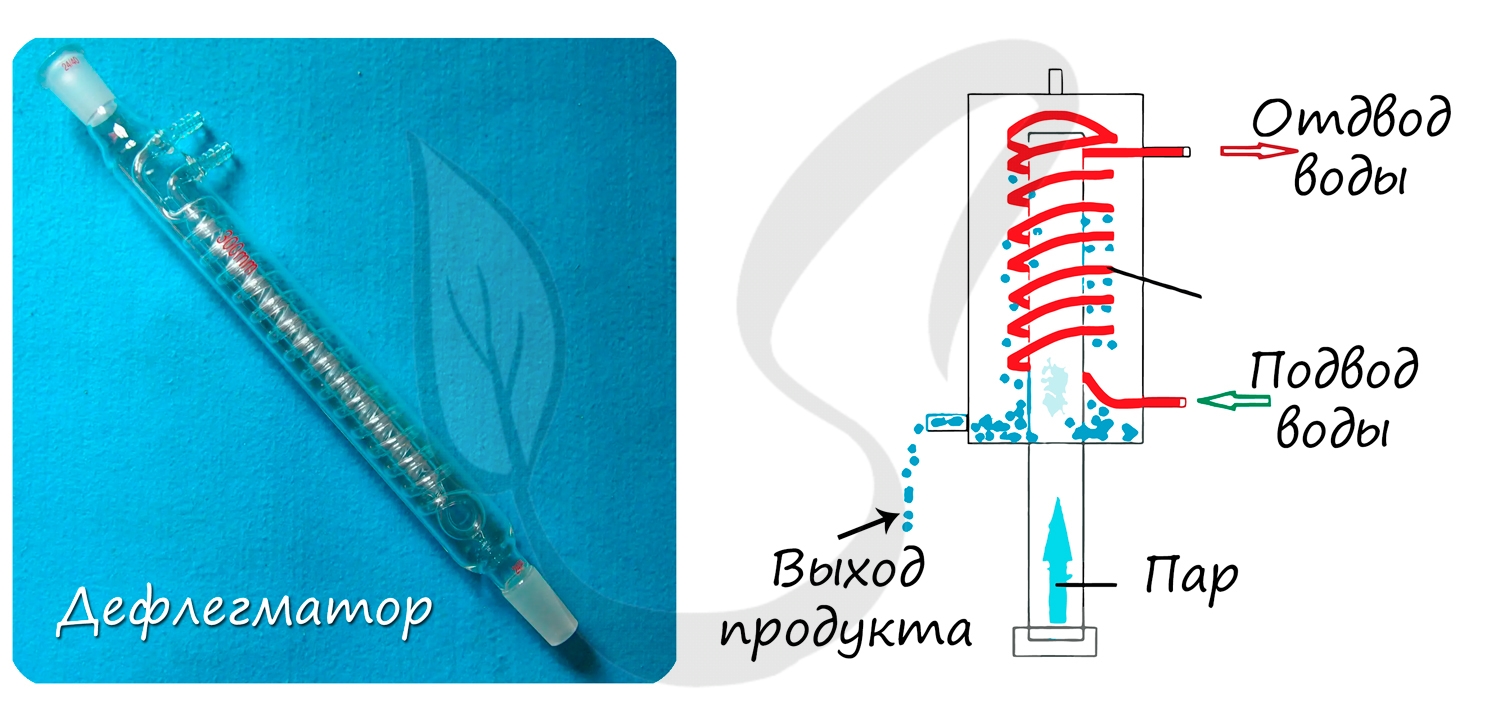
- Дефлегматор
- Эксикатор
- Склянка для промывания газов (склянка Дрекселя)
- Трубки различной формы (хлоркальцевые U-образные трубки)
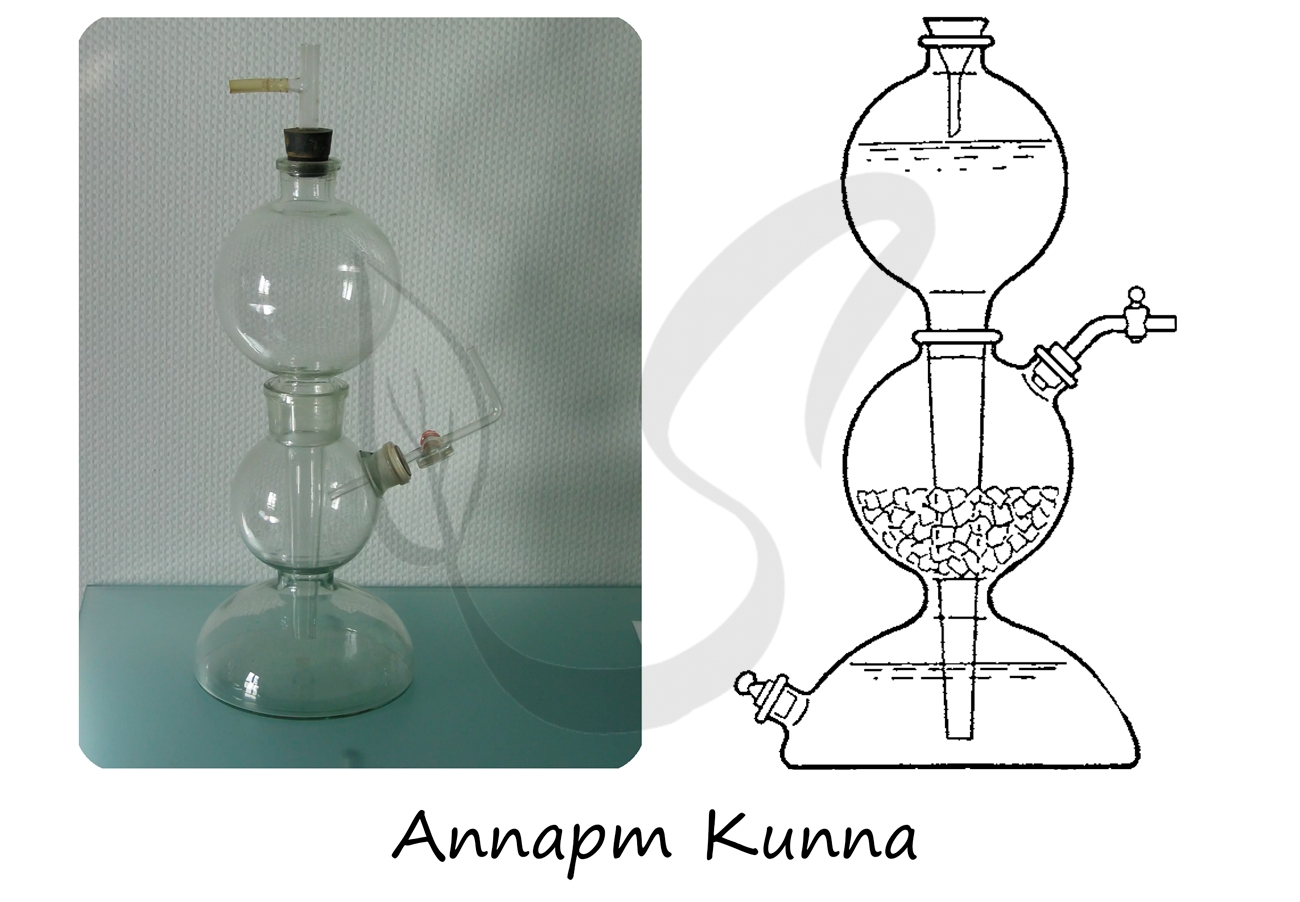
- Аппарт Киппа
- Тигли, чашки для выпаривания
- Ступка с пестиком
- Лодочки
Круглодонная колба с отводом для вставки прямоточного холодильника. Используется для перегонки различных веществ.

Плоскодонная коническая колба, которая применяется для вакуумного фильтрования.

Применяется для фильтрования растворов при помощи фильтровальной бумаги под вакуумом.
Фильтр Шотта представляет собой стеклянную пористую пластинку. Фильтр Шотта используют в ходе вакуумного фильтрования.

Применяется для конденсирования паров и отвода образовавшегося конденсата из системы, сбор конденсата происходит в колбу-приемник.
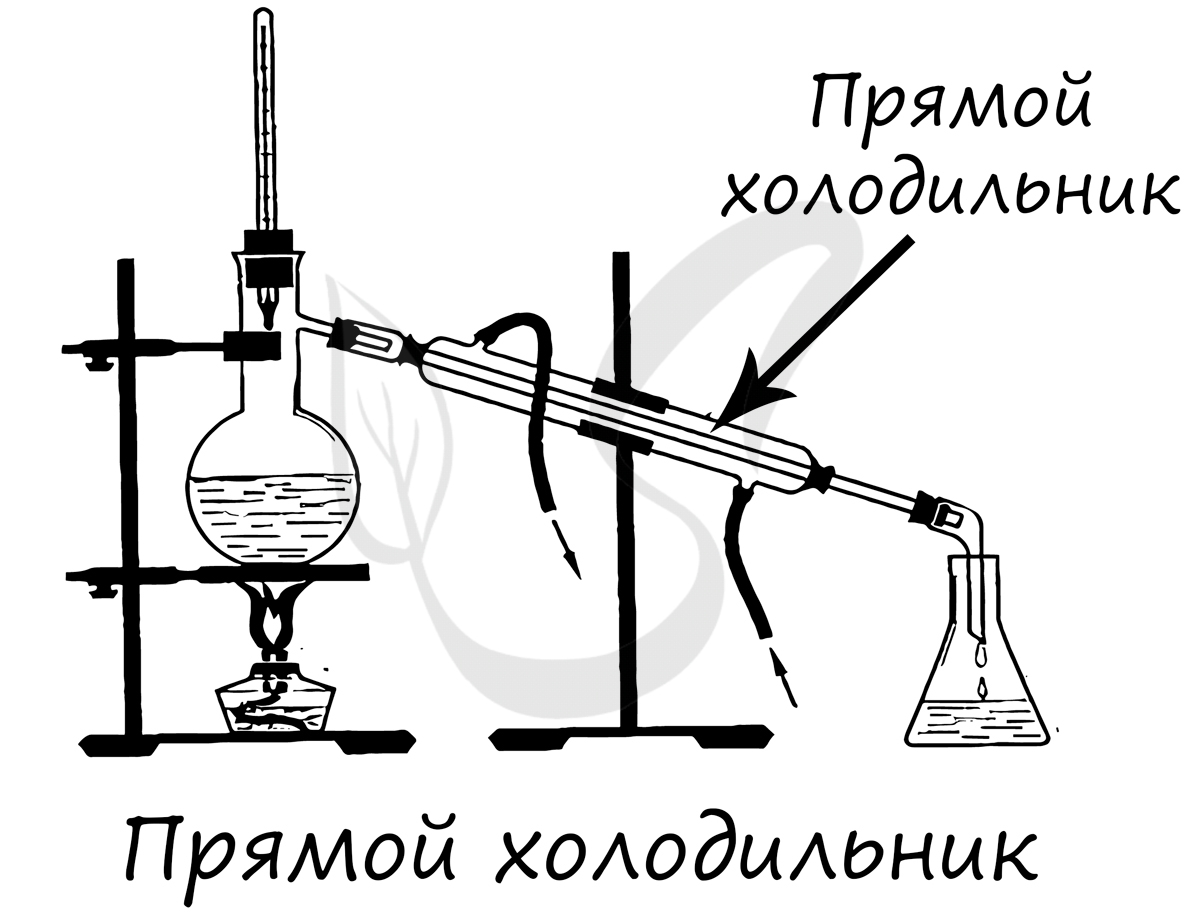
Применяется для конденсирования паров и возврата конденсата в реакционную массу. Обычно устанавливается вертикально.
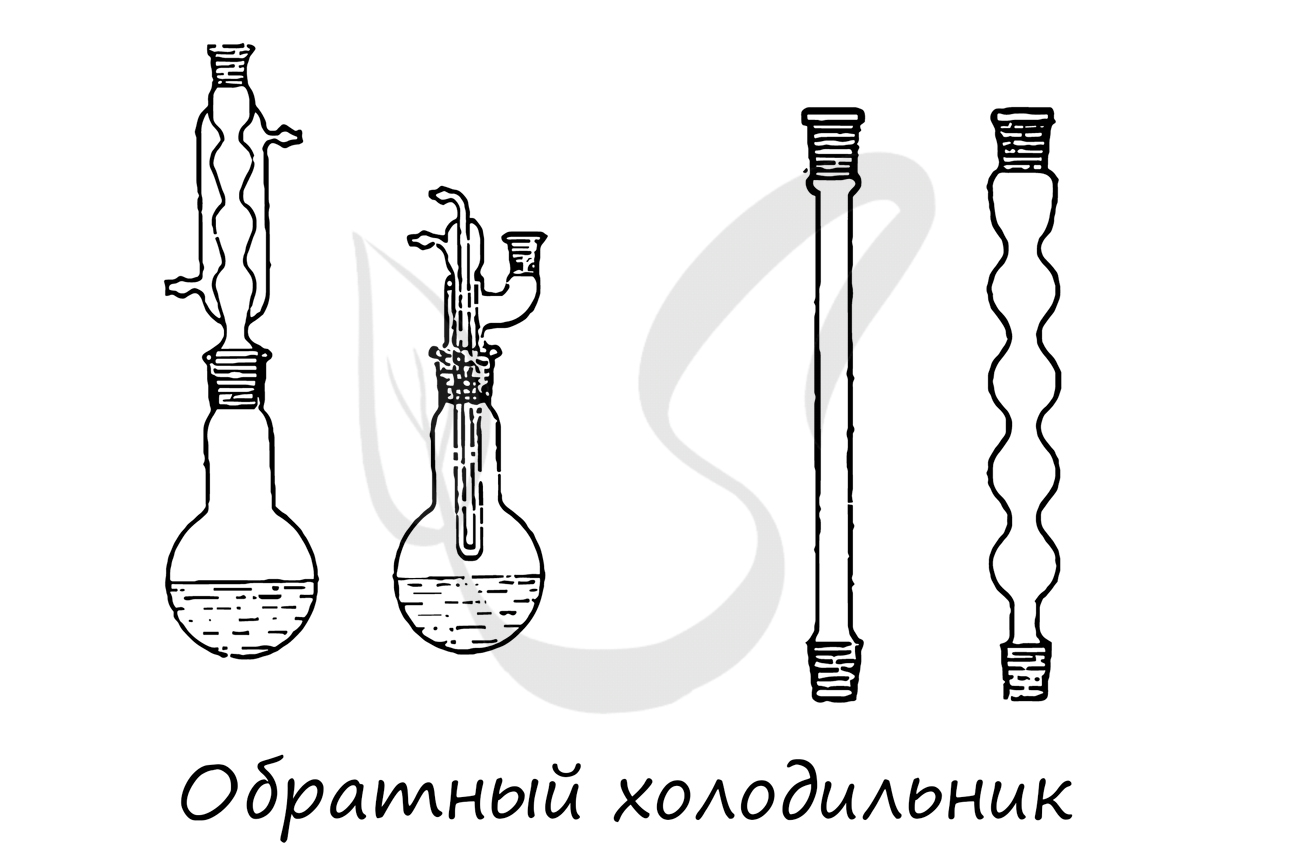
Конструктивный элемент химических приборов, чаще всего используется для соединения холодильника с приемником.
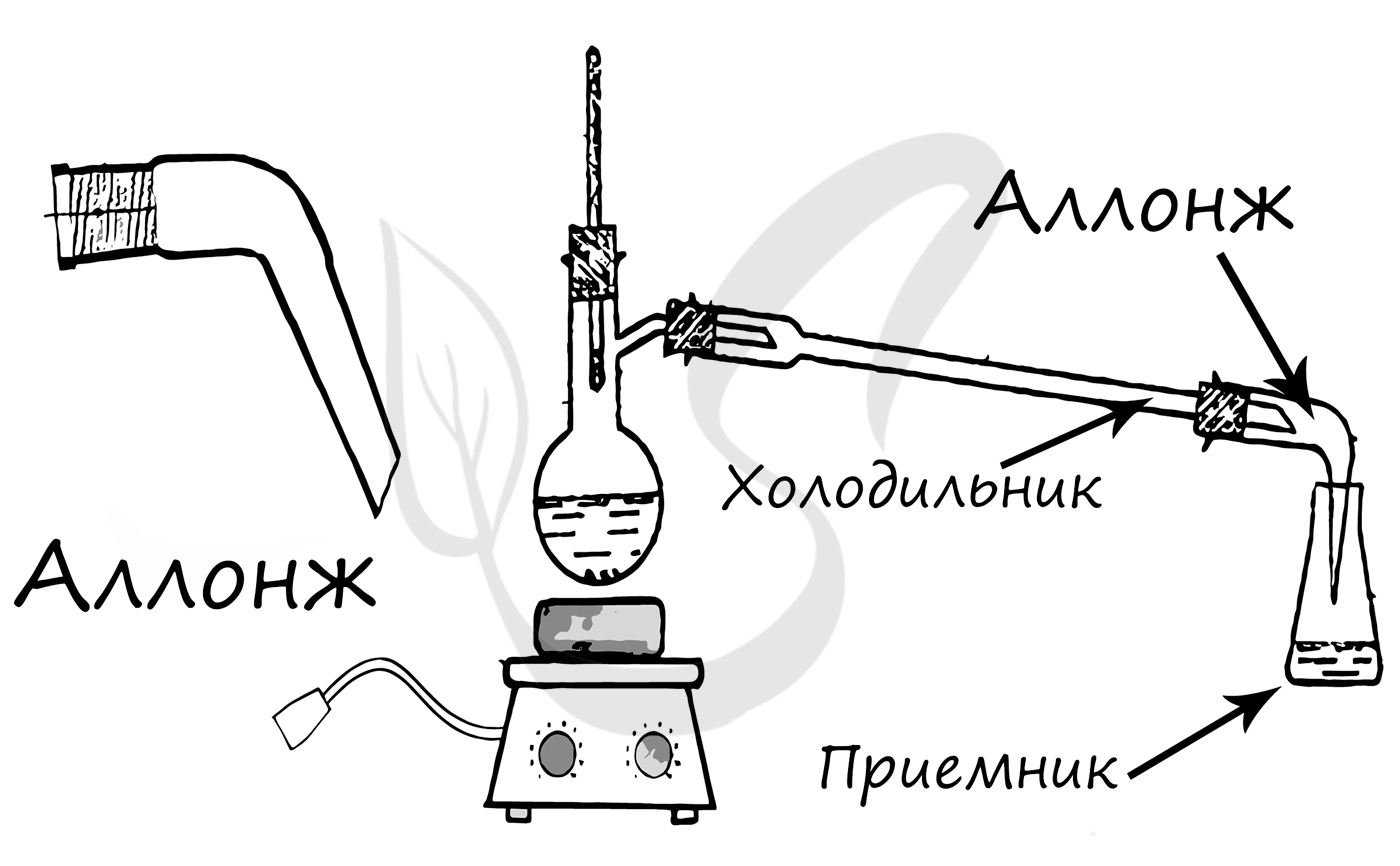
Используется в качестве приемника при перегонке. Одним из предназначений колбы Кьельдаля является
определения азота в веществах по методу Кьельдаля.

Используется для частичной или полной конденсации паров жидкостей, которые разделяют перегонкой или ректификацией (разделение, основанное
на многократной дистилляции.)
Толстостенный стеклянный сосуд, с пришлифованной крышкой, на дно которого помещают влагопоглощающее вещество, в результате чего в
эксикаторе поддерживается влажность воздуха приблизительно равная нулю. Эксикатор используется для высушивания и хранения различных веществ.

Склянка Дрекселя – сосуд, используемый для промывания и очистки газов. В результате пропускания газа через склянку Дрекселя он освобождается
от механических примесей.

Служат для очистки газов от механических примесей. Также хлоркальцевые трубки применяют для предохранения растворов от попадания в них
воды и углекислого газа: с этой целью их заполняют нужным поглотителем.

Применяется для получения газов при действии на твердые вещества растворов кислот и щелочей.

Тигель (от нем. Tiegel — горшок) – термостойкий сосуд-чаша (фарфоровый, глиняный) для нагрева, высушивания, сжигания и обжига различных материалов.
Применяют для сплавления.
Чашки для выпаривания используют для выпаривания (упаривания) растворов.
Применяется для измельчения твердых веществ.

Применяются для прокаливания веществ в печи.

© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Источник
Неделя естественны наук
Неделя естественны наук
Цели проведения:
-повышение интереса обучающихся к предметам естественно-математического цикла, познанию действительности и самого себя, развитие индивидуальных, творческих и интеллектуальных способностей
Задачи:
– Привлечь всех учащихся для организации и проведения недели естественно-математических дисциплин.
– Создать условия для проявления и дальнейшего развития индивидуальных творческих и интеллектуальных способностей каждого ученика.
– Провести мероприятия, содействующие развитию познавательной деятельности учащихся, формированию творческих способностей, расширению знаний по математике, информатике, физике, химии, биологии.
– Организовать самостоятельную, индивидуальную, коллективную и практическую деятельность учащихся, содействуя воспитанию коллективизма и товарищества, культуры чувств.
– Поддержать у детей состояние активной заинтересованности овладением новыми, более глубокими знаниями по предметам естественно-математического цикла.
План проведения недели естественных наук
Дата | Мероприятие | Учитель |
14.03. (понедель-ник) | 1.Открытие Недели естественных наук. Общешкольная линейка. Открытие сменного стенда « В мире наук». Объявление конкурсов. ЧВМ в 6 классе. | |
15.03. (вторник) | Конкурс грамотности 5-9кл. Весёлые перемены. «Смотр знаний» пробное ОГЭ по математике 9кл. Игра « Эрудит» 8кл. « В мире занимательной химии» 7кл. | |
16.03. (среда) | Смена стенда « Конкурс ребусов и кроссвордов». Занимательные перемены. Выставка лучших тетрадей по математике, биологии, физике, химии. 1-9кл. | |
17.03. (четверг) | Международная олимпиада « Кенгуру» 2-9кл. Выставка аппликаций и рисунков на тему по математике, физике, химии, биологии, поделок из пластилина и др. материала. 1-9кл Занимательные перемены. | |
18.03. (пятница) | « Смотр знаний» пробное ОГЭ по биологии 9кл. Оформление стенда « Галерея великих ученых». Общешкольное мероприятие « Поезд знаний» 5-9кл. ( 7 урок) | Кл. рук. |
19.03. (суббота) | « Интеллектуальный марафон» 5кл. Подведение итогов. Сдача ответов викторин, конкурсов по предметам. |
Цель:Расширение знаний в области различных наук, вовлечение учащихся в научную деятельность, стимулирование школьников принимать участие в школьных проектах, в научных исследованиях.
Задачи:
– Углубление знаний о классификации научных ветвей;
– Систематизирование знаний предметного цикла;
– Воспитание у учащихся стремления к новым знаниям;
– Создать условия для формирования школьной научной среды.
Действующие лица: Ведущий, математика, физика, химия, биология.
Все действующие лица одеты в костюмы (желательно мантии) соответствующие наукам. У всех детей в руках некая атрибутика, а на головах одеты кафедралки (квадратная академическая шапочка) определенного цвета:
Физика – золотой цвет;
Химия – зелёный цвет;
Математика – желтый цвет;
Биология – салатный цвет;.
Ход мероприятия
Ведущий
Все, что есть в этой жизни полезного,
Уникального, интересного,
Все придумано, братцы, наукой
И тем, кто с ней связан, совсем не до скуки.
В суетном мире, сквозь пространство, годы,
Для человечества другого нет пути:
Секреты отнимать и тайны у природы,
Искать, учиться и вперед идти!
Идёт парад миров научных,
Мечта учёных докторов,
Где мир наш дом, и он изучен
Но знаем ли мы все о нем?
Физика
Знаете, как говорят в народе?
Физика – царица всех наук о природе!
Физика много разделов включает,
Каждый вопросы свои изучает.
Например, проводов «величество»
Изучает раздел «Электричество».
«Механика» все изучает движения,
Действия сил, точки их приложения.
Тепловых процессов динамику
Изучает «Термодинамика».
Химия
В жизни химия нужна,
Как предмет она важна.
И учить ее прилежно
Мы должны от А до Я.
Что мы носим, что едим,
Чем здоровью мы вредим?
Как кислоты выливать,
Чтобы что-то не взорвать?
На все вопросы эти
Нам химия ответит!
Математика
Вперед науку двигают ученые,
И опытом, и знаньем окрыленные,
Но впереди идет любого практика
Прекрасная наука – математика.
Ты нам, математика, даёшь
Для победы трудностей закалку,
Учится с тобою молодёжь
Развивать и волю и смекалку.
Биология
Биология наука о Земной всей красоте…
О букашках, насекомых о лесах всех на Земле…
То наука о прекрасном, что нам Бог всем подарил…
Ведь не зря он всю Планету, красотою наделил…
Сохранит и приумножит всё живое на Земле…
Всё изучит и поможет выжить в не простой борьбе…
Ведь законы всей Вселенной не отменишь, не сотрёшь…
Выживает там сильнейший, если слабый то умрешь…
Ведущий
Всё в нашей жизни закономерно,
Всё очень точно, а не примерно.
Логика жизни состоит в том,
С каким багажом мы на Землю идём.
От простого к сложному,
От невозможного к возможному –
Человек – частичка Мироздания,
Он должен выполнять своё задание.
Науки стоит развивать
Чтобы природу лучше знать!
Эта фраза и станет девизом нашей недели науки.
Парад наук объявляется открытым!



Науки стоит развивать
чтобы природу лучше знать!
Занимательные химические загадки.
1.Гость из космоса пришел, в воздухе приют себе нашел.
2. В доме выше всех живем, вдвоем тепло и свет даем.
3. Он безжизненный зовется, но жизнь без него не создается.
4. Красив в кристаллах и парах, на детей наводит страх.
5. Из горы кусочек вынули, в деревянный ствол задвинули.
6. Гордиться уголек невзрачным негорючим братом, и братом прозрачным.
7. Прокаленный уголек дышать пожарнику помог.
8. Белый воздуха боится, покраснел чтоб сохраниться.
9. Какой газ утверждает, что он – это не он.
10. Какой неметалл является лесом.
“Все мы связываем с химической наукой прогресс в познании окружающего мира, новые методы его перестройки и усовершенствования. И не может быть в наши дни специалиста, который мог бы обойтись без знания химии.”
()
Химии никоим образом научиться невозможно, не видав самой практики и не принимаясь за химические операции».
()
Ближайший предмет химии составляет изучение однородных веществ, из сложения которых составлены все тела мира, превращений их друг в друга и явлений, сопровождающих такие превращения.
(Дмитрий Менделеев)
О, химия – ты такова,
Что без тебя нам – грош цена!
И знаю, все твои пути
К успеху могут привести!
Великая, могучая, красивая,
Всегда ты будешь справедливая!
И бром, и иод, и водород,
И осмий, радий, кислород,
Сульфат, хлорид, бромид, фосфат –
Ты самый лучший химикат!
О, Менделеев, как ты мог
Так поздно показать нам всем,
Что химию – не заменить ничем!
Тут серебро и водород,
Тут натрий, ртуть и кислород,
Вы человека исцелите,
А, если надо, и казните!
Физика – строение атома
1.Заряд протона…
2.Атом состоит из…
3.Ядро состоит из…
4.Атом, какого элемента самый легкий?
5.Заряд электрона …
6.Элемент с зарядом атома +6
7.Число электронов в атоме углерода…
Химия – химические свойства веществ
1.Щелочи и кислоты можно распознать с помощью…
2.При взаимодействии вещества с кислородом образуются …
3.Реакции, протекающие между кислотами и основаниями с образованием воды и соли называются…
4.Назовите любые три признака химической реакции
5.К какому классу веществ относятся: хлорид натрия, сульфат меди, карбонат кальция?
6.Степень окисления натрия в соединениях
7.Для прекращения реакции горения необходимо…(на выбор: накрыть брезентом, засыпать песком, залить водой, прекратить доступ воздуха)

1. Признаки, по которым одни вещества отличаются от других.
2. Явления, в результате которых из одних веществ образуются другие.
3. Вещества, состоящие из одинаковых структурных единиц.
4. Вещество, образованное атомами разных элементов.
5. Разновидность атомов с определённым положительным зарядом ядра.
6. Наука, которая изучает состав, строение и свойства веществ, их взаимные превращения и способы управления этими превращениями.
7. Совокупность структурных частиц, которые обладают определёнными свойствами.
8. Запись с помощью химических формул и численных коэффициентов, показывающая в каких количественных соотношениях взаимодействуют вещества и образуются продукты реакции.
9. Знаки химических элементов и числовых индексов показывающие состав веществ.
10. Вещество, образованное атомами одного химического элемента.
11. Системы, состоящие из нескольких веществ, не изменяющих в результате смешивания своих физических и химических свойств.
12. Явления, при которых состав участвующих веществ сохраняется.

У каждого элемента есть свое название, свой символ и произношение. Необходимо ответить, какое произношение соответствует элементам списка, и вписать это слово в сетку кроссворда.
1. Ртуть
2. Медь
3. Олово
4. Кремний
5. Золото
6. Серебро
7. Железо
8. Мышьяк
9. Свинец
КРОССВОРД «ЛАБОРАТОРНОЕ ОБОРУДОВАНИЕ»

По горизонтали:
4. Устройство для обжима пробок, 5. Прибор из стекла для хранения и сушки веществ. 7. Толстостенный сосуд, в котором нагревают вещества. 9. Приспособление для переливания жидкости. 11. Материал, из которого изготовлена лабораторная посуда. 15. Замы-кательное устройство делительной воронки. 16. Насадка на конец холодильника. 18. Приспособление для изготовления отверстий в пробках. 21. Деталь спиртовки. 22. Стеклянная посуда для проведения эксперимента. 28. Мерный цилиндр. 29. Приспособление для
закрывания емкостей с реактивами. 30. Прибор для очистки осадка. 31. Прибор для нагревания легковоспламеняющихся веществ.
По вертикали: 1. Нагревательный прибор. 2, Емкость фарфоровая для выпаривания. 3. Прибор для получения озона. 5. Нагревательный прибор. 6. Химическая посуда цилиндрической формы. 8. Химическая посуда округлой формы. 10. Прибор для титрования. 12. Приспособление для перекрывания хода газа в резиновой трубке. 13. Прибор для перегонки воды. 14. Приспособление для резания веществ. 17. Емкость для перегонки воды. 19. Газовый нагревательный прибор. 20. Приспособление для отбирания и перекладывания твердых веществ. 23. Фарфоровая формочка для сжигания веществ при анализе.24. Приспособление для отмеривания объемов жидкостей.
25. Деталь для соединения частей прибора. 26. Деталь штатива. 27. Приспособление для измельчения твердых веществ.
КРОССВОРД “ХИМИЯ И ЖИЗНЬ”

По горизонтали:
5. Индикатор, который вырабатывают из некоторых видов лишайников.6. Сырье для получения кислорода в промышленности. 9. Тяжелый шпат. 10. Фунгицид для обработки сельскохозяйственных культур в период вегетации. 11. Топливо будущего.14. Металл, используемый в ядерных реакторах в качестве теплоносителя.15. Составная часть атомного ядра.18. Ароматический углеводород, выделяемый из продуктов каталитического риформинга бензинов.19. Элемент, входящий в состав молекулы питьевой соды. 23. Латинское название элемента, входящего в состав мазей для лечения кожных заболеваний. 25. Углеводород, получаемый из керосиновых фракций нефти. 26. Аминокислота, входящая в состав пищевых белков. 27. Антисептическое средство, выделяемое из эвкалиптового масла. 28. Сырье для производства азотных удобрений.
По вертикали:
1. Незаменимая аминокислота.2. Черная вязкая масса, остающаяся после отгонки легких и большей части тяжелых фракций из нефти. 3. “Элемент жизни и мысли” (). 4. Русский ученый, первым высказавший мысль о существовании веществ, названных впоследствии витаминами. 7. Металл, входящий в состав молекулы хлорофилла. 8. Ароматический углеводород, применяемый в производстве стирола, фенола, анилина и многих других веществ. 12. Ученый, открывший реакцию получения уксусного альдегида из ацетилена. 13. Основной резервный углевод растений. 16. Фосфорорганический эфир, применяемый для уничтожения эктопаразитов животных. 17. Побочный продукт при производстве целлюлозы. 20. Элементарная частица.21. Соль ртути, сильный яд.
22. Элемент, поддерживающий автоматизм и тонус сердца. 24. Составная часть природного газа.
1. Химические загадки.
Зачитываются стихи-загадки о химических элементах
Стихи-загадки:
1.
А это что за элемент?
В нем изменений нет,
Ты измени в нем только ударенье
Построишь ты сооруженье. (платина)
2.
При Менделееве последним в системе элементов был,
Недавно стал он не последним и исключительным прослыл,
Он от того стал знаменитым, что в нем цепной распад
И оказался вдруг открытым так, как долго в ядрах скрытый склад (уран)
3.
Река на Украине есть,
Долин ее не перечесть,
В ней одного лишь слога нет,
Чтоб получился элемент (Радон)
4.
Он яркой звездой загорается,
Белый и легкий металл,
Он в 13 клетке таблицы
Почетное место занял (алюминий)
5.
Рассеян по земле он повсюду,
Немного есть его в морской воде
Рассказывать не буду, как обнаружен он везде,
Летучий, темный, кристалличный
Он мало растворим в воде,
Раствор спиртовый столь типичный
В аптеке встретится везде (Йод)
6.
Тяжелый, жидкий и пахучий, подвижен, сильно ядовит
Удушлив и весьма летучий сквозь поры пробки он летит
В солях почти везде бесцветен,
Есть в Сакском озере в Крыму,
Лечебным действием замечен и всем известен потому. (Бром)
7.
Белы его соединения, в воде бывает иногда,
Не вызывает то сомненья, что это жесткая вода
В Финляндии и на Урале цветные карбонаты есть его,
А белоснежные в Карраре
Таким в дворцах, большая честь. (Кальций)
8.
Хранят обычно в керосине
И бегает он по воде
Отныне знай – в свободном виде
В при роде нет его нигде.
В солях открыть его возможно,
Желтеет пламя от него
И получить из соли можно
Как Деви, получил его. (Натрий)
9.
Он режется ножом,
В воде газует, выделяя водород
И, исчезая в весе,
В растворе щелочь образует,
Горит лиловым в кислороде,
Находят лишь в соединениях
И в нем нуждаются растения. (Калий)
10.
В воде обычно он хранится,
Свет излучает в темноте,
Искать в природе лучше не трудитесь,
Свободным нет его нигде,
Воспламеняться сам он может,
К тому же сильно ядовит,
Так отвечай без промедленья,
Коль в пятой группе он стоит (Фосфор)
11.
Он нужен всем, когда лишь связан,
А вяжется с большим трудом,
Весь мир живых существ обязан
Ему растительным белком.
Распространен во всех трех царствах,
Освобождается в огне,
Есть он и в красках, и в лекарствах,
Он нужен в мире и в войне (Азот)
12.
В солях бесцветен, безопасен, полезен
Безусловно всем
Становится весьма опасен, когда свободен,
И совсем тогда он ядовит, окрашен,
Может слаться по земле.
Удушлив, казался страшен, как первый газ
Из отравляющих веществ. (Хлор)
13.
Достоин газ тот удивленья,
Его применяют сейчас
Для резки металлов и сталеваренья,
И в доменных разных печах,
Ведет его летчик в небесные дали,
Подводник с собою берет,
Вы верно уже догадались,
Что газ этот (Кислород)
14.
Он тверд, тяжел и тугоплавок
И сталь прекрасную дает,
А от небольших его добавок,
Ржаветь она перестает
Его валентность, нет сомненья,
Бывает шесть лишь иногда
А у его соединений окраска разная всегда (хром)
15.
Бесчисленны его соединения, какие образует он
В них происходят изменения, которым имя легион
Он в чистом виде – черный, мрачный, не плавкий и едва горит
Бывает как кристалл прозрачный, в котором блещет солнца луч. (Углерод)
16.
Везде в нашей жизни привычный,
Металл тот сопутствует нам,
На вид он блестящий и в общем обычный,
Активный и мягкий металл,
Он в войнах нашел примененье
И в сельском хозяйстве, в быту.
Металлом войны, преступленья
Я этот металл назову. (Железо)
17.
Ослепительным пламенем ярким
Как звездочка, чудо горит,
Металл тот и белый и легкий
В двенадцатой клетке стоит
Он в сплавах легчайших, нашел примененье
Как стойкий и легкий металл,
И в деле самолетостроения
Он видное место занял. (Магний)
18.
Прославлен всеми именами
Металл испытанный огнем,
Манил к себе людей веками,
Алхимик жил мечтой о нем!
Но как кумир он свергнут нами,
Уж блеск его нас не манит
Ведь хорошо мы знаем с вами
Не все так ценно, что блестит. (Золото)
19.
Заменит букву “й” на “я”
Увидишь дивные поля,
Узнаешь чудную страну
Скажите элемент мне, ну? (Индий)
20.
Едва ли знаете свободным тот элемент,
Который здесь мы обсуждаем!
Однако помните, он весь, скрывается от наших взоров
В стекле, песке и хрустале!
И без сомненья, вы найдете его повсюду на Земле! (Кремний)
21.
Давно известна человеку,
Она тягуча и красна,
Еще по бронзовому веку
Знакома в сплавах всем она,
С горячей серной кислотою дает нам синий купорос! (Медь)

S Aq C N Si C u O Fe Pb H Sn


1. Число химических связей, которыми данный атом соединен с другими.
2. Цифры стоящие перед формулами веществ в уравнении реакции и показывающие, в каких мольных соотношениях взаимодействуют реагенты и образуются продукты реакции.
3. Единица количества вещества.
4. Взаимодействие атомов, приводящее к образованию молекул или веществ, не имеющих молекулярного строения.
5. Химическая связь между двумя элементами, которая осуществляется за счёт образования общих электронных пар.
6. Масса молекулы, выраженная в атомных единицах массы.
7. Наименьшая частица данного вещества, обладающая его химическими свойствами.
8. Химическая связь, которая осуществляется совокупностью обобществленных валентных электронов в кристаллической решётке металла.
9. Величина, равная отношению массы вещества к количеству вещества.
10. Слабая связь, возникающая между атомом водорода и электроотрицательным элементом, имеющим свободную пару электронов.
11. Электронейтральная частица, состоящая из положительно заряженного ядра и отрицательно заряженных электронов.
12. Химическая связь, возникающая между ионами за счёт электростатического притяжения.
Ответы:
1. Валентность
2. Коэффициенты
3. Моль
4. Связь
5. Ковалентная
6. Молярная
7. Молекула
8. Металлическая
9. Масса
10. Водородная
11. Атом
12. Ионная
СТАНЦИЯ «КЛЕТКА»
1. Прибор микроскоп.
А) Как устроен микроскоп?
Б) Установить изображение микропрепарата «растительная клетка»
– ответить на вопрос: Почему клетка зеленого цвета?(3б)
2. Торс человека.
– показать органы: печень, сердце, пищевод, легкие, почки.
– ответить на вопросы:
А) К какой системе органов относятся?
Б) Какова функция органа?(3б)



Станция «Протон»
1. Даны приборы:
амперметр, вольтметр, реостат, электроскоп.
– Назвать прибор и его назначение.(2б)
2. Собрать электрическую цепь: источник питания, электрическая лампа, ключ, амперметр.(1б)
– Ответить на вопрос:
А) Как соединяется амперметр?(1б)
Б) Измерить напряжение электрической лампы.(1б)



Станция атом




Источник
