Транспозиция магистральных сосудов детей
Транспозиция магистральных сосудов – тяжелая врожденная патология сердца, характеризующаяся нарушением положения главных сосудов: отхождением аорты от правых отделов сердца, а легочной артерии – от левых. Клинические признаки транспозиции магистральных сосудов включают цианоз, одышку, тахикардию, гипотрофию, сердечную недостаточность. Диагностика транспозиции магистральных сосудов основана на данных ФКГ, ЭКГ, рентгенологического исследования органов грудной клетки, катетеризации полостей сердца, вентрикулографии. Методами оперативной коррекции транспозиции магистральных сосудов служат паллиативные вмешательства (баллонная атриосептостомия) и радикальные операции (Мастарда, Сеннинга, Жатене, Растелли, артериального переключения).
Общие сведения
Транспозиция магистральных сосудов – врожденный порок сердца, анатомическую основу которого составляет неправильное расположение аорты и легочной артерии относительно друг друга и их обратное отхождение от желудочков сердца. Среди различных ВПС транспозиция магистральных сосудов составляет 7–15%; в 3 раза чаще встречается у мальчиков. Транспозиция магистральных сосудов входит в число «большой пятерки» – наиболее часто встречающихся врожденных аномалий сердца, наряду с дефектом межжелудочковой перегородки, коарктацией аорты, открытым артериальным протоком, тетрадой Фалло.
В кардиологии транспозиция магистральных сосудов относится к критическим порокам сердца синего типа, не совместимым с жизнью, поэтому требует хирургического вмешательства в первые недели жизни.
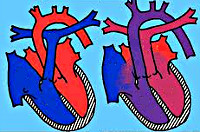
Транспозиция магистральных сосудов
Причины транспозиции магистральных сосудов
Аномалии развития магистральных сосудов формируются в первые 2 месяца эмбриогенеза в результате хромосомных аберраций, неблагоприятной наследственности или отрицательных внешних воздействий. Экзогенными факторами могут выступать вирусные инфекции, перенесенные беременной (ОРВИ, краснуха, ветряная оспа, корь, эпидемический паротит, герпес, сифилис), токсикозы, радиоактивное облучение, лекарственные вещества, алкогольная интоксикация, полигиповитаминоз, заболевания матери (сахарный диабет), возрастные изменения в организме женщины старше 35 лет. Транспозиция магистральных сосудов встречается у детей с синдромом Дауна.
Непосредственные механизмы транспозиции магистральных сосудов до конца не изучены. По одной из версий, порок обусловлен неправильным изгибом аортально-пульмональной перегородки в процессе кардиогенеза. Согласно более современным представлениям, транспозиция магистральных сосудов является результатом неправильного роста субаортального и субпульмонального конуса при разветвлении артериального ствола. При закладке сердце в норме резорбция инфундибулярной перегородки приводит к формированию аортального клапана кзади и книзу от клапана легочной артерии, над левым желудочком. При транспоцизии магистральных сосудов процесс резорбции нарушается, что сопровождается расположением клапана аорты над правым желудочком, а клапана легочной артерии – над левым.
Классификация транспозиции магистральных сосудов
В зависимости от количества сопутствующих коммуникаций, выполняющих компенсирующую роль, и состояния малого круга кровообращения различают следующие варианты транспозиции магистральных сосудов:
1. Транспозиция магистральных сосудов, сопровождающаяся гиперволемией или нормальной величиной легочного кровотока:
- с дефектом межпредсердной перегородки или открытым овальным окном (простая транспозиция)
- с ДМЖП
- с открытым артериальным протоком и наличием дополнительных коммуникаций.
2. Транспозиция магистральных сосудов, сопровождающаяся уменьшением легочного кровотока:
- со стенозом выносного тракта левого желудочка
- с ДМЖП и стенозом выносного тракта левого желудочка (сложная транспозиция)
В 80% случаев транспозиция магистральных сосудов сочетается с одной или несколькими дополнительными коммуникациями; у 85-90% больных порок сопровождается гиперволемией малого круга кровообращения. Для транспозиции магистральных сосудов характерно параллельное расположение аорты относительно легочного ствола, тогда как в нормальном сердце обе артерии перекрещиваются. Чаще всего аорта находится впереди легочного ствола, в редких случаях сосуды располагаются в одной плоскости параллельно, или аорта локализуется кзади от легочного ствола. В 60% наблюдений обнаруживается D-транспозиция – положение аорты справа от легочного ствола, в 40%- L-транспозиция – левостороннее положение аорты.
Особенности гемодинамики при транспозиции магистральных сосудов
С позиций оценки гемодинамики важно различать полную транспозицию магистральных сосудов и корригированную. При корригированной транспозиции аорты и легочной артерии имеет место желудочково-артериальная и предсердно-желудочковая дискордантность. Другими словами, корригированная транспозиция магистральных сосудов сочетается с инверсией желудочков, поэтому внутрисердечная гемодинамика осуществляется в физиологическом направлении: в аорту поступает артериальная кровь, а в легочную артерию венозная. Характер и выраженность гемодинамических нарушений при корригированной транспозиции магистральных сосудов зависят от сопутствующих пороков – ДМЖП, митральной недостаточности и др.
Полная форма сочетает в себе дискордантные желудочково-артериальные взаимоотношения при конкордантном взаимоотношении других отделов сердца. При полной транспозиции магистральных сосудов венозная кровь из правого желудочка поступает в аорту, разносится по большому кругу кровообращения, а затем вновь поступает в правые отделы сердца. Артериальная кровь выбрасывается левым желудочком в легочную артерию, по ней – в малый круг кровообращения и вновь возвращается в левые отделы сердца.
Во внутриутробном периоде транспозиция магистральных сосудов практически не нарушает фетальное кровообращение, поскольку легочный круг у плода не функционирует; циркуляция крови осуществляется по большому кругу через открытое овальное окно или открытый артериальный проток. После рождения жизнь ребенка с полной транспозицией магистральных сосудов зависит от наличия сопутствующих коммуникаций между малым и большим кругом кровообращения (ООО, ДМЖП, ОАП, бронхиальных сосудов), обеспечивающих смешение венозной крови с артериальной. При отсутствии дополнительных пороков дети погибают сразу после рождения.
При транспозиции магистральных сосудов шунтирование крови осуществляется в обоих направлениях: при этом, чем больше размер коммуникации, тем меньше степень гипоксемии. Наиболее благоприятными являются случаи, когда ДМПП или ДМЖП обеспечивают достаточное смешивание артериальной и венозной крови, а наличие умеренного стеноза легочной артерии предотвращает чрезмерную гиперволемию малого круга.
Симптомы транспозиции магистральных сосудов
Дети с транспозицией магистральных сосудов рождаются доношенными, с нормальным или несколько повышенным весом. Сразу после рождения, с началом функционирования отдельного легочного круга кровообращения, нарастает гипоксемия, что клинически проявляется тотальным цианозом, одышкой, тахикардией. При транспозиции магистральных сосудов, сочетающейся с ОАП и коарктацией аорты, выявляется дифференцированный цианоз: синюшность верхней половины тела выражена в большей степени, чем нижней.
Уже в первые месяцы жизни развиваются и прогрессируют признаки сердечной недостаточности: кардиомегалия, увеличение размеров печени, реже – асцит и периферические отеки. При осмотре ребенка с транспозицией магистральных сосудов обращает внимание деформация фаланг пальцев, наличие сердечного горба, гипотрофия, отставание в моторном развитии. При отсутствии стеноза легочной артерии переполнение кровью малого круга кровообращения приводит к частому возникновению повторных пневмоний.
Клиническое течение корригированной транспозиции магистральных сосудов без сопутствующих ВПС длительное время бессимптомное, жалобы отсутствуют, ребенок развивается нормально. При обращении к кардиологу обычно выявляется пароксизмальная тахикардия, атриовентрикулярная блокада, шумы в сердце. При наличии сопутствующих ВПС клиническая картина корригированной транспозиции магистральных сосудов зависит от их характера и степени гемодинамических нарушений.
Диагностика транспозиции магистральных сосудов
Наличие у ребенка транспозиции магистральных сосудов обычно распознается еще в родильном доме. Физикальное обследование выявляет гиперактивность сердца, выраженный сердечный толчок, который смещен медиально, расширенную грудную клетку. Аускультативные данные характеризуются усилением обоих тонов, систолическим шумом и шумом ОАП или ДМЖП.
У детей в возрасте 1-1,5 месяцев по ЭКГ обнаруживаются признаки перегрузки и гипертрофии правых отделов сердца. При оценке рентгенографии грудной клетки высокоспецифичными признаками транспозиции магистральных сосудов являются: кардиомегалия, характерная конфигурация тени сердца яйцеобразной формы, узкий сосудистый пучок в переднезадней проекции и расширенный в боковой проекции, левое положение дуги аорты (в большинстве случаев), обеднение рисунка легких при стенозе легочной артерии или его обогащение при дефектах перегородки.
Эхокардиография показывает аномальное отхождение магистральных сосудов, гипертрофию стенок и дилатацию камер сердца, сопутствующие дефекты, наличие стеноза легочной артерии. С помощью пульсоксиметрии и исследования газового состава крови определяются параметры насыщения крови кислородом и парциальное давление кислорода: при транспозиции магистральных сосудов SО2 менее 30%, PaO2 – менее 20 мм рт.ст. При зондировании полостей сердца обнаруживается повышенное насыщение крови кислородом в правом предсердии и желудочке и пониженное в левых отделах сердца; одинаковое давление в аорте и правом желудочке.
Рентгеноконтрастные методы исследования (вентрикулография, атриография, аортография, коронарография) визуализируют патологическое поступление контраста из левых отделов сердца в легочную артерию, а из правых – в аорту; сопутствующие дефекты, аномалии отхождения венечных артерий. Транспозицию магистральных сосудов следует отличать от тетрады Фалло, атрезии легочной артерии, атрезии трикуспидального клапана, гипоплазии левых отделов сердца.
Лечение транспозиции магистральных сосудов
Всем пациентам с полной формой транспозиции магистральных сосудов показано экстренное оперативное лечение. Противопоказанием служат случаи развития необратимой легочной гипертензии. До операции новорожденным проводится медикаментозная терапия простагландином Е1, помогающим сохранить артериальный проток незаращенным и обеспечить адекватный кровоток.
Паллиативные вмешательства при транспозиции магистральных сосудов необходимы в первые дни жизни для увеличения размера естественного или создания искусственного дефекта между малым и большим кругами кровообращения. К такого рода операциям относятся эндоваскулярная баллонная атриосептостомия (операция Парка–Рашкинда) и открытая атриосептэктомия (резекция межпредсердной перегородки по Блелоку–Хенлону).
К числу гемокорригирующих вмешательств, выполняемых при транспозиции магистральных сосудов, относятся операции Мастарда и Сеннинга – внутрипредсердное переключение потоков артериальной и венозной крови с помощью синтетической заплаты. При этом топография магистральных артерий остается прежней, по внутрипредсердному туннелю из легочных вен кровь поступает в правое предсердие, а из полых вен – в левое.
Варианты анатомической коррекции транспозиции магистральных сосудов включают различные способы артериального переключения: операцию Жатене (пересечение и ортотопическую реплантацию магистральных сосудов, перевязку ОАП), операцию Растелли (пластику ДМЖП и устранение стеноза легочной артерии), артериальное переключение с пластикой МЖП. Специфическими послеоперационными осложнениями, сопровождающими коррекцию транспозиции магистральных сосудов, могут служить СССУ, стеноз устьев легочных и полых вен, стеноз выносящих трактов желудочков.
Прогноз транспозиции магистральных сосудов
Полная транспозиция магистральных сосудов – критический, несовместимый с жизнью порок сердца. При отсутствии специализированной кардиохирургической помощи половина новорожденных погибает в первый месяц жизни, более 2/3 детей – к 1 году от тяжелой гипоксии, недостаточности кровообращения и нарастания ацидоза.
Хирургическая коррекция простой транспозиции магистральных сосудов позволяет достичь хороших отдаленных результатов в 85–90% случаев; при сложной форме порока – в 67% случаев. После операций пациенты нуждаются в наблюдении кардиохирурга, ограничении физических нагрузок, профилактике инфекционного эндокардита. Важное значение имеет пренатальное выявление транспозиции магистральных сосудов с помощью фетальной ЭхоКГ, соответствующее ведение беременности и подготовка к родам.
Источник
Перемещение (транспозиция) магистральных сосудов у ребенка. Тетрада Фалло
При истинной транспозиции не состоялся нормальный спиральный поворот, поэтому аорта отходит спереди из правого желудочка (с трехстворчатой заслонкой), а легочный ствол сзади из левого желудочка (с двустворчатой заслонкой) . При корригированной транспозиции аорта отходит спереди из левого желудочка (с трехстворчатой заслонкой) и легочный ствол сзади из правого желудочка.
Дети с истинной транспозицией могут жить только при наличии компенсирующей аномалии: дефекта межпредсердной или межжелудочковой перегородки, открытого артериального протока, аномалий легочных вен.
Характерен цианоз, появляющийся с самого рождения. При наличии открытого артериального протока, компенсирующего основной порок, нижняя половина тела менее цианотична (так называемый диссоциированный цианоз).
Наряду с цианозом одышка является другим характерным симптомом. Иногда она настолько тяжелая, что затруднены прием пищи и питание грудного ребенка.
Границы сердца при рождении нормальные, расширяются в первые недели и месяцы в отличие от состояния сердца при тетраде Фалло.
Шум над сердцем не характерен, зависит от сопутствующей аномалии, чаще всего от дефекта межжелудочковой перегородки. При отсутствии последнего шум отсутствует, развивается резкий цианоз и ребенок погибает в первые недели жизни.
Рентгенологическое исследование выявляет расширение границ сердца. Характерна яйцевидная форма сердца и относительно узкая тень средостения, поскольку аорта располагается кпереди от легочного ствола. Получается узкая тень сосудов в сагиттальной проекции и расширение ее в косых положениях. Отмечается переполнение сосудов малого круга кровообращения. ЭКГ указывает на гипертрофию правого желудочка.

В неясных случаях диагноз могут уточнить ангиокардиография и катетеризация сердца, однако они не безопасны для этих детей. Поэтому при постановке диагноза обычно обходятся без них.
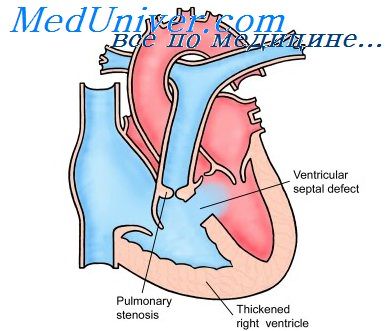
Тетрада Фалло — самый частый врожденный порок сердца. По дант ным И. Литтманна, она встречается в 31,1%, А. Н. Бакулева и Е. Н. Мегаалкина (1955) — в 52,7%, В. И. Мишура и П. А. Куприянова (1957) — в 33% и Института грудной хирургии (1960) —в 41,29% случаев. Характерна комбинация четырех аномалий: декстропозиции аорты, дефекта межжелудочковой перегородки, стеноза или атрезии легочного ствола и гипертрофии миокарда правого желудочка, которые могут быть выражены неодинаково.
Симптомы зависят от выраженности анатомических признаков тетрады Фалло и от стадии заболевания. При значительном сужении легочного ствола, по данным литературы, половина детей умирает на первом году жизни и только 1 ребенок из 4 достигал возраста 10 лет.
Во время внутриутробного развития плода сужение легочного ствола не является препятствием, поскольку большая часть крови идет непосредственно из правого в левое предсердие через овальное окно. Декстропози ция аорты и дефект межжелудочковой перегородки не отражаются на развитии плода: примешивание крови из правого желудочка не вредно, поскольку аорта у плода содержит смешанную кровь. Поэтому новорожденный с тетрадой Фалло нормально развит.
После рождения с началом дыхания кровь из правого предсердия полностью направляется в правый желудочек. Правому желудочку сразу приходится преодолевать троякое препятствие: сужение легочного ствола, высокое давление крови в левом желудочке и аорте и повышенный приток крови через обе полые вены.
Количество крови, поступающей из обоих желудочков в аорту, различно в зависимости от декстропозиции последней: насыщенность кислородом низкая, если в аорте преобладает кровь из правого желудочка, более высокая при заполнении из левого желудочка).
Цианоз появляется вскоре после рождения у одной трети больных, в течение первого года жизни — у другой трети и в ближайшие годы — у последней трети (Kirklin, Payne) от небольшой синюшности до темно-синего цвета — «цвета черной сливы». Поэтому тетраду Фалло считают основным представителем «синей болезни» (morbus coeruleus, blue baby).
Цианоз сопровождается одышкой. В первые недели жизни она появляется во время крика ребенка или сосания, у детей постарше — при движениях, играх, физической нагрузке. Поэтому такие дети избегают движений, принимают положение на корточках. Нередко наблюдаются приступы резкого усиления цианоза и одышки, даже с потерей сознания, что объясняется спазмом выходной части правого желудочка: в это время просвет резко суживается, венозная кровь устремляется в аорту, минуя легкие (И. Литтманн, Р. Фоно).
– Также рекомендуем “Инструментальная диагностика тетрады Фалло. Оксигенация при тетраде Фалло”
Оглавление темы “Комбинированные пороки сердца у детей”:
1. Аорто-легочное сообщение у ребенка. Сужение отверстия аорты
2. Врожденное сужение отверстия легочного ствола. Признаки стеноза легочного ствола
3. Врожденная аневризма аортального синуса. Аномалии полых вен у ребенка
4. Перемещение (транспозиция) магистральных сосудов у ребенка. Тетрада Фалло
5. Инструментальная диагностика тетрады Фалло. Оксигенация при тетраде Фалло
6. Триада Фалло у ребенка. Пентада (пенталогия) Фалло
7. Общий артериальный ствол у ребенка. Тетрада Фалло с атрезией легочного ствола
8. Комплекс Эйзенменгера у ребенка. Синдром (комплекс) Тауссиг — Бинга
9. Дефекты межпредсердной перегородки у ребенка. Открытое овальное окно
10. Незаращение общего атрио-вентрикулярного отверстия у ребенка. Синдром (комплекс) Лутембахера
Источник
