Уплотненные стенки сосудов селезенки

Людмила | (Жен., 35 лет, Иваново, Беларусь) | 06.05.2011 11:02
Спасибо за ответ. Мы недавно лежали на стационаре по поводу сердечка. Биохимический анализ крови: Мочевина-3, 4; Кретинин-85, Общий белок-66,6, Альбумин- 43.0; Анти-Щ-стрептол-100; СРБ-2, Холестерин -4,24; АСаТ-0,; АЛаТ- 0,23; Щ Ф- 9,2; КФ К- 2,32; Mg-0, 79; К-4,3; Na-140; Cl-101.
Анализ мочи: удельный вес-1014;реакция-кислая, лейкоциты-1-2;эпителий пл.в п.зр.-1-2;
Кал на я/г, цисты лямблий, соскоб на энтометриоз-без паталогии.
Это все анализы, котрые мы прошли в больнице. Ещё мазок из зева, где выявили стрептококк А, В группы, но думаю это к делу не имеет отношения…
Позже, по рекомендации, был сдан анализ крови на лямблии и токсокороз- результат отрицательный.
Скажите пожалуйста, наши анализы в норме и что всё таки вызвало данные нарушения в ОБП?
Людмила | (Жен., 35 лет, Иваново, Беларусь) | 06.05.2011 13:43
Извините, я не могу расшифровать эти буквы. Если можно, расшифруйте пожалуйста.
Людмила | (Жен., 35 лет, Иваново, Беларусь) | 06.05.2011 13:52
В интернете нашла, что это Дискинезия желчновыводящих путей. Это правильно? С питанием у нас всё нормально, жирного мы не едим, это скорее всего от того, что у нас аномалия желчного пузыря? А причём здесь тогда увеличение печени?
может быть застой желчи. Принимайте желчегонные, типа одестон по 1 т х 3 р в день за 40 мин до еды – не менее 1 мес. А еще обследуейтесь на гепатиты. В нашей жизни все возможно
Людмила | (Жен., 35 лет, Иваново, Беларусь) | 06.05.2011 18:42
Спасибо большое за ответ. Всё может быть, но у такого маленького ребёнка- не дай Бог! Мы сейчас принимаем препараты Актовигин и Тенотен(лечим нарушение ритма сердечка), поедем на повторное обследование, и если будет на узи ОБП такая же проблема, тогда будем разговаривать с врачом.
Людмила | (Жен., 35 лет, Иваново, Беларусь) | 06.05.2011 19:45
Скажите, а причём здесь увеличение печени и и утолщены сосуды селезёнки, если дело в желчном пузыре?
застой желчи может давать воспаление в печени, которое приводит к увеличению ее размеров. Это олчень приметивное объяснение, но чтобы было понятно. Может быть за счет токсического поражения на фоне застоя. А может и за счет сердца (это отдельная лекция)
Людмила | (Жен., 35 лет, Иваново, Беларусь) | 06.05.2011 21:39
Спасибо вам. Просто хочется понять, почему только недавно всё было нормально, а сейчас есть такие ухудшения неприятные в другой органах. Неужели все проблемы «вытекают» из-за аномальной формы желчного пузыря?
дискинезия, как следствие аномальной формы может влиять на все отраны, т.к. застой желчи или плохое ее отхождение – причина интоксикации, при которой все органы в организме поражаются (отравляются)
СОЗДАТЬ НОВОЕ СООБЩЕНИЕ.
Но Вы – неавторизованный пользователь.
Если Вы регистрировались ранее, то “залогиньтесь” (форма логина в правой верхней части сайта). Если вы здесь впервые, то зарегистрируйтесь.
Если Вы зарегистрируетесь, то сможете в дальнейшем отслеживать ответы на свои сообщения, продолжать диалог в интересных темах с
другими пользователями и консультантами. Помимо этого, регистрация позволит Вам вести приватную переписку с консультантами и другими пользователями сайта.
Зарегистрироваться Создать сообщение без регистрации
Источник
Атеросклероз, инфаркт миокарда, ишемическая болезнь сердца— эти тяжелые диагнозы, как правило, становятся неожиданностью для пациента. Предвестником этих заболеваний часто является дисбаланс жиров в крови — дислипидемия, наследственная или приобретенная. Вовремя ее выявить и начать лечение означает предотвратить или как минимум облегчить серьезные последствия этой патологии для организма.
С чего же все начинается и что делать, если у вас обнаружена дислипидемия? Давайте разбираться по порядку.
Дислипидемия и ее типы
Дислипидемией называется нарушение нормального баланса жироподобных веществ в человеческой крови. Патология часто является одним из факторов развития атеросклероза — распространенного заболевания, которое характеризуется уплотнением стенок и сужением просветов крупных кровеносных сосудов.
Дислипидемия в разных странах может быть диагностирована у каждого 2–15 жителя. Около 60% взрослого населения планеты имеют концентрацию общего холестерина в крови выше нормы (5,55 ммоль/л). У 20% этот показатель превышает 6,5 ммоль/л, что подвергает их высокому риску развития сердечно-сосудистых заболеваний.
Существует несколько классификаций дислипидемии.
- По происхождению:
- Первичная. Не является следствием других заболеваний, может быть обусловлена наследственностью или воздействием внешней среды.
- Вторичная. Развивается вследствие некоторых заболеваний.
- Алиментарная (пищевая). Возникает из-за неправильного питания с высоким содержанием животных жиров.
- По соотношению холестерина и других жировых компонентов:
- Чистая (изолированная) гиперхолестеринемия — повышение уровня холестерина, входящего в состав липопротеидов (повышение уровня «плохого» холестерина).
- Смешанная (комбинированная) гиперлипидемия — повышение в крови как холестерина, так и триглицеридов.
- Классификация по Фредриксону:
- 1 тип — наследственная гиперхиломикронемия. Повышена концентрация только хиломикронов — это липопротеиды, на 90% состоящие из триглицеридов и на 10% — из холестерина. В отличие от других видов, не доказано, что этот тип может вызывать атеросклероз.
- 2а тип — наследственная гиперхолестеринемия, либо обусловленная еще и внешними факторами, повышена концентрация липопротеидов низкой плотности.
- 2b тип — комбинированная гиперлипидемия: повышена концентрация липопротеидов низкой и очень низкой плотности, а также триглицеридов.
- 3 тип — наследственная дис-бета-липопротеидемия: повышена концентрация липопротеидов низкой плотности («плохого» холестерина).
- 4 тип — эндогенная гиперлипидемия: повышена концентрация липопротеидов очень низкой плотности («плохого» холестерина).
- 5 тип — наследственная гипертриглицеридемия: повышена концентрация липопротеидов очень низкой плотности и хиломикронов.
Определить наличие дислипидемии и правильно ее классифицировать может только врач высокой квалификации, поскольку ставить диагноз приходится на основе результатов множественных лабораторных исследований.
Признаки патологии
В большинстве случаев дислипидемию можно определить только по анализу крови — липидограмме. Однако иногда можно увидеть специфические внешние признаки этой патологии:
- Ксантомы. Это плотные узелковые образования, содержащие холестерин. Их можно увидеть или прощупать над сухожилиями пациента — чаще на конечностях, реже на других участках тела.
- Ксантелазмы. Узелки желтого или телесного цвета под кожей век, также содержат холестерин.
- Липоидная дуга роговицы. По краю роговицы глаза можно увидеть белый либо сероватый ободок. Это отложившийся холестерин. Может появиться с возрастом либо передаться по наследству.
Низкая вероятность проявления подобных признаков ведет к тому, что дислипидемия может не обнаруживаться годами, и пациент узнает о ней только уже на стадии лечения ее последствий.
Причины уплотнения стенок сосудов и уменьшения просвета артерий
Дислипидемия закономерно приводит к нарушению липидного и белкового обмена в стенках кровеносных сосудов. При длительном ее существовании, происходит системное поражение артерий — атеросклероз, которое проходит несколько стадий развития, по большей части напрямую связанных с «поведением» липидов в крови:
- Липидное пятно. Если в стенках артерий есть микроповреждения — например, при повышенном сахаре в крови — в этих местах задерживаются липиды.
- Липосклероз. Вокруг липидных отложений разрастается соединительная ткань, формируя атеросклеротическую бляшку. Стенка сосуда в этом месте трескается и изъязвляется, что приводит к образованию тромбов.
- Атерокальциноз. Бляшка уплотняется и кальцинируется, повышая вероятность острой закупорки просвета артерии тромбом с развитием участка инфаркта (разрыва и некроза) или гангрены в той конечности или органе, которые получают кровоснабжение от этой артерии. Поражение коронарных артерий ведет к ишемической болезни сердца.
Таким образом, простой на первый взгляд дисбаланс липидов в крови приводит в действие сложные механизмы, затрагивающие самые разные органы.
Диагностика
Основными методами диагностики дислипидемии являются липидограмма и биохимический анализ крови. Также делаются общий анализ крови и мочи. Обязательно следует проверить пациента на наличие сопутствующих заболеваний, подробно расспросить о его наследственности, питании и образе жизни в целом. Особенно важно прояснить состояние печени, потому что дислипидемия – это системное обменное нарушение, вовлекающее также печень. И заподозрить дислипидемию можно, в том числе, при обследовании печени, на основании выявления признаков НАЖБП. Например, около 50% больных дислипидемией страдают неалкогольной жировой болезнью печени (НАЖБП).
Как лечить дислипидемию?
Немедикаментозное лечение дислипидемии состоит в снижении факторов риска: нормализации веса пациента за счет диеты и физической активности, а также в отказе от алкоголя и курения.
В медикаментозном лечении дислипидемии ведущую роль играют статины — препараты, снижающие синтез холестерина в печени и содержание этого соединения в крови. Они способствуют нормализации липидного обмена, снижают вязкость крови и препятствуют прогрессированию атеросклероза. Однако, у статинов есть побочные эффекты — возможны повреждения печени и мышц, поэтому в курсе лечения необходимо проверять кровь на наличие продуктов распада клеток печени (трансаминаз — аланинаминотрансферазы (АлАт) и аспартатаминотрансферазы (АсАт)) и мышц (креатин-фосфокиназа (КФК)).
Терапия статинами противопоказана, если уровень трансаминаз превышает норму более, чем в 3 раза.
Помимо статинов пациенту могут быть прописаны фибраты, омега-3 полиненасыщенные жирные кислоты.
Профилактика патологии, или Как укрепить сосуды?
Чтобы предотвратить дислипидемию и не допустить развития уже имеющейся (например, наследственной), необходимо следить за массой тела, отказаться от жирной, сладкой и соленой пищи, алкоголя и курения, правильно подбирать физические нагрузки, избегать стрессов, вовремя проходить лечение заболеваний щитовидной железы. Все это в совокупности способствует восстановлению и укреплению сосудов.
Для профилактики и прогрессирования последствий дислипидемии следует вовремя начать ее лечение медикаментозными и немедикаментозными средствами под наблюдением врача.
Источник

SonoAce-R7
Универсальный ультразвуковой сканер высокого класса, ультракомпактный дизайн и инновационные возможности.
Введение
К очаговым образованиям селезенки традиционно относят злокачественные и доброкачественные опухоли, истинные, ложные и паразитарные кисты, а также абсцессы. Эти заболевания встречаются достаточно редко и составляют от 0,5 до 2% всех ее поражений [1-3]. L. Morgenstern даже назвал очаговые изменения селезенки казуистикой [4].
По данным 72 237 аутопсий, выполненных в медицинском центре университета в Южной Калифорнии за период с 1950 по 1974 г., было выявлено 32 случая (1:2257) образований селезенки [5]. На основании анализа более чем 42 000 аутопсий L. Morgenstern пришел к выводу, что частота образований селезенки составляет 0,07% [4], а, по мнению N. Borner, частота очаговых образований селезенки достигает 3,2-4,2% на 100 000 населения [6].
S. Natsugoe и соавт. привели данные W.L. Bostick (1945), который на основании аутопсий и интраоперационных ревизий (более 8000 наблюдений) выявил, что доброкачественные опухоли селезенки встречаются у 0,007% населения [7].
Обращает на себя внимание частота диагностических ошибок, которая даже при использовании современных методов диагностики достигает 75-80% [8]. Правильный диагноз нередко устанавливается только во время операции с использованием срочного морфологического исследования. Ошибки диагностики во многом связаны с недостаточным знанием практическими врачами особенностей обследования подобных больных. В работах, основанных на единичных наблюдениях, нет достаточного описания признаков, характерных для соответствующих патологических образований селезенки, которые выявляются современными методами исследования.
Гамартома (спленаденома, спленома) – термин, используемый для обозначения узловых поражений селезенки, состоящих исключительно из элементов красной пульпы [2, 9]. Чаще гамартома трактуется как неопухолевое образование, состоящее из различных сочетаний нормальных компонентов селезенки [10, 11]. Считается, что это врожденное состояние, однако убедительных данных, подтверждающих это, пока недостаточно [12]. В некоторых случаях гамартома селезенки может сочетаться с подобными образованиями любой локализации [10].
Впервые данная “доброкачественная опухоль” была описана в 1861 г. Rokitansky под названием “спленома” [13]. Публикуемые сообщения посвящены единичным наблюдениям, считается, что к началу нашего столетия описано не более 150 клинических случаев подобного поражения селезенки [14].
Гамартома образуется в результате нарушения морфогенеза и гистологически представлена пролиферирующими фиброзно-мышечными элементами в сочетании с эпителиальными включениями с частичной метаплазией без признаков атипии [15, 16]. Выделяют два подтипа гамартом: образования белой пульпы, состоящие из абберантной лимфоидной ткани, и образования красной пульпы, состоящие из аббератных комплексов синусов [10]. Однако большинство гамартом содержат оба типа элементов. При гистологическом исследовании определяеться отсутствие атипичных фигур митозов и клеток Reed-Sternberg. Важно отметить, что компрессия окружающей селезеночной паренхимы, а не ее инвазия позволяет дифференцировать гамартому от лимфомы селезенки [10].
Гамартома встречается у больных обоего пола, но чаще у женщин [10] пожилого возраста [17]. Клинически практически всегда отмечается бессимптомное течение [2, 10, 11], либо гамартома проявляется последствиями увеличения органа или гиперспленизмом (анемия, тромбоцитопения) [11, 14, 18]. При тяжелых осложнениях – разрыв селезенки, развитие внутрибрюшного кровотечения – появляются соответствующие клинические признаки. Обращает на себя внимание тот факт, что в литературе, несмотря на редкость подобного поражения, описано уже несколько случаев спонтанного разрыва селезенки с гамартомой [13]. Таким образом, специфических синдромов гамартомы селезенки нет.
При ультразвуковом исследовании гамартома выглядит как солидное гомогенное образование с четкими контурами, реже отмечаются кистозная деформация и кальцификация. При дуплексном сканировании имеет место повышенная васкуляризация [19, 20].
При лучевом исследовании гамартому следует дифференцировать с лимфомой, метастатическим поражением, воспалительной миофибробластической опухолью, распространенной грибковой и микобактериальной инфекцией, саркоидозом и сосудистыми опухолями селезенки, такими как гемангиома, “прибрежноклеточная” ангиома (littoral cell angioma), лимфангиома, гемангиоэндотелиома, склерозирующие ангиоматозные узлы и ангиосаркома [4, 19].
Макроскопически патологический очаг выглядит в виде четко отграниченного узла более темного цвета, выбухающего над поверхностью органа, отмечается компрессия окружающей ткани селезенки без ее инфильтрации [14]. В отличие от лимфомы гамартома селезенки красного цвета, часто с геморрагическими проявлениями [21]. Обычно это единичный очаг, который редко может содержать кальцинаты [22], однако описаны наблюдения нескольких патологических узлов в селезенке [14].
При гистологическом исследовании обращают на себя внимание отсутствие фолликулов и дендритических клеток, слабо развитые фиброзные трабекулы, могут наблюдаться очаги экстрамедуллярного кроветворения.
При иммуногистохимическом исследовании клетки сосудистых структур экспрессируют эндотелиальные маркеры, такие как CD-31 и фактор VIII, а также CD-8 и виментин. Реакция на CD-21 и CD-68 в этих клетках отрицательная, хотя CD-68 положителен в рассеянных тромальных макрофагах [23].
Методом лечения больных с данными образованиями является хирургический. Кроме общепризнанного объема операции – спленэктомии, описаны единичные наблюдения резекций селезенки [7, 10].
Материалы и методы
В Институте хирургии им. А.В. Вишневского накоплен опыт диагностики и лечения более 300 пациентов с различными очаговыми образованиями селезенки, но с гамартомами столкнулись лишь в 3 наблюдениях.
Характеристика пациентов: 2 мужчин и 1 женщина в возрасте 50, 54 и 58 лет с образованиями селезенки размерами 6,6×7,5×8,3 см. Из клинических проявлений все трое больных отмечали лишь периодические тянущие боли в правом подреберье.
Всем пациентам предоперационно выполняли УЗИ в полном объеме: исследование в В-режиме, дуплексное сканирование в режимах цветового допплеровского картирования (ЦДК), энергии отраженного допплеровского сигнала (ЭОДС) и импульсной допплерографии.
Во всех случаях проведено оперативное лечение, а образования морфологически верифицированы.
Результаты
При УЗИ во всех случаях отмечали увеличение селезенки в размерах и наличие в разной степени васкуляризированного образования с частично внеорганным расположением. Данные предоперационного УЗИ были представлены следующим образом.
Наблюдение 1
При УЗИ больного Т. селезенка увеличена (площадь – 68 см²), контуры ее неровные, четкие, структура паренхимы неоднородная за счет наличия в средней трети образования, деформирующего латеральный контур селезенки, однако не доходящего до ее ворот. Образование округлой формы, по структуре солидное, гипоэхогенное, с четкими ровными контурами, размером 65x60x53 мм (рис. 1).
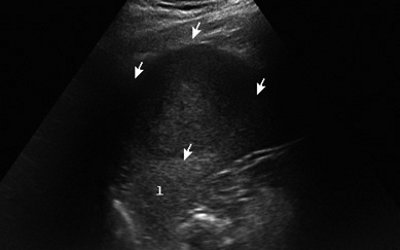
Рис. 1. Эхограмма гамартомы селезенки (В-режим), гамартома указана стрелками.
При дуплексном сканировании образование по контуру огибают селезеночные сосуды без локальных изменений скоростных показателей (рис. 2).
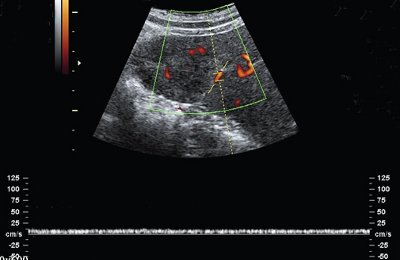
Рис. 2. Регистрация кровотока по огибающим образование сосудам при дуплексном сканировании.
В структуре образования лоцируются два венозных сосуда диаметром 1,5-2,0 мм (рис. 3).
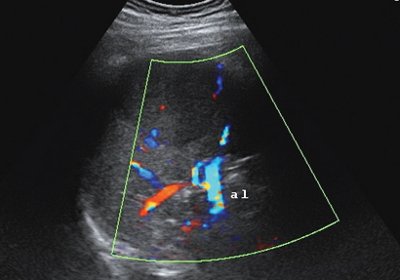
Рис. 3. Дуплексное сканирование селезенки. Кровоток в структуре образования и в паренхиме селезенки (режим ЦДК, al – селезеночная артерия).
Заключение: опухоль селезенки средней степени васкуляризации, наиболее вероятно, гемангиома.
Наблюдение 2
При УЗИ больной М. селезенка увеличена в размерах (площадь – 45 см²), контуры ровные, четкие, структура паренхимы неоднородная за счет наличия в проекции нижнего полюса округлого образования размером 61,3×52,5 мм, расположенного частично экзоорганно. Структура его солидная, гипоэхогенная, незначительно неоднородная, контуры четкие, ровные (рис. 4).
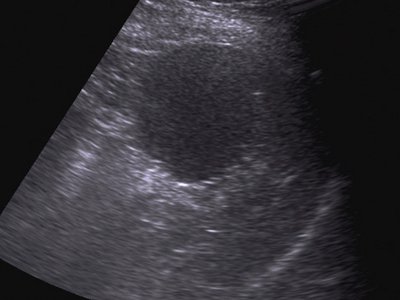
Рис. 4. Эхограмма гамартомы селезенки, В-режим.
При дуплексном сканировании в структуре образования определяются сосуды (рис. 5, а): регистрируются артерии (линейная скорость кровотока – ЛСК – от 0,33 до 0,47 м/с) и вены (ЛСК от 0,08 до 0,12 м/с) (см. рис. 5, б). Вокруг образования отмечается некоторое обеднение сосудистого рисунка, наиболее вероятно, за счет компрессии окружающей ткани селезенки.
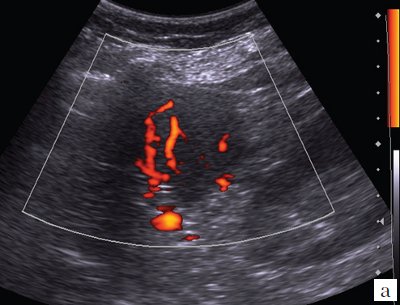
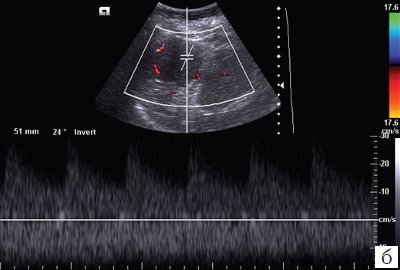
б) Режим цветового допплеровского картирования и импульсной допплерографии с регистрацией спектра допплеровских частот.
Заключение: солидное гиперваскулярное образование нижнего полюса селезенки, наиболее вероятно, гемангиома.
Наблюдение 3
При УЗИ больного С. селезенка увеличена (площадь – 80 см²). В области верхнего полюса селезенки определяется образование с четкими, несколько неровными контурами. Образование распространяется до ворот селезенки и частично экзоорганно, достигая места деления селезеночной артерии на ветви 1-го порядка. Размер образования составляет 70x56x64 мм. Капсула не прослеживается. Структура образования преимущественно однородная, повышенной эхогенности, с наличием лишь небольших отдельных гипоэхогенных зон (рис. 6).
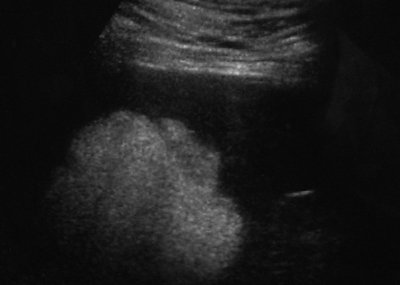
Рис. 6. Эхограмма гамартомы селезенки, В-режим.
В структуре образования по периферии регистрируются два сосуда с венозным спектром кровотока (рис. 7). К медиальному контуру образования тесно прилежит сегментарная селезеночная вена без признаков экстравазальной компрессии. Далее в области ворот селезенки визуализируется анатомический ход еще двух сегментарных вен, которые сопровождают одноименные артерии 2-го порядка.
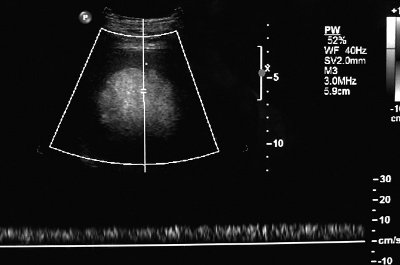
Рис. 7. Регистрация венозного кровотока в структуре гамартомы, дуплексное сканирование.
Заключение: солидная опухоль селезенки умеренной степени васкуляризации.
Таким образом, в двух случаях (см. рис. 1-5) предположительно диагностировали гемангиому, в одном диагноз был сформулирован следующим образом: солидное образование умеренной степени васкуляризации (см. рис. 6, 7). Обращала на себя внимание выраженная гиперваскуляризации образования в одном случае и нетипичная картина солидного образования в другом, вследствие чего в 2 из 3 случаев, нельзя было полностью исключить злокачественную природу очагового поражения селезенки. Эти предположения были также подтверждены по данным компьютерной томографии с контрастным усилением.
Все 3 больных были оперированы. В первом наблюдении (больной Т.), учитывая локализацию образования, произвели спленэктомию. При морфологическом исследовании выявлена гамартома селезенки (рис. 8). Ткань гамартомы характеризовалась стертым рисунком, была нормального гистологического строения за счет утолщения межсинусоидальных пространств с убылью лимфоидной ткани и очаговыми скоплениями призматических клеток.
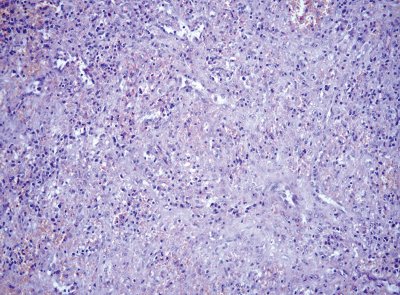
Рис. 8. Микропрепарат гамартомы. Окраска гематоксилином и эозином, x200.
Во втором наблюдении (больная М.) выполнили резекцию селезенки из традиционного доступа в объеме удаления нижней доли вместе с образованием (рис. 9).
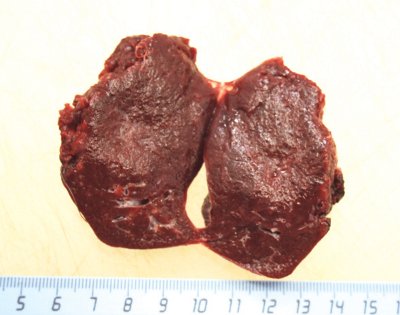
Рис. 9. Макропрепарат, удаленная нижняя доля селезенки вместе с образованием.
При морфологическом исследовании также была выявлена гамартома селезенки (рис. 10). Структура образования напоминала строение красной пульпы селезенки с наличием большого числа сосудистых каналов, выстланных эндотелиоподобными клетками. Выявлялись небольшие участки некроза, четкой границы с нормальной тканью селезенки не определялось, лимфоидные фолликулы отсутствовали.
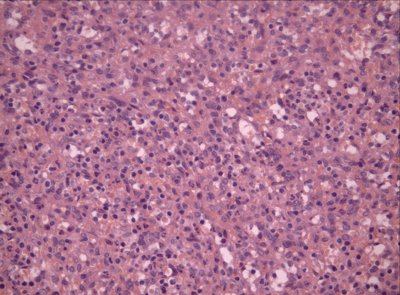
Рис. 10. Микропрепарат гамартомы. Окраска гематоксилином и эозином, x200.
В третьем случае (больной С.) произвели спленэктомию (рис. 11) дополненную с учетом данных срочного гистологического исследования, гетеротопической аутотрансплантацией селезеночной ткани. В нижнем полюсе удаленной селезенки выявили очаг в хорошо выраженной капсуле. Центр образования практически полностью был замещен плотными белесоватыми массами.
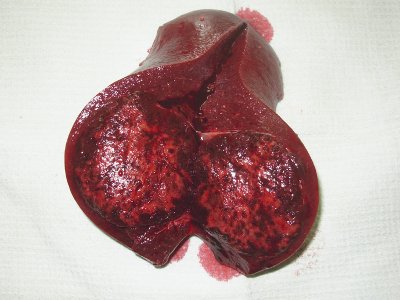
Рис. 11. Макропрепарат, удаленная селезенка вместе с образованием.
При морфологическом исследовании выявлена липоматозная гамартома (рис. 12).
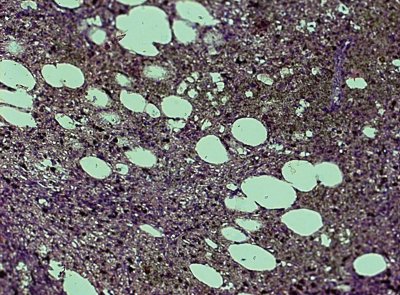
Рис. 12. Микропрепарат липоматозной гамартомы. Окраска гематоксилином и эозином, x200. Определяются группы липоцитов, располагающихся среди измененной полнокровной ткани селезенки.
Образование селезенки в последнем наблюдении представляло наибольший интерес, так как, по данным обследования, макро- и микроскопически отличалось от двух первых. Наличие жировых включений позволило нам установить диагноз – липоматозная гамартома. В медицинской литературе лишь однажды был описан случай первичной липомы селезенки [24], по-видимому, то образование отличалось от описанного в данной статье.
У больного Т. (самый молодой в представленной группе) после спленэктомии, по данным обследования, отмечены выраженные изменения в системе как иммунной защиты, так и гемостаза. Со времени выполнения спленэктомии прошло менее 1 года, за это время были отмечены появление тромбоза вен нижних конечностей, два эпизода пневмонии.
Пациентка М. после резекции селезенки полностью вернулась к привычному образу жизни. При контрольных обследованиях – без особенностей.
Больной С., перенесший спленэктомию, дополненную гетеротопической аутотрансплантацией селезеночной ткани, был вынужден перейти на более легкую работу, в настоящее время продолжает вести активный образ жизни.
Оценивая ретроспективно данные предоперационных обследований и результаты интраоперационной ревизии, можно сказать, что во всех наблюдениях пациентам могли быть выполнены резекционные вмешательства на селезенке (при условии срочного морфологического исследования), что обеспечило бы более высокое качество жизни.
Заключение
Приведенные наблюдения представляют интерес в связи с редким выявлением гамартомы селезенки, что во многом объясняет возникшие трудности дооперационной диагностики. Дважды были заподозрены злокачественные образования селезенки, что в итоге определило объем и характер выполненных хирургических вмешательств. Селезенка была сохранена лишь в одном случае. Срочное морфологическое исследование, исключившее злокачественную природу опухоли, в одном наблюдении позволило произвести гетеротопическую трансплантацию селезеночной ткани. По-видимому, несмотря на редкость гамартомы, вероятность такого поражения селезенки следует учитывать при проведении дифференциально-диагностического поиска.
Литература
- Барта И. Селезенка. Анатомия, физиология, патология и клиника. Будапешт: Издательство АН Венгрии. 1976. 264 с.
- Ершов Ю.А., Суворова Е.В., Минкина С.М., Гласко Е.Н. // Гамартома селезенки. Гематология и трансфузиология. 1988. N 8. С. 53-56.
- Mignon F., Brouzes S., Breitel D.L. et al. Preoperative selective embolization allowing a portial Splenectomy for splenic hamartoma // Ann. Chir. 2003. N 2. P. 112-116.
- Morgenstern L. Nonparasitis splenic cysts (NPSCs): pathogenesis, classification and treatment // J. Am. Coll. Surg. 2002. V. 194. N 3. P. 306-314.
- Uranus S. Current spleen surgery // Munchen: W. Zuckschwerdt Publishers. 1995; 100 p.
- Borner N., Blank W., Bonhof J., Frank K. Echogenic splenic lesions – incidence and differential diagnosis // Ultraschall. Med. 1990. V. 11. N 3. P. 112-118.
- Natsugoe S., Ohwaki T., Tsubouti H. Inflammatory pseudotumor of the spleen: Report of a case // Jpn. J. Surg. 1993. V. 23. P. 246-250.
- Mambrini P., Sabbah P., Le-Toquart J.P. et al. Kystes epidermoides de la rate. A propos de deux cas: revue de la litterature // J. Chir. Paris. 1994. V. 131. N 4. P. 184-190.
- Krishnan J., Frizzera G. Two splenic lesions in need of clarification: hamartoma and inflammatory pseudotumor // Semin. Diagn. Pathol. 2003. V. 20. P. 94-104.
- Lozzo R.V., Haas J.E., Chard R.L. Symptomatic splenic hamartoma: a report of two cases and a review of the literature // Pediatrics. 1980. V. 66. P. 261-265.
- Pinto P.O., Advigo P., Garcia H. et al. Splenic hamartoma: a case report // Eur. Radiol. 1995. V. 5. P. 93-95.
- Morgenstern L., McCafferty L., Rosenberg J. et al. Hamartomas of the spleen // Arch Surg 1984. V. 119. P. 1291-1293.
- Ballardini P., Incasa E., Del Noce A. et al. Spontaneous splenic rupture after start of lung cancer chemotherapt. A case report // Tumori. 2004. V. 90. N 1. P. 144-146.
- Colovic N., Cemerikic V., Colovic R. et al. Hamartoma of the spleen // Srp. Arch. Celor Lek. 2005. V. 128. N 9-10. P. 331-334.
- Itoh H., Yanagi M., Setoyama T. et al. Solitary fibroleiomyomatous shamartoma of the lungina patient without a preexisting smooth – muscle tumor // Pathology. 2001. V. 51. P. 661-665.
- Lee H., Maeda K. Hamartoma of the spleen // Arch. Pathol. Lab. Med. 2009. V. 133. N 1. P. 147-151.
- Morgenstern L., Robenberg J., Geller S.A. Tumors of the spleen // World J. Surg. 1985. V. 9. P. 468-476.
- Tsitouridis I., Michaelies M., Tsitouridis K. et al. Symptomatic splenoma (hamartoma) of the spleen // A case report. Hippokratia. 2010. V. 14. N 1. P. 54-56.
- Brinkley A.A., Lee JK. Cystic hamartoma of the spleen: CT and sonographic findings // JCU. 1981. V. 9. P. 136-138.
- Nakanishi S., Shiraki K., Yamamoto K. et al. Basket pattern blood flow signals discovered in a case of splenic hamartoma by power Doppler ultrasonography // World J. Gastroenterol. 2005. V. 7. N 11. P. 5235-5238.
- Коротких И.Ю., Баранин А.А., Пробатова Н.А. О гамартомах селезенки // Вестн. РОНЦ им. Н.Н. Блохина РАМН. 1994. V. 5. N 5. P. 68-71.
- Komaki S., Gombas O.F. Angiographic demonstration of a calcified splenic hamartoma // Radiology. 1976. V. 121. P. 77-78.
- Arber D.A., Strickler J.G., Chen Y.-Y. B.S., Weiss L.M. Splenic vascular tumors: a histologic, immunophenotypic and virologic study // Am. J. Surg. Pathol. 1997. V. 21. P. 827-835.
- Easler R.E., Dowlin W.M. Primary lipoma of the spleen. Report of a case // Arch. Pathol. 1969. V. 88. P. 557-559.

SonoAce-R7
Универсальный ультразвуковой сканер высокого класса, ультракомпактный дизайн и инновационные возможности.
Источник
