Узи плода магистральные сосуды
УЗИ аппарат RS85
Революционные изменения в экспертной диагностике. Безупречное качество изображения, молниеносная скорость работы, новое поколение технологий визуализации и количественного анализа данных УЗ-сканирования.
Введение
Актуальность темы пренатальной диагностики врожденных пороков сердца (ВПС) понятна всем врачам, которые связаны с пренатальной диагностикой, неонатологией, педиатрией, кардиологией, генетикой. ВПС являются одной из ведущих причин перинатальной смертности и регистрируются с частотой 4-13 на 1000 живорожденных [1]. В связи с тем, что профилактические мероприятия по предупреждению ВПС не имеют должного успеха, представляется актуальной и необходимой их пренатальная ультразвуковая диагностика.
В многочисленных исследованиях зарубежных и отечественных коллег неоднократно формулировались и изучались различные группы риска по возникновению ВПС. Это делалось для того, чтобы потенциально сузить группу беременных женщин, которым показана эхокардиография в специализированном центре. Среди этих групп риска выделяли:
- Семьи, имеющие ребенка с ВПС.
- Семьи с ВПС у одного или обоих супругов.
- Женщин, страдающих сахарным диабетом, системными заболеваниями соединительной ткани, гипотиреозом.
- Беременных с тератогенной экспозицией в ранние сроки беременности (герпес ранее 6-7-й недели) [2].
Однако параллельно другими учеными эти группы риска отвергались, потому что большинство ВПС встречались у плодов и детей, матери которых не входили ни в одну из предложенных групп риска. Единственными разумными критериями так называемого селективного отбора были признаны беременные, попавшие в группу риска после проведения скрининга I триместра и беременные с подозрением на ВПС при ультразвуковом исследовании (УЗИ) плода [3].
Неоспоримо, что оптимальными сроками беременности для исследования сердца плода являются 20-22 недели, однако большинство летальных и клинически значимых пороков сердца могут быть диагностированы в конце I триместра беременности. Позволим себе процитировать слова главы Fetal Medicine Foundation Кипраса Николаидеса, высказанные им на страницах сайта FMF (www.fetalmedicine.com): “Специалист ультразвуковой диагностики с 12 недели беременности должен заверить большинство родителей, что у их ребенка нет крупных врожденных пороков сердца. В случае крупных врожденных пороков сердца их раннее выявление может привести к постановке правильного диагноза или хотя бы вызвать подозрение для осуществления ультразвукового мониторинга”.
Главная цель пренатальной диагностики сформулирована специалистами пренатальной диагностики всего мира – это обеспечение женщины максимально возможной информацией о пороке как можно раньше. Мы должны дать право женщине и семье в целом решать вопрос о пролонгировании беременности с грубыми пороками развития у плода [4].
С каждым годом все большее количество публикаций посвящается диагностике ВПС в ранние сроки – в I триместре беременности [5-8]. Практически ни один из выпусков журнала ISUOG (Ultrasound In Obstetrics and Gynecology, или “белого” журнала, как его называют специалисты) не обходит своим вниманием тему ранней диагностики врожденных пороков развития.
На самом знаменитом сайте в мире пренатальной диагностики www.thefetus.net (Philippe Jeanty, USA) опубликовано уже более 30 случаев находок ВПС в I триместре беременности. Однако в отечественной периодике встречаются лишь единичные работы по этой теме. Все они пренадлежат “перу” специалистов пренатальной диагностики Российской ассоциации врачей ультразвуковой диагностики в перинатологии и гинекологии, хотя для многих специалистов как раньше, так и сейчас осмотр сердца плода в сроки 11-14 недель заключается лишь в констатации числа сердечных сокращений.
Цель эхокардиографии в I триместре беременности состоит в выявлении летальных и клинически значимых ВПС. Это исследование не ставит целью выявление стенозов и гипоплазий выносящих трактов, диагностику мелких дефектов перегородок, патологий дуги аорты и артериального протока. Многие из этих пороков не только технически невозможно заподозрить в I триместре, манифестируют они после 30-й недели беременности, т.е. их диагностика является прерогативой исследования III триместра.
Точность пренатальной диагностики ВПС во все сроки беременности варьирует в широком диапазоне. Причинами этого могут быть разный опыт специалистов, ожирение беременной, частота использованных ультразвуковых трансдьюсеров и класс ультразвукового аппарата, перенесенные ранее абдоминальные операции, срок беременности, количество околоплодных вод и положение плода. Однако заметим, что многие из этих факторов теряют свою актуальность именно при проведении трансвагинальной эхокардиографии в I триместре беременности. Своевременная диагностика ВПС позволяет идентифицировать плоды высокого риска по генетическим синдромам, что имеет важное значение при проведении пренатального консультирования и оказывает существенное влияние на акушерскую тактику.
Результаты
С 2006 по 2011 г. пренатально в I триместре беременности были выявлены 125 ВПС. Из них 68 (55%) ВПС сочетались с различными хромосомными аномалиями (ХА) плода, 30 (24%) входили в состав различных множественных врожденных пороков развития (МВПР), 27 (21%) ВПС были изолированными.
При эхокардиографии изучались четырехкамерный срез сердца плода (рис. 1) и срез через три сосуда (рис. 2). УЗИ проводилось трансабдоминальным датчиком, лишь при необходимости (затрудненная визуализация) использовался внутриполостной датчик. Четырехкамерный срез сердца плода при ультразвуковом сканировании трансабдоминальным датчиком визуализировался в 85% случаев, срез через сосуды – в 73%, при использовании трансвагинального датчика эти цифры существенно возрастали до 100 и 91% соответственно. Оптимизация пренатальной диагностики ВПС может быть достигнута путем строгого соблюдения основных методических правил. При оценке четырехкамерного среза плода необходимо оценить нормальное расположение сердца плода, исключив его эктопию (рис. 3), положение оси сердца плода, что не представляет никаких трудностей, нормальные пропорции и размеры камер сердца, движение створок атриовентрикулярных клапанов должно быть свободным, септальная створка трикуспидального клапана должна располагаться ближе к верхушке сердца (рис. 4). При оценке среза через три сосуда необходимо оценить взаиморасположение сосудов и их диаметр.
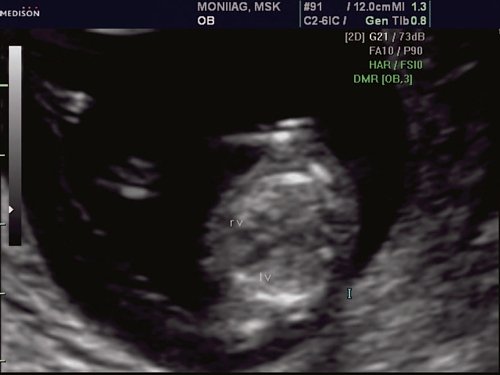
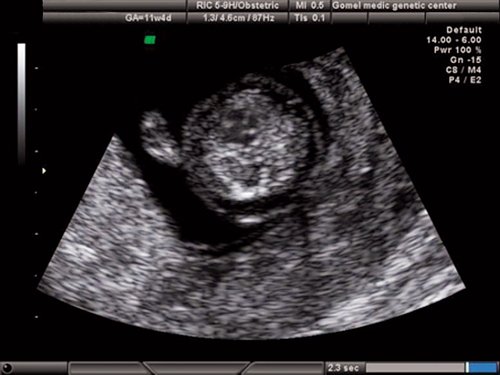
Рис. 1. Беременность 12 недель. Четырехкамерный срез сердца плода. Отчетливо видны камеры сердца.
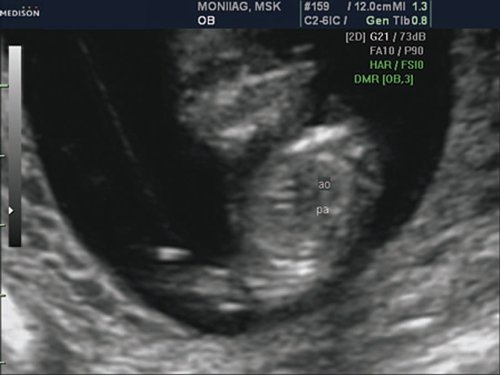
Рис. 2. Беременность 12 недель. Срез через три сосуда. Визуализируются аорта, легочной ствол. Сосуды расположены в одну линию и имеют нормальные размеры.
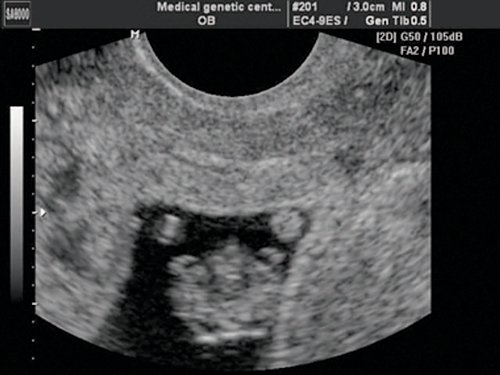
Рис. 3. Беременность 8 недель. Эктопия сердца. Сердце расположено снаружи грудной полости.
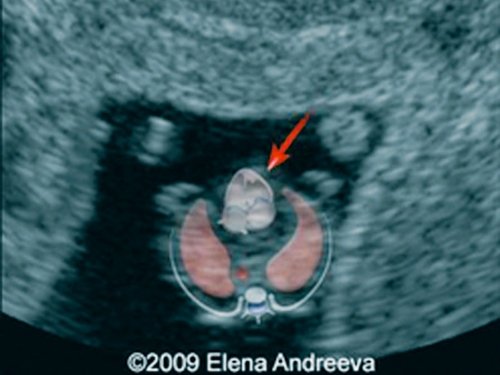
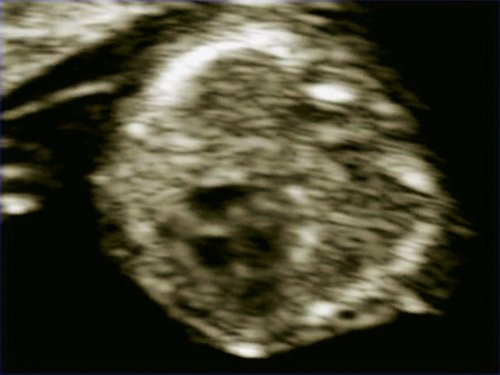
Рис. 4. Беременность 13 недель. Четырехкамерный срез сердца плода. Отчетливо видны камеры сердца. Положение атриовентрикулярных клапанов.
Расширенная эхокардиография предполагает применение дополнительных режимов и срезов – среза через дугу аорты (рис. 5), среза через выносящий тракт левого желудочка (рис. 6), режима ЦДК (рис. 7), импульсной допплерометрии, технологии STIC (рис. 8-11). Это обследование проводится при обнаружении аномальных скрининговых проекций сердца плода, маркеров ХА [расширение толщины воротникового пространства – ТВП, гипоплазия/отсутствие носовой кости (рис. 12, 13), регургитации в венозном протоке (рис. 14), трикуспидальной регургитации (рис. 15)] и/или врожденных пороков развития плода.
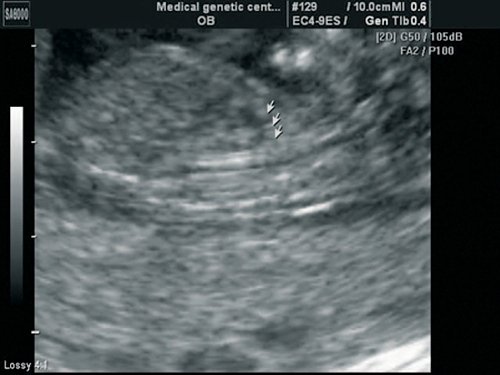
Рис. 5. Беременность 13 недель. Срез через дугу аорты. Отчетливо видны три плечеголовных сосуда, отходящих от дуги.
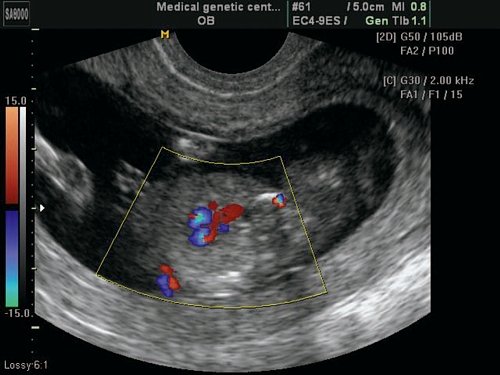
Рис. 6. Беременность 12 недель. Тетрада Фалло. Режим ЦДК. Срез через выносящий тракт левого желудочка. Видна “аорта-наездница”, сидящая над ДМЖП. Случай опубликован на сайте www.thefetus.net.
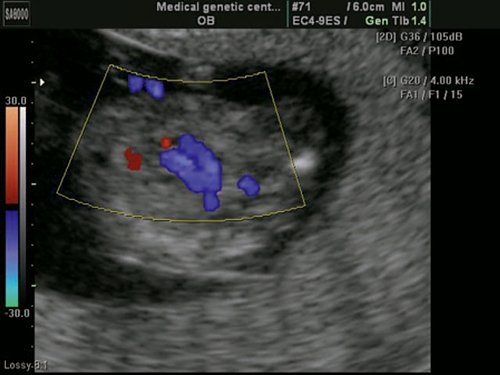
Рис. 7. Беременность 13 недель. Двойной выход сосудов из правого желудочка. Режим ЦДК. Параллельный выход сосудов из правого желудочка.
Рис. 8. Беременность 12 недель. Атриовентрикулярная коммуникация (АВК) при синдроме Дауна. Режим STIC.
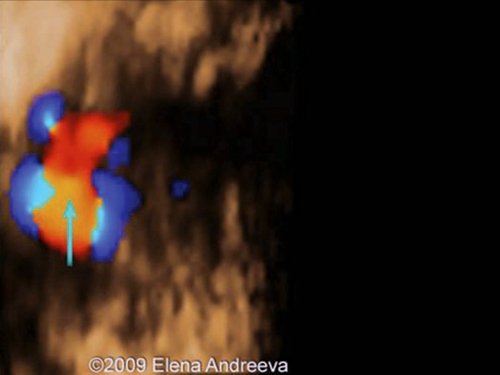
Рис. 9. Беременность 12 недель. Тетрада Фалло. Режим STIC. Аорта “наездница”, сидящая над ДМЖП. Случай опубликован на сайте www.thefetus.net.
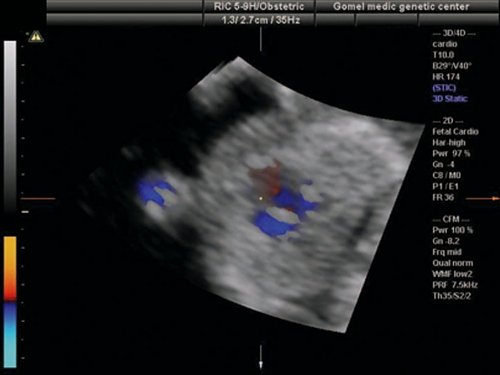
Рис. 10. Беременность 13 недель. Транспозиция магистральных сосудов. Режим STIC. Виден параллельный ход выносящих сосудов, верхний из которых выходит из левого желудочка и делится на бифуркацию (легочная артерия).
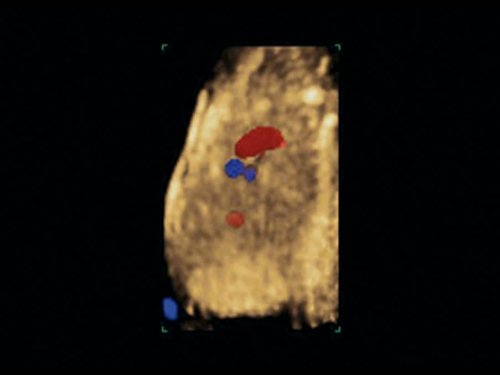
Рис. 11. Беременность 12 недель. Общий артериальный ствол. Режим STIC. Виден единый выносящий сосуд из двух желудочков.
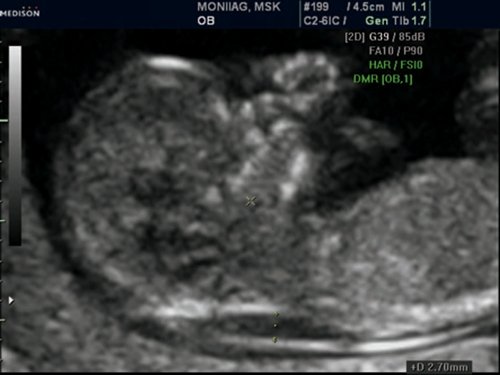
Рис. 12. Беременность 11,4 недель. Множественные маркеры ХА. Синдром Патау (трисомия 13). Увеличение ТВП, аномальный профиль с гипоплазией носовой кости, протуберансом на верхней челюсти (признак расщелины лица), полидактилия. У плода выявлена гипоплазия левых отделов сердца.
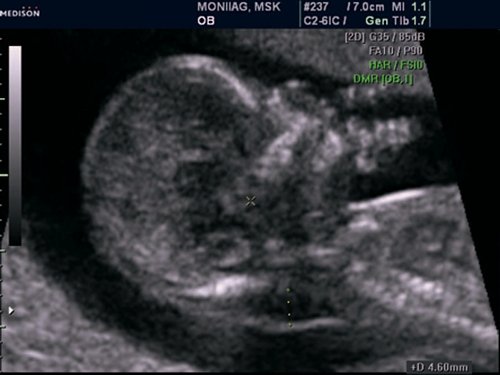
Рис. 13. Беременность 12 недель. Множественные маркеры ХА. Синдром Дауна (трисомия 21). Увеличение ТВП, аномальный профиль с гипоплазией носовой кости. У плода выявлена АВК.
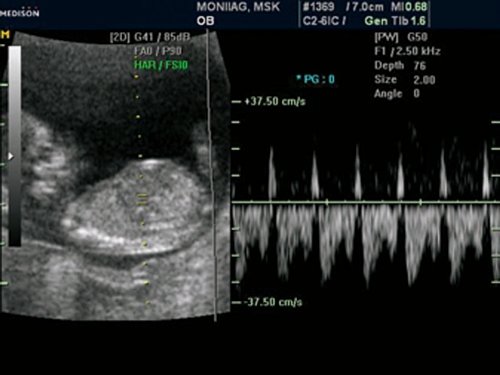
Рис. 14. Беременность 12 недель. Реверсный кровоток в венозном протоке у плода с гетеротаксией.
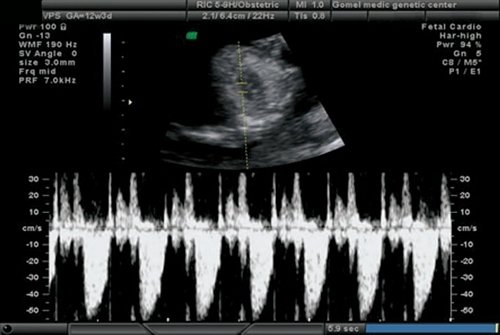
Рис. 15. Беременность 12 недель. Трикуспидальная регургитация у плода с общим артериальным стволом.
Нозология выявленных нами ВПС была следующей:
- синдром гипоплазии левых отделов сердца (СГЛОС) – 29 случаев (рис. 16);
- атриовентрикулярная коммуникация (АВК) – 23 (рис. 17, 18);
- дефект межжелудочковой перегородки (ДМЖП) – 19 (рис. 19);
- патология магистральных сосудов – 19 (из них транспозиция – 3, двойное отхождение сосудов из правого желудочка – 2, тетрада Фалло – 5, общий артериальный ствол – 9);
- патология правых отделов сердца (патология трикуспидального клапана) – 3;
- синдром гетеротаксии – 6;
- единственный желудочек – 4;
- эктопия сердца – 7;
- сочетанные формы ВПС встретились в 15 случаях.
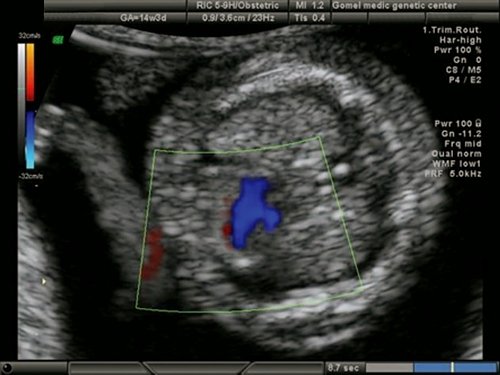
Рис. 16. Беременность 13 недель. Синдром гипоплазии левых отделов сердца у плода с синдромом Тернера (45Х). Единый поток через трикуспидальный клапан. Сброс крови в гипоплазированный левый желудочек через ДМЖП.

Рис. 17. Беременность 11,4 недель. Четырехкамерный срез сердца. Единый атриовентрикулярный клапан. Отсутствует “крест” нормального взаимоотношения атриовентрикулярных клапанов и сердечных перегородок.
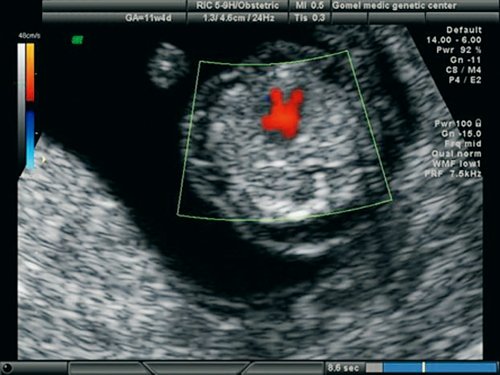
Рис. 18. Беременность 11,4 недель. Четырехкамерный срез сердца. Режим ЦДК. Единый атриовентрикулярный клапан.
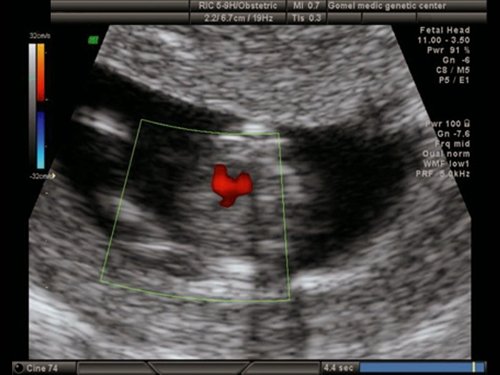
Рис. 19. Беременность 12 недель. Режим ЦДК. Обширный ДМЖП у плода с синдромом Эдвардса (трисомия 18).
При кариотипировании плодов с пренатально установленным диагнозом ВПС в 11-14 недель было диагностировано 68 хромосомных аномалий:
- трисомия 21 (синдром Дауна) выявлена в 23 (34%) случаях,
- трисомия 18 (синдром Эдвардса) – в 19 (28%);
- трисомия 13 (синдром Патау) – в 7 (10%);
- моносомия Х (синдром Тернера) – в 6 (9%);
- триплоидия – в 8 (12%);
- другие хромосомные дисбалансы – в 5 (7%).
Особо следует отметить, что в 8 случаях обнаруженных ХА показанием к кариотипированию было выявление ВПС. У этих плодов было нормальное значение как ТВП, так и длины носовой кости.
При ХА выявленные ВПС по нозологии имели следующие особенности: у большинства плодов с синдромом Дауна диагностировались АВК и ДМЖП; с синдромом Патау – СГЛОС и ДМЖП; с синдромом Эдвардса – ДМЖП, тетрада Фалло и ОАС; при синдроме Тернера – СГЛОС и патология аорты – коарктация аорты в типичном месте (рис. 20).
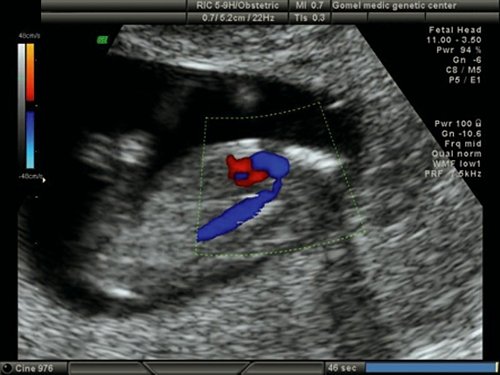
Рис. 20. Беременность 12 недель. Срез через дугу аорты. Режим ЦДК. Сужение аорты в “типичном” месте у плода с синдромом Тернера (45Х).
Необходимо отдельно рассмотреть вопрос верификации ультразвукового диагноза. Все беременности с изолированными ВПС в I триместре пролонгировались до срока II триместра, когда возможна 100% морфологическая верификация диагноза. В современных условиях верификация диагнозов после прерывания беременности в I триместре представляет довольно значимую проблему. Однако при специализированном обучении специалистов-морфологов верификация ВПС возможна и при прерывании беременности в I триместре (рис. 21, 22). Это, несомненно, зависит от качества полученного материала, квалификации морфолога и специального оборудования, необходимого в некоторых случаях, а также от общих методологических подходов к анатомо-морфологической диагностике независимо от срока гестации.
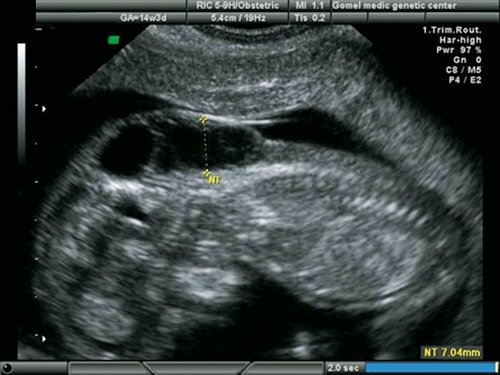
Рис. 21. Беременность 13 недель. Увеличенная ТВП у плода с гипоплазией левых отделов сердца.
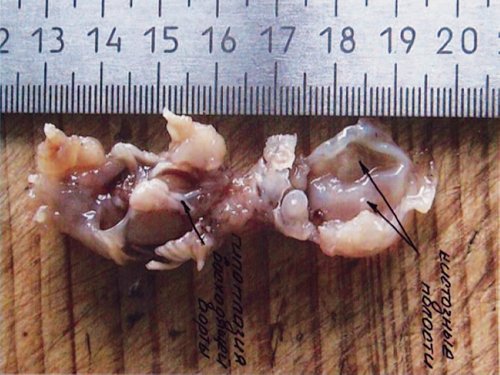
Рис. 22. Тот же плод. Морфологическое обследование – гипоплазия восходящей аорты и кистозные полости (отмечены стрелками).
Заключение
Из сказанного выше можно сделать следующие выводы.
Сердце плода необходимо оценивать у всех беременных при скрининговом осмотре в I триместре (11-14 нед). Так как современная концепция развития пренатальной диагностики в рамках “пилотного” проекта МЗ РФ подразумевает скрининговое обследование в I триместре врачом-экспертом, именно он и должен оценить сердце плода и заподозрить ВПС уже в конце I триместра беременности.
Для исключения летальной и клинически значимой сердечной патологии в I триместре обязательна оценка четырехкамерной проекции сердца плода и среза через три сосуда.
Расширенная эхокардиография должна проводиться при обнаружении аномальных скрининговых проекций сердца плода, маркеров ХА и/или ВПР плода.
При выявлении ВПС в I триместре показано кариотипирование плода.
Литература
- Office for National istics. Mortality istics. Childhood, Infancy and Perinatal. Series DH3. ionary Office: London, 2007; 40.
- Новикова И.В., Прибушеня О.В., Румянцева Н.В. Формирование групп риска по дородовой диагностике врожденных пороков сердца. Инструкция по применению. Минск, 2004.
- Carvalho J.S., Moscoso G., Tekay A. et al. Clinical impact of first and early second trimester fetal echocardiography on high risk pregnancies. Heart. 2004; 90: 921-926.
- Becker R., Wegner R.-D. Detailed screening for fetal anomalies and cardiac defects at the 11-13 week scan. Ultrasound Obstet Gynecol 2006; 27; 613-618.
- Allan L.D., Sharland G.K., Milburn A. et al. Prospective diagnosis of 1,006 consecutive cases of congenital heart disease in the fetus. J Am Coll Cardiol 1994; 23: 1452-1458.
- Huggon I.C., Ghi T., Cook A.C. et al. Fetal cardiac abnor-malities identified prior to 14 weeks’ geion. Ultrasound. Obstet. Gynecol. 2011; 20: 22-29.
- Persico N., Moratalla J., Lombardi C.M. et al. Fetal echocardiography at 11-13 weeks by transabdominal high-frequency ultrasound Ultrasound Obstet. Gynecol. 2011; 37: 296-301
- Allan L.D. Echocardiographic detection of congenitalheart disease in the fetus: present and future. Br. Heart. J. 1995; 74: 103-106.

УЗИ аппарат RS85
Революционные изменения в экспертной диагностике. Безупречное качество изображения, молниеносная скорость работы, новое поколение технологий визуализации и количественного анализа данных УЗ-сканирования.
Источник
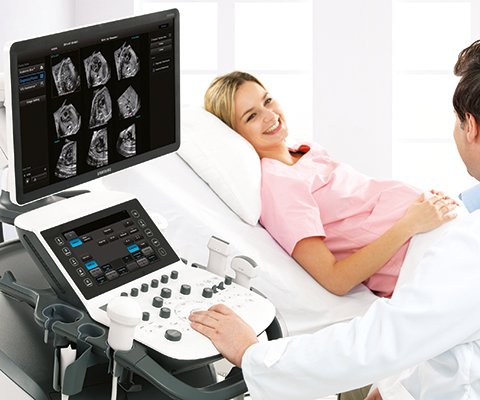
УЗИ сканер WS80
Идеальный инструмент для пренатальных исследований. Уникальное качество изображения и весь спектр диагностических программ для экспертной оценки здоровья женщины.
Важной задачей внутриутробной эхокардиографии является диагностика сложных пороков развития конотрункуса у плода. Цель нашего исследования – проанализировать основные моменты внутриутробной эхокардиографической диагностики пороков конотрункуса. С помощью комплексной эхокардиографии с 1995 по 1999 г. было обследовано 430 беременных женщин из группы риска по врожденным порокам сердца. Внутриутробно диагностировано 11 различных врожденных пороков сердца, обусловленных дефектами формирования конотрункуса. У 2 плодов врожденный порок сердца сочетался с экстракардиальной и хромосомной патологией. На основании аутопсии верифицировано 4 порока, по данным постнатальной эхокардиографии – 6 конотрункальных аномалий. В 1 случае допущена неточность в постановке топического диагноза.
Метод комплексной эхокардиографии позволяет диагностировать с достаточно высокой степенью точности пороки развития конотрункуса у плода. Основным фактором точной пренатальной диагностики пороков данной группы служит качество ультразвукового окна. При плохой визуализации главной проблемой исследования является определение желудочко-сосудистых соединений.
Внутриутробное выявление конотрункальной патологии позволяет оценить возможность адекватной хирургической коррекции порока в постнатальный период.
Введение
Морфологической основой аномалий конотрункуса является нарушение морфогенеза сердца плода на 27±1-37±1 день гестации и как следствие – сбой в сложном ряду постепенных преобразований в формировании перегородки артериального ствола и разделении его проксимальной части на аортальную и легочную ветви [1]. К порокам развития конотрункуса следует относить тетраду Фалло, различные варианты транспозиции магистральных артерий, двойное отхождение магистральных сосудов от правого желудочка, общий артериальный ствол.
Настоящее исследование основано на пятилетнем опыте внутриутробной диагностики врожденных пороков сердца, в частности, аномалий конотрункуса, с помощью метода эхокардиографии.
Материалы и методы
В период 1995-1999 гг. обследовано 430 беременных женщин. Отбор беременных на пренатальную эхокардиографию проводился на основании следующих факторов риска: семейный фактор риска, материнский фактор риска (врожденный порок сердца у матери, сахарный диабет, возраст старше 40 лет), влияние тератогенов (вирусная инфекция, прием медикаментозных препаратов) на ранних сроках гестации, фетальная аритмия, наличие экстракардиальных аномалий у плода. В остальных случаях прицельное изучение сердечно-сосудистой системы плода проводилось при подозрении на сердечную патологию или увеличении размеров сердца во время рутинного обследования в женской консультации.
Всем беременным выполнялось полное эхокардиографическое обследование по разработанной для каждого врожденного порока сердца программе, включающей установление топического диагноза, анатомическую детализацию порока, функциональную оценку желудочков сердца, оценку гемодинамических нарушений в фетоплацентарной системе, выявление сопутствующей патологии. Пренатальное и постнатальное ультразвуковое исследование проводилось на УЗ сканерах SSA-140А (Toshiba), Sonos-1000 (Hewlett Packard), SA-8800 “GAIA” (Medison) с использованием дуплексных и секторальных датчиков 3,5 и 5 Мгц в одномерном, двухмерном эхорежимах; применялось допплеровское исследование в импульсном и цветном режимах.
В первой части нашего анализа осуществлялась диагностика порока сердца, исключение экстракардиальной патологии, динамический контроль с целью уточнения диагноза и наблюдения за функциональными показателями сердечно-сосудистой системы плода. Во второй части – проводилась верификация пренатальных данных с помощью постнатальной прекардиальной, трансэзофагиальной эхокардиографии, ангиографии и аутопсии.
Результаты исследований
Из 430 обследованных беременных женщин у 11 были диагностированы пороки конотрункуса у плода, в том числе у двух плодов врожденный порок сердца сочетался с экстракардиальной и хромосомной патологией (таблица).
Таблица. Пороки конотрункуса, выявленные пренатально.
| Порок | Количество |
|---|---|
| Тетрада Фалло | 3 |
| Транспозиция магистральных артерий | 4 |
| Отхождение аорты и легочной артерии от правого желудочка | 2 |
| Общий артериальный ствол | 2 |
Топический диагноз основного порока оказался правильным в 10 случаях. В 1 случае была допущена диагностическая ошибка. У 4 женщин диагноз был подтвержден данными аутопсии в связи с прерыванием беременности по пороку сердца. В 6 случаях пренатальный диагноз подтвержден на основании прекардиальной и трансэзофагиальной постнатальной эхокардиографии, ангиографии и операционных данных. Ошибка в диагнозе у 1 плода установлена сразу после рождения ребенка.
По нашим данным, качественное изображение внутрисердечных структур плода позволяет точно диагностировать тетраду Фалло уже на 19-20-й неделе гестации. В нашей серии наблюдений 1 беременность была прервана на 24-й неделе. Диагноз верифицирован на основании аутопсии, 2 остальные беременности сохранены. После рождения детей диагноз подтвержден данными постнатальной прекардиальной эхокардиогарфии, а анатомические нюансы порока были уточнены с помощью интраоперационной трансэзофагиальной эхокардиографии (рис. 1).
Рис. 1. В-сканирование сердца плода на 20-й неделе гестации.
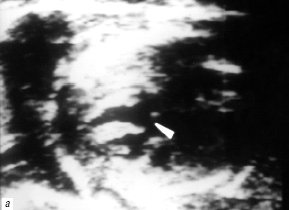
а) Проекция 5 камер сердца. Тетрада Фалло. Стрелкой обозначен подаортальный дефект мезжелудочковой перегородки.
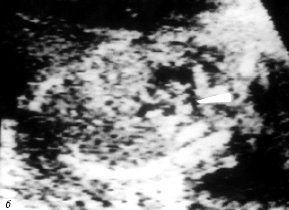
б) Проекция выводного отдела правого желудочка. Стрелкой обозначен стеноз легочной артерии с выраженной гипоплазией ствола и ветвей.
Другой порок развития конотрункуса – транспозиция магистральных артерий – был правильно диагностирован у 3 из 4 изученных плодов. В 1 случае беременность была прервана на 24-й неделе гестации. Диагноз – транспозиция магистральных артерий с дефектом мезжелудочковой перегородки верифицирован на аутопсии. Другая пациентка решила сохранить беременность. Пренатально на 24-й неделе нами выявлена простая полная транспозиция магистральных артерий (рис. 2). Диагноз подтвержден с помощью прекардиальной эхокардиографии через 24 ч после рождения ребенка во время проведения процедуры атриосептостомии – разрыва межпредсердной перегородки с помощью баллона Рашкинда (рис. 3).
Рис. 2. В-сканирование сердца плода на 20-й неделе гестации.
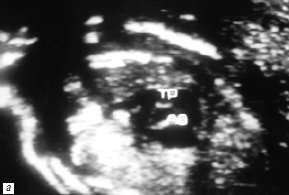
а) Проекция выводного отдела ЛЖ. Параллельный ход сосудов (TP – легочная артерия, Ao – аорта).
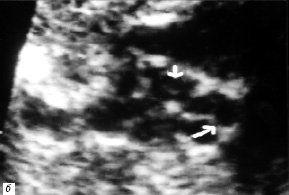
б) Проекция магистральных сосудов по короткой оси. Стрелками обозначены клапаны аорты и легочной артерии. Аорта расположена кпереди и слева от легочной артерии.
Рис. 3. Процедура атриосептостомии, 2-е сутки жизни (RA – правое предсердие, LA – левое предсердие).
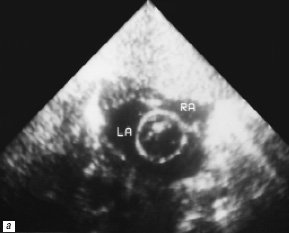
а) Под эхокардиографическим контролем.
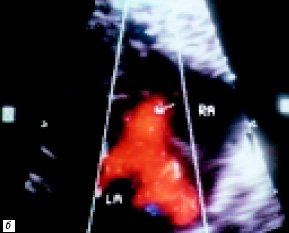
б) Прекардиальная эхокардиограмма. Стрелкой обозначено вторичное межпредсердное сообщение после процедуры атриосептостомии.
У следующего плода на 35-й неделе гестации была диагностирована транспозиция магистральных артерий с выраженным стенозом легочной артерии в сочетании с общим желудочком сердца (рис. 4). Сразу после рождения ребенок переведен в НЦССХ им. А. Н. Бакулева РАМН, где порок сердца был подтвержден по данным постнатальной эхокардиографии.
Рис. 4. В-сканирование сердца плода на 26-й неделе гестации.
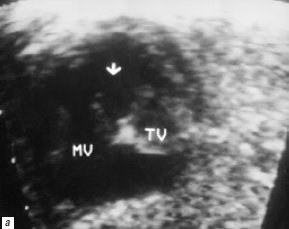
а) Проекция 4 камер сердца. Стрелкой обозначено отсутствие межжелудочковой перегородки (MV – митральный клапан, TV – трикуспидальный клапан).
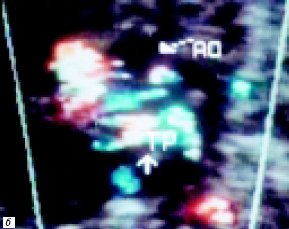
б) Параллельный ход магистральных сосудов. Стрелкой обозначен измененный кровоток в легочной артерии (TP – легочная артерия, Ao – аорта).
У 4-й пациентки визуализация внутрисердечных структур плода даже в проекции 4 камер сердца была крайне затруднена, определить ориентацию магистральных сосудов не удалось и, как следствие, была допущена диагностическая ошибка. Мы заподозрили полную форму открытого атриовентрикулярного канала. Однако после рождения была определена транспозиция магистральных артерий, дефект мезжелудочковой перегородки, гипоплазия кольца митрального клапана, атрезия легочной артерии.
У 2 плодов при ультразвуковом исследовании на 23-й и 27-й неделях беременности заподозрено отхождение магистральных сосудов от правого желудочка в сочетании с дефектом мезжелудочковой перегородки. Дополнительно у одного из плодов выявлены гидроцефалия и хондродисплазия бедренных костей (рис. 5). В данном случае будущая мама решила прервать беременность и диагноз был верифицирован на аутопсии.
Рис. 5. В-сканирование сердца плода на на 23-й неделе гестации.
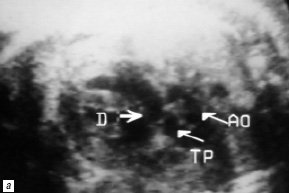
а) Проекция выводного отдела правого желудочка. Отхождение аорты и легочной артерии от правого желудочка (TP – легочная артерия, Ao – аорта, D – подартериальный дефект мезжелудочковой перегородки).
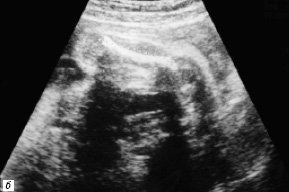
б) Хондродисплазия. Укорочение и деформация бедренной кости.
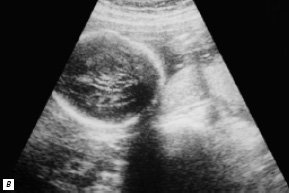
в) Гидроцефалия.
Другая женщина сохранила беременность. Диагноз двойное отхождение магистральных сосудов от правого желудочка с подаортальным дефектом мезжелудочковой перегородки был подтвержден на основании постнатальной эхокардиографии и ангиокардиографии.
Эхокардиография плода позволила выявить в 2 случаях такой сложный порок, как общий артериальный ствол 1-го типа на 25-й и 30-й неделях беременности. В первом случае общий артериальный ствол сочетался с множественными пороками развития. Череп плода деформирован, структуры головного мозга изменены, определяется асимметрия полушарий мозга, деформация полости прозрачной перегородки, изменение формы боковых желудочков и их выраженная асимметрия.
Грудная клетка гипоплазирована. Выявлена выраженная асимметричная гипоплазия легких. Отмечается омфалоцеле, содержащее печень плода (рис. 6). Кроме того, имела место и фетальная хромосомная патология – трисомия 13. Диагноз был подтвержден на аутопсии после прерывания беременности. Во втором случае женщина приняла решение сохранить беременность. На 38-й неделе ей сделана операция кесарева сечения. Диагноз – общий артериальный ствол 1 тип – подтвержден на основании прекардиальной эхокардиографии и на операции.
Рис. 6. В-сканирование сердца плода на 25-й неделе гестации.
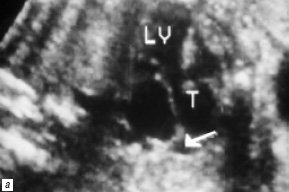
а) Проекция 5 камер сердца (LV – левый желудочек, T – трункус). Стрелкой обозначено отхождение устья легочной артерии от боковой поверхности трункуса.
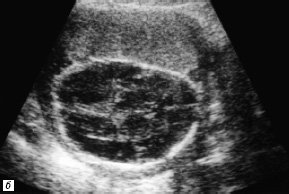
б) Деформация черепа плода, изменение структур головного мозга.
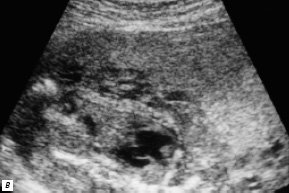
в) Омфалоцеле, содержащее печень плода.
Обсуждение
Диагностическая точность. Результаты нашего исследования, как и данные других авторов [2, 3], демонстрируют возможность выявления аномалий конотрункуса у плода с достаточно высокой степенью точности. В нашей серии наблюдений врожденная патология сердца этой группы чаще встречалась в семьях, уже имеющих детей с врожденным пороком сердца, в 6 случаях из 11, что еще раз подтверждает мнение некоторых авторов [4, 5], отмечающих широкий диапазон колебаний рецидива врожденного порока сердца в семье – от 2-5 до 8-9%.
Основным принципом диагностики аномалий конотрункуса у плода, как и у новорожденного, должна быть ориентация на прямые анатомические признаки порока [6]. Однако в отличие от постнатального исследования главным лимитирующим фактором в диагностике пороков конотрункуса служит плохая визуализация сердца плода в связи с избыточным весом матери (более 85-95 кг), выраженными периферическими отеками или выраженным маловодием.
При плохом ультразвуковом окне возникают проблемы в определении желудочкососудистых соединений. Особенно сложно дифференцировать аорту и легочную артерию при стенозе последней [7, 8], так как узкий сосуд накладывается на сосуд более широкого диаметра, что может создать ложное впечатление о том, от какого желудочка сердца он отходит. В некоторых случаях сложно определить ориентацию магистральных сосудов при двойном отхождении магистральных сосудов от правого желудочка, так как у плода признаки нарушения митрально-полулунного контакта видны нечетко.
Обязательным моментом исследования является определение соотношения диаметров аорты и легочной артерии, что поможет заподозрить пороки конотрункуса со стенозом одного из сосудов [9].
Высока степень совершения ошибки при простой транспозиции магистральных сосудов. В этом случае 4-камерная проекция сердца соответствует норме и следует особое внимание уделять изучению желудочко-сосудистых соединений [10 ]. Необходимо помнить, что основным анатомическим признаком аорты является локация створок и коронарных артерий в поперечном сечении, отхождение брахиоцефальных сосудов в проекции дуги аорты и кривая скорости кровотока в режиме импульсного допплера. Основным анатомическим признаком легочной артерии служит визуализация бифуркации ствола на правую и левую легочные артерии и кривая скорости кровотока в режиме импульсного допплера.
При недостаточно четкой видимости сердца плода в некоторых случаях сложно дифференцировать общий артериальный ствол и тетраду Фалло с выраженной гипоплазией ствола и легочных артерий [11], поэтому чрезвычайно важно проводить пренатальную эхокардиографию на сроках гестации, оптимальных для детального сканирования. Полагаем, что для исключения пороков конотрункуса оптимальными сроками фетальной эхокардиографии являются 22-25 нед гестации.
Выводы
- Пренатальная эхокардиография позволяет диагностировать аномалии конотрункуса у плода с достаточно высокой степенью точности.
- Исследование сердца плода на предмет конотрункальной патологии оптимально проводить на 22-25-й неделях гестации.
- Основным принципом диагностики пороков конотрункуса у плода служит ориентация на прямые анатомические признаки порока.
- Определяющим фактором точного выявления врожденного порока сердца этой группы является качество визуализации внутрисердечных структур плода.
- Основные проблемы в диагностике аномалий конотрункуса связаны с определением ориентации магистральных сосудов.
- Внутриутробное выявление аномалий конотрункуса позволяет оценить возможность адекватной хирургической коррекции порока в постнатальный период.
Литература
- Банкл Г. Врожденные пороки сердца и крупных сосудов. М.: Медицина, 1980. – 37-39 с.
- Davis G.K., Farguhar C.M., Allan L.D. et al. Structural cardiac abnormalities in the fetus: reliability of prenatal diagnosis and outcome. Br J Obstet Gynaecol, 1990; 97:27-31.
- Allan L.D., Sharland G.K., Milburn A. et al. Prospective diagnosis of 1,006 consecutive cases of congenital heart disease in the fetus. J Am Coll Cardiol, 1994;23:1452-58.
- Allan L.D., Crawford D.C., Chita S.K. et al. Familian reccurence of congenital heart disease in a prospective series of mothers reffered for fetal echocardiography. Am J Cardiol, 1986;58:334.
- Nora J.J. Etiologic aspects of heart diseases. Heart disease in infants, children and adolescents, 3rd ed. Williams-Wilkins, 1983:2-10.
- Зубкова Г.А. Двухмерная и допплерэхокардиография в диагностике врожденных пороков сердца у новорожденных и детей первого года жизни /Дис. д-ра мед. наук. – М., 1992.
- Allan L.D., Crawford D.C., Tynan M.J. Pulmonary atresia in prenatal life. J Am Coll Cardiol, 1986;8:1131.
- Fyler D.C. D-Transposition of the great arteries. In: Fyler DC, ed. Nadas Pediatric Cardiology. Philadelphia: Hanely-Belfus, 1992:557-76.
- Comstock C.H., Riggs T., Lee W. et al. Pulmonary-to-aorta diameter ratio in the normal and abnormal fetal heart. Am J Obstet Gynecol, 1991;165:1038-44.
- Kirklin J.M., Colvan E
