Узи плода сердце срез через три сосуда
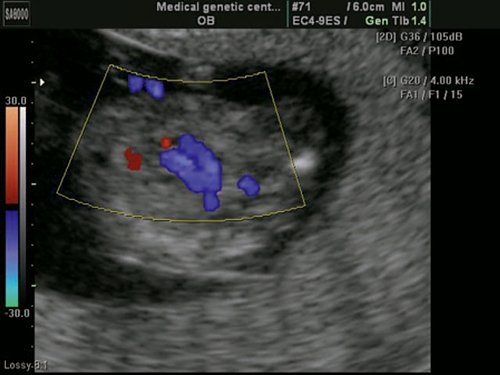
Хотя четырехкамерный срез сердца плода является достаточно информативным для диагностики многих ВПС, он имеет существенные ограничения для пренатальной диагностики аномалий главных артерий. В последние годы в клинической практике для пренатальной диагностики ВПС, сопровождающихся изменением главных артерий, стал использоваться срез через три сосуда. За непродолжительный период времени этот срез стал обязательной составляющей скрининговой оценки ультразвуковой анатомии плода.
Обязательное включение в скрининговое пренатальное исследование сердца и главных артерий плода среза через три сосуда стало одним из основных решений участников специализированного семинара «Допплерография в акушерстве. Эхокардиография плода», который проходил в рамках IV Всероссийской зимней школы врачей ультразвуковой диагностики с 13 по 20 октября 2001 г. Отныне протокол скринингового ультразвукового исследования в 20-24 нед беременности обязательно должен содержать информацию об этой плоскости сканирования. Ее оценка реально повышает диагностику ВПС и особенно трудно выявляемых пороков магистральных сосудов.
Получение изображения среза через три сосуда увеличивает продолжительность ультразвукового исследования плода не более чем на одну минуту. Техника получения изображения этой плоскости очень проста, необходим лишь короткий тренинг специалистов, организация которого возможна на базе региональных пренатальных диагностических центров силами местных ведущих специалистов.
Для получения изображения среза через три сосуда необходимо после оценки четырехкамерного среза сердца сместить трансдьюсер в сторону головы плода, сохраняя поперечную плоскость сканирования, или слегка наклонить трансдьюсер к голове плода. Основными изучаемыми сосудами при оценке среза через три сосуда являются основной ствол легочной артерии, восходящая аорта и верхняя полая вена. Дополнительно в этих плоскостях визуализируются деление основной легочной артерии на левую и правую ветви и грудной отдел аорты. Продолжая смещать трансдьюсер в сторону головы плода и сохраняя сканирование в поперечной плоскости, можно также оценить срезы через артериальный проток и через дугу аорты.
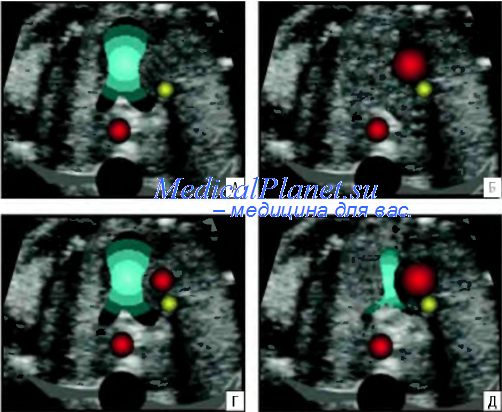
При оценке среза через три сосуда при каждом ультразвуковом исследовании целесообразно отвечать всего натри основных вопроса.
1. Видны ли все три сосуда? В норме отчетливое изображение трех сосудов удается получить достаточно легко. При этом они всегда располагаются в следующем порядке. Центральное расположение занимает основной ствол легочной артерии, справа от него – восходящая аорта, а правее нее – верхняя полая вена. В случаях, когда все три сосуда не видны, следует помнить, что расширение легочной артерии и отсутствие изображения восходящей аорты чаще всего отмечается при атрезии аорты, выраженной гипоплазии дуги аорты и/или левого желудочка. Расширение восходящей аорты и отсутствие изображения легочной артерии наблюдается при атрезии легочной артерии и общем артериальном стволе. При оценке трех сосудов не следует забывать и об аномалиях расположения верхней полой вены. В случаях, когда верхняя полая вена не будет визуализироваться в обычном месте (справа от аорты), необходимо внимательно осмотреть область левее легочной артерии, что позволит пренатально диагностировать аномалии ее впадения в предсердие.
2. Располагаются ли сосуды в одну линию? При ответе на этот, казалось бы, банальный вопрос следует помнить, что он имеет решающее значение для эффективной пренатальной диагностики транспозиции главных артерий. В норме основание легочной артерии, восходящей аорты и поперечный срез верхней полой вены располагаются в одну линию. При транспозиции главных артерий расположение сосудов изменяется за счет смещение аорты кпереди.
3. Нормальные ли размеры сосудов? В норме легочная артерия всегда больше аорты, которая всегда больше верхней полой вены. Однако это превалирование должно быть не более чем в 1,3 раза. Обнаружение диспропорции диаметров главных артерий (диаметр легочной артерии существенно больше аорты или диаметр аорты больше легочной артерии) является важным диагностическим критерием их аномалий. Расширение легочной артерии при нормальных размерах восходящей аорты чаще всего отмечается при объемной перегрузке правого желудочка и стенозе клапана легочной артерии. О нормальных размерах аорты в этих случаях судят по отношению ее размеров к верхней полой вене. Обнаружение расширения восходящей аорты и сужения легочной артерии позволяет диагностировать как тетраду Фалло, так и изолированную гипоплазию легочной артерии. Расширение восходящей аорты при нормальныхразмерахлегочной артерии чаще всего отмечается при больших мышечных дефектах межжелудочковой перегородки и по-стстенотическом расширении в случаях стеноза аортального клапана. Нормативные показатели диаметра восходящей аорты и основного ствола легочной артерии представлены на рисунке.
В последнее время на страницах специализированных журналов, освещающих вопросы пренатальной ультразвуковой диагностики, срез через три сосуда все чаще начинают называть срезом через три сосуда и трахею. Это вызвано тем обстоятельством, что оценка расположения трахеи позволяет более точно устанавливать пороки системы дуги аорты. При правой дуге аорты и двойной дуге аорты трахея локализуется между главными артериями.
Констатация нормального четырехкамерного среза сердца и среза через три сосуда, оцениваемых в скрининговом режиме, осуществляется только при отсутствии изменений при изучении каждого показателя. В случае обнаружения тех или иных изменений необходимо получение дополнительных срезов для уточнения нозологической формы ВПС.
Учебное видео УЗИ сердца плода в норме
– Читать далее “Срезы через главные артерии. Возможности при исследовании плода через главные артерии.”
Оглавление темы “Аномалии сердца плода. УЗИ диагностика пороков сердца.”:
1. Четырехкамерный срез сердца. Методика четырехкамерного среза сердца.
2. Оценка ав-клапанов у плода. Исследование эндокарда у плода.
3. Срез через три сосуда. Основные вопросы перед УЗИ обследованием через три сосуда.
4. Срезы через главные артерии. Возможности при исследовании плода через главные артерии.
5. Цветовое допплеровское картирование сердца плода. Импульсная допплерография сердца плода.
6. Аномалии расположения сердца плода. УЗИ определение положения сердца плода.
7. Дефекты интракардиальных перегородок. Диагностика интракардиальных перегородок плода.
8. Общий предсердно-желудочковый канал. Диагностика общего предсердно-желудочкового канала плода.
9. Гипопластический синдром левых отделов сердца. Диагностика гипопластического синдрома левых отделов сердца плода.
10. Единственный желудочек сердца плода. Диагностика единственного желудочка сердца плода.
Источник
Основные пороки сердца у плода формируются в 1 триместре беременности на сроке 12-14 недель. Это может быть реакция на внешние факторы либо генетические проблемы. К этому сроку происходит формирование сердечной мышцы плода, поэтому будущей матери необходимо пройти УЗИ обследование на выявление патологий органа.

Во внутриутробном развитии пороки сердца возникают как реакция организма на нарушение плацентарного кровообращения либо воздействие канцерогенных веществ (формальдегиды, никотин, токсические вещества).
Аномалии положения сердца плода
Среди аномалий расположения сердца выделяют эктопию сердца (размещение вне грудной клетки). К таким патологиям относят декстрокардию (смещение сердца в правую сторону относительно нормального положения) и мезокардию (расположение сердца не с левой стороны грудины, а по срединной линии тела).
Эктопия сердца у плода возникает на сроке 14-18 дней с момента зачатия мезадерма начинает развиваться неправильно, что вызывает неправильное срастание брюшной стенки. У плода либо отсутствует диафрагма вообще, либо нет диафрагмального сегмента перикарда.
Из-за отверстия в стенке между правым и левым желудочком слышны интракардиальные шумы. Также у плода эктопия сердца нередко сопровождается другими аномалиями — гидроцефалией, энцефалоцеле и пр.
Надо сказать, что существует высокая вероятность ошибочного диагноза по установки положения сердца. При тазовом предлежании плода на УЗИ сердца визуализируется справа, хотя на самом деле оно располагается в положенном месте.
В 71% случаев эктопия сердца вызывается плевральным выпотом, кистозным аденоматозным пороком развития лёгкого, диафрагмальной грыжей.
Различают четыре вида эктопии:
- абдоминальная (сердце находится в брюшине);
- грудная (сердце выходит наружу через дефекты грудины);
- торакоабдоминальная (пентада Кантрелла — сложнейшая патология, имеющая комплекс отклонений от нормы);
- шейная (сердце смещается в область сердца).
Грудная эктопия встречается в 55-60% случаев, торакоабдоминальная — в 38%, шейная — почти в 3%. Выживаемость составляет около 10%. В большинстве случаев при эктопии младенец либо рождается мёртвым, либо умирает сразу после рождения.
Патология сопровождается смещением других внутренних органов, которые не защищены от механических повреждений и подвержены инфекциям и вирусам больше обычного.
Врождённые дефекты сердца
Пять наиболее встречаемых дефектов — это тетрада Фалло, дефект межжелудочковой перегородки, транспозиция магистральных сосудов, коарктация аорты, гипоплазия левых камер.
Оптимальным сроком для проведения ультразвуковой диагностики сердца плода считается период 24-26 недель беременности. Именно в это время анатомические структуры сердца максимально визуализируются, а на более ранних сроках можно увидеть только явные и глобальные пороки сердца.
Наиболее информативен ультразвуковой осмотр 4-камерного среза сердца. После которого при любом отклонении от нормы женщина отправляется на более детальное обследование плода с использованием допплеровской эхокардиографии. Также проводится кариотипирование, потому что в 30% случаев аномалии являются результатом хромосомных нарушений.
Что выявляет УЗИ
В нашей клинике используется современное 4D оборудование, имеющее допплеровский режим. С его помощью можно получить изображение 3-х главных сосудов — верхней полой вены, лёгочного ствола и восходящей аорты. Во время обследования выявляется не только расположение сосудов, но и их диаметр и другие параметры.
На экране монитора будут видны следующие патологии плода:
- Уменьшение диаметра аорты при расширении лёгочного ствола можно говорить об гипоплазии (недоразвитости) левых отделов сердца малыша, отвечающих за начало кровообращения;
- Уменьшение ствола лёгочной артерии в размерах при сохранении в норме диаметров аорты и верхней полой вены указывает на стеноз (сужение) лёгочной артерии. У плода выявляются только выраженные формы;
- Маленький диаметр аорты при нормальном 4-камерном строении сердца является следствием коарктации аорты (сужение аорты сердца в определённом сегменте);
- Визуализация 2 сосудов вместо 3 может быть следствием соединения сосудов в общий артериальный ствол;
- Смещение аорты вперёд или правее лёгочной артерии наблюдается при транспозиции магистральных сосудов;
- Диаметр аорты расширен, но при этом сужен диаметр лёгочной артерии, а аорта смещена вперёд. Это может является тетрадой Фалло (очень тяжёлая сочетанная аномалия сердца). Проблема включает в себя стеноз или гипертрофию выходного отдела правого желудочка, дефект межжелудочковой перегородки, декстропозицию аорты (отхождение в правую сторону). Диагностика плода крайне затруднительна, поэтому на помощь приходит допплеровский режим, помогающий визуализировать поток крови в аорту из обоих желудочков;
- Гипоплазия (недоразвитость) правых камер сердца определяется по уменьшению их размеров относительно левых камер. Эта патология сопровождается обычно дисплазией (провисанием или выбуханием) митрального клапана;
- Общий предсердно-желудочковый канал виден как дефект перегородки сердца с расщеплением атриовентрикулярного клапана;
- Гипопластический синдром левых отделов сердца проявляется в виде недоразвития желудочка и митрального и аортального клапанов;
- Единственный желудочек также не является нормой, потому что их должно быть два и они хорошо просматриваются в четырёхкамерном срезе;
- При недоразвитости трёхстворчатого клапана кровь из правого предсердия не попадает в левое, что хорошо видно при допплеровском исследовании;
- Со 2 триместра фиброэластоз эндокарда визуализируется как утолщение миокарда и ухудшении его сокращения;
- Недоразвитие миокарда одного из желудочков (аномалия Уля) заметна на 2 триместре.
Какие патологии сердца у плода сложно выявить на скрининговом УЗИ
Трудности в диагностике заболеваний сердца на УЗИ вызывают следующие патологии органа:
- дефект межпредсердной перегородки;
- дефект межжелудочковой перегородки;
- транспозиция главных артерий.
При подозрении на их наличие, пациентка должна регулярно наблюдаться и соблюдать все рекомендации гинеколога.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter
Поделиться ссылкой:
Источник

SonoAce-R7
Универсальный ультразвуковой сканер высокого класса, ультракомпактный дизайн и инновационные возможности.
Введение
Актуальность темы пренатальной диагностики врожденных пороков сердца (ВПС) понятна всем врачам, которые связаны с пренатальной диагностикой, неонатологией, педиатрией, кардиологией, генетикой. ВПС являются одной из ведущих причин перинатальной смертности и регистрируются с частотой 4-13 на 1000 живорожденных [1]. В связи с тем, что профилактические мероприятия по предупреждению ВПС не имеют должного успеха, представляется актуальной и необходимой их пренатальная ультразвуковая диагностика.
В многочисленных исследованиях зарубежных и отечественных коллег неоднократно формулировались и изучались различные группы риска по возникновению ВПС. Это делалось для того, чтобы потенциально сузить группу беременных женщин, которым показана эхокардиография в специализированном центре. Среди этих групп риска выделяли:
- Семьи, имеющие ребенка с ВПС.
- Семьи с ВПС у одного или обоих супругов.
- Женщин, страдающих сахарным диабетом, системными заболеваниями соединительной ткани, гипотиреозом.
- Беременных с тератогенной экспозицией в ранние сроки беременности (герпес ранее 6-7-й недели) [2].
Однако параллельно другими учеными эти группы риска отвергались, потому что большинство ВПС встречались у плодов и детей, матери которых не входили ни в одну из предложенных групп риска. Единственными разумными критериями так называемого селективного отбора были признаны беременные, попавшие в группу риска после проведения скрининга I триместра и беременные с подозрением на ВПС при ультразвуковом исследовании (УЗИ) плода [3].
Неоспоримо, что оптимальными сроками беременности для исследования сердца плода являются 20-22 недели, однако большинство летальных и клинически значимых пороков сердца могут быть диагностированы в конце I триместра беременности. Позволим себе процитировать слова главы Fetal Medicine Foundation Кипраса Николаидеса, высказанные им на страницах сайта FMF (www.fetalmedicine.com): “Специалист ультразвуковой диагностики с 12 недели беременности должен заверить большинство родителей, что у их ребенка нет крупных врожденных пороков сердца. В случае крупных врожденных пороков сердца их раннее выявление может привести к постановке правильного диагноза или хотя бы вызвать подозрение для осуществления ультразвукового мониторинга”.
Главная цель пренатальной диагностики сформулирована специалистами пренатальной диагностики всего мира – это обеспечение женщины максимально возможной информацией о пороке как можно раньше. Мы должны дать право женщине и семье в целом решать вопрос о пролонгировании беременности с грубыми пороками развития у плода [4].
С каждым годом все большее количество публикаций посвящается диагностике ВПС в ранние сроки – в I триместре беременности [5-8]. Практически ни один из выпусков журнала ISUOG (Ultrasound In Obstetrics and Gynecology, или “белого” журнала, как его называют специалисты) не обходит своим вниманием тему ранней диагностики врожденных пороков развития.
На самом знаменитом сайте в мире пренатальной диагностики www.thefetus.net (Philippe Jeanty, USA) опубликовано уже более 30 случаев находок ВПС в I триместре беременности. Однако в отечественной периодике встречаются лишь единичные работы по этой теме. Все они пренадлежат “перу” специалистов пренатальной диагностики Российской ассоциации врачей ультразвуковой диагностики в перинатологии и гинекологии, хотя для многих специалистов как раньше, так и сейчас осмотр сердца плода в сроки 11-14 недель заключается лишь в констатации числа сердечных сокращений.
Цель эхокардиографии в I триместре беременности состоит в выявлении летальных и клинически значимых ВПС. Это исследование не ставит целью выявление стенозов и гипоплазий выносящих трактов, диагностику мелких дефектов перегородок, патологий дуги аорты и артериального протока. Многие из этих пороков не только технически невозможно заподозрить в I триместре, манифестируют они после 30-й недели беременности, т.е. их диагностика является прерогативой исследования III триместра.
Точность пренатальной диагностики ВПС во все сроки беременности варьирует в широком диапазоне. Причинами этого могут быть разный опыт специалистов, ожирение беременной, частота использованных ультразвуковых трансдьюсеров и класс ультразвукового аппарата, перенесенные ранее абдоминальные операции, срок беременности, количество околоплодных вод и положение плода. Однако заметим, что многие из этих факторов теряют свою актуальность именно при проведении трансвагинальной эхокардиографии в I триместре беременности. Своевременная диагностика ВПС позволяет идентифицировать плоды высокого риска по генетическим синдромам, что имеет важное значение при проведении пренатального консультирования и оказывает существенное влияние на акушерскую тактику.
Результаты
С 2006 по 2011 г. пренатально в I триместре беременности были выявлены 125 ВПС. Из них 68 (55%) ВПС сочетались с различными хромосомными аномалиями (ХА) плода, 30 (24%) входили в состав различных множественных врожденных пороков развития (МВПР), 27 (21%) ВПС были изолированными.
При эхокардиографии изучались четырехкамерный срез сердца плода (рис. 1) и срез через три сосуда (рис. 2). УЗИ проводилось трансабдоминальным датчиком, лишь при необходимости (затрудненная визуализация) использовался внутриполостной датчик. Четырехкамерный срез сердца плода при ультразвуковом сканировании трансабдоминальным датчиком визуализировался в 85% случаев, срез через сосуды – в 73%, при использовании трансвагинального датчика эти цифры существенно возрастали до 100 и 91% соответственно. Оптимизация пренатальной диагностики ВПС может быть достигнута путем строгого соблюдения основных методических правил. При оценке четырехкамерного среза плода необходимо оценить нормальное расположение сердца плода, исключив его эктопию (рис. 3), положение оси сердца плода, что не представляет никаких трудностей, нормальные пропорции и размеры камер сердца, движение створок атриовентрикулярных клапанов должно быть свободным, септальная створка трикуспидального клапана должна располагаться ближе к верхушке сердца (рис. 4). При оценке среза через три сосуда необходимо оценить взаиморасположение сосудов и их диаметр.
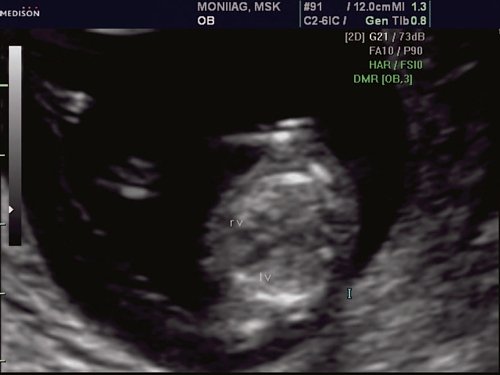
Рис. 1. Беременность 12 недель. Четырехкамерный срез сердца плода. Отчетливо видны камеры сердца.
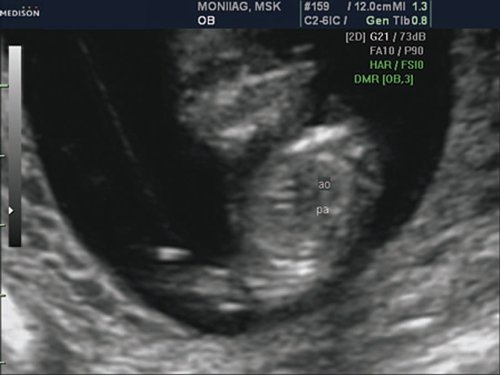
Рис. 2. Беременность 12 недель. Срез через три сосуда. Визуализируются аорта, легочной ствол. Сосуды расположены в одну линию и имеют нормальные размеры.
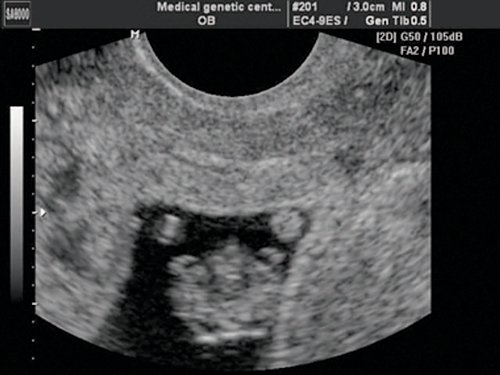
Рис. 3. Беременность 8 недель. Эктопия сердца. Сердце расположено снаружи грудной полости.
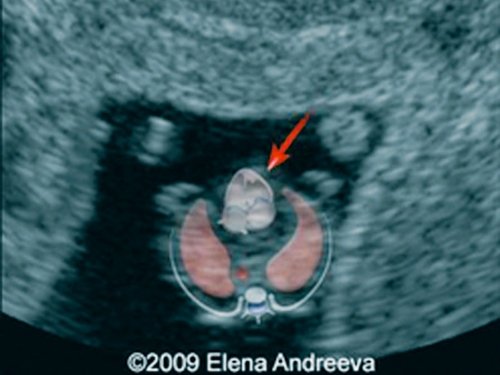
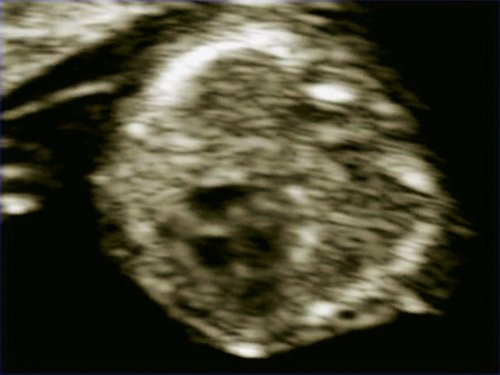
Рис. 4. Беременность 13 недель. Четырехкамерный срез сердца плода. Отчетливо видны камеры сердца. Положение атриовентрикулярных клапанов.
Расширенная эхокардиография предполагает применение дополнительных режимов и срезов – среза через дугу аорты (рис. 5), среза через выносящий тракт левого желудочка (рис. 6), режима ЦДК (рис. 7), импульсной допплерометрии, технологии STIC (рис. 8-11). Это обследование проводится при обнаружении аномальных скрининговых проекций сердца плода, маркеров ХА [расширение толщины воротникового пространства – ТВП, гипоплазия/отсутствие носовой кости (рис. 12, 13), регургитации в венозном протоке (рис. 14), трикуспидальной регургитации (рис. 15)] и/или врожденных пороков развития плода.
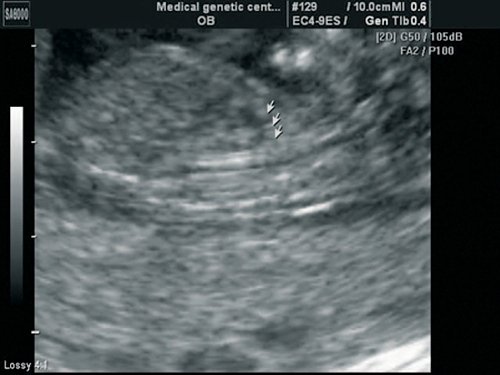
Рис. 5. Беременность 13 недель. Срез через дугу аорты. Отчетливо видны три плечеголовных сосуда, отходящих от дуги.
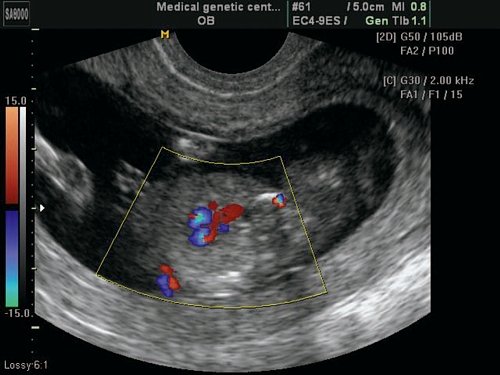
Рис. 6. Беременность 12 недель. Тетрада Фалло. Режим ЦДК. Срез через выносящий тракт левого желудочка. Видна “аорта-наездница”, сидящая над ДМЖП. Случай опубликован на сайте www.thefetus.net.

Рис. 7. Беременность 13 недель. Двойной выход сосудов из правого желудочка. Режим ЦДК. Параллельный выход сосудов из правого желудочка.
Рис. 8. Беременность 12 недель. Атриовентрикулярная коммуникация (АВК) при синдроме Дауна. Режим STIC.
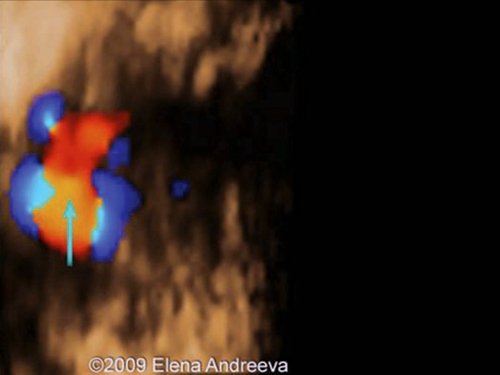
Рис. 9. Беременность 12 недель. Тетрада Фалло. Режим STIC. Аорта “наездница”, сидящая над ДМЖП. Случай опубликован на сайте www.thefetus.net.
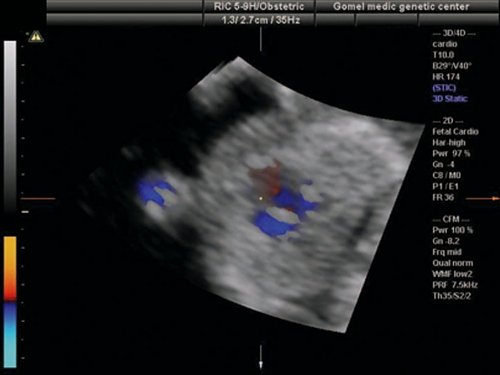
Рис. 10. Беременность 13 недель. Транспозиция магистральных сосудов. Режим STIC. Виден параллельный ход выносящих сосудов, верхний из которых выходит из левого желудочка и делится на бифуркацию (легочная артерия).
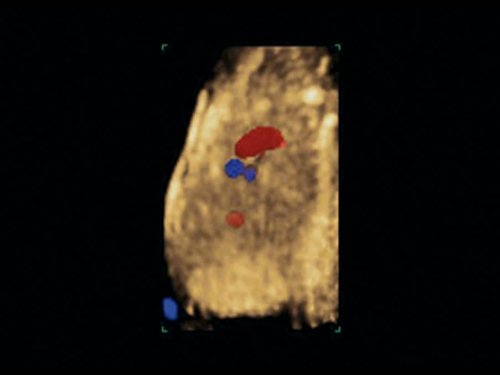
Рис. 11. Беременность 12 недель. Общий артериальный ствол. Режим STIC. Виден единый выносящий сосуд из двух желудочков.
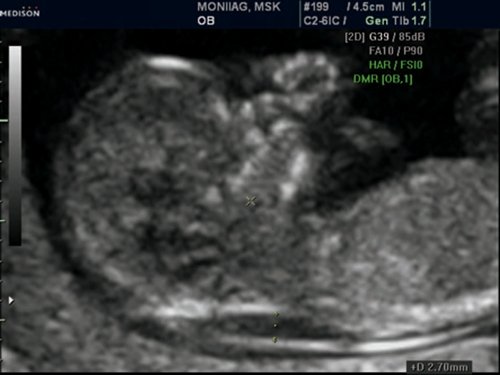
Рис. 12. Беременность 11,4 недель. Множественные маркеры ХА. Синдром Патау (трисомия 13). Увеличение ТВП, аномальный профиль с гипоплазией носовой кости, протуберансом на верхней челюсти (признак расщелины лица), полидактилия. У плода выявлена гипоплазия левых отделов сердца.
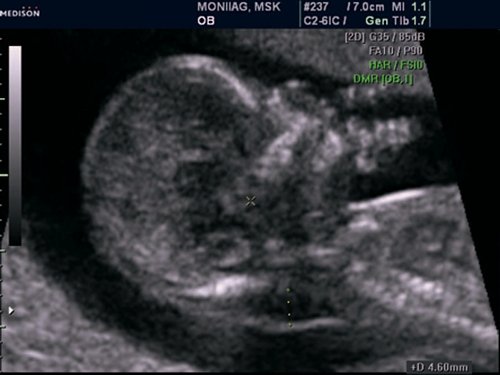
Рис. 13. Беременность 12 недель. Множественные маркеры ХА. Синдром Дауна (трисомия 21). Увеличение ТВП, аномальный профиль с гипоплазией носовой кости. У плода выявлена АВК.
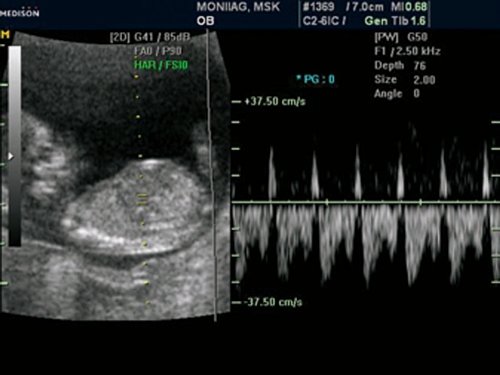
Рис. 14. Беременность 12 недель. Реверсный кровоток в венозном протоке у плода с гетеротаксией.
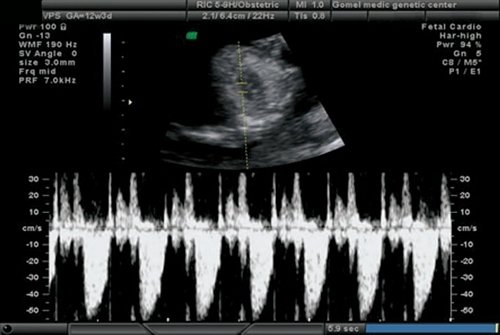
Рис. 15. Беременность 12 недель. Трикуспидальная регургитация у плода с общим артериальным стволом.
Нозология выявленных нами ВПС была следующей:
- синдром гипоплазии левых отделов сердца (СГЛОС) – 29 случаев (рис. 16);
- атриовентрикулярная коммуникация (АВК) – 23 (рис. 17, 18);
- дефект межжелудочковой перегородки (ДМЖП) – 19 (рис. 19);
- патология магистральных сосудов – 19 (из них транспозиция – 3, двойное отхождение сосудов из правого желудочка – 2, тетрада Фалло – 5, общий артериальный ствол – 9);
- патология правых отделов сердца (патология трикуспидального клапана) – 3;
- синдром гетеротаксии – 6;
- единственный желудочек – 4;
- эктопия сердца – 7;
- сочетанные формы ВПС встретились в 15 случаях.
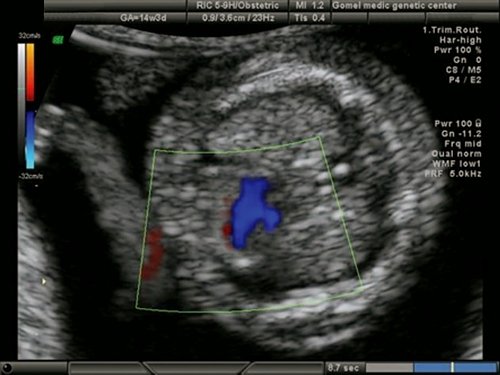
Рис. 16. Беременность 13 недель. Синдром гипоплазии левых отделов сердца у плода с синдромом Тернера (45Х). Единый поток через трикуспидальный клапан. Сброс крови в гипоплазированный левый желудочек через ДМЖП.
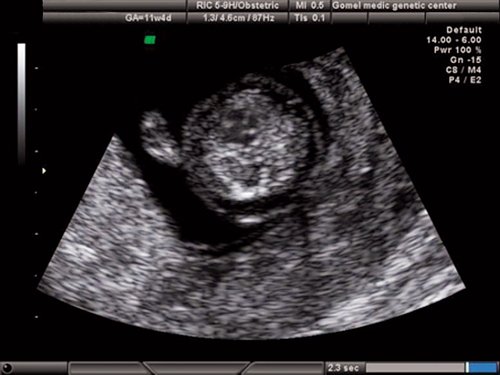
Рис. 17. Беременность 11,4 недель. Четырехкамерный срез сердца. Единый атриовентрикулярный клапан. Отсутствует “крест” нормального взаимоотношения атриовентрикулярных клапанов и сердечных перегородок.
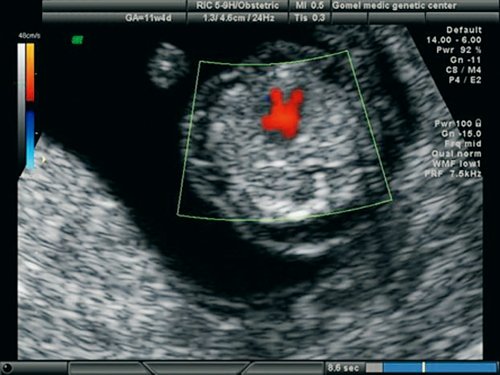
Рис. 18. Беременность 11,4 недель. Четырехкамерный срез сердца. Режим ЦДК. Единый атриовентрикулярный клапан.
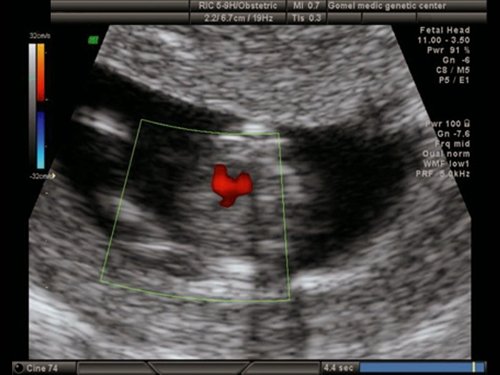
Рис. 19. Беременность 12 недель. Режим ЦДК. Обширный ДМЖП у плода с синдромом Эдвардса (трисомия 18).
При кариотипировании плодов с пренатально установленным диагнозом ВПС в 11-14 недель было диагностировано 68 хромосомных аномалий:
- трисомия 21 (синдром Дауна) выявлена в 23 (34%) случаях,
- трисомия 18 (синдром Эдвардса) – в 19 (28%);
- трисомия 13 (синдром Патау) – в 7 (10%);
- моносомия Х (синдром Тернера) – в 6 (9%);
- триплоидия – в 8 (12%);
- другие хромосомные дисбалансы – в 5 (7%).
Особо следует отметить, что в 8 случаях обнаруженных ХА показанием к кариотипированию было выявление ВПС. У этих плодов было нормальное значение как ТВП, так и длины носовой кости.
При ХА выявленные ВПС по нозологии имели следующие особенности: у большинства плодов с синдромом Дауна диагностировались АВК и ДМЖП; с синдромом Патау – СГЛОС и ДМЖП; с синдромом Эдвардса – ДМЖП, тетрада Фалло и ОАС; при синдроме Тернера – СГЛОС и патология аорты – коарктация аорты в типичном месте (рис. 20).
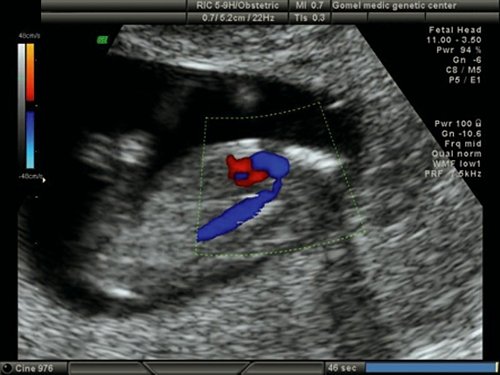
Рис. 20. Беременность 12 недель. Срез через дугу аорты. Режим ЦДК. Сужение аорты в “типичном” месте у плода с синдромом Тернера (45Х).
Необходимо отдельно рассмотреть вопрос верификации ультразвукового диагноза. Все беременности с изолированными ВПС в I триместре пролонгировались до срока II триместра, когда возможна 100% морфологическая верификация диагноза. В современных условиях верификация диагнозов после прерывания беременности в I триместре представляет довольно значимую проблему. Однако при специализированном обучении специалистов-морфологов верификация ВПС возможна и при прерывании беременности в I триместре (рис. 21, 22). Это, несомненно, зависит от качества полученного материала, квалификации морфолога и специального оборудования, необходимого в некоторых случаях, а также от общих методологических подходов к анатомо-морфологической диагностике независимо от срока гестации.
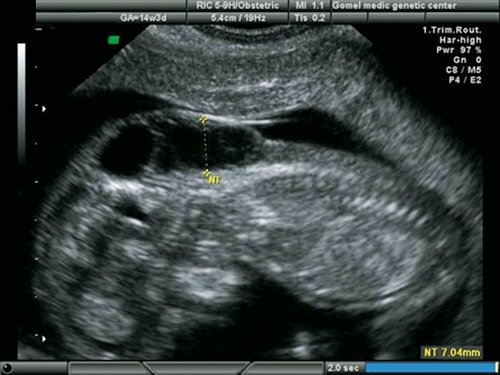
Рис. 21. Беременность 13 недель. Увеличенная ТВП у плода с гипоплазией левых отделов сердца.
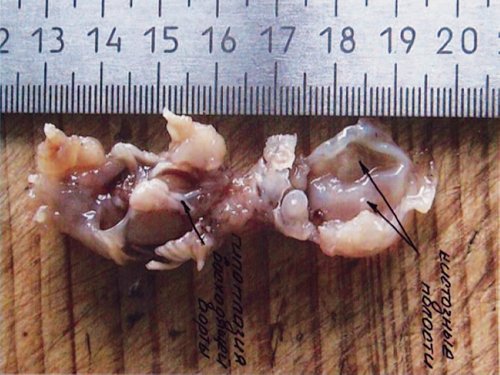
Рис. 22. Тот же плод. Морфологическое обследование – гипоплазия восходящей аорты и кистозные полости (отмечены стрелками).
Заключение
Из сказанного выше можно сделать следующие выводы.
Сердце плода необходимо оценивать у всех беременных при скрининговом осмотре в I триместре (11-14 нед). Так как современная концепция развития пренатальной диагностики в рамках “пилотного” проекта МЗ РФ подразумевает скрининговое обследование в I триместре врачом-экспертом, именно он и должен оценить сердце плода и заподозрить ВПС уже в конце I триместра беременности.
Для исключения летальной и клинически значимой сердечной патологии в I триместре обязательна оценка четырехкамерной проекции сердца плода и среза через три сосуда.
Расширенная эхокардиография должна проводиться при обнаружении аномальных скрининговых проекций сердца плода, маркеров ХА и/или ВПР плода.
При выявлении ВПС в I триместре показано кариотипирование плода.
Литература
- Office for National Statistics. Mortality Statistics. Childhood, Infancy and Perinatal. Series DH3. Stationary Office: London, 2007; 40.
- Новикова И.В., Прибушеня О.В., Румянцева Н.В. Формирование групп риска по дородовой диагностике врожденных пороков сердца. Инструкция по применению. Минск, 2004.
- Carvalho J.S., Moscoso G., Tekay A. et al. Clinical impact of first and early second trimester fetal echocardiography on high risk pregnancies. Heart. 2004; 90: 921-926.
- Becker R., Wegner R.-D. Detailed screening for fetal anomalies and cardiac defects at the 11-13 week scan. Ultrasound Obstet Gynecol 2006; 27; 613-618.
- Allan L.D., Sharland G.K., Milburn A. et al. Prospective diagnosis of 1,006 consecutive cases of congenital heart disease in the fetus. J Am Coll Cardiol 1994; 23: 1452-1458.
- Huggon I.C., Ghi T., Cook A.C. et al. Fetal cardiac abnor-malities identified prior to 14 weeks’ gestation. Ultrasound. Obstet. Gynecol. 2011; 20: 22-29.
- Persico N., Moratalla J., Lombardi C.M. et al. Fetal echocardiography at 11-13 weeks by transabdominal high-frequency ultrasound Ultrasound Obstet. Gynecol. 2011; 37: 296-301
- Allan L.D. Echocardiographic detection of congenitalheart disease in the fetus: present and future. Br. Heart. J. 1995; 74: 103-106.

SonoAce-R7
Универсальный ультразвуковой сканер высокого класса, ультракомпактный дизайн и инновационные возможности.
Источник
